
了解新型冠状病毒肺炎(COVID-19)轻症和重症患者的临床特征及其重症化的危险因素。
回顾性分析2020年1月20日至2月29日广州医科大学附属第八人民医院所收治的148例COVID-19患者的临床资料,将患者分为轻症组(包括轻型、普通型)和重症组(包括重型、危重型)。比较两组患者的临床特征和实验室检查结果。组间比较采用t检验、Mann-Whitney U检验、χ2检验或Fisher确切概率法。
148例COVID-19患者中,轻症组94例,重症组54例。轻症组患者年龄为(40.8±17.9)岁,低于重症组患者的(60.1±13.2)岁,差异有统计学意义(t=7.093,P<0.01);轻症组患者合并基础疾病(高血压、糖尿病、肥胖)的比例为17.0%(16/94),低于重症组的61.1%(33/54),差异有统计学意义(χ2=32.862,P<0.01)。重症组患者的C反应蛋白、降钙素原、D-二聚体和乳酸脱氢酶分别为46.34(30.65,68.13) mg/L、0.090(0.053,0.161) μg/L、(2 047.44±1 070.78) μg/L和(375.95±124.31) U/L,分别高于轻症组患者的4.11(1.13,12.70) mg/L、0.037(0.027,0.630) μg/L、(834.43±429.28) μg/L和(171.77±42.19) U/L;而重症组的淋巴细胞计数、嗜酸性粒细胞计数、氧合指数和白蛋白分别为0.77(0.53,1.02)×109/L、0、(202.87±96.35) mmHg(1 mmHg=0.133 kPa)和(32.70±4.64) g/L,分别低于轻症组患者的1.42(1.22,2.20)×109/L、0.04(0.10,0.12)×109/L、(468.74±70.82) mmHg和(39.78±4.49) g/L,差异均有统计学意义(Z=-7.999、Z=-5.584、t=-7.153、t=-10.259、Z=-7.712、Z=-6.738、t=-14.933和t=-8.254,均P<0.05)。血液2019新型冠状病毒(2019 novel coronavirus,2019-nCoV)核酸阳性者皆为重症患者。所有轻症组患者均治愈出院,重症组患者中31例治愈出院,16例病情好转,1例死亡。
与COVID-19轻症患者比较,重症患者年龄较大,合并基础疾病较多,C反应蛋白、降钙素原、D-二聚体、乳酸脱氢酶较高,而淋巴细胞计数、嗜酸性粒细胞计数、氧合指数、白蛋白较低;高龄、合并基础疾病、血液2019-nCoV核酸阳性可能是重症化的危险因素。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
新型冠状病毒肺炎(COVID-19)起病比较隐匿,病程一般为3~4周,重症患者常可出现急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)和多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS),有一定的病死率[1,2,3]。因此必须高度重视病情进展,加强重症病例的早期识别和救治,以提高治愈率,降低病死率。本研究回顾性分析2020年1月20日至2月29日广州医科大学附属第八人民医院收治的148例COVID-19患者的临床资料,比较轻症组和重症组患者的临床特征和实验室检查结果。
纳入2020年1月20日至2月29日广州医科大学附属第八人民医院收治的148例COVID-19患者,其中男78例,女70例,年龄范围为1.5~91.0岁,年龄为(48.2±18.5)岁。本研究通过广州医科大学附属第八人民医院医学伦理委员会审核批准(科202001134)。所有检测和治疗均获得患者亲属的知情同意。
COVID-19的诊断标准和临床分型参照《新型冠状病毒肺炎诊疗方案(试行第六版)》[4]。确诊病例具备以下病原学证据之一:①呼吸道标本或血液标本实时荧光反转录PCR检测2019新型冠状病毒(2019 novel coronavirus,2019-nCoV)核酸阳性;②呼吸道标本或血液标本病毒基因测序与2019-nCoV高度同源。临床分型为4型。轻型为临床症状轻微,影像学检查未见肺炎表现。普通型为有发热、呼吸道等症状,影像学检查可见肺炎表现。重型为符合下列任何一项:①呼吸窘迫,呼吸≥30次/min;②静息状态下指氧饱和度≤93%;③氧合指数(动脉血氧分压/吸氧浓度)≤300 mmHg(1 mmHg=0.133 kPa)。危重型为符合下列任何一项:①出现呼吸衰竭,且需要机械通气;②出现休克;③合并其他器官功能衰竭需ICU监护治疗。轻症组包括轻型和普通型,重症组包括重型和危重型。
一般资料主要包括性别、年龄、基础疾病、流行病史等。临床资料主要包括症状、体征、实验室检查和影像学检查结果等。
采用SPSS 20.0软件进行统计学分析。呈正态分布的计量资料以 ±s表示,组间比较采用t检验;呈偏态分布的计量资料以M (P25,P75)表示,组间比较采用Mann-Whitney U检验;计数资料以例数(百分数)表示,组间比较采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
±s表示,组间比较采用t检验;呈偏态分布的计量资料以M (P25,P75)表示,组间比较采用Mann-Whitney U检验;计数资料以例数(百分数)表示,组间比较采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
148例COVID-19患者中,轻型38例(25.7%),普通型56例(37.8%),重型40例(27.0%),危重型14例(9.5%)。148例COVID-19患者的咽拭子经广州市CDC和广州医科大学附属第八人民医院P2实验室进行2019-nCoV核酸检测,结果均为阳性;有13例患者血液2019-nCoV核酸检测为阳性,其中重型2例,危重型11例。患者病程均>7 d。发病前99例(66.9%)患者有湖北省居住或旅行史,29例(19.6%)患者明确为家庭聚集发病。52例(35.1%)患者有基础疾病,其中高血压29例(19.6%),糖尿病9例(6.1%),慢性阻塞性肺病5例(3.4%),慢性肾病5例(3.4%),冠状动脉粥样硬化性心脏病5例(3.4%),慢性肝病4例(2.7%),睡眠呼吸暂停综合征4例(2.7%),其他基础疾病包括肺结核、脑梗死后遗症、高血压性心脏病、膀胱癌、结肠癌等,6例(4.1%)患者合并2种及以上基础疾病。肥胖患者11例(7.4%)。
轻症组94例,重症组54例。两组患者的临床特征和实验室检查结果比较见表1。与轻症组比较,重症组患者年龄较大,合并基础疾病较多,差异均有统计学意义(均P<0.05)。两组患者性别,流行病学史,发热,咳嗽,鼻塞、流涕,肌肉、关节酸痛,头痛,乏力,消化道症状等比较差异均无统计学意义(均P>0.05)。重症组患者CRP、降钙素原、D-二聚体、乳酸脱氢酶较高,淋巴细胞计数、嗜酸性粒细胞计数、氧合指数、白蛋白较低,与轻症组比较差异均有统计学意义(均P<0.05),而两组白细胞计数、中性粒细胞计数、血红蛋白、血小板计数、凝血酶原时间、APTT、血乳酸、血肌酐、肌酸激酶比较差异均无统计学意义(均P>0.05)。两组间ALT和AST虽差异有统计学意义,但中位数值均低于正常参考值上限,根据正常参考值转换为分类变量后再比较,两组间差异无统计学意义(均P>0.05)。住院期间有6例危重型患者的痰液或肺泡灌洗液培养发现鲍曼不动杆菌、多噬伯克霍尔德菌、布氏柠檬酸杆菌、弗劳地柠檬酸杆菌、肺炎克雷伯菌和白念珠菌等病原体。
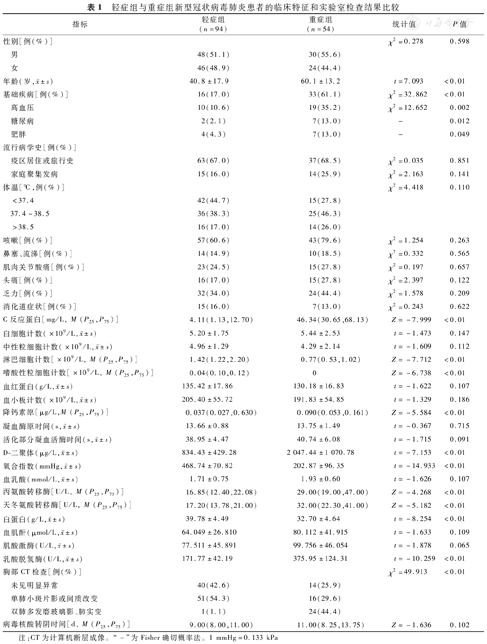
轻症组与重症组新型冠状病毒肺炎患者的临床特征和实验室检查结果比较
轻症组与重症组新型冠状病毒肺炎患者的临床特征和实验室检查结果比较
| 指标 | 轻症组(n=94) | 重症组(n=54) | 统计值 | P值 | |
|---|---|---|---|---|---|
| 性别[例(%)] | χ2=0.278 | 0.598 | |||
| 男 | 48(51.1) | 30(55.6) | |||
| 女 | 46(48.9) | 24(44.4) | |||
年龄(岁, ±s) ±s) | 40.8±17.9 | 60.1±13.2 | t=7.093 | <0.01 | |
| 基础疾病[例(%)] | 16(17.0) | 33(61.1) | χ2=32.862 | <0.01 | |
| 高血压 | 10(10.6) | 19(35.2) | χ2=12.652 | 0.002 | |
| 糖尿病 | 2(2.1) | 7(13.0) | - | 0.012 | |
| 肥胖 | 4(4.3) | 7(13.0) | - | 0.049 | |
| 流行病学史[例(%)] | |||||
| 疫区居住或旅行史 | 63(67.0) | 37(68.5) | χ2=0.035 | 0.851 | |
| 家庭聚集发病 | 15(16.0) | 14(25.9) | χ2=2.163 | 0.141 | |
| 体温[℃,例(%)] | χ2=4.418 | 0.110 | |||
| <37.4 | 42(44.7) | 15(27.8) | |||
| 37.4~38.5 | 36(38.3) | 25(46.3) | |||
| >38.5 | 16(17.0) | 14(26.0) | |||
| 咳嗽[例(%)] | 57(60.6) | 43(79.6) | χ2=1.254 | 0.263 | |
| 鼻塞、流涕[例(%)] | 14(14.9) | 10(18.5) | χ2=0.332 | 0.565 | |
| 肌肉关节酸痛[例(%)] | 23(24.5) | 15(27.8) | χ2=0.197 | 0.657 | |
| 头痛[例(%)] | 16(17.0) | 15(27.8) | χ2=2.397 | 0.122 | |
| 乏力[例(%)] | 32(34.0) | 24(44.4) | χ2=1.578 | 0.209 | |
| 消化道症状[例(%)] | 15(16.0) | 7(13.0) | χ2=0.243 | 0.622 | |
| C反应蛋白[mg/L, M (P25,P75)] | 4.11(1.13,12.70) | 46.34(30.65,68.13) | Z=-7.999 | <0.01 | |
白细胞计数(×109/L, ±s) ±s) | 5.20±1.75 | 5.44±2.53 | t=-1.473 | 0.147 | |
中性粒细胞计数(×109/L, ±s) ±s) | 4.96±1.29 | 4.29±2.14 | t=-1.609 | 0.112 | |
| 淋巴细胞计数[×109/L, M (P25,P75)] | 1.42(1.22,2.20) | 0.77(0.53,1.02) | Z=-7.712 | <0.01 | |
| 嗜酸性粒细胞计数[×109/L, M (P25,P75)] | 0.04(0.10,0.12) | 0 | Z=-6.738 | <0.01 | |
血红蛋白(g/L, ±s) ±s) | 135.42±17.86 | 130.18±16.83 | t=-1.622 | 0.107 | |
血小板计数(×109/L, ±s) ±s) | 205.40±55.72 | 191.83±54.85 | t=-1.329 | 0.186 | |
| 降钙素原[μg/L,M (P25,P75)] | 0.037(0.027,0.630) | 0.090(0.053,0.161) | Z=-5.584 | <0.01 | |
凝血酶原时间(s, ±s) ±s) | 13.66±0.88 | 13.75±1.49 | t=-0.367 | 0.715 | |
活化部分凝血活酶时间(s, ±s) ±s) | 38.95±4.47 | 40.74±6.08 | t=-1.715 | 0.091 | |
D-二聚体(μg/L, ±s) ±s) | 834.43±429.28 | 2 047.44±1 070.78 | t=-7.153 | <0.01 | |
氧合指数(mmHg, ±s) ±s) | 468.74±70.82 | 202.87±96.35 | t=-14.933 | <0.01 | |
血乳酸(mmol/L, ±s) ±s) | 1.71±0.75 | 1.93±0.60 | t=-1.626 | 0.107 | |
| 丙氨酸转移酶[U/L, M (P25,P75)] | 16.85(12.40,22.08) | 29.00(19.00,47.00) | Z=-4.268 | <0.01 | |
| 天冬氨酸转移酶[U/L, M (P25,P75)] | 17.20(13.78,21.00) | 32.00(22.30,41.00) | Z=-5.182 | <0.01 | |
白蛋白(g/L, ±s) ±s) | 39.78±4.49 | 32.70±4.64 | t=-8.254 | <0.01 | |
血肌酐(μmol/L, ±s) ±s) | 64.049±26.810 | 80.112±41.915 | t=-1.633 | 0.109 | |
肌酸激酶(U/L, ±s) ±s) | 77.511±45.891 | 99.756±46.054 | t=-1.878 | 0.065 | |
乳酸脱氢酶(U/L, ±s) ±s) | 171.77±42.19 | 375.95±124.31 | t=-10.259 | <0.01 | |
| 胸部CT检查[例(%)] | χ2=49.913 | <0.01 | |||
| 未见明显异常 | 40(42.6) | 14(25.9) | |||
| 单肺小斑片影或间质改变 | 51(54.3) | 16(29.6) | |||
| 双肺多发磨玻璃影、肺实变 | 1(1.1) | 24(44.4) | |||
| 病毒核酸转阴时间[d, M (P25,P75)] | 9.00(8.00,11.00) | 11.00(8.25,13.75) | Z=-1.636 | 0.102 | |
注:CT为计算机断层成像。"-"为Fisher确切概率法。1 mmHg=0.133 kPa
所有患者入院后均接受抗病毒治疗,抗病毒药物包括阿比多尔(200 mg,3次/d)、洛匹那韦/利托那韦[(每片含洛匹那韦200 mg,利托那韦50 mg)2片,2次/d]和α干扰素(500万单位雾化吸入,2次/d),部分患者两种药物联用。抗病毒治疗后,呼吸道标本2019-nCoV核酸转阴时间为9.00(8.00,12.00) d。重症组31例患者接受糖皮质激素治疗,使用时间为3.0(2.5,5.0) d,其中24例病情好转。63例患者接受不同级别氧疗,其中49例接受高流量氧疗,14例因病情进展需有创通气支持,8例患者行体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)支持治疗,5例重度ARDS患者予俯卧位通气治疗,短时间(6 h至2 d)内虽能改善氧合,但最终仍需要ECMO支持治疗,9例患者使用连续性血液净化治疗。所有轻症组患者治愈出院,重症组31例患者治愈出院,16例病情好转,1例死亡,6例病情无变化。出院患者住院时间为(12.2±4.7) d。
目前,人类对2019-nCoV普遍缺乏免疫力,病毒感染人体后,易发生全身炎症反应,其导致的病理变化与临床表现密切相关,病情轻重与炎症反应的程度、肺部病灶的范围等相对应,因此临床早期可能无明显特异性症状[5]。本研究发现,COVID-19患者的临床早期症状与严重急性呼吸综合征(severe acute respiratory syndrome,SARS)、禽流感等传染病类似[6,7,8],有发热、咳嗽、鼻塞、流涕、肌肉关节酸痛、头痛、乏力、消化道症状等,重症组中老年患者和有基础疾病者所占比例高于轻症组。文献报道,中东呼吸综合征(Middle East respiratory syndrome,MERS)患者白蛋白和淋巴细胞计数减少、CRP升高[9],SARS重症患者乳酸脱氢酶升高[10]。本研究实验室检查结果显示,重症组患者CRP、降钙素原、D-二聚体、乳酸脱氢酶较高,淋巴细胞计数、嗜酸性粒细胞计数、氧合指数、白蛋白较低,与轻症组比较差异均有统计学意义,而两组白细胞计数、中性粒细胞计数、血红蛋白、血小板计数、凝血酶原时间、APTT、血乳酸、血肌酐、肌酸激酶等比较差异均无统计学意义。COVID-19患者的免疫功能下降,且病情越重,免疫功能受损越严重,容易继发感染[11]。本研究中有6例危重型患者的痰液或肺泡灌洗液中培养出细菌和真菌。因此临床医师在诊治过程中需全面综合考虑,在制订早期治疗方案时应注意抗病毒药物和抗菌药物的合理应用。本研究中所有患者入院后均接受了抗病毒治疗,轻症组与重症组患者呼吸道标本病毒核酸转阴时间差异无统计学意义。Chen等[12]发现,病毒血症与疾病的严重程度呈正相关。本研究有13例重症患者的血液2019-nCoV核酸检测阳性,轻症患者血液标本中均未检测到2019-nCoV核酸。既往研究发现,MERS和H1N1流行性感冒都可能存在短期、少量的病毒血症,且与预后可能存在相关性[13,14]。目前,关于2019-nCoV病毒血症的研究鲜见,患者在病程的哪个时期会发生病毒血症,是否会通过血液传播等问题尚待进一步研究。
从现有临床资料看,COVID-19早期症状并不典型,一些轻型患者在发病7~10 d突然进展为重型,部分患者出现ARDS和MODS,增加了病死率[1,2,3]。因此,及时识别重症患者的早期征象,提高对病程进展的预见性,尽早采取干预措施,是降低病死率的关键。Huang等[15]采用logistic回归分析方法对COVID-19重症因素进行研究,提示高龄、合并基础疾病、入院时即出现胸闷气促、CRP升高、乳酸脱氢酶升高是COVID-19重症化的重要危险因素。在治疗过程中,对肺部病变明显、症状较重、呼吸频率较快的患者,普通鼻导管吸氧流量、氧浓度和通气压力等难以满足机体实际需要,可能导致"沉默性"低氧血症,机体氧债持续加重,组织持续缺氧加重MODS,而早期使用低氧浓度、经鼻高流量氧疗,可能有助于度过危险期。
综上所述,高龄、合并基础疾病、血液2019-nCoV核酸阳性可能是COVID-19重症化的危险因素,重症病例早期主要表现为呼吸衰竭和免疫功能损伤,容易继发其他病原体感染,需要ICU的综合救治,不同级别的呼吸支持治疗也是主要的救治措施。
所有作者均声明不存在利益冲突



























