
急性肺栓塞发病隐匿且可危及生命,所以早期诊断、及时治疗以及规范管理至关重要。2019年8月31日,欧洲心脏病学会与欧洲呼吸病学会联合颁布了“2019年急性肺栓塞诊断与治疗指南”,新版指南着眼于肺栓塞的临床诊治与管理,对其诊断、治疗、长期随访等相关策略进行了相应更新,包括:D-二聚体诊断界值的确定,影像学诊断方法中辐射剂量及优缺点,血流动力学不稳定的明确定义,肺栓塞危险分层,高危肺栓塞急性期治疗、延展期抗凝治疗的潜在适应证、复发风险因素分级,恶性肿瘤及妊娠合并肺栓塞的诊疗方案,长期随访的管理策略。本文就新版指南的重要更新部分进行解读,以期为临床医生提供相关的理念和知识。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
急性肺栓塞(PE)的诊治和管理策略近年来备受关注。由于发病隐匿,急性PE的诊断经常被忽略,其严重程度也常被低估,许多患者在还没有得到及时的诊断和恰当的治疗前就已经死亡。即使存活,由于缺乏规范的长期随访,部分患者可能会复发或发展为肺动脉高压(PH)。因此,早期的识别与诊断、及时的抢救与治疗、规范的随访与管理至关重要。2019年8月31日,欧洲心脏病学会与欧洲呼吸病学会联合发布了最新版“2019年急性肺栓塞诊断与治疗指南”(以下简称新版指南)[1]。与2014年版的指南相比,新版指南更新要点主要包括以下内容:D-二聚体界值的确定、影像学诊断方法的辐射剂量及优缺点,血流动力学不稳定的明确定义,急性PE危险分层,高危PE急性期治疗、延展期抗凝治疗的潜在适应证、复发风险因素分级、恶性肿瘤及妊娠合并PE诊疗方案,长期随访的管理策略等。
随着人们对PE认识的提高以及非创伤性检查手段(如CT和核素等)的日益普及,临床医生对疑诊PE患者进行确诊检查的频率较过去有了显著升高,但对诊断策略的具体实施过程仍有争议。新版指南中对PE诊断方面的主要更新包括以下几个方面。
1.D-二聚体检测的评价与应用:D-二聚体的阴性预测价值很高,D-二聚体正常时,PE或深静脉血栓形成(DVT)发生的可能性很小。D-二聚体升高可见于肿瘤、严重感染或炎症、妊娠或住院患者,所以其阳性预测价值较低[2, 3, 4]。另外,D-二聚体检测方法众多,不同方法的敏感度及特异度不同,所以临床医生应知晓自己医院D-二聚体检测方法的诊断效能[1, 5]。
D-二聚体诊断界值的确定在新版指南中得到了更新。D-二聚体水平受很多因素影响,如年龄。随年龄的增长,D-二聚体水平上升。但在实际临床工作中,D-二聚体的诊断界值往往是固定的。如果对老年人群使用与年轻人群一样的界值,可能会造成不必要的检查,在40岁以下的患者中,D-二聚体检测正常可排除60%左右的PE,但在80岁以上的患者中,仅能排除5%左右的PE[6]。D-二聚体在不同年龄层的差异导致更多的高龄患者被划入高风险人群。Douma等[7]在回顾性验证分析中提出年龄校正方案:年龄>50岁的患者,D-二聚体界值设定为年龄×10 μg/L。75岁及以上的患者能从基于年龄校正的D-二聚体界值中获益,特别是临床评估为低中度可能的患者,无需进一步影像学检查,就可以排除PE的患者比例增加了5倍。后续的前瞻性研究纳入了3 346例患者,在PE临床评估为低中度可能或不太可能的患者中(使用修订版Geneva评分或Wells评分),通过年龄校正的D-二聚体界值排除PE的患者占比从6.4%上升到30%[8],这项研究验证了该方案的诊断效能。
对于年轻患者,尤其是处于育龄期的女性,临床医生也在探索适合这些人群的快速而可靠的诊断策略,以减少不必要的辐射暴露。有研究提出了适用于所有人群的“YEARS”临床风险决策原则。该原则综合了三项临床危险因素(DVT的临床症状、咯血以及PE是否为最可能的诊断)与D-二聚体水平,诊断流程如下:(1)患者无临床危险因素且D-二聚体<1 000 μg/L,可排除PE;(2)患者有1个或更多临床危险因素,且D-二聚体<500 μg/L时,也可排除PE;(3)除此以外,其他患者均需进行CT肺动脉造影(CTPA)。一项前瞻性研究评估了“YEARS”临床风险决策原则的诊断效能,结果表明在所有人群中,“YEARS”原则可将不必要的CTPA检查数目降低14%[9]。目前在临床中,依据D-二聚体年龄矫正方案还是“YEARS”原则来确定D-二聚体的诊断阈值仍有争议,一项回顾性研究发现后者能更有效地排除未发生静脉血栓栓塞症(VTE)的患者[10]。
在临床实践工作中,临床医生仍应谨慎地综合初筛的D-二聚体结果、患者的临床表现来判断患者是否需要进一步检查。如果初步评估为PE低度可能的患者,在充分识别的前提下,尽量降低因过度检查而带来的高额理疗费用和检查相关风险。
关于D-二聚体的临床应用,新版指南有以下推荐意见:(1)对于门诊或急诊评估临床可能性较低或中等可能的患者,建议采用高敏度检测方法测定血浆D-二聚体,以减少不必要的放射影像检查;(2)对于D-二聚体界值,应考虑根据年龄进行校正[>50岁患者为年龄(岁)×10 μg/L],以排除临床评估低中度可能或那些不太可能的PE患者;(3)将临床可能性评估调整的D-二聚体临界值(“YEARS”原则),替代固定的及年龄调整的D-二聚体界值以排除PE;(4)对于临床评估高度可能的患者,不推荐进行D-二聚体检测,因为即使应用高敏感度检测方法结果正常,仍不能安全地排除PE。
综上,新版指南更加强调了D-二聚体界值的标准不能一概而论,而应个体化选择,临床医生需要根据“YEARS”原则或年龄选择不同的D-二聚体标准,以指导后续诊疗。另外,新版指南提出对于临床高度怀疑PE的患者,不必检测D-二聚体水平,因为即使应用高敏感度检测方法检测出D-二聚体结果正常,仍然不能可靠地排除PE,针对这些PE高度可能的患者可直接行CTPA等确诊检查[1]。然而,该指南的证据主要来源于欧美人群,是否可以直接应用于我国临床实践尚待论证。对于我国的急诊或门诊患者,可能很难快速精准地判断患者的危险因素,而D-二聚体检测相对简便快捷,临床医生仍应综合具体的临床情况谨慎决策。
2.影像学检查的选择与辐射暴露:诊断PE的影像学检查有很多种,包括CTPA、核素通气/灌注肺显像(V/Q显像)、V/Q单光子发射计算机断层扫描(V/Q SPECT)、肺动脉造影等。新版指南针对这几种重要影像学检查方法的选择、各自的优缺点以及相关辐射问题进行了更新(表1)。每种影像学检查方法有各自的适应证,在临床实践中,考虑到不同患者存在血栓的位置、大小、数目的差异或者血栓不能完全解释患者症状等问题,临床医生可适当地选择两种/多种检查方法的联合。

急性肺栓塞诊断的影像学检查方法比较
急性肺栓塞诊断的影像学检查方法比较
| 检查方法 | 优点 | 缺点 | 辐射问题 |
|---|---|---|---|
| CTPA | 1.在大多数医院均可随时进行检查 2.准确性较好 3.在前瞻性研究中得到强有效性验证 4.结果不确定率较低(3%~5%) 5.若排除PE,可提出替代诊断 6.检查时间短 | 1.辐射暴露 2.碘造影剂暴露 (1)碘过敏和甲亢患者慎用 (2)妊娠及哺乳期妇女慎用 (3)严重肾功能衰竭禁用 3.因容易实施造成过度应用 4.对亚段PE的诊断意义尚不明确 | 1.有效辐射剂量3~10 mSva 2.年轻女性乳腺组织辐射暴露显著 |
| V/Q显像 | 1.几乎没有禁忌证 2. 相对便宜 3. 在前瞻性研究中得到强有效性验证 | 1.并非所有医院均可进行 2.判读报告者间存在差异性 3.报告结果存在可能性 4.50%患者存在不确定的结果 5.若排除肺栓塞,无法提供替代诊断 | 1.比CTPA辐射剂量低,有效辐射剂量~2 mSva |
| V/Q SPECT | 1. 几乎没有禁忌证 2.“非诊断性异常”诊断率最低(<3%) 3. 根据所获数据诊断准确性高 4. 二元解释(对PE诊断“是”与“否”) | 1.技术的不确定性 2.诊断标准的不确定性 3.若排除PE,无法提供替代诊断 4.未在前瞻性结果研究中进行有效性验证 | 1.比CTPA辐射剂量低,有效辐射剂量~2 mSva |
| 肺动脉造影 | 1. 确诊PE的“金标准” | 1.侵入性操作 2.并非所有医院均可进行 | 1.辐射剂量最大,有效辐射剂量10~20 mSva |
注:CTPA:CT肺动脉造影; V/Q:通气/灌注(肺显像);SPECT:单光子发射计算机断层扫描;a单次胸部X线检查的全身有效辐射剂量为0.1 mSv[11]
1.危险分层:对于确诊急性PE的患者,临床医生应综合临床评估、实验室检验及影像学检查对其进行危险分层,采取个体化的治疗决策。在各类临床评分中,肺栓塞严重指数(PESI)和简化PESI评分(sPESI)是使用最广泛的2种,二者的主要优势在于能可靠地识别出30 d内死亡风险较低的患者[12, 13, 14]。
关于PE的危险分层详见表2。新版指南明确了血流动力学不稳定的定义(见表3)[1]。血流动力学稳定的患者中,如其PESI为Ⅲ~Ⅴ级或sPESI≥Ⅰ级,则归为中危组,否则归为低危组(即PESI评分Ⅰ-Ⅱ级或sPESI评分0分)。鉴于后续疾病进展、治疗策略以及预后结果有所不同,指南建议进一步细分中危组患者。根据是否有右心室功能障碍和心肌损伤标志物升高(尤其是肌钙蛋白升高)将中危组患者分为中高危组和中低危组,对于前者,应进行密切监测,以便及早发现血流动力学失代偿,从而及时抢救。而中低危组患者虽然只存在右心室功能不全或心肌钙蛋白水平升高,但与低危患者相比仍有较高的早期死亡风险[15],所以仍应住院密切观察。通过将患者分为高危、中高危、中低危以及低危这四类人群,临床医生可评估PE患者的严重程度从而指导进一步的治疗决策。

肺栓塞(PE)严重程度和与早期(住院或30 d)死亡相关的危险分层
肺栓塞(PE)严重程度和与早期(住院或30 d)死亡相关的危险分层
| 危险分层 | 血流动力学不稳定 | PE严重程度和(或)合并症的临床参数:PESI Ⅲ~Ⅴ级或sPESI≥Ⅰ级 | TTE或CTPA显示右心室功能不全 | 心肌钙蛋白水平升高 |
|---|---|---|---|---|
| 高危 | + | + | + | + |
| 中高危 | - | + | + | + |
| 中低危 | - | + | +/-a | -/+a |
| 低危 | - | - | - | -/未查 |
注:PESI:肺栓塞严重指数;sPESI:简化肺栓塞严重指数;TTE:经胸超声心动图;CTPA:CT肺动脉造影;aTTE或CTPA上显示右心室功能不全与心肌钙蛋白水平升高两者之一阳性或无阳性

血流动力学不稳定相关定义
血流动力学不稳定相关定义
| 血流动力学不稳定a | 定义 |
|---|---|
| 心脏骤停 | 需要心肺复苏 |
| 梗阻性休克 | 收缩压<90 mmHg或在血容量足够的情况下,仍需升压药物使血压≥90 mmHg且外周器官低灌注状态(表现为精神状态改变;皮肤寒冷,潮湿;少尿/无尿;血乳酸水平升高) |
| 持续低血压 | 收缩压<90 mmHg或收缩压下降≥40 mmHg,持续时间超过15 min,且除外由新发心律失常、低血容量或脓毒症引起的血压下降 |
注:a具有3种情况中任意1种即可诊断为血流动力学不稳定;1 mmHg=0.133 kPa
2.治疗决策:急性期治疗中,新版指南全面修订了针对高危PE患者血流动力学支持和呼吸支持部分,提出了针对高危PE患者的精细化管理策略。对于高危患者,首选静脉溶栓治疗,如有溶栓禁忌/无效的患者,推荐行外科肺动脉血栓切除术或经皮导管介入治疗,必要时可联合血管升压药。对于顽固性循环衰竭/心脏骤停的高危患者,首次推荐体外膜氧合(ECMO)联合下的外科手术或介入治疗。
对于中危组及低危组患者,不建议常规行溶栓治疗,只有抗凝治疗效果不佳,出现血流动力学不稳定的患者,才考虑进行升级治疗。在初始抗凝治疗中,新版指南指出如果患者无口服新型抗凝药物(NOACs)的禁忌证,应首选NOACs,维生素K拮抗剂是替代治疗,因为二者疗效类似但NOACs的大出血风险更低。但针对一些特殊情况如抗磷脂抗体综合征的患者,仍推荐使用维生素K拮抗剂进行终生治疗。
新版指南针对早期出院和门诊治疗也提出相关标准:如果门诊可以提供合适的照护和抗凝治疗,经过谨慎选择(Hestia排除标准与PESI/sPESI联合判断)的低危PE患者可以考虑早期出院。Hestia排除标准列出了一系列能在床旁获得或回答的临床参数及问题,综合了PE严重性、合并症以及家庭治疗的可行性等各个方面的评价指标[16](表4)。如果对≥1个问题的答案为“是”,那么患者不能早期出院。将Hestia标准与PESI或sPESI联合后似乎能更加有效地识别出低PE相关风险和无严重合并症的患者[16, 17]。

Hestia排除问卷
Hestia排除问卷
| 问题 |
|---|
| 是否存在血液动力学不稳定?a |
| 是否需要溶栓或外科血栓切除术? |
| 是否为活动性出血或高出血风险?b |
| 是否需要吸氧24 h以上来维持血氧饱和度>90%? |
| 是否在抗凝治疗期间发生PE? |
| 是否因为剧痛需要静脉注射止痛药超过24 h? |
| 是否因医疗或社会原因在医院接受超过24 h的治疗(如感染、恶性肿瘤或无家庭支持)? |
| 肌酐清除率是否低于30 ml/min?c |
| 是否存在严重的肝功能损害?d |
| 是否怀孕? |
| 是否存在肝素诱导的血小板减少病史? |
注:a包括以下标准,但可由临床医生根据临床情况决策:收缩压<100 mmHg(1 mmHg=0.133 kPa)伴心率>100次/min;病情需要进入重症监护病房;b14 d内出现消化道出血、近期脑卒中(<4周前)、近期手术史(<2周前)、出血性疾病或血小板减少(血小板<75×109/L)、未经控制的高血压(收缩压>180 mmHg或舒张压>110 mmHg);c根据Cockroft-Gault公式计算肌酐清除率;d由医生根据临床情况决策
对于PE患者,推荐初始抗凝治疗时间至少3个月。3个月后是否继续进行延展期抗凝治疗,需要根据患者的具体情况。对于没有高危因素(如卧床、手术、感染、久坐等)的患者,他们有可能存在其它潜在高凝因素,如恶性肿瘤、抗磷脂抗体综合征等疾病,停药后容易复发,影响预后。因此,对这部分不明原因的PE患者,临床医生需要延长抗凝治疗时间,同时进一步寻找可疑病因。
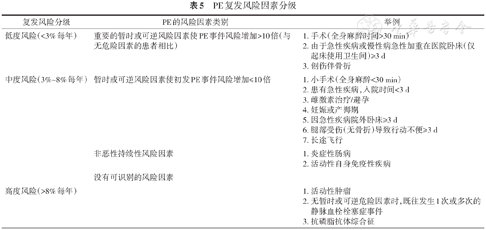
考虑到对治疗决策影响不大,新版指南取消了“诱发性”和“非诱发性”PE等术语。另外,指南更新了针对PE复发风险因素的分级,便于临床医生制定慢性期治疗方案(表5)。
PE复发风险因素分级
PE复发风险因素分级
| 复发风险分级 | PE的风险因素类别 | 举例 |
|---|---|---|
| 低度风险(<3%每年) | 重要的暂时或可逆风险因素使PE事件风险增加>10倍(与无危险因素的患者相比) | 1. 手术(全身麻醉时间>30 min) 2. 由于急性疾病或慢性病急性加重在医院卧床(仅起床使用卫生间)≥3 d 3. 创伤伴骨折 |
| 中度风险(3%~8%每年) | 暂时或可逆风险因素使初发PE事件风险增加≤10倍 | 1. 小手术(全身麻醉<30 min) 2. 患有急性疾病,入院时间<3 d 3. 雌激素治疗/避孕 4. 妊娠或产褥期 5. 因急性疾病院外卧床≥3 d 6. 腿部受伤(无骨折)导致行动不便≥3 d 7. 长途飞行 |
| 非恶性持续性风险因素 | 1. 炎症性肠病 2. 活动性自身免疫性疾病 | |
| 没有可识别的风险因素 | ||
| 高度风险(>8%每年) | 1. 活动性肿瘤 2. 无暂时或可逆危险因素时,既往发生1次或多次的静脉血栓栓塞症事件 3. 抗磷脂抗体综合征 |
1.恶性肿瘤合并PE:对于恶性肿瘤合并PE的患者,除胃肠道肿瘤之外,依度沙班或利伐沙班可以替代低分子量肝素。考虑到胃肠道肿瘤患者服用依度沙班或利伐沙班可能会增加出血风险,故建议低分子量肝素抗凝。对于恶性肿瘤患者,不能轻易停用抗凝治疗,应尽量考虑终生抗凝或持续到肿瘤治愈。恶性肿瘤患者若偶然发现PE,即使患者无症状,也应与症状性PE采取相同的管理策略。
2.妊娠合并PE:针对妊娠合并PE的诊治需要更加细致的疑诊及管理流程,在尽量减少母体和胎儿辐射暴露的同时诊断疾病(具体流程见图1)。另外,新版指南基于新的研究总结出影像学检查对于母体乳房组织和胎儿的辐射剂量估测,这对于临床医生选择何种诊断方式有重要的参考价值(表6)。
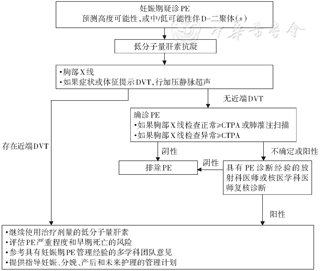

注:DVT:深静脉血栓形成;CTPA:CT肺动脉造影
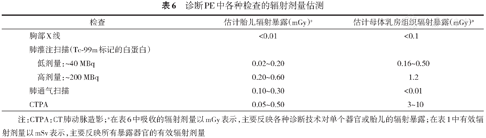
诊断PE中各种检查的辐射剂量估测
诊断PE中各种检查的辐射剂量估测
| 检查 | 估计胎儿辐射暴露(mGy)a | 估计母体乳房组织辐射暴露(mGy)a |
|---|---|---|
| 胸部X线 | <0.01 | <0.1 |
| 肺灌注扫描(Tc-99m标记的白蛋白) | ||
低剂量:~40 MBq | 0.02~0.20 | 0.16~0.50 |
高剂量:~200 MBq | 0.20~0.60 | 1.2 |
| 肺通气扫描 | 0.10~0.30 | <0.01 |
| CTPA | 0.05~0.50 | 3~10 |
注:CTPA:CT肺动脉造影;a在表6中吸收的辐射剂量以mGy表示,主要反映各种诊断技术对单个器官或胎儿的辐射暴露;在表1中有效辐射剂量以mSv表示,主要反映所有暴露器官的有效辐射剂量
近年来,随着对PE研究的深入,临床医生已发现众多PE相关的长期并发症如慢性血栓栓塞性肺动脉高压(CTEPH)、肺栓塞后综合征等,这些并发症严重影响了患者的生活质量。新版指南对于患者的随访与管理十分关注(详见图2),强调在急性PE发生后3~6个月内对患者进行常规的临床评估和随访。通过随访,临床医生不仅可以评估患者呼吸困难或呼吸功能受限的持续时间及严重程度,还能及时发现患者有无疾病复发或出血征象,从而为每位患者提供个体化抗凝方案[18]。如果患者未出现呼吸困难及功能受损的症状,但存在明确的CTEPH风险因素/诱发因素,则需继续随访,并告知患者出现症状时及时就诊。
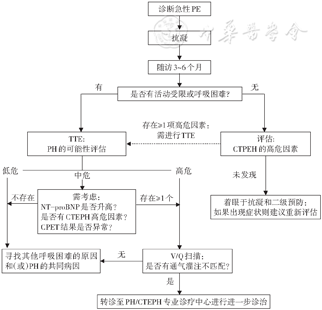

注:TTE:经胸超声心动图;PH:肺动脉高压;CTEPH:慢性血栓栓塞性肺动脉高压;NT‑proBNP:N末端B型利钠肽原;CPET:心肺功能运动试验;V/Q:通气/灌注(肺显像)
如果患者存在持续性呼吸困难,临床医生应行超声心动图检查以评估是否出现长期并发症如PH。如果超声心动图提示PH高度可能,或者PH中度可能且合并NT-proBNP升高,存在CTEPH的高危因素时,临床医生应考虑进行V/Q显像检查。当V/Q显像提示通气/灌注不匹配时,建议患者转诊到PH/CTEPH专业诊疗中心进一步诊治。如果V/Q显像结果阴性但对患者的症状无法找到合理解释,临床医生可以考虑进行心肺运动试验(CPET)来进一步衡量患者呼吸和循环系统储备能力。CPET结果提示最大有氧运动能力降低时,建议进一步随访[19, 20],另外,CPET对于识别可疑CTEPH患者以及合并左心疾病和(或)其他呼吸系统疾病患者也有参考价值。
在随访过程中,指南推荐以护士为主导的随访模式,这一模式在急性冠脉综合征及慢性疾病管理中已经初见成效[21, 22, 23]。最近一项研究发现,42例接受以护士为主导的门诊随访策略的PH/CTEPH患者可以更好地控制病情并且提高生活质量[24]。在患者随访期间,护士会询问患者有无PE相关的症状、体征,并评估患者药物治疗的依从性。通过与患者的合作,医护人员可及时识别相关危险因素并给予处理(如戒烟、节食、加强体育活动和锻炼等)。此外,护士可帮助患者提升自我管理能力,包括分级加压弹力袜的使用方法,如何在安全范围内增加活动量等。
除了以上建议的随访策略外,新版指南还推荐建立治疗后整合照护模式(包括临床专家、护理人员和社区医生),以确保从医院到社区的最佳过渡[23, 24, 25]。这一模式需要多学科医生的共同合作以及社区与医院专科之间的双向转诊制度。这一模式能确保临床专家与社区医生之间顺利交接,临床专家给予患者及时合理的治疗方案,社区医生为患者提供持续便捷的症状监测及患者教育。
新版指南在PE诊断和治疗方面有所更新,但更关注于PE的随访管理以及特殊人群合并PE的诊治,相信随着新的研究数据的支持,指南能更好地指导临床医生,从而对急性PE患者进行更为科学有效的诊治管理。另一方面,在PE领域仍有许多悬而未决的问题,如急性PE患者存在持续性呼吸困难的症状时,相应的随访策略及评估标准是否需要进一步的前瞻性研究加以明确。同时,鉴于国人及国情的特殊性,期待临床医生在日常诊疗中发现相关问题进行研究,以便更新和完善我国的PE指南,更好地应用于中国的临床实践。
所有作者均声明不存在利益冲突



























