
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
三尖瓣病变是最为常见的心脏瓣膜病之一,其中绝大多数是三尖瓣反流(tricuspid regurgitation,TR ),即三尖瓣在右心室收缩期关闭不全而导致血液由右心室向右心房反流。TR发病率较高,整体发病率高于主动脉瓣病变。Nath等[1]回顾分析了5 223例因考虑心脏疾病而接受超声检查的患者,发现高达88.8%的患者存在轻度以上TR,Stuge等[2]报道美国人口中约有160万中度以上的TR患者。Chorin等[3]报道严重TR患者1年死亡率高达36%~45.6%。TR因常继发于左心瓣膜病变以及较长的无症状期而长期被临床忽视,然而越来越多的研究表明中至重度TR是影响患者预后的高危因素,相较于非TR患者,TR患者住院时间延长,再住院率及死亡率明显升高[4,5]。
TR传统的外科治疗方式是体外循环下三尖瓣成形术(tricuspid valvuloplasty,TVP)或三尖瓣置换术(tricuspid valve replacement,TVR)。然而,无论是原发TR或左心术后继发TR患者在接受外科手术时均面临着极高的手术风险,同时有大量重度TR患者因存在手术禁忌证而无法手术[6,7,8],美国每年心脏外科手术例数高达50万例,然而,每年单纯三尖瓣手术不到1 000例。Axtell等[9]回顾性分析了3 276例孤立性TR患者,其中171例接受了外科手术治疗,对这些接受外科手术的患者匹配分析后发现外科治疗并不能改善患者的远期预后,笔者认为,造成这种出乎意料的结果的主要原因是接受外科三尖瓣手术的患者时机太晚,导致右心衰竭加剧以致术后预后不佳。近年来,伴随技术的进步多种介入瓣膜治疗技术开始应用于TR的治疗,并在前期临床试验中取得了可靠的治疗效果,这为中重度TR的治疗提供了全新的策略。
笔者使用tricuspid regurgitation,transcatheter tricuspid valve replacement,transcatheter tricuspid valve repair作为关键词在PubMed数据库对三尖瓣介入治疗相关文献进行检索,就近1年来三尖瓣介入治疗的进展进行综述。
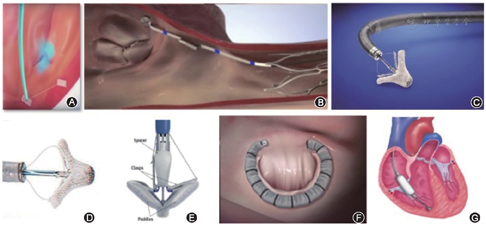
Trialign (Trialign公司,美国)是一种介入时通过瓣环折叠及瓣叶二瓣化以期消除TR的技术(图1A)。其在X线及经食管超声心动图(transesophageal echocardiography,TEE)引导下通过颈静脉途径植入导管,分别于前-后瓣交界以及隔-后瓣交界处的瓣环由右心室向右心房穿孔并植入垫片。最后通过专用的垫片闭锁装置将两个垫片闭合在一起,起到三尖瓣二瓣化及缩小瓣口面积从而消除TR的作用。Schofer等[10]于2017年首次报道了使用Trialign技术治疗TR的病例。使用Trialign技术的SCOUT临床试验共纳入15例接受治疗的TR患者。结果显示Trialign在30 d的成功率为80%,患者术后的瓣环面积及反流口面积均明显下降并伴随心功能好转[11]。TriValve临床试验显示共有18例严重高危TR患者接受Trialign治疗,占所有三尖瓣植入装置的6%,植入成功率为69.2%,无30 d死亡[12]。

Trialign的不足之处是植入成功率偏低,其垫片闭锁装置不牢固,存在崩开可能,SCOUT报道的30 d失败病例均为此原因;同时其通过介入装置由右心室向右心房穿瓣环打孔的过程中存在损伤右冠状动脉的可能,需要精确定位,对于操作技术要求较高。TriValve临床试验包含多种三尖瓣介入装置,并未对Trialign的数据进行进一步亚组分析,其中期临床预后尚未明确。
TriCinch (4Tech Cardio有限责任公司,爱尔兰)通过牵拉缩小瓣环消除TR(图1B)。TriCinch由穿刺螺母、腔静脉支架以及连接两者的涤纶带组成。TriCinch植入需要X线,心内超声或TEE引导,经股静脉置入导管,首先行右冠状动脉造影明确右冠状动脉解剖位置,定位穿刺螺母至前-后瓣交界处瓣环并穿刺固定,固定后通过牵拉链接穿刺螺母的涤纶带缩小瓣环,待TEE显示反流量改善满意后于下腔静脉释放支架以提供持续牵拉力。Latib等[13]于2015年报道了首例接受TriCinch治疗的72岁左心术后重度TR患者,患者接受TriCinch治疗后三尖瓣反流量明显减少,并且在术后6个月随访时三尖瓣功能及生活质量改善。PREVENT临床试验结果显示,TriCinch的植入成功率为81%,94%患者植入后TR至少减轻1级[14]。Calen等[15]报道了1例接受TriCinch植入后TR未能改善的病例,虽然通过再次植入的TriCinch-in-TriCinch技术获得了TR改善,但仍反映了TriCinch疗效的不稳定性。同时,TriCinch的穿刺螺母植入过程中同样存在损坏瓣环周围结构(尤其是右冠状动脉),其远期临床疗效仍有待进一步明确。
MiltraClip (Abbott Vascular公司,美国)通过经导管植入夹闭器,夹闭隔瓣与前瓣使三尖瓣二瓣化以减小瓣口面积,消除TR(图1C)。其通过股静脉植入导管,在TEE引导下夹闭器定位至三尖瓣瓣叶并夹闭。MiltraClip首先被设计用于治疗二尖瓣反流。Schofer等[16]于2016年报道了首例接受MitraClip治疗的重度TR患者,术后患者TR由重度改善为轻度。Nickenig等[17]报道了64例接受MitraClip治疗的患者,术后91%的患者TR程度有所改善,但仍有13%的患者TR程度在重度以上,同时42%的患者植入了2个或以上夹闭器,只有78%的患者夹闭器成功定位于前隔瓣。TriValve临床试验报道了210例接受MiltraClip植入的严重TR患者,其植入成功率为70.4%,30 d死亡率为2.8%[12]。
MiltraClip的主要技术难点在于因下腔静脉与三尖瓣瓣环夹角较大导致夹闭器定位困难,同时MitraClip设计用于治疗二尖瓣病变,其尺寸相对三尖瓣较小,定位成功率较低,多数患者为实现有效治疗需要植入多个装置,为了克服这些缺点,改进后夹闭器尺寸增大的MitraClip XTr装置已开始应用于临床,但其疗效有待于进一步确认[18]。
TriClip (Abbott公司,美国)是基于MiltraClip改进而专用于三尖瓣的介入修复装置,其在X线及TEE引导下经股静脉途径导管下植入夹闭器,夹闭三尖瓣前瓣与隔瓣使三尖瓣二瓣化以纠正TR(图1D)。评价TriClip临床安全性及有效性的TRILUMINATE临床试验于2019年发布6个月的随访结果,显示85例中度以上TR患者术中植入成功率为100%,80%的患者植入了2个及以上夹闭器,6个月数据显示有28%的患者TR仍在轻度及以下,6个月死亡率为5%, 7%的患者出现夹闭器单瓣叶脱落,9%的患者出现无症状的三尖瓣狭窄[19]。这些结果显示TriClip因基于MiltraClip改进而来,继承了MiltraClip的大部分特点,其瓣叶夹闭成功率、锚定可靠性以及远期临床效果仍需改进。
PASCAL (Edwards Lifesciences公司,美国)最初被设计用于二尖瓣介入修复,其通过股静脉经导管在X线及TEE引导下送入瓣叶夹闭器,通过夹闭三尖瓣瓣叶实现二瓣化纠正TR(图1E)。PASCAL相对MiltraClip的优势是其夹闭器尺寸更大,夹闭瓣叶成功率较高。PASCAL于2017年首次应用于TR治疗,Fam等[20]2019年公布了PASCAL救治性临床试验结果,共有28例重度及以上TR患者接受了PASCAL植入治疗,植入成功率为86%,共有40个夹闭器植入,其中28个成功定位于前隔瓣,术中无1例死亡,30 d死亡率为7.1%,85%的患者TR降低至重度以下,2例发生夹闭器单瓣叶脱落。这些结果显示其植入锚定定位较为困难,多数患者需植入多个夹闭器以实现有效治疗,此外,植入PASCAL后的长期预后仍有待进一步研究。
Cardioband (ValtechCardio公司,以色列)是一种通过介入植入的涤纶三尖瓣成形环,缩小三尖瓣瓣口面积消除TR(图1F)。在X线及TEE引导下经股静脉植入导管,将成形环自前-隔瓣交界向隔-后瓣交界顺时针释放并进行锚定,通过调整成形环形状缩小瓣口面积消除TR。Kuwata等[21]于2017年首次报道使用Cardioband治疗一位74岁女性重度TR患者,植入Cardioband后TR程度由重度转为轻度。Nickenig等[22]报道了TRI-REPAIR临床试验的中期结果,30例中度以上TR患者接受了Cardioband植入,植入成功率为100%,平均植入时间254.5 min,但3例患者在植入过程中损伤了右冠状动脉,其中1例发生右冠状动脉穿孔,1例患者术后三度出现房室传导阻滞并植入永久起搏器,在院死亡率为3.3%,死亡原因为器械导致心包填塞,6个月死亡率为10%,6个月随访数据显示Cardioband植入使反流束流颈宽度由平均12 mm降低至8.8 mm,但仍有28%的患者存在重度以上反流。
因需沿成形环植入多个锚定装置,Cardioband的植入过程较为复杂,其植入时间较长,存在损伤瓣环周围结构的风险,尤其是右冠状动脉损伤的发生率较高;同时,Cardioband基于缩小瓣环设计,仅适用于单纯瓣环扩张TR,适应证较为严格,远期临床效果有待确认。
FORMA (Edwards Lifesciences公司,美国)通过在三尖瓣瓣口处植入泡沫聚合物填充气囊,通过缩小反流口面积以及为瓣叶提供附着点而消除TR(图1G)。FORMA包括气囊、连接于气囊心室面的锚定器以及心房面的固定导管。在X线及TEE引导下经左侧腋静脉植入导管,右心室造影后送入锚定器及气囊,锚定器定位于右心室心尖部,气囊定位于三尖瓣瓣环中央,固定锚定器,心房面的固定导管远端于穿刺处埋入皮下锚定。Perlman等[22]于2015年首次报道使用FORMA植入治疗7例重度TR患者,植入后3例患者由重度转为中度,4例由重度转为轻度。18例患者的1年随访结果显示FORMA植入在改善了患者TR的同时伴随右心室容积减小,但在植入过程中出现右心室穿孔及锚定装置脱位各1例[24]。Asmarats等[25]报道了19例接受FORMA植入的重度TR患者长期临床预后结果,植入成功率为89%,无一例30 d死亡发生,平均随访时间为32个月,累计死亡率为24.0%,随访期间口服抗凝药物下发生肺栓塞1例,67%的患者末次随访时TR仍维持在重度以下。FORMA锚定器定位于右心室心尖,出血相关并发症发生率高,同时由于腔内留置物较多,存在血栓相关并发症发生的可能,同时,其适应证较为严格,仅适用于中心性TR,目前临床结果显示远期效果有待改善。
上述所有介入三尖瓣修复技术,主要通过瓣叶夹闭、瓣环环缩以及增加对合面积3类机制达到减少或消除TR的目的,所有公开报道的临床试验,受试者临床表现有不同程度的改善,显现了该类器械的临床应用前景。然而,从目前实施的临床试验结果观察,此类器械应用还存在以下局限性:(1)器械植入成功率不够高,除了FORMA技术,其他产品的植入成功率一般都不超过90%;(2)部分器械对患者三尖瓣解剖特点有一定的应用限制,三尖瓣瓣叶对合间距过大,瓣环过大,存在起搏或除颤电极,以往曾接受三尖瓣外科修复等,无法满足更多临床需求;(3)目前三尖瓣修复的临床终点往往只是减少三尖瓣反流程度1~2级(与前面的轻中重度不一致),术后部分患者TR程度仍较严重,是否影响远期疗效,有待进一步观察;(4)外科三尖瓣成形术后,5年三尖瓣关闭不全复发率高达40%,主要与右心室持续扩大导致腱索牵拉有关,介入修复是否也会面临类似问题,也需要深入研究。
TricValve (GmbH公司,澳大利亚)是一种腔静脉自膨胀牛心包人工瓣膜,通过在上下腔静脉植入人工瓣膜阻止右心室收缩期血液通过上下腔静脉反流至体循环(图2A)。Lauten等[26]于2011年报道了首例接受TricValve治疗的重度TR患者,其在接受下腔静脉瓣膜植入后下腔静脉压力较植入前明显下降。然而,到目前为止接受TricValve治疗的5例患者术后随访期间死亡率高达80%,且TricValve植入并未改善三尖瓣本身的反流程度,其临床效果仍需要进一步验证[27]。
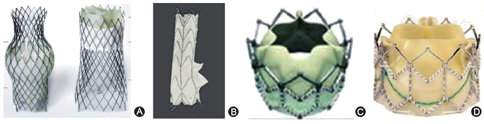

Tricento (New Valve Technology公司,瑞士)是一种腔静脉自膨胀猪心包瓣膜,其结构较为独特,包括一个锚定在上下腔静脉的覆膜支架以及右心房部位的二叶猪心包瓣膜,其通过24 F的导管经股静脉植入,并且其在释放后可通过输送系统进行位置调整或回撤(图2B)。Toggweiler等[26]于2018年报道了首例接受Tricento植入的重度TR患者,目前报道Tricento植入患者4例,均植入成功,但2例植入后3个月再次出现严重右心衰竭表现,分析表明较软的支架强度以及植入后右心房心室化导致了严重的支架收缩期缩窄,最终导致上下腔静脉压力增高并出现临床右心衰竭表现[28,29,30]。这些结果说明此装置仍需进一步改进。
Sapien/Sapien XT (Edwards Lifesciences公司,美国)是设计用于介入下治疗主动脉瓣狭窄的球囊扩张牛心包人工瓣膜,Laule等[31]于2013年首次报道将其用于治疗TR,通过右侧股静脉置管,首先在拟定瓣膜释放区域释放一枚裸支架以提供Sapien/Sapien XT球扩瓣的锚定区,随后在锚定区内释放人工瓣膜(图2C、图2D)。目前共有10例患者接受了此类治疗,但其中9例患者仅在下腔静脉处植入瓣膜,术后30 d死亡率为20%[27]。
异位三尖瓣置换并未消除TR,仅控制了腔静脉水平的回流,会引起右心房的持续性扩大,这也是导致该类装置中远期疗效下降的原因,在原位置换装置成熟后,预计此类技术将被替代。
NaviGate (NaviGate Cardiac Structures公司,美国)是设计用于原位三尖瓣置换的介入自膨胀生物瓣膜(图3 A)。Navia等[32]于2017年首次报道了接受NaviGate治疗的2例重度TR患者。在X线、TEE及心内超声引导下,通过经心房/颈静脉途径植入导管并释放生物瓣膜,术后1例患者TR由重度转为轻度,另1例由重度转为中度瓣周漏并在随访第6个月时死于缺血性结肠炎并发败血症。目前共有11例患者接受Navi Gate植入,所有患者术后TR均有改善,1例患者发生房室传导阻滞并需要植入起搏器,随访期间3例患者死亡[33]。NaviGate瓣膜依靠瓣周的锚定装置锚定于瓣环上,为获得可靠的锚定及预防瓣周漏,常选取大于瓣环5%~10%的规格植入,这影响了房室环收缩以及术后右心功能恢复,并增加了瓣周结构损伤导致发生房室传导阻滞的可能性。


LuX-valve (Jenscare Biotechnology公司,中国)是中国原创的介入原位三尖瓣置换自膨胀牛心包生物瓣膜(图3B)。其具有独特的锚定装置,通过夹持三尖瓣前瓣以及室间隔获得瓣膜锚定,避免了NaviGate等直接锚定于瓣环易导致瓣周结构损伤以及妨碍右心室房室环收缩的弊端;同时其专门设计的瓣裙结构能够可靠地贴附于三尖瓣瓣叶及瓣环,并有效防止术后瓣周漏[33]。LuX-valve通过经右心房途径植入,定位后首先释放前瓣夹持装置,随后释放室间隔锚定装置以及瓣膜。目前的动物实验及前期临床试验结果显示LuX-valve植入后TR程度均明显改善[34,35]。
原位三尖瓣置换能有效消除TR,迅速改善患者心力衰竭等临床症状,具有较好的临床效果,但鉴于三尖瓣瓣环组织无钙化,内径往往超过5~6 cm,显然采用依赖径向支撑力的装置如Navigate,将会压迫三尖瓣瓣环,容易引起传导阻滞,同时巨大的支架也影响三尖瓣瓣环的收缩活动,可能对远期心功能的恢复带来不利。采用非径向支撑力依赖的装置不会造成对瓣环组织压迫,可避免的上述两个不良后果,更重要的是,LuX-valve在操作时,待瓣膜释放开始工作后,不会影响血流动力学稳定,因不依赖径向支撑,还能在心脏超声指引下进行位置的微调整,确保消除瓣周漏后,再最终释放瓣膜。
TR是一种既往被忽视的严重右心疾病,TR的外科治疗在目前欧美心血管领域的指南中,推荐级别不高,仅在左心瓣膜手术时,对于合并三尖瓣瓣环扩张的情况予以同期处理。经导管三尖瓣介入治疗技术目前处于起步阶段,但已经显示出了相较于传统手术治疗的优势并扩大了三尖瓣瓣膜手术的适应证。介入成形技术均需要心内复杂有创操作而存在较大风险;非原位三尖瓣介入技术虽然改善了体循环淤血,但对原位TR缺乏有效干预;介入下三尖瓣原位置换技术具有心内创伤小,且瓣膜原位替代符合人体生理的优势,但由于起步较晚,相关产品的治疗效果仍需进一步临床研究验证。


























