
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
急性心肌梗死(acute myocardial infarction,AMI)后心室重构与心力衰竭(heart failure,HF)发生以及疾病预后密切相关[1],《中国心力衰竭诊断和治疗指南2018》、2016年欧洲心脏病学会(European Society of Cardiology,ESC)急、慢性心力衰竭诊断和治疗指南和2013年美国心脏病学会(American College of Cardiology,ACC )/美国心脏协会(American Heart Association,AHA)等指南的部分章节均提出了AMI后心室重构的治疗建议[2,3,4],但目前尚无针对该领域的指南或共识。基于此,由中国医师学会胸痛专业委员会、中华心血管病杂志(网络版)编辑委员会以及急性心肌梗死后心室重构防治专家共识起草组共同制定本共识,内容涉及AMI后心室重构的定义、流行病学与发病机制、评估指标与诊断工具、诊断与治疗及随访管理等,旨在规范AMI后心室重构的早期防治,提高我国AMI后心室重构临床诊治水平。
AMI后心室重构,是指AMI后心室持续发生的大小、形态、结构和功能的改变过程,可表现为左心室扩大、左心室射血分数(left ventricular ejection fraction,LVEF)降低和/或局部室壁活动异常,是决定AMI后心脏事件发生率和远期预后的主要因素[5]。在患者出现HF症状前,心室重构多表现为无症状的结构和功能异常(心脏的收缩或舒张功能不全)。AMI后心室重构可分为早期重构和晚期重构:(1)早期心室重构常在AMI后24~72 h内发生,主要表现为梗死面积扩大和心室腔扩张,心肌细胞坏死及心肌顿抑;(2)晚期心室重构主要表现为心肌细胞肥大、凋亡和弥漫性纤维化,通常在数周内(偶尔在数月内)发生,晚期心室重构个体化差异大,可以延续数月甚至1年。早期心室重构与晚期心室重构间主要差异见表1[6]。

AMI后早期心室重构与晚期心室重构比较
AMI后早期心室重构与晚期心室重构比较
| 指标 | 早期心室重构 | 晚期心室重构 |
|---|---|---|
| 发作时间 | 常在AMI后24~72 h内发生 | 可能在潜伏期延长后数月甚至1年 |
| 个体差异 | 小 | 大 |
| 初始梗死面积 | 通常为广泛性(伴中度至重度LV收缩功能不全) | 通常受限(临界或轻度LV收缩功能不全) |
| 主要决定因素 | 梗死面积和神经激素激活 | 特定炎症途径,包括IL-23/IL-17A轴、某些促纤维化标志物和可溶性ST2 |
| 进展速度 | 可变 | 高度可变,具有隐匿和缓慢进展的模式 |
| 恶性心律失常和/或心源性猝死风险 | 可能 | 很可能 |
注:AMI:急性心肌梗死;LV:左心室;IL:白细胞介素;ST2:致癌抑制因子2
AMI后患者中出现无症状左心室收缩功能障碍(left ventricular systolic dysfunction,LVSD)的比率高达30%~60%[7]。心肌梗死患者即使已行经皮冠状动脉介入治疗(percutanous coronary intervention,PCI),心肌梗死后HF发生率仍然倍增[8]。一项连续入选284例接受经皮腔内冠状动脉成形术治疗的AMI患者的研究,在观察了24 h、1个月、6个月的心电图(electrocardiograph,ECG)和心脏造影后,30%的AMI患者在PCI后6个月发生了心室重构[心室重构定义:6个月时左心室舒张末期容积(left ventricular end-diastolic volume,LVEDV)较基线≥ 20%][9]。因此,AMI后心室重构是HF发生的独立预测因素,同时是影响患者预后的主要因素之一[1]。
AMI后心室重构受性别、年龄、吸烟、肥胖、糖尿病、高血压、血脂异常、心肌梗死部位、是否为多支血管病变、是否为慢性完全闭塞性病变(chronic total occlusion,CTO)及是否合并瓣膜病变等多种危险因素的影响[10,11,12,13,14,15]。其中,前壁心肌梗死发生心室重构的风险较其他部位增加了1.9倍[12],多支病变患者心室重构的风险较单支病变患者高1.2倍[13],CTO病变和瓣膜病的严重程度与心脏重构的程度密切相关[14,15]。
AMI后心室重构的发生涉及心肌梗死、肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone system,RAAS )、交感神经系统与利钠肽(natriuretic peptide,NP)系统等神经内分泌系统的激活以及炎症免疫反应等病理机制。RAAS对不良心室重构的影响主要源于血管紧张素Ⅱ表达的增加。在大鼠模型中,持续输注血管紧张素Ⅱ可导致血管周围和间质胶原含量增加[16]。近年来,NP系统的激活在AMI后心室重构中的重要作用颇受关注,如NP能控制血压和血容量。研究发现B型利钠肽(B-type natriuretic peptide, BNP)能发挥强大的抗心肌肥大与抗心肌纤维化效应[17],BNP升高可拮抗被激活的交感及RAAS系统的活性,AMI后心功能越差,BNP水平越高[10]。此外,可溶性致癌抑制因子2 (suppression of tumorigenicity 2,ST2)参与心肌梗死区的炎症反应,与心肌纤维化和心室重构有关,从而影响心肌梗死预后[18,19]。近些年来的研究发现,心肌梗死后常发生室性心动过速、心房颤动等多种电生理活动紊乱,即电重构。当前对电重构发生机制了解尚有限,有待进一步深入研究[20]。
所有AMI患者入院时均要及时行心电图、胸片、初始血液检查(包括全血细胞计数、血清电解质、血尿素氮、肌酐、肝功能检测、空腹血糖、血脂和促甲状腺激素)、高敏肌钙白与NP水平等,有条件的医院可同时检测血液ST2水平。
一般检查中生物标志物NP在AMI后心室重构的预测中具有重要的价值。AMI患者在急诊室、住院期间或行PCI前后,应及时测定血浆NP水平,包括BNP与N末端B型利钠肽前体(N-terminal pro-B-type natriuretic peptide,NT-proBNP )。在患者之后的随访中,应对BNP与NT-proBNP的浓度进行多次检测,有助于识别患者是否正在发生心室重构。若患者血清BNP或NT-proBNP浓度低且波动不大(阈值:BNP<100 ng/L,NT-proBNP<300 ng/L),提示患者AMI后预后较好[3]。若血清BNP或NT-proBNP浓度高或呈持续增高趋势,提示患者心室发生重构,未来发生HF风险可能性高,应尽早重视与干预[21]。此外,高敏肌钙蛋白、半乳糖凝聚素-3与可溶性ST2等亦具有重要的预测价值[22]。
心脏影像学的检查对心肌梗死后心室重构的诊断与治疗具有重要意义。心室重构常用的影像学检查方法包括超声心动图检测、心脏磁共振成像(cardiac magnetic resonance imaging,CMRI )与放射性核素显像等。超声心动图因使用简单、可及性(包括便捷性)、安全性与可动态观察心脏的结构和功能等特点,是临床评价心脏收缩与舒张功能首选的方法。
在条件允许的情况下,建议确诊AMI患者即刻行超声心动图检查;若条件不允许,建议确诊为AMI后24~48 h内,患者须行超声心动图检查[23],并在以后3~6个月的随访中,联合生物标志物、临床症状及体征,加强超声心动图的定期监测。超声心动图主要观察内容包括:(1)二维超声心动图评价心脏结构与形态。评价指标有各腔室径线、室壁节段运动与形态改变、瓣膜结构与活动及腔室是否有异常回声等。(2)彩色多普勒超声检查评价血流动力学。评价内容主要有各瓣膜是否存在关闭不全、二尖瓣口与三尖瓣口血流频谱类型、室间隔或室壁是否有穿孔的异常血流信号等。(3)心功能评价。收缩功能主要评价指标有LVEF,强调采用双平面辛普森法测量。LVEDV和左心室收缩末期容积(left ventricular end-systolic volume,LVESV)也是评价心脏收缩功能的常用参数[24]。舒张功能评价常用指标是二尖瓣口血流频谱类型改变。另外、应变率成像能对心肌的力学参数改变进行有价值的评价。超声心动图评价AMI后患者心室重构时,应注意以下几点:(1)必须了解患者病史,超声心动图像须结合临床症状与体征。(2)各种超声成像技术综合运用,各种超声参数一定要综合分析。(3)强调超声心动图的及时随访检查。
AMI后心室重构诊断依赖于病史、实验室检查、心脏影像学检查和功能检查,具体诊断流程可参考图1。首先通过心电图、BNP/NT-proBNP检测等判断有无心室重构的可能性,再通过经胸超声心动图、CMRI等心脏影像学检查明确是否存在心室重构。目前心肌梗死后心室重构的诊断尚无统一明确标准。台湾学者建议,AMI后通过超声心动图双平面法测量左心室容积,LVESV从初始检测到随访6个月如增加>15%,则将其诊断为左心室重构[29]。有专家建议心肌梗死后无症状左心室收缩功能障碍患者的LVEF阈值范围为<50%即可诊断为心肌梗死后心室重构[30]。另有学者支持LVEDV增高达到20%可诊断为心室重构[17]。
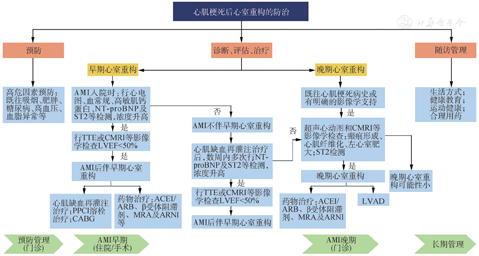

注:AMI:急性心肌梗死;NT-proBNP:N末端B型利钠肽前体;ST2:致癌抑制因子2; TTE:经胸超声心动图;CMRI:心脏磁共振成像;LVEF:左心室射血分数;PPCI:急诊经皮冠状动脉介入治疗;CABG:冠状动脉旁路移植术;ACEI/ARB:血管紧张素转化酶抑制剂/血管紧张素Ⅱ受体拮抗剂;MRA:盐皮质激素受体拮抗剂;ARNI:血管紧张素受体-脑啡肽酶抑制剂;LVAD:左心室辅助装置
预防、减缓或逆转心室重构以降低HF与死亡发生风险是心肌梗死后心室重构的主要治疗目标,干预措施主要包括危险因素预防、早期血运重建及择期行相关梗死血管开通、药物治疗以及基于器械的辅助治疗等。
心肌缺血再灌注治疗包括抗血小板治疗、静脉溶栓治疗、PCI及冠状动脉旁路移植术(coronary artery bypass grafting,CABG)等,是防止和逆转心室重构的根本治疗措施,可有效防止心肌梗死后心室重构,从而改善患者的心功能和预后。AMI患者应尽早血运重建(如行PCI ),若条件不允许,可考虑早期溶栓。早期溶栓治疗(出现症状<3 h)有助于控制左心室室壁异常活动的幅度[31]。
所有AMI患者均应尽早使用ACEI以降低心室重构而引起的HF和死亡风险。对不能耐受ACEI的患者推荐ARB[32,33],并按指南要求将ACEI/ARB滴定到靶剂量或最大耐受剂量。
所有AMI患者均应尽早使用β受体阻滞剂以预防或延缓HF的进程,降低死亡风险,并能降低无症状的左心室收缩功能障碍患者发生心律失常的风险[34]。应按指南要求滴定到靶剂量或最大耐受剂量,将静息心率控制在60次/min左右。
AMI后且LVEF ≤ 40%,有HF症状或合并糖尿病患者,尽早使用醛固酮受体拮抗剂(又称为盐皮质激素受体拮抗剂),联合ACEI/ARB及β受体阻滞剂,可使纽约心脏病学会(New York Heart Academy,NYHA)心功能分级Ⅱ~ Ⅳ级的射血分数减少的HF (ejection fraction reduced heart failure,EFrHF)患者获益,降低全因死亡、心血管死亡、猝死和HF住院率[35]。AMI后左心室收缩功能障碍的患者中应用醛固酮受体拮抗剂治疗可升高白细胞介素-33 (interleukin-33,IL-33),并且降低可溶性ST2,减缓心室重构的发生进程[36]。
沙库巴曲缬沙坦(LCZ696)是全球首个ARNI类药物。有研究证实,在EFrHF患者中,沙库巴曲缬沙坦治疗不仅能够降低NT-proBNP水平、提高LVEF,而且在改善心脏结构和功能及逆转心室重构方面均显著优于ACEI/ARB[37,38,39],应按指南要求将ARNI滴定到靶剂量或最大耐受剂量。还有研究证实,沙库巴曲缬沙坦能通过降低EFrHF患者非持续性室性心动过速与室性期前收缩发生风险,从而缓解心脏电重构的发生[40]。2016年已经启动更大规模的AMI后早期沙库巴曲缬沙坦预防心血管事件的研究[41],将为AMI后患者治疗开启新篇章。
严重心室重构、HF症状重且药物治疗效果差的D期患者,必要时可植入左心室辅助装置(left ventricular assist device,LVAD),LVAD可显著缩小腔室内径,并调节多种分子变化,从而有效地促进可逆性重构的发生[44]。在电重构猝死的预防上,指南建议以下人群可考虑植入型心律转复除颤器(implantable cardioverter defibrillator,ICD):(1)心肌梗死后至少40 d或血运重建后至少90 d,在接受合理药物治疗的基础上,如果LVEF仍≤ 35%且NYHA心功能分级Ⅱ级以上的患者;(2)无症状的AMI后患者,LVEF仍≤ 30%,并且期望有1年以上良好生活质量的患者[44]。
推荐心肌梗死患者出院后每2周随访1次,病情稳定后改为每1~2个月1次,随访的内容包括测量血压及心率、临床评估心功能分级、肾功能与电解质、治疗依从性与不良反应;根据病情行BNP/NT-proBNP、经胸超声心动图和动态心电图检查,通常在规范治疗3个月后,患者临床状况可发生变化,建议每6个月进行1次病情评估,根据评估结果及时进行药物调整等措施。
建议药物治疗的同时进行患者教育和康复治疗,患者教育主要内容包括药物治疗依从性、饮食指导与生活方式干预等;康复治疗有助于更好地控制危险因素、提高运动耐量和生活质量。如患者病情允许,应在住院期间尽早开始康复治疗,出院后根据情况循序渐进的进行康复治疗。
共同执笔人:金泽宁(首都医科大学附属北京天坛医院);孔洪(四川省人民医院)
参与共识制定的专家(按姓氏拼音排序):
陈良龙(福建医科大学附属协和医院);陈玉国(山东大学齐鲁医院);陈韵岱(解放军总医院);傅向华(河北医科大学第二医院);高传玉(阜外华中心血管病医院);黄恺(华中科技大学同济医学院附属协和医院);黄岚(陆军军医大学新桥心血管病专科医院);霍勇(北京大学第一医院);金泽宁(首都医科大学附属北京天坛医院);孔洪(四川省人民医院);李保(山西医科大学第二医院);李浪(广西医科大学第一附属医院);廖玉华(华中科技大学同济医学院附属协和医院);吕晓希(中国医学科学院药物研究所);马依彤(新疆医科大学第一附属医院);邱春光(郑州大学第一附属医院);苏晞(武汉亚洲心脏病医院);王焱(厦门大学附属心血管病医院);向定成(解放军南部战区总医院);谢明星(华中科技大学同济医学院附属协和医院);徐亚伟(上海市第十人民医院);周京敏(复旦大学附属中山医院)

























