
探讨综合干预策略对胎龄<32周且出生体重<1 500 g的极早产儿院际转运时体温的影响。
选择2016年10月至2019年7月中国人民解放军总医院第七医学中心儿科医学部极早产新生儿重症监护病房(neonatal intensive care unit,NICU)收治的院际转运的胎龄<32周且出生体重<1 500 g的极早产儿进行回顾性分析,2016年10月至2018年3月常规转运的早产儿为干预前组,2018年4月至2019年7月实施综合干预策略的早产儿为干预后组,分析比较两组早产儿转运前和转运至NICU时的体温、并发症及治疗结局。
共纳入1 194例极早产儿,干预前组630例,干预后组564例。两组患儿及母亲一般情况、单程转运时间比较,差异均无统计学意义(P>0.05)。干预后组转运前及入住NICU时体温高于干预前组[(36.8±0.5)℃比(36.0±0.4)℃、(36.7±0.5)℃比(36.3±0.6)℃],差异有统计学意义(P<0.01);低血糖发生率[3.7%(21/564)比8.4%(53/630)]及病死率[4.8%(27/564)比7.9%(50/630)]低于干预前组,差异有统计学意义(P<0.05)。
综合保暖干预策略在院际转运中能有效提高早产儿转运出发前和转运后的入室体温,降低早产儿低血糖发生率和病死率。

新生儿正常体温为36.5~37.5℃,低于36.5℃为低体温[1]。临床发现早产儿在产房、到达新生儿病房时普遍存在低体温现象,国际上报道极低/超低出生体重儿(very low birth weight infant,VLBWI)/(extremely low birth weight infant,ELBWI)入院低体温发生率为31%~78%[2, 3]。我国山东省一项多中心研究结果显示,VLBWI/ELBWI入院低体温发生率高达89.3%,各医疗机构的产房和新生儿科医生对出生到转运至新生儿重症监护病房(neonatal intensive care unit,NICU)时早产儿体温的重视程度与欧美国家仍有差距[4]。文献对低体温预防措施实施现状的调查报道较少,且多以塑料薄膜包裹保暖作为单一研究因素[5, 6]。中国人民解放军总医院第七医学中心为北京市危重症新生儿三级转诊救治中心之一,本研究针对VLBWI/ELBWI生后及转运中常出现的低体温现象进行综合保暖干预策略,取得了一定成效,现报道如下。
选择2016年10月至2019年7月通过新生儿转运网络转入我院儿科医学部极早产NICU的胎龄<32周且出生体重<1 500 g的早产儿进行回顾性研究。排除标准:(1)严重先天性畸形如脊柱裂、脐膨出等;(2)严重皮肤破损;(3)生后>12 h再行转运;(4)病历资料不完整。本研究通过我院伦理委员会批准(2019-083)。2016年10月至2018年3月常规转运早产儿为干预前组,2018年4月至2019年7月经综合保暖干预策略转运的早产儿为干预后组。
1.资料收集:通过查阅电子病历收集患儿及母亲资料,包括患儿性别、胎龄、出生体重、Apgar评分、单程转运时间、体温及救治结局,母亲年龄、分娩方式、妊娠期并发症等。
2.综合保暖干预策略:(1)产前准备:胎龄<32周孕母分娩前由产科通知我院转运处,转运救护小组在分娩前进入产房或手术室进行分娩前准备。(2)预热婴儿用品:提前30 min将转运暖箱设置在37℃进行预热,同时将早产儿可能接触到的物品,如包被、小帽、纸尿裤、生理盐水、皮肤消毒液等放置在转运暖箱内预热。(3)规范转运流程:将转运暖箱推至产房或手术室门口,使早产儿在生后最短时间内进入转运暖箱。转运救护小组在分娩现场与产儿科医生合作使用预热好的婴儿用物进行救护,减少冷刺激源传导散热。(4)规范保暖流程:必要的复苏及处置后快速使用塑料薄膜(食品级聚乙烯PE保鲜膜)包裹患儿躯干及四肢(留出脐部及会阴部,松紧度以不妨碍患儿活动为宜)[5, 6],头戴棉质小帽,再用预热好的包被包裹患儿,抱入预热至37℃的双壁式转运暖箱,推转运暖箱回急救车,急救车内温度设置在26~28℃。根据早产儿体温及体重调整箱温,褪去包被,保留小帽和保鲜膜继续包裹,连接心电监护。(5)保持保暖链的持续性:司机评估路途转运时间,医生护士集束化处置早产儿途中病情变化。到达我院前0.5 h,转运组通知科室提前将保暖辐射台预热至36℃。到达后推转运暖箱由新生儿专用绿色通道直接送至NICU。实施综合干预策略前的转运流程为新生儿娩出后,对口医院根据患儿病情需要或家长转诊意愿通知本院转运。转运组成员按照排班的方式轮流出车转运救护,到达对口医院后,对患儿进行评估及交接,沿用该院原有保暖方式,用包被包裹将患儿抱上转运救护车、安置于转运暖箱后出发。
3.观察指标:(1)体温:在早产儿出发前、转入我院NICU时,采用电子耳温枪(博朗ERT3000)调至婴幼儿测温模式,置于早产儿耳廓内测量[7, 8]。(2)并发症及结局定义参考《实用新生儿学》[1]:①低血糖:末梢血快速血糖<2.2 mmol/L;②晚发型败血症:入院3 d后继发的血培养阳性或临床诊断败血症;③重度脑室内出血(intraventricular hemorrhage,IVH):住院7 d内行头颅超声检查,按Papile分度法Ⅲ级以上为重度IVH;④死亡:出院前确定为临床死亡,或放弃治疗、自动出院后经电话回访确定已死亡。
应用SPSS 22.0统计软件进行数据分析。正态分布的计量资料以表示,组间比较采用t检验;计数资料以例(%)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2016年10月至2018年3月我院收治院际转运胎龄<32周且出生体重<1 500 g早产儿938例,排除脊柱裂2例、先天性表皮缺如1例、>12 h转运及病历资料不完整305例,最终干预前组纳入630例;2018年4月至2019年7月院际转运胎龄<32周且出生体重<1 500 g早产儿763例,排除皮肤破损5例、>12 h转运194例,最终干预后组纳入564例。两组患儿性别、胎龄、出生体重、1 min及5 min Apgar评分、母亲年龄、分娩方式、妊娠期并发症等比较,差异均无统计学意义(P>0.05),见表1、2。
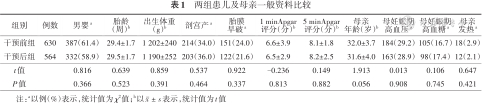
两组患儿及母亲一般资料比较
两组患儿及母亲一般资料比较
| 组别 | 例数 | 男婴a | 胎龄(周)b | 出生体重(g)b | 剖宫产a | 胎膜 早破a | 1 minApgar评分(分)b | 5 minApgar评分(分)b | 母亲 年龄(岁)b | 母妊娠期 高血压a | 母妊娠期高血糖a | 母亲 发热a |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 干预前组 | 630 | 387(61.4) | 29.4±1.7 | 1 202±240 | 214(34.0) | 151(24.0) | 6.6±3.9 | 8.1±1.8 | 32.0±3.7 | 184(29.2) | 105(16.7) | 18(2.9) |
| 干预后组 | 564 | 332(58.9) | 29.5±1.7 | 1 190±252 | 203(36.0) | 122(21.6) | 6.5±2.9 | 8.2±2.5 | 31.6±4.0 | 163(28.9) | 98(17.4) | 12(2.1) |
| t值 | 0.816 | 0.639 | 0.859 | 0.537 | 0.922 | -0.236 | 0.149 | 1.913 | 0.013 | 0.106 | 0.647 | |
| P值 | 0.366 | 0.523 | 0.391 | 0.464 | 0.337 | 0.813 | 0.882 | 0.056 | 0.908 | 0.745 | 0.421 |
注:a以例(%)表示,统计值为χ2值;b以表示,统计值为t值
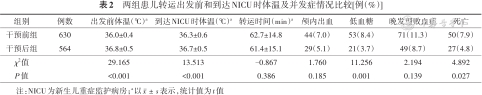
两组患儿转运出发前和到达NICU时体温及并发症情况比较[例(%)]
两组患儿转运出发前和到达NICU时体温及并发症情况比较[例(%)]
| 组别 | 例数 | 出发前体温(℃)a | 到达NICU时体温(℃)a | 转运时间(min)a | 颅内出血 | 低血糖 | 晚发型败血症 | 死亡 |
|---|---|---|---|---|---|---|---|---|
| 干预前组 | 630 | 36.0±0.4 | 36.3±0.6 | 62.7±14.8 | 44(7.0) | 53(8.4) | 71(11.3) | 50(7.9) |
| 干预后组 | 564 | 36.8±0.5 | 36.7±0.5 | 61.4±15.1 | 29(5.1) | 21(3.7) | 49(8.7) | 27(4.8) |
| χ2值 | 29.165 | 13.513 | -0.867 | 1.760 | 11.256 | 2.194 | 4.892 | |
| P值 | <0.001 | <0.001 | 0.386 | 0.185 | 0.001 | 0.139 | 0.027 |
注:NICU为新生儿重症监护病房;a以表示,统计值为t值
两组患儿转运时间比较差异无统计学意义(P>0.05),干预后组在对口医院转诊出发前、以及到达NICU时体温均高于干预前组,差异有统计学意义(P<0.05),见表2。
干预后组患儿入院后低血糖发生率和病死率低于干预前组,差异均有统计学意义(P<0.05);两组颅内出血及晚发型败血症发生率差异无统计学意义(P>0.05)。见表2。
环境温度低是低体温发生的重要因素,新生儿出生后由于外部环境寒冷和蒸发散热导致热量急剧散失。文献报道44.0%~56.1%的VLBWI在产房及转运途中出现低体温[9]。早产儿生后15 min内体温可下降0.9℃,生后1 h内体温可下降2.5℃[10]。早产儿体重越低,越容易发生低体温,在黄金1 h内对VLBWI在包被包裹等常规保暖基础上增加额外针对性的保暖措施,如减少散热及冷刺激源,保持所处环境温暖等非常重要[11]。但早产儿从娩出至院际转运入NICU时生存环境发生变化,涉及到不同学科、环节、流程的衔接与配合,易发生低体温[12, 13]。所以本院NICU建立基于循证的以对口医院产儿科为中心的跨学科合作,采取综合保暖干预策略,结果显示干预后组转运出发前体温和入住NICU时体温均高于干预前组,差异有统计学意义。
低体温可以引起寒冷损伤,导致代谢性酸中毒、低血糖、微循环障碍等病理生理改变,并与晚发型败血症、IVH等密切相关[14, 15]。有研究报道VLBWI入院体温每下降1℃,病死率增加28%[15, 16]。本研究中干预后组低血糖发生率与病死率均低于干预前组。低血糖可严重影响早产儿疾病或病理过程,应积极预防,尽早识别并积极处理[17]。本研究显示两组晚发型败血症发生率差异无统计学意义,考虑可能原因为干预后组体温低于36℃的早产儿较少,而晚发型败血症主要与体温低于36℃密切相关[18]。潘亚等[16]和袁瑞琴等[19]报道低体温组与正常体温组颅内出血发生率并无差异,与本研究结果一致。一方面可能与本研究中患儿低体温持续时间较短、复温较快有关;另一方面,颅内出血可能是缺氧、低血糖等多因素共同作用的结果[19, 20]。预防低体温可有效降低早产儿低血糖、硬肿症、酸中毒等并发症的发生,提高存活率和生存质量[21, 22],增加家长救治VLBWI/ELBWI的信心。本研究显示采取综合干预措施后,VLBWI/ELBWI病死率从7.9%下降至4.8%,差异有统计学意义。
国际上已经出台多项指南和干预模式对早产儿出生前、出生后、产房、到达NICU后的4个环节进行体温干预,如提高环境温度、加热复苏液体、包裹保鲜膜等,以减少早产儿入院低体温的发生[23, 24, 25]。本研究针对需进行院际转运的极早产儿加强跨院区、跨学科合作,进行综合保暖干预策略,取得了一定成效。但产前干预等候的人力成本、时间成本耗费比较高;且聚乙烯保鲜膜使用的适宜时间及胎龄、有无相关并发症等目前缺乏指南指导[6,26]。其次,本研究中有关低体温与相关并发症的关系可能存在局限性,有待进行多中心大样本量的研究进一步论证。
所有作者均声明不存在利益冲突



























