
探讨David手术在治疗主动脉根部瘤合并主动脉瓣二叶畸形中应用的临床效果。
回顾性研究。纳入南京大学医学院附属鼓楼医院心胸外科2016年1月—2019年1月行David手术治疗主动脉根部瘤合并主动脉瓣二叶畸形的11例患者临床资料。其中男8例、女3例,年龄18~60(35±13)岁;主动脉瓣轻度反流7例、轻中度反流4例,心功能Ⅱ级5例、Ⅲ级5例、Ⅳ级1例。观察患者围术期指标;术后定期复查心脏超声,观察人工血管通畅情况及主动脉瓣反流情况,包括左室射血分数、主动脉瓣反流程度、平均跨瓣压差、峰值跨瓣压差及最大血流速度。
11例患者均成功实施手术。围术期观察指标:体外循环时间(246.1±27.2)min,主动脉阻断时间(207.5±21.5)min,术后机械通气时间4.5(3.25,9.25)h,重症监护时间(2.8±1.5)d,术后24 h引流量(418.2±299.0)mL。所有患者术后随访18~30个月,平均22.5个月,未见死亡及二次手术病例。随访期间心脏超声显示患者人工血管血流均通畅,主动脉瓣轻微反流8例、轻度反流3例,平均跨瓣压差均<10 mmHg(1 mmHg=0.133 kPa),末次随访时,患者心功能Ⅰ级8例、Ⅱ级3例,较术前明显改善。
采用David手术结合主动脉瓣修复技术治疗主动脉根部瘤合并中度以下反流的主动脉瓣二叶畸形,其临床疗效满意。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
David手术是保留主动脉瓣的根部替换手术的重要构成部分,与Yacob手术相对应,最早被用于治疗三叶主动脉瓣升主动脉根部扩张的患者[1,2]。与主动脉瓣替换相比,David手术保留了患者自身的瓣膜,避免了机械瓣需要终身抗凝、生物瓣会逐渐衰败以及人工瓣膜引发感染性心内膜等不良后果,具有明显优势[3,4]。20多年前国外学者就将David手术应用于主动脉根部瘤合并主动脉瓣二叶畸形(bicuspid aortic valve,BAV)的患者,目前该手术在国外开展较为广泛,结合瓣叶修复技术,可以提供良好的中、远期疗效[3,5,6,7]。但是,由于David手术操作有一定难度,学习曲线长,目前国内很多医院还不能常规开展,关于David手术在主动脉根部瘤合并BAV患者中运用的报道较少,经验有限[8]。本研究对采用David手术治疗的主动脉根部瘤合并BAV 11例患者的临床资料进行总结分析,旨在探讨David手术治疗主动脉根部瘤合并BAV的临床效果,为该技术在临床的推广提供参考。
纳入标准:(1)术前经胸超声检查明确诊断BAV;(2)术前经胸超声及CT提示主动脉根部直径>5.0 cm;(3)术前经胸超声主动脉瓣反流为中度以下。排除标准:(1)术中探查排除BAV者;(2)主动脉瓣瓣叶交界存在明显粘连、钙化和狭窄,估计修复效果不佳者。
回顾性研究。纳入南京大学医学院附属鼓楼医院心胸外科2016年1月—2019年1月行David手术治疗主动脉根部瘤合并BAV的11例患者的临床资料,其中男8例、女3例,年龄18~60(35±13)岁。主动脉瓣轻度反流7例,轻中度反流4例;术前心功能Ⅱ级5例,Ⅲ级5例,Ⅳ级1例。11例中,合并Stanford A型夹层1例,合并脊柱侧弯、房间隔缺损各1例。
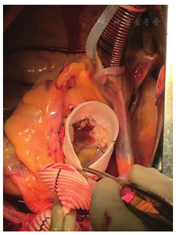
所有患者采用全身静脉麻醉,取仰卧位,经胸骨正中切口进胸。经升主动脉及腔房管插管建立体外循环,需处理弓部的患者改为股动脉插管,需处理房缺、二尖瓣的患者改为上下腔静脉插管,常规建立体外循环。经冠状动脉开口直接灌注心脏停搏液,经冠状静脉窦插入逆灌管,术中心肌保护采用间断顺行灌注结合逆行灌注。如行弓部次全切除手术,采用深低温停循环,先完成远端吻合;需二尖瓣成形患者先完成二尖瓣手术。探查主动脉瓣瓣叶,根据术中测量主动脉瓣瓣环直径,选择较瓣环直径大3~5 mm的人工直血管:David Ⅰ型术式的8例患者选择了32# Terumo直血管;David Ⅴ型术式的3例选用了30# Terumo带窦血管。两种术式均行主动脉根部常规游离至主动脉瓣环以下水平,完全游离出左、右冠状动脉开口呈"钮扣"状,主动脉瓣环以上保留5 mm左右主动脉壁缝合缘。4-0 Prolene滑线带垫片,沿主动脉瓣环下缘间断缝合9~12针,固定人工血管于主动脉瓣环以下,再以5-0 Prolene滑线连续缝合主动脉瓣环以上残留主动脉壁,将其固定于人工血管内壁。人工血管对应冠状动脉开口的位置打孔,以6-0 Prolene滑线连续缝合重建冠状动脉开口。脱垂的主动脉瓣瓣叶以6-0 Prolene滑线连续缝合行对合缘折叠(图1);对右-无融合(RN融合)形成的脊在靠近主动脉内膜侧予以部分切除松解瓣叶,保持瓣叶的中心对合缘在8 mm以上,然后与远端自体血管或人工血管连续缝合。

(1)围术期观察指标:体外循环时间、主动脉阻断时间、术后机械通气时间、重症监护时间以及术后24 h引流量。(2)随访观察人工血管通畅情况及主动脉瓣反流情况:术后早期(患者术后转出监护病房时)以及术后3、6、12个月患者常规复查心脏超声心动,包括左室射血分数、主动脉瓣反流程度[9]、平均跨瓣压差、峰值跨瓣压差及最大血流速度。采用超声连续多普勒法测量最大血流速度,用血流包绕速度积分计算平均跨瓣压差,流速带入伯努利方程计算峰值压差。(3)随访患者是否出现因主动脉瓣反流需二次手术情况。
应用SPSS 19.0统计学软件进行数据分析。服从正态或近似正态分布的计量资料用 ±s表示,偏态分布的计量资料以M(P25, P75)表示。
±s表示,偏态分布的计量资料以M(P25, P75)表示。
术中探查见瓣叶对称、无"脊"型二叶畸形6例(瓣叶中心与两个交界的角度均为180°),右-无融合(RN融合)5例(瓣叶中心到两个交界的角度2例150°、3例160°)。David Ⅰ型手术8例,David Ⅴ型手术3例;所有患者同期行主动脉瓣成形,行次全弓置换4例,行房间隔缺损修补1例,行二尖瓣成形2例。患者无围术期死亡及二次开胸手术。
围术期指标:体外循环时间(246.1±27.2)min,主动脉阻断时间(207.5±21.5)min,术后机械通气时间4.5(3.25, 9.25)h,重症监护时间(2.8±1.5)d,术后24 h引流量(418.2±299.0)mL。
随访观察:11例患者获随访18~30个月,平均22.5个月,截至2020年6月未出现死亡或因主动脉瓣反流所致的二次手术病例。复查心脏超声显示,患者人工血管血流均通畅,主动脉瓣轻微反流8例、轻度反流3例,平均跨瓣压差均<10 mmHg(1 mmHg=0.133 kPa),心功能Ⅰ级8例、Ⅱ级3例,情况较术前明显改善。具体指标见表1。
11例主动脉根部瘤合并主动脉瓣二叶畸形患者David手术前后脏超声指标
11例主动脉根部瘤合并主动脉瓣二叶畸形患者David手术前后脏超声指标
| 观察时间 | 左室射血分数(%, ±s) ±s) | 主动脉瓣反流(例) | 跨瓣压峰压差(mmHg, ±s) ±s) | 跨瓣平均压差(mmHg, ±s) ±s) | 主动脉瓣最大流速(m/s, ±s) ±s) | ||
|---|---|---|---|---|---|---|---|
| 轻微 | 轻度 | 轻中度 | |||||
| 术前 | 50.10±2.98 | 0 | 7 | 4 | 7.36±1.12 | 3.36±0.67 | 1.12±0.15 |
| 术后早期 | 53.36±3.47 | 10 | 1 | 0 | 9.00±1.84 | 5.45±1.29 | 1.27±0.17 |
| 术后3个月 | 54.45±2.81 | 9 | 2 | 0 | 9.00±1.61 | 5.55±1.29 | 1.27±0.11 |
| 术后6个月 | 57.45±3.30 | 8 | 3 | 0 | 9.36±1.50 | 5.91±0.94 | 1.28±0.12 |
| 术后12个月 | 56.64±3.14 | 8 | 3 | 0 | 9.73±1.42 | 6.55±0.93 | 1.32±0.09 |
保留主动脉瓣根部的手术是以David和Feindel[1]提出的Reimplantation术式(David手术)及Sarsam和Yacoub[2]提出的Remodeling术式(Yacob手术)为主,包括基于上述两种术式的改良术式构成的手术方式,在治疗主动脉根部瘤时,可有效地避免人工瓣的植入和终身抗凝、感染性心内膜炎、瓣膜毁损等风险,手术安全性高,远期疗效满意,在全世界范围内广泛开展。在主动脉根部瘤合并BAV的患者中,如果瓣叶无严重钙化等难以修复的情况,保留主动脉瓣的主动脉根部手术联合瓣叶修复安全有效,可避免瓣膜置换,同时远期疗效满意[3,5,10]。Schneider等[10]在20年间进行了357例Yacob手术+主动脉瓣修复术治疗主动脉根部瘤合并BAV,围术期死亡率0.6%,15年79.3%患者无需再次手术。Beckmann等[5]运用David手术治疗了582例主动脉根部瘤患者,其中50例合并BAV的患者均无围术期死亡,10年及20年分别有79%和74%的患者免于二次手术,与三叶瓣患者相比临床疗效相当。Kari等[11]的多中心研究报道此类患者8年免于再次手术率为84%,Mastrobuoni等[12]报道的10年免再手术率为89%。保留主动脉瓣根部的手术运用于主动脉根部瘤合并BAV患者的治疗在国外研究中已经证实安全有效,远期疗效满意,但国内数据较少。刘克敏等[8]对43例主动脉根部瘤合并BAV采用David手术方案,平均随访34个月无死亡及再手术病例。本文报道的11例患者均成功的实施了David术式,术后平均随访22.5个月,患者无死亡和再次手术。根据目前有限的数据提示,该术式用于治疗国人主动脉根部瘤合并BAV,尤其是瓣膜轻度或轻中度反流的患者,可以达到有效避免瓣膜置换的目的,近期疗效满意,具有推广的价值。
根据文献报道,David或Yacob手术在主动脉根部瘤合并BAV的患者中具有安全有效,远期疗效满意的特点,且两种术式并不是再手术的危险因素[3,5,10]。但David[13]指出,在关于保留主动脉瓣的根部手术中,针对BAV的患者主动脉瓣瓣环的扩张是引起瓣膜反流及远期再手术的关键因素,David术式可稳定瓣环,避免远期瓣环扩张,因此更为推荐David术式。
David手术指征的把控及患者的选择是取得良好远期疗效的关键。根据2016年美国主动脉瓣BAV患者主动脉扩张外科治疗指南(推荐等级Ⅱa、证据等级B)、2017年美国瓣膜病指南(推荐等级Ⅱa、证据等级C)及2017年欧洲瓣膜病指南(推荐等级Ⅱa、证据等级C)推荐,对于不合并主动脉瓣关闭不全或者合并少量主动脉瓣反流的BAV患者,其主动脉根部或者升主动脉直径>5.0 cm则需外科手术治疗[9,14,15]。因此,本组纳入的病例主动脉根部直径均>5.0 cm。
主动脉瓣反流加重,需再手术治疗是影响保留主动脉瓣的根部手术远期疗效的关键因素,其危险因素包括:(1)如BAV患者为2个主动脉窦,瓣叶关闭时其中心点与两个交界的夹角约180°时,手术效果较为理想;而在3个主动脉窦的BAV患者中,瓣叶中心到两个交界形成的夹角多在120°到180°之间,夹角越接近180°,远期疗效越满意[3,5,16]。(2)瓣叶钙化,尤其是清除钙化后需要心包片修补瓣叶者,是术后远期主动脉瓣反流复发的主要危险因素[3,10,13]。(3)术前主动脉瓣反流程度在中度及以上,是保留主动脉瓣根部手术术后瓣膜反流复发的独立危险因素[3,17,18]。(4)针对瓣叶脱垂,主动脉瓣交界悬吊修复技术与远期主动脉瓣反流明显相关,而对合缘折叠缩短技术更具备优势[3,19]。(5)瓣叶修复后需维持对合高度在(10.2±3.3)mm,可获得较好的远期疗效[17]。(6)术中食道超声检查,主动脉瓣存在中度及以上的反流也是再次手术的高危因素,针对中度及以上的反流需再次阻断重新修复瓣膜或选择置换[5]。
根据上述危险因素,本组患者在选择时,BAV以2个窦、无融合脊的患者为主,共计6例;3个窦的患者也尽量选择角度接近180°的,5例≥150°。在瓣叶钙化方面,选择交界无明显钙化的,瓣叶钙化灶为散发,不影响瓣叶活动度,且清除钙化后无需心包片重建瓣叶的患者;术前主动脉瓣反流程度均为中度以下,其中轻度7例,轻中度4例;脱垂瓣叶均采取对合缘折叠技术,保持对合缘高度在8 mm以上,同时修复后食道超声检查主动脉瓣反流均在中度以下。本组术中无再次阻断修复的病例。运用上述策略本组患者近期效果良好,平均随访22.5个月,最长30个月无反流复发或加重需要再次手术情况,疗效满意。
综上,对主动脉根部直径>5.0 cm且合并BAV的患者,选择主动脉瓣中度以下反流、瓣叶中心点与两个交界的夹角接近180°、瓣叶钙化不影响瓣叶活动且清除后无需瓣叶重建的患者实施David手术可有效地避免瓣膜置换,术中使用脱垂瓣叶对合缘折叠技术,保证对合缘高度在8 mm以上,食道超声检测修复后主动脉瓣反流控制在中度以下,可取得较好的近期疗效。但由于本组病例数相对偏少,平均随访时间也较短,且为回顾性经验总结,缺乏对照研究,目前所得临床结论仍需扩大样本量及延长随访时间进行进一步的论证。
所有作者均声明不存在利益冲突



























