
了解极低出生体重儿粪便钙卫蛋白(fecal calprotectin,FC)水平的变化趋势及其影响因素,探讨FC检测在极低出生体重儿坏死性小肠结肠炎(necrotizing enterocolitis,NEC)诊断中的应用价值。
选择2018年6月至2019年5月泉州市儿童医院新生儿科收治住院的极低出生体重儿为研究对象,进行前瞻性研究。连续收集出生后第1、7、14、21、28、35天的粪便标本,以及发生NEC急性期及恢复期的粪便标本,采用免疫荧光法定量测定FC含量。
(1)生后1~35 d非NEC极低出生体重儿FC水平为143.5(47.8,391.2)μg/g。单因素分析显示,FC水平随日龄波动,21 d日龄时FC水平最高,随后下降;配方奶喂养、胎膜早破、新生儿败血症、喂养不耐受及孕母产前没有应用糖皮质激素者,FC水平明显升高,差异有统计学意义(P<0.05)。(2)多元协方差分析结果显示,产前应用糖皮质激素(F=10.550,P=0.001)、胎膜早破(F=13.311,P<0.001)、新生儿败血症(F=8.001,P=0.005)、喂养不耐受(F=4.751,P=0.030)、NEC(F=54.566,P<0.001)对FC水平影响差异有统计学意义。在控制产前应用糖皮质激素、胎膜早破、新生儿败血症及喂养不耐受影响后,NEC组和非NEC组患儿FC水平边缘估计均值及其95%CI分别为3 162.3(1 412.5~7 244.4)μg/g、141.3(125.9~162.2)μg/g,差异有统计学意义(t=-7.541,P<0.001)。NEC组患儿急性期及恢复期FC水平分别为3 166.9(1 745.1,6 806.4)μg/g、130.9(97.4,273.9)μg/g,差异有统计学意义(t=10.304,P<0.001);而NEC组轻度与中重度FC水平分别为2 347.9(1 404.4,5 893.4)μg/g、4 114.7(2 764.5,9 208.4)μg/g,差异无统计学意义(t=1.131,P=0.280)。
极低出生体重儿FC水平随日龄波动,并受众多因素的影响。对极低出生体重儿进行FC水平检测,可协助NEC诊断及疗效评估。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
近年来,有关探索早期诊断新生儿坏死性小肠结肠炎(necrotizing enterocolitis,NEC)的生物学标志物一直是国内外研究的热点,然而迄今仍缺少一种可以应用于临床、能够早期识别诊断NEC的客观指标[1,2]。钙卫蛋白(calprotectin)是一种主要存在于中性粒细胞及单核细胞、巨噬细胞中的异源二聚体。粪便中钙卫蛋白主要来自于肠黏膜层内活化的中性粒细胞,当胃肠道存在炎症反应时,中性粒细胞被激活迁移渗出到肠腔内,导致粪便中钙卫蛋白水平升高[3]。目前国内外有关粪便中钙卫蛋白在新生儿胃肠道疾病应用的研究报道甚少,且多以足月儿或生后2周内的早期早产儿为研究对象[4,5]。考虑NEC主要发生于生后2~4周的小早产儿,本研究选择生后5周内的极低出生体重儿为研究对象,动态监测其粪便中钙卫蛋白水平变化,探讨可能影响因素及在NEC诊断中的应用价值。
选择2018月6月至2019年5月泉州市儿童医院新生儿救护中心收治住院的极低出生体重儿为研究对象,进行前瞻性研究。纳入标准:出生体重<1 500 g;入院日龄小于24 h。排除标准:除外先天性胃肠道发育畸形(如先天性巨结肠、肠道闭锁、肠旋转不良、先天性肥厚性幽门狭窄等)、先天性心脏病等先天发育畸形和遗传代谢病患儿。剔除标准:研究终点前收集粪便标本≤4次的患儿。本研究获得医院伦理委员会审核批准(批号:2018年伦审第9号)。
纳入研究的极低出生体重儿于出生后1、7、14、21、28、35 d采集足量粪便标本;并发NEC时,在确诊NEC 24 h内、NEC治疗后重新开奶的24 h内(NEC急性期及恢复期)收集粪便标本。所有收集的粪便标本及时放入无菌塑料管中,密封后置-70 ℃冰箱冷冻保存待检。
具体步骤:(1)从-70 ℃低温冰箱取出冷冻储存的粪便样本,在室温下解冻;(2)将装有3 mL稀释液的15 mL离心管连同采样勺一起称重,将电子天平归零,并用采样勺刮取50 mg样本(准确称重),放入装有稀释液的离心管中;(3)在涡旋混合仪上涡旋至样本无明显块状或只剩白色奶瓣后予置离心机高速离心5 min(转速5 000转/min);(4)取上清液50 μL至700 μL稀释液,于1.5 mL EP管中混匀。取90 μL至粪便钙卫蛋白检测卡,计时15 min后上机检测。
母孕期资料:有无妊娠期糖尿病、先兆子痫、胎膜早破、胎盘早剥,有无发热、咳嗽、绒毛膜羊膜炎等产前感染病史,产前糖皮质激素、硫酸镁及抗生素使用情况。新生儿资料:出生胎龄,性别,出生体重,分娩方式,生后Apgar评分,首次开奶时间,达全肠道喂养时间,喂养方式,母乳喂养有无添加母乳强化剂(human milk fortifier,HMF),相应日龄的24 h喂养量、体重、氧疗方式,有无合并新生儿败血症、新生儿肺炎、新生儿呼吸窘迫综合征(respiratory distress syndrome,RDS)、喂养不耐受、NEC、动脉导管未闭(patent ductus arteriosus,PDA)、支气管肺发育不良(bronchopulmonary dysplasia,BPD)、早产儿视网膜病变(retinopathy of prematurity,ROP)等早产儿并发症及谷氨酰胺、抗生素使用情况。
胎膜早破时间定义为胎膜早破>18 h。NEC诊断标准[6]:按照《实用新生儿学》(第5版)修正Bell分期标准进行诊断和分期,其中NEC轻度指NECⅡA期,NEC中重度包括ⅡB期、ⅢA期、ⅢB期。研究过程中其他早产儿并发症的诊治依据《实用新生儿学》(第5版),并实施标准化喂养方案[7]。研究终点:(1)治愈出院或自动出院或死亡;(2)生后5周;(3)NEC恢复期。符合以上其中1项。
使用SPSS 17.0统计学软件进行统计分析。计量资料选用Kolmogorov-Smirnov检验数据是否符合正态分布;非正态分布、方差不齐的计量资料以中位数(四分位间距)[M(P25,P75)]表示,并进行对数转换成正态分布后以均数±标准差(Mean±SD)表示,两组间均数比较采用独立样本t检验,多组间均数比较采用单因素方差分析(One-Way ANOVA)。计数资料以例(率)表示,组间比较采用卡方检验。对单因素分析有统计学意义及临床可能有意义的影响因素行多元协方差分析。P<0.05为差异有统计学意义。
共纳入极低出生体重儿165例,符合剔除标准78例,最终纳入极低出生体重儿87例,男45例,女42例,胎龄(30.11±1.75)周,出生体重(1 284.59±163.54)g;其中,14例并发NEC,包括轻度NEC 6例,中重度NEC 8例,3例行手术治疗,14例NEC患儿全部治愈出院。纳入研究的87例极低出生体重儿实际收集到粪便标本515份;其中,487份为非NEC极低出生体重儿的粪便标本,NEC急性期、恢复期的粪便标本分别为14份。
487份非NEC粪便标本中钙卫蛋白水平为143.5(47.8,391.2)μg/g,生后第1、7、14、21、28、35天的钙卫蛋白水平分别为165.1(57.4,408.2)、92.3(27.3,329.1)、175.0(59.2,556.8)、276.6(138.5,762.3)、151.2(42.8,296.4)、48.3(31.9,125.6)μg/g,差异有统计学意义(F=10.388,P<0.001)。粪便钙卫蛋白水平随日龄波动,21 d日龄时粪便钙卫蛋白水平最高,极低出生体重儿粪便钙卫蛋白水平变化趋势见图1。


极低出生体重儿粪便钙卫蛋白水平与产前有无胎膜早破、有无应用糖皮质激素相关,有胎膜早破及孕母产前没有应用糖皮质激素者,粪便钙卫蛋白水平明显升高,差异有统计学意义(P<0.05);生后应用配方奶喂养及合并新生儿败血症、喂养不耐受者,粪便钙卫蛋白水平明显升高,差异有统计学意义(P<0.05)。患儿胎龄、性别、分娩方式、出生体重、生后有无低Apgar评分(5 min),孕母有无合并妊娠期糖尿病、先兆子痫、胎盘早剥,产前有无应用抗生素,患儿生后相应日龄的24 h喂养量、氧疗方式,有无合并新生儿肺炎、RDS、PDA等对粪便钙卫蛋白水平影响差异均无统计学意义(P>0.05),见表1。
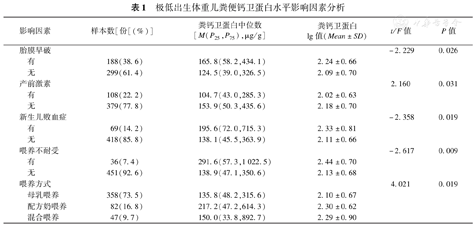
极低出生体重儿粪便钙卫蛋白水平影响因素分析
极低出生体重儿粪便钙卫蛋白水平影响因素分析
| 影响因素 | 样本数[份[(%)] | 粪钙卫蛋白中位数[M(P25,P75),μg/g] | 粪钙卫蛋白lg值(Mean±SD) | t/F值 | P值 | |
|---|---|---|---|---|---|---|
| 胎膜早破 | -2.229 | 0.026 | ||||
| 有 | 188(38.6) | 165.8(58.2,434.1) | 2.24±0.66 | |||
| 无 | 299(61.4) | 124.5(39.0,326.5) | 2.09±0.70 | |||
| 产前激素 | 2.160 | 0.031 | ||||
| 有 | 108(22.2) | 104.7(43.0,285.3) | 2.02±0.63 | |||
| 无 | 379(77.8) | 153.9(50.3,435.6) | 2.18±0.70 | |||
| 新生儿败血症 | -2.358 | 0.019 | ||||
| 有 | 69(14.2) | 195.6(72.0,715.3) | 2.33±0.81 | |||
| 无 | 418(85.8) | 138.1(45.5,363.9) | 2.11±0.66 | |||
| 喂养不耐受 | -2.617 | 0.009 | ||||
| 有 | 36(7.4) | 291.6(57.3,1 022.5) | 2.44±0.70 | |||
| 无 | 451(92.6) | 138.9(47.1,350.6) | 2.13±0.68 | |||
| 喂养方式 | 4.021 | 0.019 | ||||
| 母乳喂养 | 358(73.5) | 135.8(48.2,315.6) | 2.10±0.67 | |||
| 配方奶喂养 | 82(16.8) | 217.2(47.2,614.3) | 2.30±0.62 | |||
| 混合喂养 | 47(9.7) | 150.0(33.8,892.7) | 2.29±0.90 | |||
NEC组粪便钙卫蛋白水平高于非NEC组,两组间差异有统计学意义(t=-14.243,P<0.001),见表2。

极低出生体重儿NEC组与非NEC组粪便钙卫蛋白水平(μg/g)比较
极低出生体重儿NEC组与非NEC组粪便钙卫蛋白水平(μg/g)比较
| 组别 | 样本数[份(%)] | 粪钙卫蛋白中位数[M(P25,P75),μg/g] | 粪钙卫蛋白lg值(Mean±SD) |
|---|---|---|---|
| NEC组 | 14(2.8) | 3 166.9(1 745.1,6 806.4) | 3.55±0.35 |
| 非NEC组 | 487(97.2) | 143.5(47.8,391.2) | 2.15±0.69 |
注:NEC:新生儿坏死性小肠结肠炎。
为控制众多因素对粪便钙卫蛋白水平的影响,以粪便钙卫蛋白水平的对数值为因变量,是否发生NEC为固定变量(NEC=1,无=0),以单因素分析及临床可能有意义的因素为协变量,进行协方差分析,结果见表3。结果显示,产前应用糖皮质激素、胎膜早破、新生儿败血症、喂养不耐受对极低出生体重儿粪便钙卫蛋白影响差异有统计学意义(P<0.05);在控制其他因素对粪便钙卫蛋白水平的影响后,极低出生体重儿NEC组与非NEC组间粪便钙卫蛋白水平差异仍有统计学意义(F=54.566,P<0.001)。
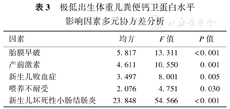
极低出生体重儿粪便钙卫蛋白水平影响因素多元协方差分析
极低出生体重儿粪便钙卫蛋白水平影响因素多元协方差分析
| 因素 | 均方 | F值 | P值 |
|---|---|---|---|
| 胎膜早破 | 5.817 | 13.311 | <0.001 |
| 产前激素 | 4.611 | 10.550 | 0.001 |
| 新生儿败血症 | 3.497 | 8.001 | 0.005 |
| 喂养不耐受 | 2.076 | 4.751 | 0.030 |
| 新生儿坏死性小肠结肠炎 | 23.848 | 54.566 | <0.001 |
极低出生体重儿NEC组和非NEC组粪便钙卫蛋白水平对数值边缘估计均值及其95%CI分别为3.50(3.15~3.86)、2.15(2.09~2.21),反对数后的原粪便钙卫蛋白水平边缘估计均值及其95%CI分别为3 162.3(1 412.5~7 244.4)μg/g、141.3(125.9~162.2)μg/g,两组间差异仍有统计学意义(t=-7.5407,P<0.001)。
NEC组患儿急性期粪便钙卫蛋白水平高于恢复期,差异有统计学意义(t=10.304,P<0.001);NEC组轻度与中重度粪便钙卫蛋白水平差异无统计学意义(t=1.131,P=0.280),见表4。
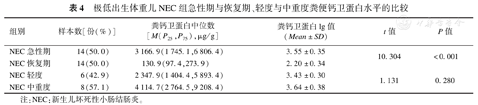
极低出生体重儿NEC组急性期与恢复期、轻度与中重度粪便钙卫蛋白水平的比较
极低出生体重儿NEC组急性期与恢复期、轻度与中重度粪便钙卫蛋白水平的比较
| 组别 | 样本数[份(%)] | 粪钙卫蛋白中位数[M(P25,P75),μg/g] | 粪钙卫蛋白lg值(Mean±SD) | t值 | P值 |
|---|---|---|---|---|---|
| NEC急性期 | 14(50.0) | 3 166.9(1 745.1,6 806.4) | 3.55±0.35 | 10.304 | <0.001 |
| NEC恢复期 | 14(50.0) | 130.9(97.4,273.9) | 2.20±0.34 | ? | ? |
| NEC轻度 | 6(42.9) | 2 347.9(1 404.4,5 893.4) | 3.43±0.30 | 1.131 | 0.280 |
| NEC中重度 | 8(57.1) | 4 114.7(2 764.5,9 208.4) | 3.64±0.38 | ? | ? |
注:NEC:新生儿坏死性小肠结肠炎。
极低出生体重儿由于胃肠道发育不成熟,喂养不耐受、NEC等胃肠道问题日益突出。有研究报道粪便钙卫蛋白检测可应用于极低出生体重儿胃肠道疾病诊疗,但极低出生体重儿粪便钙卫蛋白水平具体变化趋势及影响因素仍是未知的,存在较多争议[4,5,8]。本研究结果显示:非NEC的极低出生体重儿粪便钙卫蛋白水平中位数为143.5(47.8,391.2)μg/g。赵益伟等[4]研究显示,未并发NEC新生儿粪便钙卫蛋白水平波动于77.5~86.0μg/g,均低于本研究水平,考虑其所纳入研究对象、标本采集时间、基础疾病等与本组资料均不一致有关。本研究中单因素分析显示:不同日龄的极低出生体重儿粪便钙卫蛋白水平有差异,在生后21 d达高峰,与2018年Nakayuenyongsuk等[9]的研究结果类似,提示极低出生体重儿粪便钙卫蛋白水平呈动态变化的过程,并且于生后3~4周达高峰,与NEC发病高峰时间相吻合。本研究结果显示日龄对粪便钙卫蛋白水平影响差异无统计学意义,考虑粪便钙卫蛋白水平随日龄波动呈双向性,与本研究未对日龄进行详细的分层分析有关。
本研究显示,胎膜早破、产前糖皮质激素应用为影响极低出生体重儿粪便钙卫蛋白水平的因素之一。推测胎膜早破可能增加产前及产后感染风险,致侵入性细菌在肠道定植或激活导致肠道损伤的炎性介质,最终引起粪便钙卫蛋白水平的升高,甚至诱发NEC的发生。而产前应用糖皮质激素能降低早产儿病死率及RDS、NEC等的发生率[10]。尽管产前应用糖皮质激素的极低出生体重儿粪便钙卫蛋白水平较低,甚至对预防NEC发生存在保护作用,但其确切机制尚不明确。本研究结果显示,并发喂养不耐受的极低出生体重儿粪便钙卫蛋白更高,喂养不耐受为影响极低出生体重儿粪便钙卫蛋白水平的另一重要因素,与Jang等[11]的研究结果一致。
研究显示母乳中含有激素、细胞因子和其他免疫刺激因子可促进婴儿胃肠道免疫系统成熟,纯母乳喂养的婴儿粪便钙卫蛋白水平明显升高[12,13,14],与本研究结论不一致。我们推测与本研究中母乳喂养主要以母乳库捐赠奶喂养为主,母乳中激素、细胞因子和其他免疫刺激因子的活性可能发生变化有关。不同于先前赵益伟等[4]的研究,本研究结果显示,生后1~5周粪便钙卫蛋白水平与分娩方式无显著相关性,考虑主要与赵益伟等的研究均为胎粪有关。与其他绝大部分研究结果[15,16]一致,本研究显示胎龄、性别、体重等其他因素对粪便钙卫蛋白水平无显著影响。
寻找能够早期识别和诊断NEC的生物标志物是近年研究热点[1,2,17,18]。2015年Bin-Nun等[19]研究发现,NEC患儿粪便钙卫蛋白水平明显升高,达3 000 μg/g(2 075,7 875 μg/g)。本研究显示,NEC组患儿粪便钙卫蛋白水平明显高于非NEC组,与Bin-Nun等的研究结果相近。关于发生NEC时粪便钙卫蛋白水平升高的机制,目前还不明确。
本研究显示,极低出生体重儿NEC组急性期粪便钙卫蛋白水平明显高于恢复期。我们认为粪便钙卫蛋白水平在NEC病程中的这种变化有助于极低出生体重儿并发NEC后的疗效评估、胃肠道喂养方案的制定、预测NEC复发等。Zhang等[20]报道早产儿伴有NEC时粪便钙卫蛋白水平明显升高,同时粪便钙卫蛋白水平升高趋势与疾病分期呈正相关,粪便钙卫蛋白有助于NEC疾病严重性的判断。在本研究中,中重度NEC与轻度NEC两组间粪便钙卫蛋白水平差异并无统计学意义,考虑可能与本研究所纳入NEC病例数较少有关。
综上,极低出生体重儿粪便钙卫蛋白水平随日龄波动,并受到众多因素的影响。对极低出生体重儿进行粪便钙卫蛋白水平检测,可协助NEC诊断及疗效评估。另外,该指标的应用仍存在不足,例如:患儿粪便标本的收集受到排便时间的影响;新生儿期粪便钙卫蛋白水平波动范围极大,缺乏正常的参考值范围;同时,涉及肠道发育和损伤的众多因素均有可能影响粪便钙卫蛋白水平。
所有作者均声明不存在利益冲突



























