
报道Corpath GRX新一代介入机器人系统辅助经皮冠状动脉介入治疗手术1例,并探讨其在临床实际应用中的现状与前景。
患者男性,60岁,因"反复胸闷胸痛半年"送入海南省博鳌超级医院。入院前计算机体层血管成像(computed tomography angiography,CTA)检查提示"前降支中段及第一对角支近段重度狭窄",临床诊断为冠状动脉粥样硬化性心脏病、不稳定心绞痛、高血压、2型糖尿病、慢性肾功能不全及痛风。2021年3月13日于海南省博鳌超级医院使用新一代CorPath GRX介入手术机器人完成该系统辅助下国内首例经皮冠状动脉介入治疗术。术后3个月电话随访患者胸痛症状完全改善,无不良事件发生。
检索PubMed、Web of Science、中国知网、万方数据库,检索的英文关键词包括"robotic percutaneous" "coronary intervention" "robotic assisted" ,检索的中文关键词包括"经皮冠状动脉介入治疗术机器人" "介入手术机器人" ,检索时间截至2021年7月31日,共检出符合标准的文献203篇,经进一步筛选标题及摘要获得关于机器人辅助经皮冠状动脉介入治疗的临床研究报道及系统回顾74篇。文献分析显示,自2006年开展首例机器人辅助经皮冠状动脉介入治疗以来,至今全球已累计开展超10 000例手术,包括在慢性闭塞性病变在内的复杂病变中亦有广泛应用。无论在手术效果还是缩短手术时间方面均有较好表现,无严重并发症的相关报道。
CorPath GRX介入手术系统可为经皮冠状动脉介入治疗提供更为精准与标准化的模式,发展前景值得期待。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
1977年,Gruentzig[1]完成世界首例经皮冠状动脉腔内成形术,开启冠状动脉粥样硬化性心脏病(coronary atherosclerotic heart disease,CAHD ) (以下简称冠心病)的经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)时代。1994年起,以daVinci机器人为代表的外科手术机器人系统陆续投入临床使用[2],2012年CorPath第一代介入手术机器人系统获批用于PCI治疗,在精准、稳定的基础上同时解决了介入医生长期处于放射暴露下所带来的放射损伤等相关职业风险,为冠心病介入治疗带来了新的手术模式。CorPath GRX系统在第一代基础上添加"TechnIQ"导丝操控技术,从而对复杂冠状动脉病变的介入治疗带来更大的辅助作用。本文将结合国内首例使用最新一代CorPath GRX系统辅助PCI术病例,探讨介入机器人系统使用现状及发展前景。
患者男性,60岁,因"反复胸闷胸痛半年"送入海南省博鳌超级医院。入院前计算机体层血管成像(computed tomography angiography,CTA )检查提示"前降支中段及第一对角支近段重度狭窄",临床诊断为冠心病、不稳定心绞痛、高血压病(3级,极高危)、2型糖尿病、慢性肾功能不全及痛风。入院期间仍有反复心前区压榨感疼痛。
患者入院后体检提示心率70次/min,血压128/82 mmHg (1 mmHg=0.133 kPa );实验室检查:血肌酐167.2 µmol/L,肝功能、空腹血糖、血常规、肌钙蛋白、肌酸激酶同工酶均正常,排除碘过敏等手术禁忌证后行冠状动脉造影术。患者在充分知情同意后,2021年3月13日于海南省博鳌超级医院接受CorPath GRX机器人辅助PCI介入治疗手术。
CorPath GRX系统是美国食品和药品监督管理局(Food and Drug Administration,FDA)批准的首个应用于冠状动脉介入和外周介入治疗的机器人精准辅助医疗系统。CorPath GRX系统可将介入医师的手工动作转换为精确的机器人辅助下机械动作,并有助于对解剖结构进行精确测量从而确定病变的长度与位置。该系统允许医师在辐射防护下的远程工作站上进行手术,从而大大减少介入医师暴露于电离辐射以及佩戴沉重防护装备而导致的危害。
CorPath GRX系统由床旁操作单元区域和远程操控区域组成(图1),床旁操作单元为模块式设计,由可灵活移动的机械臂和一次性操控盒组成,操控盒内的动力装置可分别操控导管、导丝、球囊或者支架,接受远程操控区域指令完成推送、牵拉和旋转等动作,精细度可精确到1 mm。远程操控区域可放置于射线辐射以外区域,由触摸屏操控系统以及导管、导丝和球囊支架等快速交换设备操控系统组成(图2)。
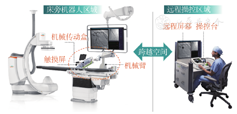

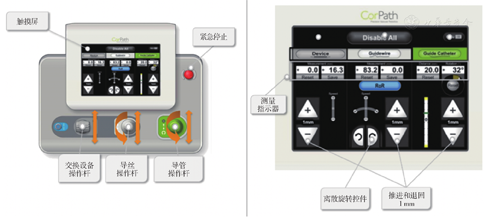

最新一代CorPath GRX系统对于器械的操控更加精细,可以达到亚毫米级,同时在针对术者导丝操作习惯深度学习基础上,增加了TechnIQ技术(包括RoR、Wiggle和Spin等模式),通过机器的精细操作来模拟人工操作的特点,更加符合介入手术的特点,增加机器人操控的多样性,也在一定程度上提高了机器人辅助下手术的成功率。
常规消毒铺巾后,穿刺右侧桡动脉,送入5F多功能造影导管,行冠状动脉造影。造影示左主干未见明显狭窄,左前降支近段狭窄40%,中段弥漫性病变,狭窄最重,达80%,累及第一对角支近段,狭窄50%;左回旋支未见明显狭窄,右冠状动脉近段狭窄30%,中段狭窄30%,左心室后支中段狭窄50%,后降支中段狭窄30%(图3)。
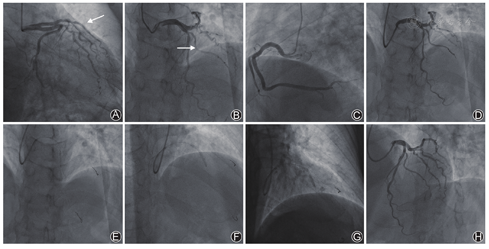

结合患者临床症状、辅助检查以及冠状动脉造影结果,考虑前降支为靶病变,决定行前降支PCI治疗,鉴于病变同时累及对角支近段,为Medina分型1,1,1真性分叉病变,但对角支开口狭窄程度< 70%,考虑首选Provisional支架术式。
选用6 F EBU3.5指引导管,经CorPath GRX辅助系统调整指引导管至左主干开口,分别将0.014 in (1 in=0.025 m)Runthrough及Sion导丝置于CorPath GRX系统不同轨道中,术者在介入操作舱通过操作控制台控制床旁机械臂对驱动盒带内导丝模块进行控制,依次将导丝送入前降支及第一对角支远端,Sion导丝通过对角支开口病变时,利用CorPath GRX系统TechnIQ智能化技术中的"RoR"模式,即将导丝送至对角支开口远处,利用"RoR"模式回退导丝同时旋转角度,从而顺利进入对角支。后续在机器人系统辅助下送入2.5 mm×20 mm半顺应性球囊进行病变预扩张,回撤球囊时利用机器人系统测量病变长度为29.8 mm,进而选用3.0 mm×32 mm药物洗脱支架,利用机械手柄精准移动功能对支架进行定位,以12 atm (1 atm = 101.325 kPa)扩张释放,送入3.25 mm×12 mm非顺应性球囊,以18~20 atm进行后续优化扩张,复查造影提示支架膨胀贴壁良好,对角支近段病变未明显加重,成功回撤全部器械,再次复查冠状动脉造影提示前降支支架植入处未见明显残余狭窄,心肌梗死溶栓治疗(thrombolysis in myocardial infarction,TIMI)血流3级(图3)。手术操作时间为50 min,造影剂用量为60 ml。
患者术后24 h复查心电图、肌钙蛋白和心肌酶,未见明显异常,无手术相关并发症及不良事件发生。出院后3个月电话随访胸痛症状完全改善,无不良事件发生。
检索PubMed、Web of Science、中国知网、万方数据库,检索的英文关键词包括"robotic" "percutaneous coronary intervention" "robotic assisted" ,检索的中文关键词包括"经皮冠状动脉介入治疗机器人" "介入手术机器人" ;检索时间截至2021年7月31日,共检出符合标准的文献203篇,经进一步筛选标题及摘要获得关于机器人辅助PCI的临床研究报道及系统回顾74篇。文献分析显示自2006年开展首例机器人辅助PCI以来,至今全球已累计开展超10 000例手术,包括在慢性闭塞性病变在内的复杂病变中亦有广泛应用。无论在手术效果还是手术时间方面均有较好表现,暂无严重并发症的相关报道。
冠状动脉介入治疗技术的出现与发展为冠心病诊疗模式、患者救治都带来巨大的革命,然而介入技术是基于医护团队放射暴露下的操作,而长时间放射暴露下累积电离辐射可以通过直接或间接作用引起生物分子的电子激发,进而引起敏感组织以及器官的生物学效应。相关研究显示,介入医生因职业风险而罹患不同程度的放射性损伤、白内障、脊柱和骨关节疾病等,亦存在诱发恶性肿瘤和遗传基因突变可能[3,4,5]。
介入机器人辅助PCI概念最早由Beyar等提出,为远程导航系统(remote navigation system, RNS),并于2005年完成早期动物实验,2006年进入临床研究,在入选的18例单支冠状动脉病变患者中,RNS辅助完成17例,导丝成功通过病变,15例置入支架,有效缩短了曝光时间和手术时间,并减少了操作人员辐射暴露剂量[6,7]。Copath200手术机器人系统由美国Corindus公司设计完成,2011年由Granada等[8]完成首项临床研究,研究中8例患者均顺利完成手术,未出现设备相关并发症;在此基础上于2013年公布的PRECISE研究是一项前瞻性、多中心、开放式注册研究,共入选9个中心的164例患者,其中160例患者成功完成手术,操作单元射线剂量较手术台下降了95.2%,证实PCI手术机器人系统已经能够满足简单病变PCI手术的需求,且能够大幅度降低射线辐射剂量[9]。CorPath GRX系统在此基础上进一步提高了器械的操控能力并增加了TechnIQ技术,增加机器人操控在精细动作方面的多样性。
新一代机器人系统的改进与更新,使得机器人辅助下PCI的发展在临床应用更加具有可行性。与单纯人工PCI相比,机器人系统辅助的介入治疗具有其独特的优势。
相对于人工操作,机器人辅助系统能够通过球囊导管穿过病变的时间和速度等参数精确测量病变长度,精度可以达到亚毫米级,避免了视觉和影像下的人工估算模式,从而有效地改善血管病变覆盖不完全的问题,实现精准解剖测量和支架定位控制,帮助术者根据病变长度并且参考血管直径选择合适的支架,进而保证充分覆盖病变和贴壁良好。有研究表明,在简单病变中机器人辅助下PCI的血管病变不完全覆盖发生率为10.7%,而传统人工PCI为28.7%;对于复杂病变,机器人辅助下PCI组的血管病变不完全覆盖发生率为15.4%,显著低于传统人工PCI组的48.0%[10]。
机器人辅助可以克服人手操作的缺陷,在人机协同的状态下使操作更加清晰、精准和稳健,以适当的角度输送导丝、导管、球囊与支架等介入器械,使得器械在输送过程中保持在系统的一定控制之下,可以适应不同导管、导丝的材质、硬度、塑性和操作,避免人工输送器械过程中的不同操作习惯而导致的相关并发症对患者造成不利影响。
机器人的标准化操作可以缩短平均手术时间,降低患者辐射剂量。PRECISE研究中对CorPath机器人辅助下PCI手术与传统人工PCI手术的安全性与有效性进行对比,研究结果显示机器人辅助下PCI组的患者透视时间更短、所受辐射剂量更低、需用造影剂剂量更少。机器人辅助下的PCI手术提高标准化水平、缩短治疗时间,为患者降低20%的射线辐射剂量,并同时降低造影剂使用量[9]。
与传统冠状动脉介入手术相比,CorPath GRX系统辅助下的冠状动脉介入手术可以为医师减少95.2%的辐射暴露。同时,CorPath GRX系统的应用也可减少因佩戴铅防护装备导致的骨科与肌肉损伤[11]。
针对新型冠状病毒肺炎(corona virus disease 2019,COVID-19)或其他接触传染类疾病,机器人的介入可有效减少术者与传染源的接触,降低暴露风险。2020年3月美国费城的Albert Einstein Jewish Hospital利用CorPath GRX系统为一名59岁疑似COVID-19感染的ST段抬高型急性心肌梗死女性患者完成机器人辅助下PCI治疗,实现了医生与患者的有效防护距离[12]。同时,介入手术机器人系统结合高速网络通信手段可开展远程介入手术。2018年12月4日至5日,印度Apex心脏研究所的Patel[13]对5例患者成功实施了世界首次远程PCI手术。相信随着通信技术的发展,这项技术将为分级诊疗的推进提供创新性解决方案。
然而,同时需要看到的是,当前介入机器人系统存在较多不足,相对于人工操作,尚缺乏触觉力学反馈;对于复杂冠状动脉病变,细化导丝等相关器械的操作仍存在较大的改进空间;对于术中需要频繁更换手术器械的病变,机器人系统目前还存在操作繁琐以及耗时较长等缺陷,术中部分操作仍无法完全脱离人工操作等。
PCI机器人手术系统的发展预示着未来PCI手术模式的改变,伴随工程技术与人工智能与5G通信技术的发展,机器人辅助下的PCI手术将为冠状动脉介入手术提供更为精准化与标准化的模式,发展前景值得期待。































