
回顾性分析1例在北京大学人民医院内分泌科新诊断的2型糖尿病患者使用胰岛素强化治疗后,转换为德谷门冬双胰岛素序贯治疗的诊疗过程并进行文献复习。患者为55岁女性,因“血糖升高1个月”入院,入院后完善各项检查,明确诊断为2型糖尿病。予胰岛素泵联合口服降糖药物治疗,逐步简化方案为德谷门冬双胰岛素早餐前16 U一针皮下注射,联合阿卡波糖(50 mg,3次/d)、西格列汀(100 mg,1次/d)、瑞格列奈(0.5 mg,2次/d),血糖控制良好,患者满意。德谷门冬双胰岛素是一种可与其他口服降糖药物联合使用、平稳降糖的新型胰岛素制剂,可用于胰岛素的起始或强化治疗。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
德谷门冬双胰岛素是一种新型可溶性双胰岛素制剂,由70%德谷胰岛素和30%门冬胰岛素组成,兼顾基础及餐时胰岛素作用,可以平稳有效控制血糖。既往临床研究结果显示,其降糖作用优于基础胰岛素。它在与磺脲类药物联用时,需减少剂量,以降低低血糖的发生风险。它还可以作为胰岛素强化治疗后的序贯治疗方案。我们报道1例新诊断的2型糖尿病患者使用胰岛素强化治疗后,转换为德谷门冬双胰岛素治疗的患者,期望为后续同类患者的治疗提供参考。
女,55岁。主因“血糖升高1个月”入院。患者1个月前检测随机血糖为19.8 mmol/L,无“三多一少”症状。后复测空腹血糖为14.69 mmol/L,糖化血红蛋白14.5%,空腹C肽1.8 ng/ml、胰岛素4.21 μU/ml,胰岛细胞抗体、胰岛素抗体及谷氨酸脱羧酶抗体均为阴性,尿糖3+,尿酮体±,尿白蛋白/尿肌酐比值为24.71 mg/g,为进一步诊治收入北京大学人民医院内分泌科。近1个月来患者偶有视物模糊,间断出现尿中有泡沫、手足麻木,无恶心、呕吐,无手套、袜套样改变,无间歇性跛行,无双下肢水肿,精神、食欲可,两便如常,体重无明显变化。既往身体健康,否认冠心病、高血压、高脂血症、慢性肾脏病史。24年前行剖宫产术,术中有输血史。否认食物及药物过敏史。否认吸烟饮酒史。家族中母亲及1个哥哥患有糖尿病,否认高血压、冠心病家族史。
入院查体:身高155.0 cm,体重70.7 kg,体重指数29.4 kg/m2,颈围33 cm,腰围93 cm,臀围104.5 cm。生命体征平稳。神志清楚,精神可。体形肥胖,浅表淋巴结无肿大。甲状腺Ⅱ度肿大,右叶可触及一直径3 cm的结节。心脏、肺、腹无明显异常。双下肢无水肿。病理征未引出。双侧足背动脉搏动正常,双下肢痛觉、温度觉、振动觉正常,双侧10 g弹力丝试验阴性。
实验室及辅助检查:(1)常规化验检查:尿葡萄糖2+,尿酮体±;血清白蛋白37.6 g/L(参考值40~55 g/L),血钾3.44 mmol/L(参考值3.5~5.3 mmol/L);血常规、大便常规、感染四项(乙肝两对半、梅毒抗体、艾滋病抗体和丙肝抗体)、肿瘤标志物筛查、凝血功能、血脂、肝功能、肾功能均未见异常。(2)甲状腺相关检查:甲状腺功能未见异常。(3)骨代谢相关检查:血钙、血磷、甲状旁腺激素及其他骨代谢指标均未见异常。(4)糖尿病相关检查:糖化血红蛋白14.3%,糖化白蛋白37.7%,尿白蛋白/肌酐比值15.31 mg/g,胰岛细胞抗体、胰岛素抗体及谷氨酸脱羧酶抗体均阴性。患者行混合餐糖耐量试验结果见表1。影像学检查腹部超声提示轻度脂肪肝;下肢血管超声提示双侧足背动脉散在斑块;甲状腺超声提示甲状腺多发囊实性结节。
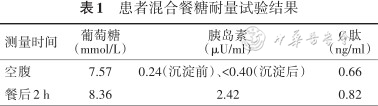
患者混合餐糖耐量试验结果
患者混合餐糖耐量试验结果
| 测量时间 | 葡萄糖 (mmol/L) | 胰岛素 (μU/ml) | C肽 (ng/ml) |
|---|---|---|---|
| 空腹 | 7.57 | 0.24(沉淀前)、<0.40(沉淀后) | 0.66 |
| 餐后2 h | 8.36 | 2.42 | 0.82 |
患者为中年女性,急性病程,多次测空腹血糖>7.0 mmol/L,随机血糖>11.1 mmol/L,糖化血红蛋白>6.5%,体型肥胖,有糖尿病家族史,病程中无“三多一少”症状,无自发酮症酸中毒倾向,考虑为2型糖尿病。患者病程较短,起病时血糖高,查C肽及胰岛素水平尚可,需警惕成年隐匿性自身免疫性糖尿病(latent autoimmune diabetes in adults,LADA)的可能,但患者谷氨酸脱羧酶抗体阴性,可排除LADA诊断。患者无急慢性胰腺炎、胰腺肿瘤、腹部创伤、胰腺切除、肾上腺疾病等其他内分泌疾病、特殊用药、病毒感染病史,可排除上述病因导致的特殊类型糖尿病。入院后予胰岛素泵(0∶00~3∶00用量为0.4 U/h,3:00~7∶00用量为0.7 U/h,7:00~19∶00用量为0.6 U/h,19:00~0∶00用量为0.5 U/h)强化治疗,逐步调整胰岛素泵泵速,患者血糖控制较前改善,逐渐减少胰岛素剂量,加用二甲双胍(0.5 g,3次/d)及西格列汀(100 mg,1次/d)口服降糖治疗。患者血糖进一步改善,空腹血糖维持在6~7 mmol/L,过渡为德谷门冬双胰岛素早餐前16 U及晚餐前14 U皮下注射联合二甲双胍及西格列汀口服治疗,逐步滴定胰岛素剂量。患者血糖控制平稳,进一步简化方案为德谷门冬双胰岛素早餐前16 U一针皮下注射,因患者不能耐受二甲双胍,调整为联合阿卡波糖(50 mg,3次/d)、西格列汀(100 mg,1次/d),并分别于午餐及晚餐前口服瑞格列奈0.5 mg,患者血糖控制良好(表2),遵医嘱出院。

患者入院后的降糖治疗方案及血糖监测结果
患者入院后的降糖治疗方案及血糖监测结果
| 住院时间 | 治疗方案 | 血糖水平(mmol/L) | ||||
|---|---|---|---|---|---|---|
| 胰岛素 | 口服降糖药物 | 空腹 | 午餐前 | 晚餐前 | 睡前 | |
| 第1天 | 胰岛素泵 | 无 | 10.7 | 7.5 | 9.4 | 12.4 |
| 第2天 | 胰岛素泵 | 无 | 8.6 | 9.7 | 11.8 | 10.9 |
| 第3天 | 胰岛素泵 | 二甲双胍 | 7.8 | 9.8 | 11.8 | 6.9 |
| 第4天 | 胰岛素泵 | 二甲双胍 | 8.2 | 12.9 | 7.3 | 6.3 |
| 第5天 | 胰岛素泵 | 二甲双胍+西格列汀 | 7.6 | 6.6 | 6.3 | 9.8 |
| 第6天 | 德谷门冬双胰岛素早餐前16 U+晚餐前14 U | 二甲双胍+西格列汀 | 6.0 | 9.1 | 9.2 | 6.4 |
| 第7天 | 德谷门冬双胰岛素早餐前16 U+晚餐前12 U | 二甲双胍+西格列汀 | 6.3 | 6.7 | 7.7 | 4.3 |
| 第8天 | 德谷门冬双胰岛素早餐前16 U | 西格列汀+阿卡波糖+瑞格列奈 | 6.1 | 8.3 | 7.4 | 6.6 |
| 第9天 | 德谷门冬双胰岛素早餐前16 U | 西格列汀+阿卡波糖+瑞格列奈 | 7.1 | 5.8 | 6.8 | 7.2 |
| 第10天 | 德谷门冬双胰岛素早餐前16 U | 西格列汀+阿卡波糖+瑞格列奈 | 6.3 | 未测 | 未测 | 未测 |
针对新诊断的2型糖尿病患者,糖化血红蛋白>9.0%,遵循《中国2型糖尿病防治指南(2020年版)》建议给予胰岛素强化治疗[1]。采用短期基础-餐时胰岛素模式作为一种强化治疗手段,可显著并持续改善β细胞功能[2],使一半以上患者实现病情逆转[3]。该患者起病时,随机血糖接近20.0 mmol/L,为尽快解除患者高糖毒性对胰岛功能的损害,给予胰岛素泵强化治疗,经过治疗后,患者血糖趋于平稳,接近院内血糖治疗目标。为了使患者院内治疗方案逐渐过渡为出院后居家治疗的方案,我们考虑将其调整为两针胰岛素治疗,选择转换为德谷门冬双胰岛素。根据《德谷门冬双胰岛素临床应用专家指导意见》[4],结合每日总胰岛素剂量,保留70%~80%胰岛素总量,分配至早、晚餐前皮下注射,随着患者胰岛功能恢复,胰岛素逐渐减量,我们进一步简化治疗方案为德谷门冬双胰岛素每日1次皮下注射,联合阿卡波糖、西格列汀、瑞格列奈进行治疗,患者得到满意的治疗效果,血糖达标,未出现低血糖。
德谷门冬双胰岛素是一种新型可溶性双胰岛素制剂,由70%德谷胰岛素和30%门冬胰岛素组成,这两种组分在制剂中独立存在,皮下注射后各自发挥作用。其中,基础成分德谷胰岛素可在皮下注射后形成稳定的可溶性多六聚体储存库,德谷胰岛素单体缓慢分离,持续地吸收入循环系统,并通过脂肪酸侧链与白蛋白可逆性结合,从而发挥超长、平稳的降糖作用[5, 6, 7, 8]。餐时成分门冬胰岛素在注射后以单体的形式,迅速起效[6],发挥餐时胰岛素的作用,有效控制餐后血糖。德谷门冬双胰岛素与基础胰岛素类似物比较,能兼顾空腹和餐后血糖控制;同时,与预混胰岛素比较,减少肩效应(即预混胰岛素的中效成分与餐时成分产生的效应叠加[3],更好地模拟生理胰岛素分泌。临床证据支持在多种临床场景下使用德谷门冬双胰岛素,并可用于胰岛素的起始或强化治疗。
德谷门冬双胰岛素的临床使用方法为随主餐每日1或2次注射。临床试验结果显示,与基础胰岛素相比,德谷门冬双胰岛素可更好地降低2型糖尿病患者的糖化血红蛋白,且不增加低血糖发生风险[9]。应用德谷门冬双胰岛素(每日1次)联合口服降糖药物与基础胰岛素(每日1次)联合速效胰岛素(每日1次)及口服降糖药物疗效相当,德谷门冬双胰岛素(每日2次)联合口服降糖药物与基础胰岛素(每日1次)联合速效胰岛素(每日2或3次)联合口服降糖药物疗效相当[10]。
德谷门冬双胰岛素可以与多种口服药物联合使用,在2型糖尿病患者的德谷门冬双胰岛素临床试验中,均允许其与二甲双胍、二肽基肽酶Ⅳ抑制剂、α-糖苷酶抑制剂、吡格列酮或钠葡萄糖共转运蛋白-2抑制剂等药物联合使用[10, 11]。但是与不同类型降糖药物联合使用时,还需结合口服降糖药物的特点,灵活调整胰岛素用量,降低低血糖、心力衰竭等不良事件发生的风险。德谷门冬双胰岛素每日1次使用时,常与磺脲类药物联合使用,需注意可适当减少磺脲类药物的剂量[12],两者不能在同餐给药[7,11]。当每天使用2次德谷门冬双胰岛素治疗时,不建议与胰岛素促泌剂联用。本例患者经过强化治疗后,胰岛功能有所恢复,过渡到德谷门冬双胰岛素每日1次治疗,联合阿卡波糖、西格列汀、瑞格列奈治疗,需要注意瑞格列奈在午餐、晚餐服用,而德谷门冬双胰岛素在早餐前注射,这样实现有效控制餐后血糖的同时,可避免低血糖的出现。
新型降糖药物的不断研发上市,为糖尿病诊疗提供了更多灵活便捷的治疗方案,帮助有效控制血糖达标,显著降低了低血糖风险,实现血糖的平稳达标,预防和延缓糖尿病及并发症的发生、发展。在应用新型胰岛素德谷门冬双胰岛素时,我们需要结合患者的年龄、胰岛β细胞功能、糖尿病病程、血糖控制目标等具体情况,制定合理的个体化治疗方案。德谷门冬双胰岛素因其独特的药物代谢动力学特点,可以每日1次或2次皮下注射,可以与多种降糖药物联合使用,同时可以作为胰岛素强化治疗后的序贯治疗方案,适宜作为患者居家治疗方案,便于提高治疗依从性,实现血糖的长期达标。
所有作者均声明不存在利益冲突



























