
总结分析儿童经胸室间隔缺损封堵术后残余分流的临床特点,并探讨其发生的危险因素。
回顾性分析2018年1月至2019年7月重庆医科大学附属儿童医院胸心外科手术治疗的127例室间隔缺损患儿的临床资料。其中男72例(56.7%),女55例(43.3%),年龄为(35.35±27.72)个月,根据术后是否发生残余分流将其分为两个组,分析术后发生残余分流的危险因素。术后住院期间残余分流的相关危险因素分析采用Logistic回归分析。
术后发生残余分流18例(14.2%),分流大小为1~2.3 mm。除2例失访外,随访显示15例患儿术后3个月残余分流消失,1例患儿于术后6个月复查提示残余分流已自愈。单因素Logistic回归分析显示术后发生残余分流的相关因素包括:年龄、体重、缺损大小、封堵器直径、缺损处压差、左心室缩短分数(P均<0.05);将上述因素放入多因素Logistic回归显示,封堵器直径与术后残余分流独立相关(OR值为1.950,95%CI为1.325~2.869,P=0.001)。
经胸室间隔缺损封堵术后可发生少量和中量的残余分流。封堵器直径与术后发生残余分流有关。经胸室间隔缺损封堵术后少量或中量残余分流可以自行消失。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
室间隔缺损(ventricular septal defect,VSD)是最常见的先天性心脏病之一,约占先天性心脏病的20%[1]。VSD的治疗方法包括传统体外循环下心内直视修补、经胸小切口室间隔缺损封堵以及经皮穿刺室间隔缺损介入封堵。经食管超声(transesophageal echocardiography,TEE)引导下VSD经胸小切口封堵具有无需体外循环、手术切口小、术后恢复快、无X线暴露、适应证较介入封堵广、安全性良好等优点,已日益得到临床医生、患儿及家长的认可[2,3,4]。与传统体外循环心内直视手术以及介入治疗相似,经胸小切口室间隔缺损封堵也可能发生残余分流、心律失常、瓣膜反流等并发症[5,6]。目前,有关TEE引导下经胸VSD封堵手术后残余分流的研究极少。本研究尝试通过分析TEE引导下经胸治疗VSD患儿术后发生残余分流的近期临床特点,探讨其发生的危险因素。
收集2018年1月至2019年7月重庆医科大学附属儿童医院胸心外科手术治疗的室间隔缺损患儿的临床资料。病例纳入标准:①年龄>3月龄;②VSD大小范围为3~12 mm,伴或不伴有轻至中度肺动脉高压;③TEE引导下经胸小切口治疗的单纯性VSD。排除标准:①经体外循环下手术修复的VSD;②合并有其他需要外科或微创介入治疗的先天性心血管畸形;③术中中转为体外循环下VSD修补;④临床资料不全。
最终有127例患儿入组。其中,男72例(56.7%),女55例(43.3%);年龄为(35.35±27.72)个月,体重为(13.36±6.33)kg。术前超声检查提示膜周型VSD96例(75.6%),干下型VSD29例(22.8%),肌部VSD2例(1.6%)。VSD的分流口大小为(5.17±1.43)mm,范围在3.0~9.9 mm;术前存在肺动脉高压100例(78.7%),术前合并主动脉瓣脱垂61例(48.0%)。
患儿经全身麻醉后,取平卧位,通过TTE评估患儿VSD位置、大小、缺损上下缘情况及主动脉瓣情况。皮肤正中行2~4 cm的小切口并悬吊心包。其中,膜周型VSD患儿皮肤切口位于胸骨下端前方,切开胸骨下段进入纵隔;干下型VSD者皮肤切口位于胸骨中段前方,向左牵拉皮肤切口,经胸骨左缘第3肋间进入纵隔。静脉常规使用0.5 mg/kg行肝素化后,TEE引导定位行右心室表面荷包缝合。干下型VSD或室间隔缺损边缘距主动脉瓣环小于2 mm者选择偏心型封堵器,其余VSD选择等边封堵器。左室面和右室面直径不一致的隧道型VSD依据右室面选择封堵器。选择偏心或等边封堵器后,套管针穿刺右心室壁,取出针芯,在TEE监视下将引导钢丝由右心室穿过室间隔缺损至左心室腔,放置鞘管,释放左室面伞盘,轻轻回拉使左伞盘紧贴室间隔,回撤鞘管至右室腔,释放封堵器腰部和右室面伞盘。偏心伞盘的标记远离主动脉瓣环。TEE即刻评估治疗效果,包括残余分流、心律、封堵器周围结构的功能、血流动力学、封堵器的稳固性、是否出现心包积液等。即刻TEE评估,如果存在残余分流,则增大封堵器型号。当达到质控标准,即无残余分流、瓣膜反流轻中度以下、封堵器稳固、心电图无传导阻滞、无心包积液,将封堵器脱离输送装置,一次性静脉推注1/2肝素总量的鱼精蛋白以中和患儿体内残存的游离肝素,右室表面荷包缝线结扎,止血关胸。如果不符合质控标准,中转为体外循环VSD修补手术。
术后3~7 d常规复查心脏彩色超声及心电图,术后1、3、6、12个月门诊随访心脏彩色超声及心电图。
本研究观察指标包括:①性别、年龄、体重;②缺损大小、缺损类型、是否存在肺动脉高压、是否合并主动脉瓣脱垂、缺损处压差、左心室射血分数(left ventricular ejection fraction,LVEF)、左心室缩短分数(left ventricular fractional shortening,LVFS)、左心室舒张末期内径(left ventricular end diastolic diameter,LVDD)、左心室收缩末期内径(left ventricular end systolic diameter,LVSD);③封堵器直径、封堵器类型、手术时间、麻醉时间;④术后残余分流的程度(分流<2 mm为少量;2 mm≤分流≤4 mm为中量;分流>4 mm为大量)。
采用SPSS 24.0软件进行统计学分析。分类变量以例表示;符合正态分布的连续变量以Mean±SD表示。术后住院期间残余分流的相关危险因素分析采用单因素Logistic回归分析,为避免有意义的因素被筛选出去,我们将P<0.1设定为有统计学意义。将单因素分析有统计学意义的因素纳入多因素Logistic回归分析,采用向前LR法,最终还有统计学意义的即为独立危险因素。P<0.05为差异有统计学意义。
所有患儿麻醉时间为(129.59±26.02)min,手术时间为(63.42±17.95)min,术中膜周型及嵴内型VSD使用等边封堵器81例(63.8%),嵴内型及干下型VSD使用偏心型封堵器46例(36.2%),术中使用封堵器直径为(6.67±1.46)mm。即刻TEE显示无残余分流。
术后3~7 d心脏彩色超声检查提示有残余分流共18例(14.2%),为残余分流组,残余分流宽度1~2.3 mm;其余109例患儿为无残余分流组。两组患儿围手术期一般资料,详见表1。
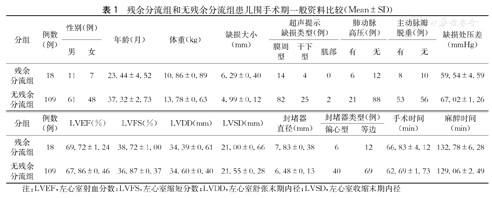
残余分流组和无残余分流组患儿围手术期一般资料比较(Mean±SD)
残余分流组和无残余分流组患儿围手术期一般资料比较(Mean±SD)
| 分组 | 例数(例) | 性别(例) | 年龄(月) | 体重(kg) | 缺损大小(mm) | 超声提示缺损类型(例) | 肺动脉高压(例) | 主动脉瓣脱垂(例) | 缺损处压差(mmHg) | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 男 | 女 | 膜周型 | 干下型 | 肌部 | 有 | 无 | 有 | 无 | ||||||
| 残余分流组 | 18 | 11 | 7 | 23.44±4.52 | 10.86±0.89 | 6.29±0.40 | 14 | 4 | 0 | 6 | 12 | 8 | 10 | 59.54±4.59 |
| 无残余分流组 | 109 | 61 | 48 | 37.32±2.73 | 13.78±0.63 | 4.99±0.12 | 82 | 25 | 2 | 21 | 88 | 53 | 56 | 67.02±1.26 |
| 分组 | 例数(例) | LVEF(%) | LVFS(%) | LVDD(mm) | LVSD(mm) | 封堵器直径(mm) | 封堵器类型(例) | 手术时间(min) | 麻醉时间(min) | |
|---|---|---|---|---|---|---|---|---|---|---|
| 偏心型 | 等边 | |||||||||
| 残余分流组 | 18 | 69.72±1.24 | 38.72±1.00 | 34.39±0.61 | 21.00±0.66 | 7.83±0.38 | 6 | 12 | 66.83±4.12 | 132.78±6.28 |
| 无残余分流组 | 109 | 67.86±0.46 | 36.87±0.37 | 34.60±0.40 | 21.55±0.28 | 6.48±0.13 | 40 | 69 | 62.69±1.73 | 129.06±2.49 |
注:LVEF,左心室射血分数;LVFS,左心室缩短分数;LVDD,左心室舒张末期内径;LVSD,左心室收缩末期内径
全部18例患儿中,有2例患儿因术后失访(1例于出院时残余分流大小为1.6 mm,出院后失访;另1例出院时残余分流大小为1 mm,术后1个月复查提示残余分流为1.6 mm,之后失访)无法获得其残余分流的结局。其余16例患儿分别于术后1、3、6、12个月行心脏彩色超声。其中,术后1个月复查心脏彩色超声提示6例存在残余分流,最大为2 mm;术后3个月再次复查心脏彩色超声提示仅1例存在残余分流,为1.6 mm;术后半年及术后1年复查心脏彩色超声所有患儿均未发现存在残余分流。
单因素分析显示术后发生残余分流的相关因素包括:年龄、体重、缺损大小、封堵器直径、缺损处压差和LVFS(表2)。将单因素分析中差异有统计学意义的因素放入多因素分析中,最终结果显示封堵器直径(OR值为1.950,95%CI:1.325~2.869,P=0.001)与术后残余分流独立相关(表2)。
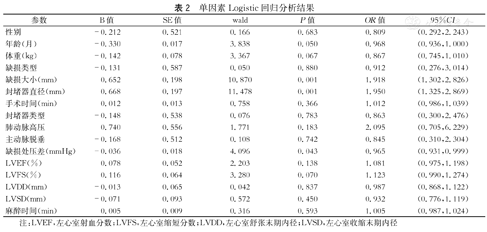
单因素Logistic回归分析结果
单因素Logistic回归分析结果
| 参数 | B值 | SE值 | wald | P值 | OR值 | 95%CI |
|---|---|---|---|---|---|---|
| 性别 | -0.212 | 0.521 | 0.166 | 0.683 | 0.809 | (0.292,2.243) |
| 年龄(月) | -0.330 | 0.017 | 3.838 | 0.050 | 0.968 | (0.936,1.000) |
| 体重(kg) | -0.142 | 0.078 | 3.367 | 0.067 | 0.867 | (0.745,1.010) |
| 缺损类型 | -0.131 | 0.587 | 0.050 | 0.880 | 0.912 | (0.276,3.014) |
| 缺损大小(mm) | 0.652 | 0.198 | 10.870 | 0.001 | 1.918 | (1.302,2.826) |
| 封堵器直径(mm) | 0.668 | 0.197 | 11.478 | 0.001 | 1.950 | (1.325,2.869) |
| 手术时间(min) | 0.012 | 0.013 | 0.758 | 0.366 | 1.012 | (0.986,1.039) |
| 封堵器类型 | -0.148 | 0.538 | 0.076 | 0.783 | 0.863 | (0.300,2.476) |
| 肺动脉高压 | 0.740 | 0.556 | 1.771 | 0.183 | 2.095 | (0.705,6.229) |
| 主动脉脱垂 | -0.168 | 0.512 | 0.108 | 0.742 | 0.845 | (0.310,2.304) |
| 缺损处压差(mmHg) | -0.036 | 0.018 | 4.096 | 0.043 | 0.965 | (0.931,0.999) |
| LVEF(%) | 0.078 | 0.052 | 2.203 | 0.138 | 1.081 | (0.975,1.198) |
| LVFS(%) | 0.116 | 0.064 | 3.280 | 0.070 | 1.123 | (0.990,1.274) |
| LVDD(mm) | -0.013 | 0.065 | 0.042 | 0.837 | 0.987 | (0.868,1.122) |
| LVSD(mm) | -0.071 | 0.093 | 0.572 | 0.450 | 0.932 | (0.776,1.119) |
| 麻醉时间(min) | 0.005 | 0.009 | 0.316 | 0.593 | 1.005 | (0.987,1.024) |
注:LVEF,左心室射血分数;LVFS,左心室缩短分数;LVDD,左心室舒张末期内径;LVSD,左心室收缩末期内径
传统心内直视修补手术效果确切,安全性高,无需术后抗凝治疗,适应证广,是普遍应用于VSD治疗的经典方法。然而,VSD修补手术存在需体外循环、心脏停跳、切开胸骨或肋间、创伤较大、手术时间较长、术后恢复较慢等不足。在过去的二十余年中,经皮穿刺VSD介入封堵术由于美观和微创的特点,在临床得到了广泛的推广,随访结果显示效果良好[3,7,8]。但经皮穿刺VSD介入封堵也有一定的局限性,首先患儿及医务人员在术中会受到放射辐射暴露,其次该术不适合于导丝不易通过的血管、患儿年龄较小、VSD较大以及干下型VSD。经胸小切口VSD封堵术是近十余年发展起来的又一微创治疗方法,其适应证较传统介入封堵更广,无需体外循环和心脏停跳、手术时间较短、无辐射暴露、微创、切口美观、安全、术后恢复快、疗效确切。和室间隔缺损直视修补、经皮介入封堵一样,经胸室间隔缺损封堵较常见的术后并发症也是术后残余分流[1,9]。
作为评价治疗室间隔缺损手术效果的重要指标之一,残余分流得到临床上较广泛的关注。Deng等[10]报道的体外循环下VSD心内直视修补术后残余分流的发生率为31.2%(113/362),Dodge-khatami等[11]报道为35.0%(35/100);Mahimarangaiah等[12]报道的经皮穿刺VSD介入封堵术后残余分流的发生率为29.4%(37/126),严帆等[13]报道为16.1%(30/186),Bai等[14]报道为6.8%(8/117);王欣等[15]报道的超声引导下经胸小切口VSD微创封堵术后残余分流的发生率为6.9%(8/116),张学勤等[16]报道为7.1%(18/255),杨新超等[17]报道为12.5%(5/40)。本研究中经胸小切口VSD微创封堵术后残余分流的发生率为14.2%(18/127),对比既往研究,本研究的结果是可以接受的。
本研究所有患儿术中经食管超声未见残余分流。术后3~7 d复查心脏彩色超声结果显示127例患儿中18例(14.2%)存在1~2.3 mm的残余分流。本研究无大量残余分流,中量残余分流5例,少量残余分流13例。推测原因可能为,术后封堵器因心脏跳动、血液冲击等原因发生位置上的微小移位,出现封堵器边缘新发的分流。Dodge-khatami等[11]发现,体外循环室间隔缺损修补手术后,82.5%(52/63)小于2 mm的VSD残余分流能够自愈,而大于2 mm的残余分流,仅33.3%(3/9)的患儿自愈。本研究中有12例患儿残余分流于术后1个月内自发愈合,3例患儿于术后1~3个月内自发愈合,另1例患儿于术后3~6个月内自发愈合。通过对比既往体外循环下手术的研究,推测经胸室间隔缺损封堵术后的残余分流可能更易于自发愈合,推测与封堵器伞盘的直径大于腰部直径的构造有关,可能有助于残余分流的自愈,当然,这需要进一步的对比研究去证实。
由于经皮介入治疗不适合干下型室间隔缺损,严帆等[13]研究发现室间隔缺损越大和右心室收缩压升高是膜周型室间隔缺损介入治疗手术后早期残余分流的危险因素。本研究单因素Logistic回归分析结果显示,干下型VSD并非术后发生残余分流的危险因素(P>0.05)。本研究显示,经胸小切口室间隔缺损封堵术后早期残余分流危险因素与使用封堵器的大小有关,考虑到术中封堵器的选择与术中超声观察到的患儿缺损大小相关,而本研究提示缺损大小与术后是否发生残余分流无关。考虑可能的原因是室间隔是一个三维立体结构,并非一个简单的二维平面缺口,室间隔缺损测量值在不同切面有差异,而封堵器的使用是确定不变的,同时封堵器的选择也需要通过立体概念综合评估,而不应简单的在缺损直径基础上增加。一般而言,本组的经验是封堵器型号是较缺损大小至少增加1~2 mm,最初选择小型号的封堵器。术中放置封堵器后立即使用TEE评估残余分流、心律、封堵器周围结构的功能、血流动力学、封堵器的稳固性、是否存在心包积液等。在保证放置封堵器安全可靠,符合质量控制标准的基础上,选择最小型号的封堵器。所以缺损大小相同的患儿术中可能选择的封堵器大小并不相同,而对于那些选择了更大型号封堵器的患儿,术后发生残余分流的风险将增加。术中应尽量在符合质量控制标准的基础上选择最小型号的封堵器以减少术后发生残余分流的风险。出院后严密规律随访,特别是3个月以内,应该仔细评估其残余分流的情况。
经胸小切口室间隔缺损封堵术后残余分流一般为中量和少量的分流,可以在术后6个月以内自发愈合。经胸小切口室间隔缺损封堵术后残余分流的发生与封堵器大小有着密切的联系。本研究也存在以下不足:①为单中心回顾性研究,且样本量较小;②本组患儿随访时间较短;③本研究未涉及手术团队(外科医师和超声医师)的学习曲线研究。
所有作者均声明不存在利益冲突



























