
观察吡仑帕奈在儿童药物难治性癫痫添加治疗中的临床疗效。
收集2020年1月至6月在福建医科大学附属协和医院儿科门诊就诊并使用吡仑帕奈添加治疗的药物难治性癫痫患儿临床资料并进行回顾性分析,评估吡仑帕奈在儿童药物难治性癫痫添加治疗中的疗效。吡仑帕奈添加治疗前、后自身对照统计有效率。
共计纳入2~12岁药物难治性癫痫患儿20例,其中男14例,女6例,年龄(5.82±2.39)岁,发病年龄(3.41±1.96)岁,病程(2.40±1.48)年。20例患儿中癫痫部分性发作1例,复杂部分性发作7例,全面性发作1例,未能明确发作6例,癫痫综合征5例。吡仑帕奈添加治疗3个月后,癫痫无发作者4例,发作频率减少>50%者8例,发作持续时间减少者2例,发作抽搐严重程度减少者1例,发作未见明显改善者4例,发作频率增加者1例。以癫痫发作频率减少≥50%为标准,吡仑帕奈添加治疗有效率为60%。
第三代抗癫痫发作药物吡仑帕奈在2~12岁儿童药物难治性癫痫添加治疗中效果明显,并且特别适用于年长患儿复杂部分性发作及特定癫痫综合征。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
癫痫是一种以神经元群高度同步异常放电为特征的神经系统疾病,全球范围内发病率约为50/10万人,患病率为(4~12)/1 000人,至少5 000万~7 000万人受其影响[1,2]。目前药物仍是抗癫痫治疗的首选,但仍有30%~40%的患者癫痫发作不受单药或联合用药控制[3,4],严重影响患者身心健康发展。第三代抗癫痫药吡仑帕奈已在国内上市,这是一种高选择性、非竞争性的α-氨基-3-羟基-5-甲基-4-异 唑丙酸(AMPA)受体拮抗剂,适用于12岁以上的儿童及成人癫痫部分性发作伴或不伴继发全面性发作的添加治疗[5]。AMPA受体是一种谷氨酸受体的亚型,吡仑帕奈通过作用于突触后膜AMPA受体,非竞争性抑制谷氨酸活性从而减少神经元兴奋性,发挥抗癫痫作用[6]。国外研究指出吡仑帕奈在儿童及成人药物难治性癫痫中治疗效果明显[7,8],然而国内儿童药物难治性癫痫的吡仑帕奈临床应用报道极少,疗效评估还有待明确。本研究报道20例2~12岁儿童药物难治性癫痫吡仑帕奈添加治疗,为临床疗效评估提供借鉴。
唑丙酸(AMPA)受体拮抗剂,适用于12岁以上的儿童及成人癫痫部分性发作伴或不伴继发全面性发作的添加治疗[5]。AMPA受体是一种谷氨酸受体的亚型,吡仑帕奈通过作用于突触后膜AMPA受体,非竞争性抑制谷氨酸活性从而减少神经元兴奋性,发挥抗癫痫作用[6]。国外研究指出吡仑帕奈在儿童及成人药物难治性癫痫中治疗效果明显[7,8],然而国内儿童药物难治性癫痫的吡仑帕奈临床应用报道极少,疗效评估还有待明确。本研究报道20例2~12岁儿童药物难治性癫痫吡仑帕奈添加治疗,为临床疗效评估提供借鉴。
病例来源为2020年1月至6月就诊于福建医科大学附属协和医院儿科门诊的药物难治性癫痫患儿。纳入标准[9]:根据发作类型合理使用2种耐受性良好的抗癫痫发作药物后,癫痫发作不能控制者。共计纳入药物难治性癫痫患儿20例。本研究通过福建医科大学附属协和医院医学伦理委员会批准(批准文号:2021KY006)。本研究为回顾性研究,不涉及患儿诊治干预,已豁免知情同意。
患儿在常规使用抗癫痫发作药物的基础上,添加吡仑帕奈(日本Eisai Co.Ltd.公司生产,2 mg)治疗。给药方式为口服,起始剂量为1~2 mg,每7 d或14 d加量1~2 mg,单日治疗剂量维持在2~8 mg,具体的起始剂量、增量以及维持治疗量由个体情况决定,连续用药3个月以上。吡仑帕奈添加治疗过程中出现癫痫发作加重或出现严重不良反应者,立即停止用药。
癫痫发作情况:通过门诊病历收集和电话随访记录患儿在吡仑帕奈添加治疗前、添加治疗后3个月癫痫发作情况;疗效评估[7]:分析患儿癫痫发作情况,定义吡仑帕奈添加治疗后发作频率减少≥50%为有效,否则为无效。
数据的处理采用SPSS 25.0统计软件,计量资料以 ±s表示;统计吡仑帕奈添加治疗前、后自身对照有效率。
±s表示;统计吡仑帕奈添加治疗前、后自身对照有效率。
20例药物难治性癫痫患儿,其中男14例,女6例,年龄2岁8个月~12岁6个月[(5.82±2.39)岁]。首次发病年龄15 d~8岁5个月[(3.41±1.96)岁];病程6个月~5年6个月[(2.40±1.48)年]。癫痫分类:部分性发作1例;复杂部分性发作7例,全面性发作1例,未能明确发作6例,癫痫综合征5例。患儿具体诊疗经过见表1。
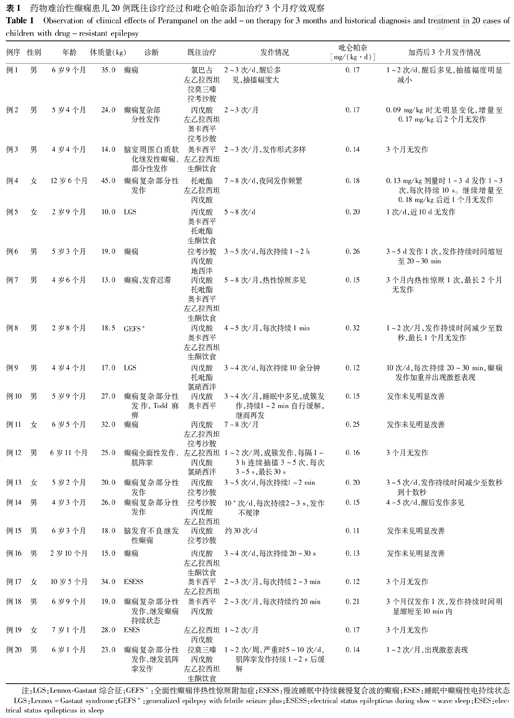
药物难治性癫痫患儿20例既往诊疗经过和吡仑帕奈添加治疗3个月疗效观察
Observation of clinical effects of Perampanel on the add-on therapy for 3 months and historical diagnosis and treatment in 20 cases of children with drug-resistant epilepsy
药物难治性癫痫患儿20例既往诊疗经过和吡仑帕奈添加治疗3个月疗效观察
Observation of clinical effects of Perampanel on the add-on therapy for 3 months and historical diagnosis and treatment in 20 cases of children with drug-resistant epilepsy
| 例序 | 性别 | 年龄 | 体质量(kg) | 诊断 | 既往治疗 | 发作情况 | 吡仑帕奈[mg/(kg·d)] | 加药后3个月发作情况 |
|---|---|---|---|---|---|---|---|---|
| 例1 | 男 | 6岁9个月 | 35.0 | 癫痫 | 氯巴占 | 2~3次/d,醒后多见,抽搐幅度大 | 0.17 | 1~2次/d,醒后多见,抽搐幅度明显减小 |
| 左乙拉西坦 | ||||||||
| 拉莫三嗪 | ||||||||
| 拉考沙胺 | ||||||||
| 例2 | 男 | 5岁4个月 | 24.0 | 癫痫复杂部分性发作 | 丙戊酸 | 2~3次/月 | 0.17 | 0.09 mg/kg时无明显变化,增量至0.17 mg/kg后2个月无发作 |
| 左乙拉西坦 | ||||||||
| 奥卡西平 | ||||||||
| 拉考沙胺 | ||||||||
| 例3 | 男 | 4岁4个月 | 14.0 | 脑室周围白质软化继发性癫痫,部分性发作 | 奥卡西平 | 2~3次/月,发作形式多样 | 0.14 | 3个月无发作 |
| 左乙拉西坦 | ||||||||
| 生酮饮食 | ||||||||
| 例4 | 女 | 12岁6个月 | 45.0 | 癫痫复杂部分性发作 | 托吡酯 | 7~8次/d,夜间发作频繁 | 0.18 | 0.13 mg/kg剂量时1~3 d发作1~3次,每次持续10 s。继续增量至0.18 mg/kg后近1个月无发作 |
| 左乙拉西坦 | ||||||||
| 丙戊酸 | ||||||||
| 例5 | 女 | 2岁9个月 | 10.0 | LGS | 丙戊酸 | 5~8次/d | 0.20 | 1次/d,近10 d无发作 |
| 奥卡西平 | ||||||||
| 托吡酯 | ||||||||
| 生酮饮食 | ||||||||
| 例6 | 男 | 5岁3个月 | 19.0 | 癫痫 | 拉考沙胺 | 3~5次/d,每次持续1~2 h | 0.26 | 3~5 d发作1次,发作持续时间缩短至20~30 min |
| 丙戊酸 | ||||||||
| 地西泮 | ||||||||
| 例7 | 男 | 4岁6个月 | 13.0 | 癫痫,发育迟滞 | 丙戊酸 | 5~8次/月,热性惊厥多见 | 0.15 | 3个月内热性惊厥1次,最长2个月无发作 |
| 托吡酯 | ||||||||
| 奥卡西平 | ||||||||
| 左乙拉西坦 | ||||||||
| 生酮饮食 | ||||||||
| 例8 | 男 | 2岁8个月 | 18.5 | GEFS+ | 丙戊酸 | 4~5次/月,每次持续1 min | 0.32 | 1~2次/月,发作持续时间减少至数秒,最长1个月无发作 |
| 奥卡西平 | ||||||||
| 左乙拉西坦 | ||||||||
| 生酮饮食 | ||||||||
| 例9 | 男 | 4岁4个月 | 17.0 | LGS | 丙戊酸 | 3~4次/d,每次持续10余分钟 | 0.12 | 10次/d,每次持续20~30 min,癫痫发作加重并出现激惹表现 |
| 托吡酯 | ||||||||
| 氯硝西泮 | ||||||||
| 例10 | 男 | 5岁9个月 | 27.0 | 癫痫复杂部分性发作,Todd麻痹 | 丙戊酸 | 3~4次/月,睡眠中多见,成簇发作,持续1~2 min自行缓解,继而再发 | 0.15 | 发作未见明显改善 |
| 奥卡西平 | ||||||||
| 例11 | 女 | 6岁5个月 | 32.0 | 癫痫 | 丙戊酸 | 7~8次/月 | 0.25 | 发作未见明显改善 |
| 左乙拉西坦 | ||||||||
| 拉考沙胺 | ||||||||
| 例12 | 男 | 6岁11个月 | 25.0 | 癫痫全面性发作,肌阵挛 | 左乙拉西坦 | 1~2次/周,成簇发作,每隔1~3 h连续抽搐3~5次,每次3~5 s,最长30 s | 0.16 | 3个月无发作 |
| 丙戊酸 | ||||||||
| 氯硝西泮 | ||||||||
| 例13 | 女 | 5岁2个月 | 20.0 | 癫痫复杂部分性发作 | 丙戊酸 | 3~5次/d,每次持续1~2 min | 0.20 | 3~5次/d,发作持续时间减少至数秒到十数秒 |
| 拉考沙胺 | ||||||||
| 例14 | 男 | 4岁3个月 | 26.0 | 癫痫复杂部分性发作 | 拉考沙胺 | 10+次/d,每次持续2~3 s,发作不规律 | 0.15 | 4~5次/d,醒后发作多见 |
| 丙戊酸 | ||||||||
| 左乙拉西坦 | ||||||||
| 例15 | 男 | 6岁3个月 | 18.0 | 脑发育不良继发性癫痫 | 丙戊酸 | 约30次/d | 0.11 | 发作未见明显改善 |
| 拉考沙胺 | ||||||||
| 例16 | 男 | 2岁10个月 | 15.0 | 癫痫 | 丙戊酸 | 3~4次/d,每次持续20~30 s | 0.13 | 发作未见明显改善 |
| 左乙拉西坦 | ||||||||
| 生酮饮食 | ||||||||
| 例17 | 女 | 10岁5个月 | 34.0 | ESESS | 奥卡西平 | 2~3次/月,每次持续2~3 min | 0.12 | 3个月无发作 |
| 左乙拉西坦 | ||||||||
| 例18 | 男 | 6岁9个月 | 19.0 | 癫痫复杂部分性发作,继发癫痫持续状态 | 奥卡西平 | 2~3次/月,每次持续约20 min | 0.21 | 3个月仅发作1次,发作持续时间明显缩短至10 min内 |
| 丙戊酸 | ||||||||
| 例19 | 女 | 7岁1个月 | 28.0 | ESES | 左乙拉西坦 | 1~2次/月 | 0.17 | 3个月无发作 |
| 丙戊酸 | ||||||||
| 例20 | 男 | 6岁1个月 | 23.0 | 癫痫复杂部分性发作,继发肌阵挛发作 | 拉莫三嗪 | 1~2次/周,严重时5~10次/d,肌阵挛发作持续1~2 s后缓解 | 0.14 | 1~2次/月,出现激惹表现 |
| 丙戊酸 | ||||||||
| 左乙拉西坦 | ||||||||
| 生酮饮食 |
注:LGS:Lennox-Gastaut综合征;GEFS+:全面性癫痫伴热性惊厥附加症;ESESS:慢波睡眠中持续棘慢复合波的癫痫;ESES:睡眠中癫痫性电持续状态 LGS:Lennox-Gastaut syndrome;GEFS+:generalized epilepsy with febrile seizure plus;ESESS:electrical status epilepticus during slow-wave sleep;ESES:electrical status epilepticus in sleep
吡仑帕奈根据个体情况给药,最终维持剂量为0.11~0.32 mg/(kg·d),平均(0.18±0.05) mg/(kg·d)。吡仑帕奈添加治疗3个月后,癫痫无发作者4例,发作频率减少>50%者8例,发作持续时间减少者2例,发作抽搐严重程度减少者1例,发作未见明显改善者4例,发作频率增加者1例。治疗过程中2例患儿出现激惹表现,考虑药物不良反应,其中1例癫痫发作加重的患儿已嘱予停药处理,另1例发作频率减少的患儿嘱予随诊观察。具体情况见表1。
通过20例药物难治性癫痫患儿吡仑帕奈添加治疗3个月的前、后自身对照发现,以癫痫发作频率减少≥50%为标准,吡仑帕奈添加治疗有效12例,无效8例,有效率为60%。此外,20例患儿中癫痫发作完全控制者4例,占20%;癫痫发作加重者1例,占5%;不良反应者2例,占10%。
国际抗癫痫联盟(ILAE)指出[9],根据发作类型合理使用2种耐受性良好的抗癫痫发作药物后,癫痫发作不能控制者称为药物难治性癫痫。目前药物难治性癫痫的发病机制尚不完全明确,可能与多药耐药相关蛋白(MRP)、P糖蛋白(PGP)、细胞凋亡、电压门控离子通道异常等因素有关[10]。第三代抗癫痫发作药物吡仑帕奈是一种非竞争性受体拮抗剂,通过抑制谷氨酸受体AMPA介导的离子通道开放从而发挥抗癫痫作用[6],在12岁以上的青少年及成人药物难治性癫痫添加治疗中效果明显[7,8]。
年龄是吡仑帕奈疗效评估的重要影响因素之一。Biró等[11]在疗效研究中纳入2~17岁药物难治性癫痫患儿58例,平均年龄10.5岁,其结果表明吡仑帕奈添加治疗3个月整体有效率为31.0%(18/58例),癫痫发作,6岁以下儿童有效率仅为9.1%(1/11例),而6~12岁儿童有效率为36.2%(17/47例),12岁以上青少年有效率为40.0%(10/25例)。de Liso等[12]在疗效研究中纳入6~18岁药物难治性癫痫患儿62例,平均年龄14.2岁,其结果表明吡仑帕奈整体有效率为50.0%(31/62例),但在12岁以下儿童中有效率仅为25.0%(2/8例),12岁以上青少年中有效率为53.7%(29/54例)。这些研究表明,年龄是吡仑帕奈疗效的重要影响因素,尽管吡仑帕奈对12岁以下患儿治疗有效,但年长儿的疗效更佳。本研究纳入药物难治性癫痫患儿20例,其中6岁以下患儿11例,6~12岁患儿9例,12岁以上患儿1例,添加吡仑帕奈治疗3个月以观察疗效。以发作频率减少>50%作为有效标准时,吡仑帕奈添加治疗总体有效率为60%(12/20例),其中6岁以下患儿有效率为54.5%(6/11例),6~12岁患儿有效率为62.5%(5/8例),12岁以上患儿有效率为100%(1/1例)。与国外研究[11,12]相比,本研究同样显示出年长患儿吡仑帕奈疗效更好的趋势。
癫痫分类是吡仑帕奈疗效评估的另一个重要影响因素。Steinhoff等[13]研究指出,吡仑帕奈在复杂部分性发作中有效率为48.0%,在全面强直-阵挛发作中有效率为57.0%。Biró等[11]发现,吡仑帕奈在症状性癫痫中有效率为38%,在癫痫综合征中有效率仅为18%,症状性癫痫疗效优于癫痫综合征。然而,他们同时也发现吡仑帕奈在Dravet综合征中有效率为50%,在Lennox-Gastaut综合征(LGS)中有效率为40%,但在West综合征中则不起作用。不同癫痫综合征的吡仑帕奈疗效可能存在较大差异。本研究纳入症状性癫痫2例,其中1例诊断为脑室周围白质软化继发性癫痫,吡仑帕奈治疗有效;另1例诊断为脑发育不良继发性癫痫,治疗无效。纳入癫痫综合征5例,其中1例患儿诊断为全面性癫痫伴热性惊厥附加症(GEFS+)伴有SCN1A杂合突变,吡仑帕奈治疗有效提示吡仑帕奈可能对离子通道异常的癫痫综合征具有一定疗效。有研究表明AMPA受体阻滞可有效消除痫样放电[14],本研究中1例诊断为慢波睡眠中持续棘慢复合波的癫痫(ESESS),另1例患儿诊断为睡眠中癫痫性电持续状态(ESES),两者均在吡仑帕奈添加治疗后2~3个月无临床发作,提示吡仑帕奈可能对睡眠期脑区广泛性或局灶性持续放电具有良好的抑制效应,但目前还未见吡仑帕奈用于ESES或ESESS的案例报道。LGS具有耐药性倾向,然而研究表明吡仑帕奈在LGS添加治疗中效果显著,69.2%的患儿癫痫发作可得到显著改善,15.4%则发作加重[15],而本研究中1例LGS治疗有效,另1例出现发作加重。癫痫复杂部分性发作伴或不伴全面发作是吡仑帕奈的适应证,本研究纳入癫痫复杂部分性发作7例,吡仑帕奈添加治疗后5例发作频率减少>50%,有效率71.4%,疗效显著。1例全面性发作癫痫患儿,吡仑帕奈添加治疗有效。6例癫痫患儿未能明确发作类型(包括上述1例脑发育不良继发性癫痫),添加治疗后3例癫痫发作得到改善。
此外,人群种族、疗效观察指标也会对吡仑帕奈的疗效评估产生影响。Tsai等[16]发现,与非亚洲人群相比,亚洲人群的吡仑帕奈的疗效与耐受性更好。本研究中纳入种族均为亚洲人群,可能对疗效评估产生正面作用。研究表明吡仑帕奈可以显著降低发作持续时间和严重程度[17]。在本研究中2例患儿在吡仑帕奈添加治疗后发作持续时间减少50%以上,1例患儿抽搐严重程度明显减轻,尽管这3例患儿添加吡仑帕奈后癫痫发作的持续时间和剧烈程度有所改善,但癫痫发作次数并没有减少,不符合疗效评估标准,未予纳入治疗有效的范畴。
20例药物难治性患儿,吡仑帕奈添加治疗有效者12例(60%),其中4例(20%)达到无癫痫发作;无效者8例(40%),其中1例(5%)癫痫发作频率加重。本研究治疗有效率与国外研究[11,12]相比较高,可能与人群种族、癫痫类型构成、随访时长、纳入例数等因素相关。吡仑帕奈在2~12岁儿童药物难治性癫痫添加治疗中的有效性,尤其适用于年长患儿复杂部分性发作及特定癫痫综合征,值得重视。未来将组织前瞻性、大样本随机对照研究,以更全面了解我国儿童癫痫添加治疗的疗效和安全性。
所有作者均声明不存在利益冲突



























