
通过筛查了解徐州地区新生儿希特林蛋白缺乏所致新生儿肝内胆汁淤积症(neonatal intrahepatic cholestasis caused by cirtin deficiency,NICCD)的发病情况、临床特征和基因突变特点。
对2015年9月至2020年9月徐州地区采用串联质谱技术进行遗传代谢病筛查的新生儿进行前瞻性研究,筛查疑似的患儿进一步通过尿有机酸及SLC25A13基因突变分析确诊,对确诊病例的临床表现、生化指标改变、基因突变特点、治疗及预后进行分析。
共筛查活产新生儿468 494名,疑似患儿112例,进行尿有机酸分析95例,SLC25A13基因突变分析95例,共确诊NICCD患儿13例,患病率1∶36 038。多数患儿早期表现为黄疸消退延迟、喂养困难及体重不增等。生化指标改变包括胆汁酸升高、肝功能异常、甲胎蛋白异常升高、低血糖、血红蛋白降低、凝血功能异常及血氨增高等。血氨基酸及酰基肉碱谱检测提示瓜氨酸、蛋氨酸、精氨酸、酪氨酸、苯丙氨酸等特异性升高,部分伴酰基肉碱轻度升高;尿有机酸分析主要表现为4-羟基苯乳酸和4-羟基苯丙酮酸升高。13例患儿均进行基因检测,共检出13种突变类型,分别为c.852_855delTATG、c.511dupG、c.1638_1660dup、IVS16ins3kb、c.1078C>T、c.615+5G>A、c.742G>A、c.44G>A、c.1311+1G>A、c.1399C>T、c.889G>T、c.1177+1G>A、c.1841+3_1841+4del,其中c.852_855delTATG最常见,5种为新发变异,新发变异中c.1841+3_1841+4del、c.511dupG和c.889G>T预测为有害变异。确诊病例予以饮食管理和对症治疗,均于1岁内症状缓解,生化指标明显改善。
徐州地区NICCD患病率为1∶36 038,c.852_855delTATG变异出现频率最高。共检测出5个新发变异位点,扩展了SLC25A13基因变异谱。NICCD患儿多数预后良好,需早期诊断和治疗,终身随访。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
希特林蛋白缺乏症是由SLC25A13基因变异所致希特林蛋白结构和功能异常而引起的一种遗传代谢病,为常染色体隐性遗传[1],包括希特林蛋白缺乏所致新生儿肝内胆汁淤积症(neonatal intrahepatic cholestasis caused by cirtin deficiency,NICCD)、希特林编码基因缺陷导致的生长发育落后和血脂异常、成年期发作的瓜氨酸血症Ⅱ型3种不同临床表型[2]。希特林蛋白主要参与体内烟酰胺腺嘌呤二核苷酸氧化、葡萄糖异生、氨基酸代谢、脂类代谢、有氧糖酵解及尿素循环等代谢过程,其缺陷可导致相应的代谢紊乱[2]。NICCD是目前儿科最主要的希特林蛋白缺乏症类型,多在新生儿期或婴儿期发病[3]。串联质谱技术应用于新生儿筛查可早期发现包括希特林蛋白缺乏症在内的多种遗传代谢病,通过早期诊断和治疗,可避免患儿智力发育落后及代谢失调的发生。
我国不同地区间NICCD患病率有显著差异,长江以南明显高于长江以北[4],北方地区报道较少。本研究基于徐州市新生儿疾病筛查中心2015年9月至2020年9月通过新生儿血氨基酸及酰基肉碱谱、尿有机酸谱筛查联合基因确诊NICCD患儿的临床资料进行分析,探讨本地区NICCD的患病率、基因谱特点及预后,为临床管理和决策提供数据支持。
选择2015年9月至2020年9月徐州地区5个区、5个县具备接产资格医院出生的、家长知情且同意参与新生儿疾病筛查的活产新生儿常规进行串联质谱筛查,对通过筛查和基因检测确诊的NICCD患儿进行前瞻性研究。本研究通过本院医学伦理委员会审批,批准号[2015]伦审第(06)号。所有研究对象监护人均签署知情同意书。
1.新生儿NICCD筛查及诊断流程:新生儿出生后72~120 h采足跟血送至我院新生儿筛查中心检测。应用Xevo TQD型液相色谱串联质谱仪(美国Waters公司)和NeoBase新生儿非衍生法筛查试剂盒(PerKin Elmer公司)进行血氨基酸谱和酰基肉碱谱检测分析。NICCD筛查阳性切值为瓜氨酸>40 μmol/L,初筛阳性者召回复查,如果第2次检测仍为阳性,则转至本中心进一步确诊。
2.基因分析:瓜氨酸连续2次以上高于阳性切值,除外早产、肝功能不全等继发因素后做基因检测。采集患儿外周静脉血4 ml EDTA抗凝,由浙江博圣生物技术股份有限公司完成检测。基因测序结果与dbSNP、1000Genomes、ESP6500、ClinVar及PubMed等公共数据库资料进行比对,获得可疑变异,并依照Sanger测序技术进行验证,对患儿父母基因DNA进行相应基因位点检测。
3.NICCD临床诊断标准[5]:(1)新生儿筛查阳性或新生儿期出现黄疸消退延迟;(2)胆汁淤积;(3)血氨基酸分析瓜氨酸、精氨酸、蛋氨酸等多种氨基酸增高;(4)尿液中半乳糖、4-羟基苯乳酸、4-羟基苯丙酮酸等升高;(5)携带SLC25A13基因致病变异。以上5项中至少符合(1)+(2)+(3)以上者考虑NICCD诊断。
4.治疗:(1)急性期:包括针对胆汁淤积性黄疸、肝损害、严重低蛋白血症、凝血功能明显异常合并出血倾向、严重贫血等对症支持治疗,高氨血症患儿每日给予精氨酸100~250 mg/kg口服;同时改无乳糖、强化中链三酰甘油特殊配方奶粉喂养。(2)恢复期:婴幼儿期继续给予无乳糖奶粉喂养,添加辅食后予饮食结构调整(高蛋白、高脂肪、低碳水化合物饮食),同时补充维生素A、D、E、K等脂溶性维生素。确诊病例急性期住我院新生儿科治疗。
5.随访:由本中心联合儿童保健科在出院后1个月、2个月随访,之后每3个月随访1次至1岁,2~3岁每4个月进行门诊及电话随访,6岁之后每半年随访1次,随访截止至2020年9月30日。随访内容包括血氨基酸、酰基肉碱谱、尿有机酸谱、血常规、肝肾功能、电解质、血糖、甲胎蛋白、血氨、肝脏超声检查,以及身长/身高、体重、智力发育评估等。身长/身高和体重标准参考文献[6],智力发育评估采用Gesell发育量表(1992年北京修订版),发育商(development quotient,DQ)<75分为智力低下。
2015年9月至2020年9月徐州地区共分娩新生儿509 798名;其中活产新生儿509 289名;家长同意参与新生儿疾病筛查468 546名;因72 h内死亡没有采集到血标本52例;完成初筛新生儿468 494名,其中99%为汉族,男∶女为1.2∶1;早产和低出生体重儿分别占8.2%(38 417)和7.1%(33 263),初筛日龄中位数为5 d(3~38 d)。
所有筛查新生儿中977例(0.21%)初筛阳性,复测后112例阳性,其中13例失访,99例转入本中心进一步诊治,82例排除诊断,4例拒绝行相关检查后失访,最终13例确诊为NICCD,本地区NICCD患病率1∶36 038。确诊病例中男8例,女5例;顺产5例,剖宫产8例;胎龄(39.0±0.9)周,出生体重(2 790±485)g,确诊日龄(57.0±9.7)d。2015年9月至2020年9月本中心筛查及确诊情况见表1。
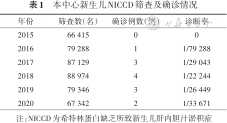
本中心新生儿NICCD筛查及确诊情况
本中心新生儿NICCD筛查及确诊情况
| 年份 | 筛查数(名) | 确诊例数(例) | 诊断率 |
|---|---|---|---|
| 2015 | 66 415 | 0 | 0 |
| 2016 | 79 288 | 1 | 1/79 288 |
| 2017 | 87 129 | 3 | 1/29 043 |
| 2018 | 88 974 | 4 | 1/22 244 |
| 2019 | 79 346 | 3 | 1/26 449 |
| 2020 | 67 342 | 2 | 1/33 671 |
注:NICCD为希特林蛋白缺乏所致新生儿肝内胆汁淤积症
1.生化检测结果:所有患儿初诊时均有总胆红素、直接胆红素、γ-谷氨酰转移酶、总胆汁酸升高;甲胎蛋白均升高,2例>正常高值5~10倍,9例>正常高值500倍,2例>正常高值1 000倍;总蛋白、白蛋白降低、谷草转氨酶升高及活化部分凝血活酶时间、凝血酶原时间延长各12例;低血糖2例、血红蛋白降低7例、血氨升高1例。
2.血氨基酸谱、酰基肉碱谱和尿有机酸检测结果:血氨基酸谱主要表现为瓜氨酸、蛋氨酸、精氨酸、酪氨酸、甘氨酸、苯丙氨酸增高;部分患儿血酰基肉碱谱升高,以游离肉碱和长链酰基肉碱C18∶1、C12、C14、C16、C18∶2、C16OH、C18OH升高为主;尿有机酸分析主要表现为4-羟基苯乳酸和4-羟基苯丙酮酸升高。见表2。
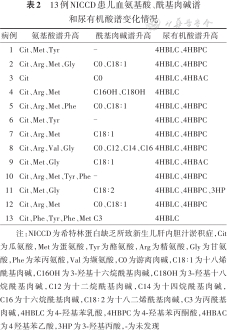
13例NICCD患儿血氨基酸、酰基肉碱谱和尿有机酸谱变化情况
13例NICCD患儿血氨基酸、酰基肉碱谱和尿有机酸谱变化情况
| 病例 | 氨基酸谱升高 | 酰基肉碱谱升高 | 尿有机酸谱升高 |
|---|---|---|---|
| 1 | Cit、Met、Tyr | - | 4HBLC、4HBPC |
| 2 | Cit、Arg、Met、Gly | C0、C18∶1 | 4HBLC、4HBPC |
| 3 | Cit | C0 | 4HBLC、4HBAC |
| 4 | Cit、Arg、Met | C16OH、C18OH | 4HBLC |
| 5 | Cit、Arg、Met、Phe | C0、C18∶1 | 4HBLC、4HBPC |
| 6 | Cit、Met、Tyr | - | 4HBLC、4HBPC |
| 7 | Cit、Arg、Met | C18∶1 | 4HBLC、4HBPC |
| 8 | Cit、Arg、Val、Gly | C0、C12、C14、C16 | 4HBLC、4HBPC |
| 9 | Cit、Met、Gly | C18∶1 | 4HBLC、4HBAC |
| 10 | Cit、Arg、Met、Tyr、Phe | - | 4HBLC、4HBPC |
| 11 | Cit、Met、Gly | C18∶2 | 4HBLC、4HBPC、3HP |
| 12 | Cit、Arg、Met | C0、C18∶1 | 4HBLC、4HBPC |
| 13 | Cit、Phe、Tyr、Phe、Met | C3 | 4HBLC |
注:NICCD为希特林蛋白缺乏所致新生儿肝内胆汁淤积症,Cit为瓜氨酸,Met为蛋氨酸,Tyr为酪氨酸,Arg为精氨酸,Gly为甘氨酸,Phe为苯丙氨酸,Val为缬氨酸,C0为游离肉碱,C18∶1为十八烯酰基肉碱,C16OH为3-羟基十六烷酰基肉碱,C18OH为3-羟基十八烷酰基肉碱,C12为十二烷酰基肉碱,C14为十四烷酰基肉碱,C16为十六烷酰基肉碱,C18∶2为十八二烯酰基肉碱,C3为丙酰基肉碱,4HBLC为4-羟基苯乳酸,4HBPC为4-羟基苯丙酮酸,4HBAC为4羟基苯乙酸,3HP为3-羟基丙酸,-为未发现
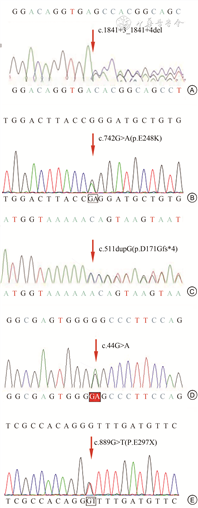
3.基因检测结果:13例患儿均应用二代高通量测序进行SLC25A13基因变异分析,共检出13种基因变异类型,分别为c.852_855delTATG、c.511dupG、c.1638_1660dup、IVS16ins3kb、c.1078C>T、c.615+5G>A、c.742G>A、c.44G>A、c.1311+1G>A、c.1399C>T、c.889G>T、c.1177+1G>A、c.1841+3_1841+4del,经验证分别来自父亲和母亲,见表3。最常见的是c.852_855del TATG移码变异;c.1841+3_1841+4del、c.742G>A、c.511dupG、c.44G>A、c.889G>T为新发变异,其中c.1841+3_1841+4del、c.511dupG和c.889G>T的致病性经MutationTaster、SIFT和FATHMM预测,提示为疑似致病变异。5种新发变异位点的外显子Sanger测序图,见图1。
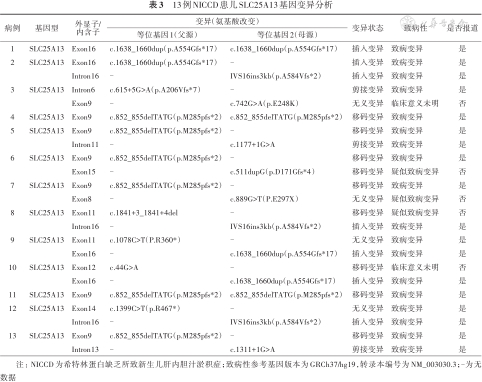
13例NICCD患儿SLC25A13基因变异分析
13例NICCD患儿SLC25A13基因变异分析
| 病例 | 基因型 | 外显子/内含子 | 变异(氨基酸改变) | 变异状态 | 致病性 | 是否报道 | |
|---|---|---|---|---|---|---|---|
| 等位基因1(父源) | 等位基因2(母源) | ||||||
| 1 | SLC25A13 | Exon16 | c.1638_1660dup(p.A554Gfs*17) | c.1638_1660dup(p.A554Gfs*17) | 插入变异 | 致病变异 | 是 |
| 2 | SLC25A13 | Exon16 | c.1638_1660dup(p.A554Gfs*17) | - | 插入变异 | 致病变异 | 是 |
| Intron16 | - | IVS16ins3kb(p.A584Vfs*2) | 插入变异 | 致病变异 | 是 | ||
| 3 | SLC25A13 | Intron6 | c.615+5G>A(p.A206Vfs*7) | - | 剪接变异 | 致病变异 | 是 |
| Exon9 | - | c.742G>A(p.E248K) | 无义变异 | 临床意义未明 | 否 | ||
| 4 | SLC25A13 | Exon9 | c.852_855delTATG(p.M285pfs*2) | c.852_855delTATG(p.M285pfs*2) | 移码变异 | 致病变异 | 是 |
| 5 | SLC25A13 | Exon9 | c.852_855delTATG(p.M285pfs*2) | - | 移码变异 | 致病变异 | 是 |
| Intron11 | - | c.1177+1G>A | 剪接变异 | 致病变异 | 是 | ||
| 6 | SLC25A13 | Exon9 | c.852_855delTATG(p.M285pfs*2) | - | 移码变异 | 致病变异 | 是 |
| Exon15 | - | c.511dupG(p.D171Gfs*4) | 移码变异 | 疑似致病变异 | 否 | ||
| 7 | SLC25A13 | Exon9 | c.852_855delTATG(p.M285pfs*2) | - | 移码变异 | 致病变异 | 是 |
| Exon8 | - | c.889G>T(P.E297X) | 无义变异 | 疑似致病变异 | 否 | ||
| 8 | SLC25A13 | Exon11 | c.1841+3_1841+4del | - | 移码变异 | 疑似致病变异 | 否 |
| Intron16 | - | IVS16ins3kb(p.A584Vfs*2) | 插入变异 | 致病变异 | 是 | ||
| 9 | SLC25A13 | Exon11 | c.1078C>T(P.R360*) | - | 无义变异 | 致病变异 | 是 |
| Exon16 | - | c.1638_1660dup(p.A554Gfs*17) | 插入变异 | 致病变异 | 是 | ||
| 10 | SLC25A13 | Exon12 | c.44G>A | - | 移码变异 | 临床意义未明 | 否 |
| Exon16 | - | c.1638_1660dup(p.A554Gfs*17) | 插入变异 | 致病变异 | 是 | ||
| 11 | SLC25A13 | Exon9 | c.852_855delTATG(p.M285pfs*2) | c.852_855delTATG(p.M285pfs*2) | 移码变异 | 致病变异 | 是 |
| 12 | SLC25A13 | Exon14 | c.1399C>T(p.R467*) | - | 无义变异 | 致病变异 | 是 |
| Intron16 | - | IVS16ins3kb(p.A584Vfs*2) | 插入变异 | 致病变异 | 是 | ||
| 13 | SLC25A13 | Exon9 | c.852_855delTATG(p.M285pfs*2) | - | 移码变异 | 致病变异 | 是 |
| Intron13 | - | c.1311+1G>A | 剪接变异 | 致病变异 | 是 | ||
注:NICCD为希特林蛋白缺乏所致新生儿肝内胆汁淤积症;致病性参考基因版本为GRCh37/hg19,转录本编号为NM_003030.3;-为无数据

13例患儿生后半个月内均有黄疸消退延迟,5例出现不同程度的肝肿大,2例有白陶土色大便,2例生后出现腹泻、喂养困难、体重不增等。
所有病例确诊后即改用无乳糖并强化中链三酰甘油配方奶粉喂养,并补充脂溶性维生素,13例患儿经保肝、利胆、退黄等对症治疗及饮食调整后,6个月内临床症状及生化结果明显改善。病例6因“呕吐伴嗜睡”住院治疗,头颅CT示蛛网膜下腔出血,生化检测示血氨、甲胎蛋白异常增高,凝血功能异常,急性期予以精氨酸降血氨、补充维生素K、输注新鲜血浆改善凝血功能等对症支持治疗,同时改用无乳糖配方奶粉喂养,1个月后临床症状及生化指标均明显改善。
13例患儿均得到随访,至2020年9月,最小5个月,最大3岁10个月。其中3例(病例3、6、11)在婴儿早期出现明显生长发育落后,身长、体重均<-2SD,给予喂养指导及营养补充后2岁时身长、体重追赶至~1SD;1例(病例8)在6月龄时智力评估明显落后(DQ<70分),辅助康复训练治疗,1岁3个月智力评估基本恢复正常(DQ>85分);3例(病例2、4、7)1岁后出现明显饮食偏好,喜食肉类、豆类,拒食或少食高碳水化合物类食物;其他患儿身长/身高、体重及智力评估均正常,13例NICCD患儿的临床资料、治疗及随访情况见表4。
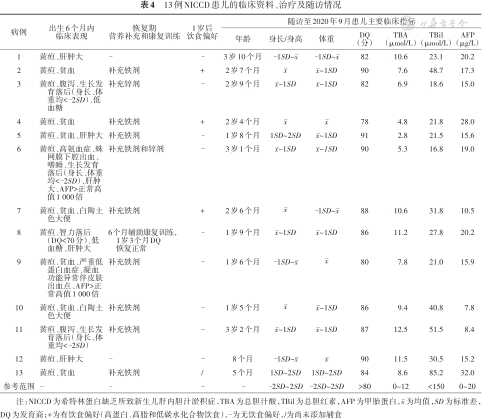
13例NICCD患儿的临床资料、治疗及随访情况
13例NICCD患儿的临床资料、治疗及随访情况
| 病例 | 出生6个月内临床表现 | 恢复期营养补充和康复训练 | 1岁后饮食偏好 | 随访至2020年9月患儿主要临床指标 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 年龄 | 身长/身高 | 体重 | DQ(分) | TBA (μmol/L) | TBil (μmol/L) | AFP (μg/L) | ||||
| 1 | 黄疸、肝肿大 | - | - | 3岁10个月 | -1SD~ | -1SD~ | 82 | 10.6 | 23.1 | 20.2 |
| 2 | 黄疸、贫血 | 补充铁剂 | + | 2岁7个月 | ~1SD | 90 | 7.6 | 48.7 | 17.3 | |
| 3 | 黄疸、腹泻、生长发育落后(身长、体重均<-2SD)、低血糖 | 补充锌剂 | - | 2岁9个月 | ~1SD | ~1SD | 82 | 6.9 | 18.6 | 15.0 |
| 4 | 黄疸、贫血 | 补充铁剂 | + | 2岁4个月 | 78 | 4.8 | 21.8 | 28.0 | ||
| 5 | 黄疸、贫血、肝肿大 | 补充铁剂 | - | 1岁8个月 | 1SD~2SD | ~1SD | 91 | 2.8 | 21.5 | 15.6 |
| 6 | 黄疸、高氨血症、蛛网膜下腔出血、嗜睡、生长发育落后(身长、体重均<-2SD)、肝肿大、AFP>正常高值1 000倍 | 补充铁剂和锌剂 | - | 3岁1个月 | ~1SD | ~1SD | 90 | 5.3 | 16.8 | 19.0 |
| 7 | 黄疸、贫血、白陶土色大便 | 补充铁剂 | + | 2岁6个月 | -1SD~ | 88 | 10.6 | 31.8 | 10.5 | |
| 8 | 黄疸、智力落后(DQ<70分)、低血糖、肝肿大 | 6个月辅助康复训练,1岁3个月DQ恢复正常 | - | 1岁9个月 | ~1SD | ~1SD | 86 | 11.2 | 27.8 | 20.2 |
| 9 | 黄疸、贫血、严重低蛋白血症、凝血功能异常伴皮肤出血点、AFP>正常高值1 000倍 | 补充铁剂 | - | 1岁6个月 | -1SD~ | 80 | 7.8 | 21.0 | 15.9 | |
| 10 | 黄疸、贫血、白陶土色大便 | 补充铁剂 | - | 1岁5个月 | ~1SD | 86 | 9.4 | 40.8 | 7.8 | |
| 11 | 黄疸、腹泻、生长发育落后(身长、体重均<-2SD) | 补充铁剂 | - | 3岁2个月 | ~1SD | ~1SD | 87 | 12.5 | 51.5 | 8.4 |
| 12 | 黄疸、肝肿大 | - | - | 8个月 | -1SD~ | 90 | 11.5 | 30.5 | 15.2 | |
| 13 | 黄疸、贫血 | 补充铁剂 | / | 5个月 | 1SD~2SD | 1SD~2SD | 84 | 8.6 | 85.2 | 32.0 |
| 参考范围 | - | - | - | - | -2SD~2SD | -2SD~2SD | >80 | 0~12 | <150 | 0~20 |
注:NICCD为希特林蛋白缺乏所致新生儿肝内胆汁淤积症,TBA为总胆汁酸,TBil为总胆红素,AFP为甲胎蛋白,为均值,SD为标准差,DQ为发育商;+为有饮食偏好(高蛋白、高脂和低碳水化合物饮食),-为无饮食偏好,/为尚未添加辅食
我国总人群SLC25A13基因变异携带率为1/65,推算NICCD患病率为1∶17 000[7]。浙江省新生儿疾病筛查中心统计的NICCD患病率为1∶64 138[8],湖南省为1∶94 197[9],本研究在徐州地区共筛查新生儿461 494名,确诊NICCD患儿13例,患病率为1∶36 038,进一步证实NICCD患病率存在地区差异。徐州地区较高的患病率是否还和地理环境、人口迁徙、饮食习惯、近亲婚配、生活方式等因素相关,还需要进一步论证。
NICCD多在新生儿期发病,临床缺乏特异性,大部分预后良好,个别患儿因肝硬化、脑水肿等严重并发症而预后不良[10, 11]。本研究中13例患儿多表现为新生儿期黄疸消退延迟、肝内胆汁淤积、肝脏体积过大、凝血功能异常,部分患儿有持续生长发育迟缓、贫血、腹泻、慢性肝病等症状。希特林蛋白缺乏症与起病年龄、生化指标、病情严重程度及预后等的相关性尚未明确[12]。本研究中13例患儿甲胎蛋白均异常升高,其中2例高出正常高值1 000倍以上,且伴有严重低蛋白血症、凝血功能异常,考虑与肝细胞损伤和甲胎蛋白向白蛋白转化延迟有关,提示其可能是肝损伤严重程度及代谢紊乱程度评估的潜在指标,但尚需更大样本的深入研究。
本研究中13例患儿血瓜氨酸明显升高,此与希特林蛋白缺乏致胞质中天冬氨酸不足、尿素循环受阻、导致瓜氨酸蓄积有关;尿有机酸分析主要表现为4-羟基苯乳酸和4-羟基苯丙酮酸升高,与之前文献报道一致[13, 14]。另外,本研究确诊病例中部分患儿伴血酰基肉碱谱升高,以游离肉碱和长链酰基肉碱升高为主。Lee等[15]表明酰基肉碱谱的变化与肝损伤关联不大,可能与胆汁淤积有关。但酰基肉碱升高水平与后续肝损伤程度是否有关仍需要进一步探讨。
SLC25A13基因变异分析是目前确诊希特林蛋白缺乏症最可靠的依据[16, 17]。SLC25A13基因位于人类7号染色体7q21.3,编码含675个氨基酸的希特林蛋白。目前SLC25A13基因已有108种致病变异被报道[18],其中c.852_855delTATG(851del4,58.41%)、c.1638_1660dup(8.85%)、IVS6+5G>A(8.41%)和IVS16ins3kb(7.52%)在中国人群中占所有变异的80%以上[19, 20]。本研究中确诊病例检出的SLC25A13变异类型中c.852_855delTATG变异频率最高。然而SLC25A13基因变异的表型效应存在不完全外显现象,同一变异类型临床表现轻重程度不同[12,21, 22],另外易发展为瓜氨酸血症Ⅱ型的变异基因型尚不明确。
本研究中病例8检测出新变异位点c.1841+3_1841+4del,可能导致蛋白质功能受到影响[23]。该患儿在6月龄时体格、运动及智力评估指标明显落后,经康复训练,1岁3个月时神经运动发育有所改善,提示该变异可能影响患儿神经发育。病例6检测出新变异位点c.511dupG(p.D171Gfs*4),为移码变异,可能导致多肽链合成提前终止,对基因功能影响较大。该患儿新生儿期即表现为高氨血症、颅内出血伴凝血功能异常,婴儿期生长发育明显落后,予以营养指导及康复训练后生长发育有所追赶。因此,c.511dupG位点变异可能与相关临床表征有关,且与希特林蛋白缺乏症起病较早且临床症状较重有关。病例7检测出新变异位点c.889G>T(p.E297X),为无义变异,可能导致多肽链合成提前终止,对基因功能影响较大。c.742G>A(p.E248K)变异位于蛋白关键功能域,附近有热点致病变异且无良性变异,根据ACMG指南,该变异被判读为临床意义未明,其导致的临床表征在本研究中未发现特异性。
NICCD的治疗主要包括无乳糖并强化中链三酰甘油特殊配方奶粉喂养和饮食结构调整,予以低碳水化合物、高蛋白、高脂饮食[22],必要时需肝移植。约20%的NICCD患儿在青春期后发展为瓜氨酸血症Ⅱ型,不发病患儿在学龄期开始出现特异性饮食偏好,喜食肉类、豆类,厌食高碳水化合物类食物[24],可能与机体自我保护机制有关。低碳水化合物可减少NICCD患儿体内半乳糖代谢毒性产物,利于肝细胞能量代谢,从而改善预后。本组患儿随访提示NICCD患儿经早期及时治疗多数在1岁内可缓解,预后良好,但这些患儿是否会发展为瓜氨酸血症Ⅱ型还需后续随访观察。
综上所述,本研究中徐州地区NICCD患病率为1∶36 038,c.852_855delTATG变异出现频率最高。本研究检测出5个新发变异位点,均为首次报道,扩展了SLC25A13基因变异谱,对完善NICCD基因分型具有重要意义,但SLC25A13基因变异的基因型和表型之间的相关性仍需进一步探讨。本研究的局限性在于仅仅是新生儿疾病筛查发现的NICCD患儿,不包括未进行新生儿筛查或者初筛阴性的确诊病例,应认识到新生儿串联质谱检测对筛查NICCD的重要性,在新生儿期积极开展串联质谱技术的群体筛查,以求早期诊断及治疗,从而改善患儿预后。
所有作者均声明不存在利益冲突



























