
心源性栓塞性卒中(CES),简称心源性卒中,是指来自心脏和主动脉弓的栓子通过循环导致脑动脉栓塞引起相应脑功能障碍的临床综合征。与其他病因所致的缺血性卒中相比,心源性卒中的病因更复杂、病情程度相对更重、预后更差。本共识主要依据其病因与发病机制制订治疗方案,在急性期应密切观察患者心功能和血压的变化,治疗时间窗内推荐静脉溶栓和(或)血管内治疗,并予以抗血小板或抗凝、他汀治疗,以尽可能最大程度地挽救缺血半暗带,减少神经功能残疾;针对CES的不同病因采取相应的治疗措施,包括药物、外科和介入治疗,以预防卒中复发,并积极进行神经康复治疗。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
心源性栓塞性卒中(cardioembolic stroke,CES),简称心源性卒中,是指来自心脏和主动脉弓的栓子通过循环导致脑动脉栓塞引起相应脑功能障碍的临床综合征。与其他病因所致的缺血性卒中相比,CES的病因更复杂、病情程度相对更重、预后更差、复发率更高[1, 2]。CES多存在明确的心脏疾病或危险因素,其中由心房颤动(atrial fibrillation,AF)所致者约占70%,近年来对CES(如卒中高危AF)的防治虽有所进步[3, 4],但仍存在对其认识不足、治疗策略差异大等问题[5, 6]。鉴于以上问题,且国内外尚无全面统一的CES治疗方案(尤其是急性期),故共识制定组以国内外近年来的临床研究为依据,结合我国实际,制订本专家共识,以期更好地规范CES治疗,进而提高CES的临床救治水平。
本共识在以往诊断共识的基础上,根据CES危险分层和特定的发病机制制订治疗方案[7, 8]。一般原则:在急性期治疗时间窗内进行静脉溶栓和(或)血管内治疗,以尽可能最大程度地挽救缺血半暗带,减少神经功能残疾;针对CES的不同病因采取相应的治疗措施,以预防卒中的复发,并积极进行神经康复治疗。治疗方案的推荐等级和证据水平根据表1所列的标准加以衡量和分级[9],由撰写组全体成员起草、表决和修订了分级建议和无等级基于共识的声明,直至达成共识。
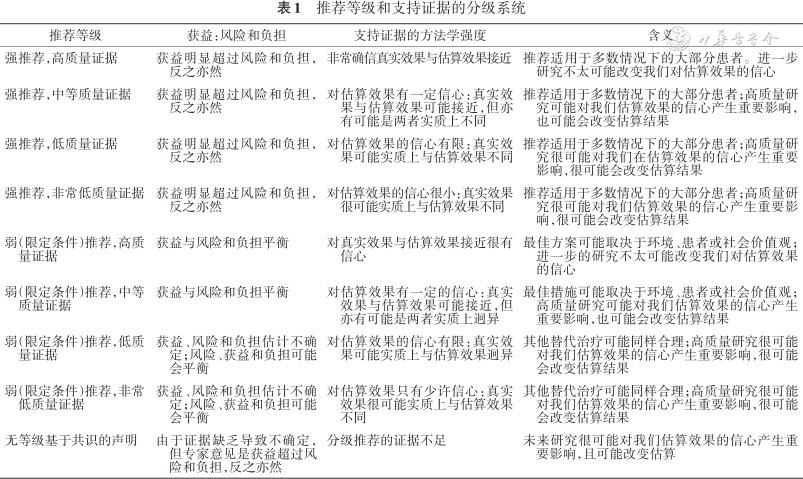
推荐等级和支持证据的分级系统
推荐等级和支持证据的分级系统
| 推荐等级 | 获益:风险和负担 | 支持证据的方法学强度 | 含义 |
|---|---|---|---|
| 强推荐,高质量证据 | 获益明显超过风险和负担,反之亦然 | 非常确信真实效果与估算效果接近 | 推荐适用于多数情况下的大部分患者。进一步研究不太可能改变我们对估算效果的信心 |
| 强推荐,中等质量证据 | 获益明显超过风险和负担,反之亦然 | 对估算效果有一定信心:真实效果与估算效果可能接近,但亦有可能是两者实质上不同 | 推荐适用于多数情况下的大部分患者;高质量研究可能对我们估算效果的信心产生重要影响,也可能会改变估算结果 |
| 强推荐,低质量证据 | 获益明显超过风险和负担,反之亦然 | 对估算效果的信心有限:真实效果可能实质上与估算效果不同 | 推荐适用于多数情况下的大部分患者;高质量研究很可能对我们在估算效果的信心产生重要影响,很可能会改变估算结果 |
| 强推荐,非常低质量证据 | 获益明显超过风险和负担,反之亦然 | 对估算效果的信心很小:真实效果很可能实质上与估算效果不同 | 推荐适用于多数情况下的大部分患者;高质量研究很可能对我们估算效果的信心产生重要影响,很可能会改变估算结果 |
| 弱(限定条件)推荐,高质量证据 | 获益与风险和负担平衡 | 对真实效果与估算效果接近很有信心 | 最佳方案可能取决于环境、患者或社会价值观;进一步的研究不太可能改变我们对估算效果的信心 |
| 弱(限定条件)推荐,中等质量证据 | 获益与风险和负担平衡 | 对估算效果有一定的信心:真实效果与估算效果可能接近,但亦有可能是两者实质上迥异 | 最佳措施可能取决于环境、患者或社会价值观;高质量研究可能对我们估算效果的信心产生重要影响,也可能会改变估算结果 |
| 弱(限定条件)推荐,低质量证据 | 获益、风险和负担估计不确定;风险、获益和负担可能会平衡 | 对估算效果的信心有限:真实效果可能实质上与估算效果迥异 | 其他替代治疗可能同样合理;高质量研究很可能对我们估算效果的信心产生重要影响,很可能会改变估算结果 |
| 弱(限定条件)推荐,非常低质量证据 | 获益、风险和负担估计不确定;风险、获益和负担可能会平衡 | 对估算效果只有少许信心:真实效果很可能实质上与估算效果不同 | 其他替代治疗可能同样合理;高质量研究很可能对我们估算效果的信心产生重要影响,很可能会改变估算结果 |
| 无等级基于共识的声明 | 由于证据缺乏导致不确定,但专家意见是获益超过风险和负担,反之亦然 | 分级推荐的证据不足 | 未来研究很可能对我们估算效果的信心产生重要影响,且可能改变估算 |
遵循“时间就是大脑(time is brain)”的原则,尽可能在到达急诊室后60 min内完成脑CT等基本评估并开始治疗,应尽量缩短进院至溶栓治疗时间(door-to-needle time,DNT),并酌情适时选择桥接[10]或直接机械取栓,以及抗血小板聚集、抗凝、降脂等治疗。
目前这部分的相关高等级研究证据较少,近期在加拿大一项纳入了683例急性缺血性卒中(≤12 h)患者的回顾性研究中,其中303例(44%)在6个月内确诊为CES,经分析显示初始收缩压与心源性栓塞病因显著相关(OR=1.15;95%CI:1.05~1.26),尤见于血压正常(≤130 mmHg,1 mmHg=0.133 kPa)者,患CES的概率增加2.62倍(95%CI:1.46~4.72),该研究提示对于伴低血压或血压正常的急性卒中患者,早期和长期进行心功能检查[超声心动图、长程心脏监护(prolonged cardiac monitoring)]能使其获益[11]。
推荐意见:(1)参照《中国急性缺血性卒中诊治指南(2018)》,监测并维持心脏与呼吸道的功能,以及控制体温、血糖水平等[10](强推荐,中等质量证据)。(2)密切观察患者心功能和血压的变化,对伴初始血压低或正常者,应考虑CES可能,推荐尽早进行超声心动图、长程心脏监护等检查(无等级基于共识的声明)。
基于缺血半暗带理论,在脑缺血超早期,通过血流再灌注可能使损伤区逆转,此段时间称为治疗时间窗。迄今针对CES静脉溶栓疗效的数据相对不多,多为观察性或小样本研究。一项意大利的回顾性研究收集了303例接受了经静脉重组组织型纤溶酶原激活剂(recombinant human tissue-type plasiminogen,rt-PA)治疗的缺血性卒中患者,分为心源性栓塞(cardioemblism,CE)和非心源性栓塞两个组,结果显示与非心源性栓塞组比较,CE组症状明显改善(P<0.012)和症状消退(P<0.057 2),尤见于伴卵圆孔未闭(patent foramen ovale,PFO)者,而两组间死亡例数比较差异无统计学意义(14例与18例)。在欧洲多国近期开展的一项卒中治疗的安全实施(safe implementation of treatments in stroke,SITS)-EAST注册研究中,对接受静脉溶栓治疗的患者数据进行了分析,其中CES占全部患者的30%,结果显示与CES组比较,动脉粥样硬化性血栓性卒中发生症状性颅内出血(symptomatic intracerebral hemorrhage,sICH)的概率更高(OR=1.63,95%CI:1.07~2.47,P=0.023),早期改善的概率更低(OR=0.79,95%CI:0.72~0.86,P<0.001),但临床预后更优(OR=0.77,95%CI:0.67~0.87,P<0.001),两组间的病死率比较差异无统计学意义[12]。与上述研究结果不同,在一项中国急性缺血性卒中溶栓治疗的实施与监测(thrombolysis implementation and monitoring of acute ischemic stroke in China,TIMS-China)队列研究中,前瞻性地随访了发病4.5 h内使用经静脉阿替普酶治疗的患者(n=827),分为CES(n=221)和大动脉粥样硬化亚型(n=606)两组,前者中2/3伴AF。发现与大动脉粥样硬化组比较,CE组在溶栓24~36 h后sICH的发生率更高(5.9% 比0.8%;P<0.000 1),发病3个月后的病死率更高(18.6%比10.3%;P=0.001 5),功能独立性更低(43.6%比55.9%;P=0.001 8)。
此外,CES亦存在静脉溶栓使用受限或复杂化的情形,如发病前接受了抗凝治疗[13, 14, 15]、近期瓣膜手术或经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI),以及感染性心内膜炎相关卒中者,对此在部分指南和专家共识中做出了相应建议或推荐[16, 17, 18]。
在一项全球开展的卒中溶栓安全实施(safe implementation of thrombolysis in stroke,SITS)注册研究中,共有45 074例患者接受了经静脉阿替普酶治疗,其中768例(1.7%,768/45 074)伴AF或充血性心力衰竭,均曾服用华法林且国际标准化比值(international normalized ratio,INR)≤1.7,结果显示在调整了潜在混杂因素后,华法林的使用与sICH无相关性(校正后OR=1.26,95%CI:0.82~1.70),并且在3个月时未见不良功能结果或死亡的增加。与之类似,在另一项北美“跟着指南走-卒中注册(Get With The Guidelines-Stroke Registry)”研究(n=23 437)中,1 802例(7.7%,1 802/23 437)接受华过法林治疗且INR≤1.7[M(IQR):1.20(1.07~1.40)],其中多数患者伴AF或心房扑动(1 229/1 802,69.2%)、冠心病/既往心肌梗死(658/1 802,37.1%)或心力衰竭(320/1 802,18.0%)等心脏疾病。在校正潜在混杂因素后发现,华法林的使用与sICH(校正后OR=1.01,95%CI:0.82~1.25)、严重的系统性出血或住院死亡无显著相关性。上述两项研究结果表明:对于急性CES患者,当服用华法林且INR≤1.7时,接受静脉溶栓治疗未增加其发生sICH或死亡的风险,对其长期神经功能预后亦无影响。此外,来自一项虚拟国际卒中试验档案(virtual international stroke trials archive,VISTA)研究(n=9 613)的亚组分析显示,在服用过华法林且INR≤1.7的患者(n=38)中,经静脉阿替普酶治疗与其功能改善结果相关(OR=2.20,95%CI:1.12~4.32)。
推荐意见:(1)针对多数处于治疗时间窗内的CES患者,可根据其适应证,排除禁忌证和相对禁忌证,充分权衡治疗的获益和风险后考虑静脉溶栓,具体治疗流程基本参照《中国急性缺血性卒中诊治指南(2018)》[10]。(2)对于仍在使用华法林但INR<1.7的患者或预防剂量低分子肝素,可考虑静脉溶栓治疗(强推荐,中等质量证据)。(3)对于使用新型口服抗凝剂(novel oral anticoagulants,NOACs)治疗患者,应尽量避免静脉溶栓治疗,除非明确其在48 h内未曾服用NOACs,同时实验室检查示其肾功能和凝血指标均正常(弱推荐,低质量证据)。(4)对于服用达比加群者,可在预先给予其拮抗剂-依达赛珠单抗(idarucizumab)处理后,考虑行静脉溶栓治疗(弱推荐,低质量证据)。(5)对于接受手术(瓣膜手术)或在侵入性检查(冠状动脉造影)过程中发病的患者,建议在权衡抗栓和(手术部位)出血风险后,慎重进行静脉溶栓治疗(无等级基于共识的声明)。(6)感染性心内膜炎患者,应避免静脉溶栓治疗(弱推荐,低质量证据)。
血管内机械取栓(mechanical thrombectomy,MT)目前作为一线的血管内治疗(endovascular treatment,EVT)方法,但迄今CES相关的研究数据相对较少,以往数项研究围绕LAA与CE亚型进行了比较研究,患者均接受了静脉溶栓-MT桥接治疗或直接MT,主要针对颈内动脉、大脑中动脉(middle cerebral artery,MCA)1~2段,结果示前者发病第90天的预后[改良Rankin评分(modified Rankin Scale,mRS)0~2分的比例]优于后者,而病死率、sICH发生率则低于后者或两者相当[19, 20, 21, 22],但近来Matusevicius等[23]所做的荟萃分析则显示上述指标在两组之间差异无统计学意义。在近期一项德国的回顾性注册研究(n=2 589)中,发现接受MT的CES患者再灌注成功率(85.6%与81.0%,P=0.002)和完全再灌注率(45.7%与38.1%,P<0.001)均显著高于非CES患者,尽管两组中患者接受的静脉溶栓治疗率有所不同(51%与29%,P<0.000 1)[24]。另一项日本的多中心观察性研究(n=688)之事后分析显示,尽管两组疾病严重程度[基线美国国立卫生研究院卒中量表(National Institute of Health stroke scale,NIHSS):18分比13分,P<0.000 1]且接受静脉溶栓治疗率(58%与29%,P<0.000 1)不同,但EVT组(n=110)和非EVT组(n=144)在90 d时的病死率、复发率和出血性卒中的发生率相似,且前者功能预后(mRS 0~2分)明显优于后者(校正后OR=1.94,95%CI:1.20~3.15,P=0.007)[25]。
推荐意见:(1)多数情况下推荐采取静脉溶栓-血管内MT桥接治疗模式[26],也可视情形(如有静脉溶栓禁忌时)直接MT(弱推荐,低质量证据)。(2)MT主要针对距最后正常时间6~16 h或6~24 h的前循环大血管(颈内动脉、MCA M1~2段)闭塞患者,治疗目标是达到改良脑梗死溶栓治疗分级(modified thrombolysis in cerebral infarction,mTICI)2b/3 级的再灌注,具体的治疗流程基本参照《中国急性缺血性卒中早期血管内介入诊疗指南(2018)》[26](弱推荐,中等质量证据)。(3)动脉溶栓、血管成形术及支架置入术对急性CES的疗效尚不明确,后二者或可作为介入取栓失败的补救治疗(无等级基于共识的声明)。
关于抗血小板药物治疗急性期CES的数据有限。既往两项阿司匹林(160或300 mg/d,发病48 h内给药)治疗急性缺血性卒中患者的大型随机对照临床试验——国际卒中试验(the international stroke trial,IST)和华人急性卒中试验(Chinese acute stroke trial,CAST)确定了其安全性和益处,且半数以上患者用药前接受了头颅CT检查,该结论在随后Sandercock等所做的Cochrane系统评价中得以进一步证实,同时鉴于潜在的药物相互作用,建议接受溶栓治疗者在24~48 h内不应开始服用阿司匹林。然而,以上研究中入组者病因分型均采用了牛津郡社区卒中项目(Oxford community stroke project,OCSP)分型标准,仅有少数患者(7%~16%)伴AF,而对CES的疗效和安全性尚不清楚。在韩国开展的一项前瞻非随机对照临床注册研究中,纳入了712例接受静脉溶栓或血管内再通治疗的急性缺血性卒中患者[344例(48.3%)为CES],其中再通治疗后24 h内启动抗栓治疗者为456例,通过回顾性分析显示再通治疗后24 h内早期应用口服抗血小板药物(半数以上为阿司匹林,少数为阿司匹林+氯吡格雷联合或者抗凝药物治疗)并未增加再通治疗后出血及症状性颅内出血的风险。
对于替罗非班,在波兰一项ST段抬高型心肌梗死(ST elevation myocardial infarction,STEMI)的临床研究中(n=341),患者被随机分为单纯接受溶栓治疗组(n=169)和经转运接受PCI治疗组(n=172),其中后者接受溶栓后在转运过程中给予替罗非班(在社区医院急诊室静脉推注10 mg/kg,然后在运输和冠状动脉手术期间持续静脉滴注0.1 mg·kg-1·min-1)。结果显示:在30 d的随访中,PCI治疗组与单纯溶栓组相比,病死率、再次心肌梗死率、卒中发生率分别为3.49%与8.88%(P=0.04)、1.16%与5.92%(P=0.02)、0.58%与1.18%(P=0.55);单纯溶栓组达到联合终点(死亡/再次心肌梗死/卒中)的频率更高(15.98%与5.23%,P=0.001),提示其在CES急性期的应用潜能。近来国内一项MT联合小剂量替罗非班(0.2~0.4 mg/h,持续滴注12~24 h)治疗急性CES的前瞻性对照研究(n=288)发现,替罗非班治疗组(n=117,其中37例先行静脉溶栓)和未接受替罗非班治疗组(n=171,其中75 例先行静脉溶栓)在sICH(11.1%与17.0%,P=0.167)、血管再闭塞(7.7%与8.8%,P=0.745)发生率和3个月后功能独立性(33.3%比25.1%,P=0.131)方面差异均无统计学意义,但与未接受替罗非班治疗组比较,替罗非班组脑疝(6.8%比20.5%)和去骨瓣减压术(2.6%与11.7%)的发生率显著降低(P<0.01),替罗非班与患者住院死亡率的降低显著相关(3.4%与12.3%;校正后OR=0.16;95%CI:0.03~0.81;P校正后=0.027)[27]。
在一项替罗非班治疗急性卒中安全性(safety of tirofiban in acute ischemic stroke,SaTIS)试验中,纳入了260例不符合静脉溶栓的急性缺血性卒中患者,NIHSS评分为4~18分,在症状出现后3~22 h采用静脉注射替罗非班(最初30 min内注射0.4 μg·kg-1·min-1,随后持续48 h内注射0.1 μg·kg-1·min-1)或安慰剂治疗,主要终点事件是发病2~7 d内的出血转化发生,结果显示脑出血转化率在治疗组和安慰剂组间未见显著异常(替罗非班 36/120;安慰剂组33/124:OR=1.18;95%CI:0.66~2.06),表明该药用于治疗急性中度缺血性卒中的安全性[22]。数项初步研究亦显示出替罗非班联合静脉溶栓或血管内治疗[28]的安全性和有效性,即使与大剂量阿替普酶(0.9 mg/kg)合用时,也优于常规的阿替普酶溶栓治疗,然而上述试验并非针对CES患者,且大多是小样本量、非随机对照设计,或缺乏长期随访结果,故证据质量不高,有待进一步确证。
何时启动抗凝治疗预防CES复发,开始和停用抗凝治疗的时机迄今尚不确定。对于大多数合并AF的患者,目前推荐在发病后的第4~14天内开始口服抗凝治疗[18],但近期一项多中心真实世界队列研究(n=2 084)中报道,在4~14 d内开始口服抗凝治疗并未显著减少缺血(与>14 d比较;OR = 0.76,95%CI:0.36~1.62,P=0.482)和出血性卒中(与0~3 d比较;OR=1.49,95%CI:0.50~4.43)的发生[29]。此外,迄今亦缺乏可靠的数据来明确急性卒中后重启口服抗凝剂(oral anticoagulant,OAC)的最佳时间,近来有观点认为需在由神经科、心血管团队(亦包括患者)共同组成的多学科诊疗前提下,针对大多数患者在发病2周内尽快重启OAC治疗[30]。在抗凝药物的选择方面,来自长期抗凝治疗的随机评价(randomized evaluation of long-term anticoagulation therapy,RE-LY)、利伐沙班每日1次口服直接Xa因子抑制剂与维生素K拮抗剂预防AF卒中和栓塞的对比试验(rivaroxaban once daily oral direct factor Xa inhibition compared with vitamin K antagonism for prevention of stroke and embolism trial in atrial fibrillation,ROCKET-AF)、阿哌沙班用于减少AF患者的卒中和其他血栓栓塞事件(apixaban for reduction in stroke and other thromboembolic events in atrial fibrillation,ARISTOTLE)和新一代Xa因子有效抗凝治疗AF-心肌梗死溶栓48(effective anticoagulation with factor Xa next generation in atrial fibrillation-thrombolysis in myocardial infarction 48,ENGAGE AF-TIMI 48)四项随机对照试验的一致性结果表明:NOACs在降低AF患者卒中或系统性栓塞的风险方面并不劣于华法林,且在颅内出血不良反应方面具有更高的安全性。
推荐意见:(1)针对不同病因所致CES,可采取相应的抗栓药物治疗,包括抗血小板和抗凝药物。(2)口服抗血小板药物治疗(如阿司匹林、氯吡格雷)应在溶栓24 h后开始选择性使用,使用前应复查头颅CT(强推荐,中等质量证据)。(3)替罗非班或可作为不符合静脉溶栓者的替代治疗,或可酌情联合静脉溶栓或血管内治疗(弱推荐,非常低质量证据)。(4)基于CES发生出血转化的风险,即便患者存在抗凝指征(如AF、瓣膜病),治疗启动或重启时间应视其病情严重程度、急性期梗死灶大小、出血风险高低于发病数天甚至数周后开始,应充分考虑NOACs较华法林起效快、安全性高的特点(无等级基于共识的声明)。
对CES的疗效尚不明确,近期一项韩国的回顾性研究(n=6 124)发现,急性期使用他汀类药物或可减少其主要血管事件、血管性死亡等发生风险[31]。在另一项纳入了857例急性缺血性卒中的韩国单中心临床注册研究(其中含心源性栓塞患者413例)中,Jeong等[32]经回顾性分析发现,在静脉溶栓或EVT后早期(发病≤72 h)应用他汀类药物在mRS(调整后OR=1.52;95%CI:1.13~2.03)和减少症状性出血转化(调整后OR=0.44;95%CI:0.24~0.83)方面均可使患者获益。
推荐意见:他汀类药物可在CES发病72 h内启动治疗,或可酌情联合静脉溶栓或血管内治疗(弱推荐,低质量证据)。
在一项针对非瓣膜性AF抗栓治疗以预防卒中的荟萃分析研究中,共纳入了29个试验(n=28 044),平均随访1.5年,结果显示:与对照组比较,华法林调整剂量组(6项试验,n=2 900)和抗血小板药物组(8项试验,n=4 876)分别使卒中发生率下降了64%(95%CI:49%~74%)和22%(95%CI:6%~35%),华法林较抗血小板药物更有效地降低了AF相关CES的相对风险(relative risk,RR)达39%(95%CI:22%~52%)(12项试验,n=12 963)。而另一项荟萃分析中共纳入了5项研究,包括8 928例亚洲患者(其中5 250 例服用NOACs,3 678服用华法林)、64 033例非亚洲患者(其中37 800例使用NOACs,26 233服用华法林),结果发现:与华法林相比,标准剂量NOACs可减少卒中或系统性栓塞[OR=0.65(0.52~0.83)比0.85(0.77~0.93),P交互作用检验=0.045];在安全性方面,亚洲人群服用NOACs较非亚洲人群更安全,尤其是在严重出血[OR=0.57(0.44~0.74)比0.89(0.76~1.04),P交互作用检验=0.004)]、出血性卒中的发生方面[OR=0.32(0.19~0.52)比0.56(0.44~0.70),P交互作用检验=0.046],而胃肠道出血在非亚洲人患者显著增加[OR=0.79(0.48~1.32)比1.44(1.12~1.85),P交互作用检验=0.041]。
在以往4项随机、双盲、安慰剂对照研究中发现,与华法林比较,口服达比加群(150 mg,每日2次)、利伐沙班(20 mg,每日1次)、阿哌沙班(5 mg,每日2次)、艾多沙班(60 mg,每日1次)可显著或非劣势减少非瓣膜性AF患者卒中和系统性栓塞的发生率,且主要出血风险低于或不劣于华法林[33]。
对于卒中和阵发性AF之间的因果关系仍有争议[34]。近来一项Kaiser Permanente AF研究中真实世界心脏监测策略评估、治疗模式和健康指标(Kaiser Permanente real-world heart monitoring strategy evaluation,treatment patterns,and health metrics in atrial fibrillation,KP-RHYTHM)回顾性队列研究(n=1 965)发现,在校正了ATRIA或CHA2DS2卒中风险评分后,未服用抗凝药物时阵发性AF负荷的最高三分位数(≥11.4%)与3倍以上的(校正后)血栓栓塞发生率相关(校正后HR=3.13,95%CI:1.50~6.56,校正后HR=33.16,95%CI:1.51~6.62)[35]。一项旨在评估AF类型对血栓栓塞、出血和病死率的影响荟萃分析中,共纳入了12项研究(n=99 996),结果显示:与阵发性AF组相比,非阵发性AF组的血栓栓塞风险和全因死亡更高(多变量校正后HR=1.384;95%CI:1.191~1.608;P<0.001;多变量校正后HR=1.217,95%CI:1.085~1.365,P<0.001),两组患者出血率则类似(校正后HR=1.025,95%CI:0.898~1.170,P=0.715)。研究者在前述RE-LY研究中发现:(1)达比加群150 mg(每日2次)对阵发性AF(HR=0.61,95%CI:0.42~0.90)、持续性AF(HR=0.64,95%CI:0.43~0.93)和永久性AF(HR=0.70,95%CI:0.48~1.01)的卒中和系统性栓塞预防比华法林更有效(P交互作用=0.833 5);(2)达比加群110 mg(每日2次)在预防持续性AF(HR=0.96,95%CI:0.69~1.35)和永久性AF(HR=1.13,95%CI:0.81~1.57)中的卒中或系统性栓塞方面与华法林相当,针对阵发性AF(HR=0.60,95%CI:0.41~0.89)则效果更明显(P交互作用=0.046 5);(3)在引起大出血方面,达比加群150 mg与华法林类似,但达比加群110 mg则可减少大出血的发生,无论是阵发性AF(HR=0.78,95%CI:0.61~0.99)、持续性AF(HR=0.74,95%CI:0.57~0.94)还是永久性AF(HR=0.92,95%CI:0.71~1.18),结果大致类似(P交互作用=0.436 7)。目前的欧美指南均推荐应根据非阵发性或阵发性AF的血栓栓塞风险使用抗凝药物预防卒中[30,36]。
在2项随机对照临床试验中,对具有卒中发病高风险的非瓣膜性AF患者,利用Watchman封堵器进行经皮左心耳(left atrial appendage,LAA)封堵术治疗,并与华法林治疗比较,分别随访了1.5年(PREVAIL研究)和3.8年(PROTECT AF研究),结果显示:(1)PREVAIL研究在主要疗效终点(卒中或随机分组后7 d内继发栓塞)方面,LAA封堵组和华法林组的发生率分别为0.025 3与0.020 0[(风险差(risk difference)=0.005 3,95% CrI:-0.019 0~0.027 3],达到非劣效性,LAA封堵组早期安全事件发生率为2.2%,亦达到预定的安全性目标;(2)PROTECT AF研究中LAA封堵组和华法林组主要事件的年发生率分别为2.3和3.8次/100例(RR=0.60;95%CI:0.41~1.05),达到非劣效性(后验概率>99.9%)和优效(后验概率96.0%)的预设标准。LAA封堵组的年心血管病死率(1.0次/100例)显著低于华法林组(2.4次/100例)(HR=0.40;95%CI:0.21~0.75;P=0.005),其全因病死率(3.2次/100例)亦显著低于华法林组(4.8次/100例,HR=0.66;95%CI:0.45~0.98;P=0.04)。一项观察研究针对有心脏病史的老年患者(伴有AF史),评估了LAA封堵术(通常伴有心房消融)联合心脏手术的术后血栓栓塞并发症风险。该研究纳入了3 892例接受了心脏手术联合外科LAA封堵术患者,平均随访时间2.6年,结果显示:与未接受LAA封堵者比较,LAA封堵者未校正的血栓栓塞再入院率(4.2%比6.2%)、全因死亡率(17.3%比23.9%)和复合终点(20.5%比28.7%)均显著降低,而出血性卒中发生率比较差异则无统计学意义(0.9%比0.9%)[37]。
一项多中心前瞻性队列研究对接受抗凝治疗的急性缺血性卒中合并新诊断的AF患者(n=1 029)进行了观察,结果显示:从发病开始第4~14天予以抗凝,其卒中、短暂性脑缺血发作(transient ischemic attack,TIA)、系统性栓塞、颅内出血及发病90 d后的预后会更好(与<4 d抗凝相比,在第4~14天开始抗凝HR=0.53,95%CI:0.30~0.93)。另一项非随机队列研究自真实国际卒中试验档案(virtual international stroke trials archive,VISTA)数据库(n=10 304)中选取1 644 例合并AF的缺血性卒中患者进行了分析,分为抗凝治疗组(n=518)、抗血小板聚集治疗组(n=162)、抗凝治疗组+抗血小板聚集联合治疗组(n=782)、未接受抗栓组(n=182),抗凝和抗血小板治疗启动时间分别为发病后2(IQR 1~3)d和1(IQR 1~3)d,联合治疗组与未接受抗血栓治疗组相比,结果显示在第90天时,复发的卒中(recurrent stroke,RS)、sICH和死亡的风险显著降低。接受治疗组(RS组,OR=0.33,95%CI:0.21~0.53;sICH组,OR=0.18,95%CI:0.09~0.37;病死率:OR=0.34,95%CI:0.24~0.50),抗血小板治疗组或抗凝治疗组的结果亦得出相似结果,RS和sICH的相对危险性在发病后2 d最高,但随着时间推移而逐渐趋于稳定。
已知华法林抗凝受多种因素影响,Apostolakis等[38]与Larsen和Lip[39]基于性别、年龄、病史、治疗药物、吸烟和种族制订了SAMe-TT2R2评分,有助于预测患者使用该药时可否有良好的抗凝控制。目前SAMe-TT2R2评分已在两个亚洲人群中得到验证,其中0~2分预测治疗(目标)范围内的时间百分比(time within therapeutic range,TTR)分别≥70%(中国香港)或TTR≥60%(新加坡),≥3分时TTR则分别<70%(中国香港)或<60%(新加坡)[40]。因此,SAMe-TT2R2评分可用以预测华法林在亚洲人群中的应用效果,并协助抗凝药物的选择决策。
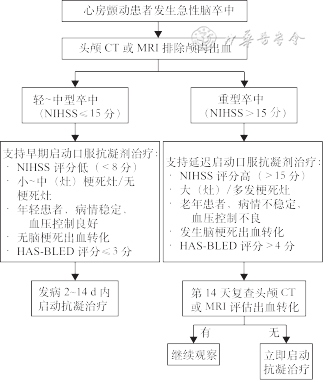
推荐意见:(1)对于伴非瓣膜性AF者,华法林和NOACs均可用于其卒中预防,当华法林抗凝强度为INR 2.0~3.0时,可有效预防卒中;与华法林比较,亚洲人群中NOACs无论在减少卒中还是降低抗凝所致出血风险方面效果更佳(强推荐,高质量证据)。(2)对于伴瓣膜性AF者,应长期华法林抗凝,中~重度二尖瓣狭窄者不推荐使用NOACs,尤其是达比加群(强推荐,中等质量证据)。(3)对于AF类型,无论是阵发性、持续性还是永久性,均应基于血栓栓塞的风险选择抗凝治疗(强推荐,中等质量证据)。(4)左心耳手术:介入性LAA封堵术(WATCHMAN封堵器)可考虑用于伴有非瓣膜性AF的高危卒中患者,有长期口服抗凝剂之禁忌;外科房颤消融应用于同时接受心脏手术者(强推荐,中等质量证据)。(5)对于大多数伴AF的缺血性卒中患者(尤其是非瓣膜性AF),可根据梗死灶大小、NIHSS评分、CHA2DS2-VASc评分和HAS-BLED评分选择性地口服抗凝剂治疗(图1),低出血风险者在发病2~14 d内启动,高出血风险者则延至14 d后启动(强推荐,中等质量证据)。(6)使用华法林时,理想的TTR应为>65%,SAMe-TT2R2评分(表2)有助于指导临床决策,0~2分者可预测华法林反应良好;≥3分者则可预测华法林反应不佳,宜换用NOACs(弱推荐,中等质量证据)。
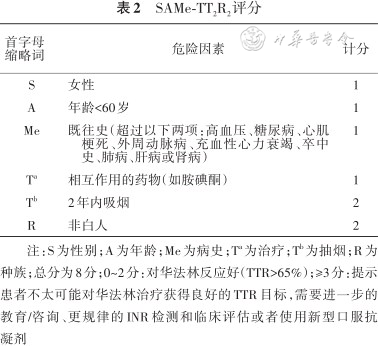
SAMe-TT2R2评分
SAMe-TT2R2评分
首字母 缩略词 | 危险因素 | 计分 |
|---|---|---|
| S | 女性 | 1 |
| A | 年龄<60岁 | 1 |
| Me | 既往史(超过以下两项:高血压、糖尿病、心肌梗死、外周动脉病、充血性心力衰竭、卒中史、肺病、肝病或肾病) | 1 |
| Ta | 相互作用的药物(如胺碘酮) | 1 |
| Tb | 2年内吸烟 | 2 |
| R | 非白人 | 2 |
注:S为性别;A为年龄;Me为病史;Ta为治疗;Tb为抽烟;R为种族;总分为8分;0~2分:对华法林反应好(TTR>65%);≥3分:提示患者不太可能对华法林治疗获得良好的TTR目标,需要进一步的教育/咨询、更规律的INR检测和临床评估或者使用新型口服抗凝剂
有4项随机临床试验比较了华法林和阿司匹林(或氯吡格雷)对心衰患者卒中风险的影响,其中WASH和HELAS试验样本量较少,不足以显示出两组的统计学差异。WATCH和WARCEF试验的样本量相对更大,尽管在死亡率方面未见明显获益,但华法林组卒中的发病风险显著降低,然而该作用被主要出血风险的增加所抵消,氯吡格雷既不优于华法林,亦不优于阿司匹林。
在一项针对AF的荟萃分析中,共纳入了包括4项随机对照试验(n=19 122),结果显示:在伴AF心衰患者中,单次和高剂量NOACs应用的疗效和安全性较好,而剂量较低时则与华法林相似。与无心衰组比较,NOACs对于伴AF心衰患者同样有效,甚至更安全(颅内出血发生少)。然而,在近来一项双盲随机COMMANDER HF 试验中,5 022例伴有慢性心衰(左心室射血分数≤40%)、不伴AF的冠心病患者被随机分配接受利伐沙班(2.5 mg,每日2次)或安慰剂治疗,主要疗效终点是由任何原因导致的死亡、心肌梗死或卒中,主要安全性终点是致命性出血或可能致使永久性残疾的出血,结果显示两组之间在主要疗效终点和安全性终点两方面均无显著差异[44]。
推荐意见:(1)在控制心衰的基础上,可视情形给予抗血小板或抗凝治疗(弱推荐,中等质量证据)。(2)对于同时合并AF者,推荐首选单次服用且高剂量的NOACs(弱推荐,中等质量证据)。
根据多项不同类型(如随机对照、观察性)的研究发现,对于所有的缺血性卒中或TIA患者,应积极控制高血压、糖尿病、高脂血症、肥胖、代谢综合征、阻塞性睡眠呼吸暂停、吸烟和缺乏身体运动等危险因素,并注意限制酒精摄入和机体营养状况。
针对以往指南推荐对ACS PCI术后AF患者的标准三联治疗[(华法林+双重抗血小板(dual antiplatelet therapy,DAPT)]方案,治疗后出血成为关注的问题。近来一项随机对照研究中,将2 124例接受了PCI的非瓣膜性AF患者,以1∶1∶1的比例随机分为以下三组:接受低剂量利伐沙班(15 mg,每日1次)+P2Y12抑制剂组(第1组)、极低剂量利伐沙班(2.5 mg,每日2次)+DAPT标准治疗组(第2组)、剂量调节的华法林(每日1次)+DAPT治疗组(第3组),随访12个月。结果显示:两组接受利伐沙班治疗的临床显著出血率低于接受标准治疗组(第1组16.8%,第2组18.0%,第3组26.7%;第1组与第3组的HR=0.59,95%CI:0.47~0.76,P<0.001;第2组与第3组的HR=0.63,95%CI,0.50~0.80,P<0.001);三组因心血管原因、心肌梗死或卒中所致的死亡率相似,组间差异均无统计学意义[45]。随后,另一项随机对照研究则观察比较了双联疗法(达比加群+氯吡格雷或替格瑞洛)与标准三联疗法后的出血率和血栓栓塞事件,结果显示接受双联疗法组的出血风险低于接受标准三联疗法者,且其预防血栓栓塞事件风险不劣于三联疗法[46]。
推荐意见:(1)非药物治疗:控制危险因素,包括高血压、糖尿病、高脂血症、肥胖、代谢综合征、阻塞性睡眠呼吸暂停、吸烟和缺乏身体运动等(中等推荐,中等质量证据)。(2)药物治疗:缺血性卒中患者出现以下情况时,为减少卒中发生或复发风险,应给予华法林抗凝治疗(目标INR值为2.5;范围:2.0~3.0)3个月:①急性心肌梗死伴左室附壁血栓形成;②急性前壁STEMI,并无左室附壁血栓形成但左室射血分数<40%,亦可针对上述情形中不能耐受华法林者,改用阿哌沙班、低分子肝素、达比加群或利伐沙班替代治疗(弱推荐,低质量证据)。(3)介入手术治疗ACS:包括PCI或冠状动脉旁路移植术(coronary artery bypass grafting,CABG)(表3),随后视情形给予标准三联治疗(华法林、阿司匹林和氯吡格雷)或两联(NOACs和阿司匹林或氯吡格雷)治疗,亦可选用利伐沙班替代华法林,替格瑞洛代替氯吡格雷,但需注意观察替格瑞洛所致的出血风险(弱推荐,中等质量证据)。
目前对于PFO相关CES的治疗方案尚未明确。以往发表的5项在欧美国家进行的随机对照试验显示,针对卒中的二级预防,经导管PFO封堵联合抗血小板治疗优于单用抗血小板治疗。这些研究表明,经导管PFO封堵术,栓塞性卒中的复发频率可从每年百例中1.1降低到0.53,对应以相对风险降低50%,绝对风险降低2.11%,随访约4年中需要治疗的人数为46.5。经导管PFO封堵和仅抗血小板治疗两组在TIA的风险、死亡率和出血率方面则无显著差异;另一方面,经导管PFO封堵术后的常见不良反应为AF频率的增加(每年百例中1.3比0.25,即约5倍相对风险增加)。令人关注的是,近期韩国在亚洲人群进行为期2年的DEFENSE PFO研究亦显示,针对伴高危PFO[房间隔膨出瘤(atral septal aneurysm,ASA)、高活动性、原发隔与继发隔间距≥2 mm]的隐源性卒中,PFO封堵明显降低了患者(n=120)主要终点(卒中、血管性死亡、心肌梗死溶栓定义的主要出血)和卒中复发[49]。
针对上述试验中使用双盘封堵器者进行了亚组分析,结果示针对以下三种患者特征,PFO封堵术可降低缺血性卒中的复发:(1)ASA(HR为0.13与0.43;P=0.005);(2)更大的分流尺寸(P=0.07);(3)不限于单根深穿支动脉病变的标引缺血性卒中(index ischemic stroke)(HR为0.34与2.25;P=0.04)[50]。以往研究亦证实了与CardioSEAL-STARflex或Helex封堵器相比,Amplatzer封堵器术后再发神经系统疾病事件的发生率更低。
推荐意见:(1)可选择抗栓治疗和(或)PFO封堵术,抗栓治疗一般首选抗血小板(阿司匹林或氯吡格雷)治疗,对伴深静脉血栓形成者则可有条件地给予抗凝(华法林或NOACs)治疗(无等级基于共识的声明)。(2)不推荐在初次栓塞事件发生后无选择性地封堵PFO(无等级基于共识的声明)。(3)PFO封堵术适用于伴有高右向左分流(right-to-left shunt,RLS)的年轻患者,且具有以下因素时:①首次栓塞发作后头颅MRI显示≥1个既往的(皮质)梗死灶;存在PFO的解剖学高危因素,包括伴有ASA、大PFO(>20个气泡或PFO直径≥4 mm)、伴有希阿里网、伴有Eustachian瓣、房间隔活动过度或静息状态下PFO存在RLS;②在首次栓塞事件发生后使用抗血小板药物或充分抗凝治疗后仍复发栓塞者(无等级基于共识的声明);③不限于单根脑深穿支动脉病变的缺血性卒中(弱推荐,中等质量证据)。(4)封堵时建议使用Amplatzer双盘封堵器,术后采取长期抗血小板或抗凝治疗(强推荐,高质量证据)。
抗生素治疗对于IE的预后非常重要,在一项前瞻性多中心队列研究中,共纳入了1 437例左侧心内膜炎入院患者,接受相应抗菌药物治疗的患者在治疗第1周的卒中发病率约为每日4.82/1 000例,第2周降至1.71/1 000,持续治疗该比率继续下降,且与瓣膜或病原体种类无关;全部患者在接受1周的抗菌治疗后,其中仅3.1%发生了卒中。
迄今为止,抗栓治疗方面的高等级研究证据较少,且以往研究报道抗凝治疗带来的出血风险结果不一,故目前对于如何启动和维持抗凝治疗以预防卒中复发尚不明确。
目前多数学者认同IE心脏手术的必要性,但亦需充分权衡围手术期风险与术后预后。法国和澳大利亚的两项队列研究发现,对于无症状脑栓塞或TIA患者,术后神经功能恶化的风险较低,如有适应证时可立即手术;而对于症状性缺血性卒中患者,除非判断其神经功能预后太差,心脏手术亦非禁忌。关于卒中和心脏手术之间最佳时间间隔的证据不相一致,在一项韩国的前瞻性队列研究中,随机将罹患左心IE、严重瓣膜病和巨大赘生物的患者分为早期手术组(随机分组后48 h内)(n=37)或常规手术组(n=39),主要终点是随机分组后6周内发生的住院死亡和栓塞事件。结果显示:早期手术组1例(3%)出现主要终点,常规手术组9例(23%)(HR=0.10,95%CI:0.01~0.82,P=0.03);两组间术后6个月的全因死亡率差异无统计学意义;早期手术组6个月时因任何原因死亡、栓塞事件或IE复发的复合终点发生率为3%,常规手术组为28%(HR=0.08,95%CI:0.01~0.65,P=0.02)。另一方面,数项队列研究发现,对于发生颅内出血的IE患者,其预后较差,手术通常应比并发缺血性卒中者更晚进行。一项西班牙观察性研究(n=12)显示,在脑出血后4周内接受手术的IE患者与手术推迟至4周后的患者相比,病死率差异有统计学意义(分别为75%和40%),而术后2周内、3周内和至少21 d后接受手术者术后新出血事件发生率则分别为50%、33%和20%。
推荐意见:(1)抗生素治疗:应尽快给予有效的抗生素治疗,以降低栓塞并发症的死亡率和发病率(强推荐,高质量证据)。(2)抗凝治疗:建议根据患者的具体情况(自体还是人工瓣膜发病、赘生物的大小及其位置、病原体的毒性、梗死灶大小、有无出血转化或真菌性动脉瘤),决定是否启动抗凝治疗(无等级基于共识的声明)。(3)心脏手术:①对于无症状性脑栓塞或TIA术后病情恶化者,存在手术指征时应及时手术治疗(弱推荐,低质量证据);②缺血性卒中并非手术禁忌证,但对于何时进行尚有争议,建议应早期手术,除非判断其预后很差(弱推荐,低质量证据);③出血性卒中应推迟至少1个月后手术(弱推荐,低质量证据);④严重神经系统症状的患者如血流动力学稳定,应推迟手术至少4周,或等到神经系统症状改善再行手术(无等级基于共识的声明)。(4)颅内感染性动脉瘤若有增大或破裂迹象,应先利用神经外科手术或血管内治疗处理动脉瘤(无等级基于共识的声明)。
RHD主要累及二尖瓣(少数为主动脉瓣),是引起二尖瓣狭窄发生的首位病因,发生系统性栓塞的风险很高,常并发AF。与无心脏瓣膜病的患者相比,心脏瓣膜病(除了中~重度二尖瓣狭窄)患者年龄更大,并发症更多,包括充血性心衰、心肌梗死和肾脏疾病[51]。在对AF和心脏瓣膜病患者的3项临床试验亚组分析中发现,针对心脏瓣膜病和非心脏瓣膜病患者,NOACs(阿哌沙班、达比加群和利伐沙班)较华法林在预防其系统性栓塞风险方面有所差异,提示将NOACs用于卒中的预防可使心脏瓣膜病患者更多获益。因此,在缺乏高质量证据的情况下,目前共识认为:对于二尖瓣狭窄患者,如果既往合并卒中或AF时,宜给予抗凝治疗;对于伴中~重度二尖瓣狭窄者,则建议长期华法林治疗(INR 2.0~3.0)[36,51]。
推荐意见:(1)对于有风湿性二尖瓣疾病和AF的CES患者,推荐长期抗凝治疗,包括华法林、NOACs(中~重度二尖瓣狭窄者除外)(弱推荐,中等质量证据)。(2)对于伴中~重度二尖瓣狭窄者,建议长期华法林治疗(目标INR值为2.5;范围:2.0~3.0)(弱推荐,低质量证据)。(3)在足量华法林治疗的基础上,可考虑联合阿司匹林治疗(无等级基于共识的声明)。
机械瓣膜相关卒中的发病风险高,需进行终身抗凝治疗[52]。针对抗凝药物的选择,在一项前瞻性、随机、二期、开放标签试验(RE-ALIGN)中,纳入了在过去7 d内接受主动脉瓣或二尖瓣机械瓣膜置换术的患者、至少3个月前接受过此类瓣膜置换术的患者两组人群,将其按2∶1的比例随机分配给达比加群或华法林。达比加群初始剂量基于入组者肾功能选择(150、220或300 mg,每日2次),剂量调整至血浆水平达到≥50 ng/ml。根据血栓栓塞风险,调整华法林剂量至获得INR 2.0~3.0或2.5~3.5的水平。该研究主要终点是达比加群的血浆谷浓度。由于达比加群组中血栓栓塞和出血事件过多,该试验在252例患者注册后提前终止。接受治疗分析(as-treated analysis)显示:162例患者中有52例(32%)需要调整达比加群剂量或停药,达比加群组中9例(5%)发生缺血性或不明原因卒中,华法林组则无;两组大出血分别发生7例(4%)和2例(2%)。该试验结果表明机械瓣膜患者中使用华法林,在疗效和安全性方面均优于达比加群。在接受了主动脉瓣置换且无其他血栓栓塞危险因素的患者中,华法林治疗后INR 2.0~3.0组与3.0~4.5组之间发生血栓栓塞事件的风险相似,但前者出血风险明显低于后者。在一项德国低强度抗凝治疗经验研究(GELIA)中发现,对于二尖瓣或者主动脉瓣机械瓣置入患者,较低的INR范围(2.0~3.5)与较高的目标INR(2.5~4.5)相比,在出血或血栓栓塞并发症方面并未见明显差异,鉴于此,有学者建议主动脉机械瓣的INR目标值为2.5(范围2.0~3.0),如有栓塞事件危险因素,可上调至3.0(范围2.5~3.5);二尖瓣机械瓣的INR目标值为在3.0(范围2.5~3.5)[53]。
与机械瓣膜相比,生物瓣膜具有较低的血栓栓塞风险,长期观察结果发现二尖瓣置换者的血栓栓塞发生率高于主动脉瓣置换者(分别为2.4%和1.9%)[53]。在以往一项前瞻性探索研究(n=75)中,单独接受主动脉瓣生物瓣膜置换的患者随机分为两组,每组接受不同的抗血栓治疗:第一组前3个月使用华法林(INR范围2.0~3.0),继之以阿司匹林(100 mg/d),第二组则单用阿司匹林(100 mg/d),结果显示:两组术后24 h至3个月发生一次脑缺血事件(2.8%与2.9%,P值无统计学意义),两组间的主要出血率、无卒中生存率和总生存率亦相似,该试验结果提示与阿司匹林抗血小板治疗相比,华法林抗凝并未为预防血栓栓塞带来明显益处。目前尚无数据支持生物瓣膜患者长期使用抗凝药物。鉴于此,有学者提出对于二尖瓣生物瓣置换者,建议用华法林(INR 2.0~3.0)抗凝3个月,然后进行抗血小板治疗;对于主动脉生物瓣膜,抗血小板治疗比抗凝治疗更有效。
推荐意见:(1)机械瓣膜推荐终生口服华法林,NOACs禁用于机械瓣膜患者,尤其是达比加群;生物瓣膜推荐长期使用阿司匹林(强推荐,高质量证据)。(2)对于曾发生缺血性卒中的机械瓣置换患者,主动脉机械瓣的INR目标值为2.5(范围2.0~3.0),如有栓塞事件危险因素(AF、左心室功能障碍或高凝状态等),可上调至3.0(范围2.5~3.5);二尖瓣机械瓣的INR目标值为3.0(范围2.5~3.5)。如出现栓塞事件,且出血风险不高,可添加低剂量阿司匹林(75~100 mg/d)治疗(弱推荐,中等质量证据)。(3)对于曾发生缺血性卒中的生物瓣置换患者,给予3~6个月的华法林,INR目标值为2.5(范围2.0~3.0),随后可长期口服低剂量阿司匹林(75~100 mg/d)(弱推荐,低质量证据)。
预防心肌病所致卒中是否使用抗凝药物取决于患者有无房性心律失常,目前指南推荐华法林用于心肌病(包括DCM)合并AF者的治疗[36],但对呈窦性心律的心肌病是否抗凝仍有争议。针对左室射血分数低但无心律失常的DCM患者,以往3项抗凝治疗的随机临床试验表明,用华法林抗凝并不能降低缺血性卒中的风险,或者其预防性获益被大出血的风险所抵消。
推荐意见:(1)对于已经有附壁血栓形成和CES并发症的DCM患者,应长期抗凝治疗,口服华法林至少3个月,需调节剂量使INR保持在1.8~2.5之间,或使用NOACs(如达比加群、利伐沙班等)(弱推荐,低质量证据)。(2)对于窦性心律的缺血性卒中患者,伴有DCM(左室射血分数≤35%)但无左房或左室血栓证据时,采用华法林、NOACs(阿哌沙班、达比加群或利伐沙班)还是抗血小板治疗应视情形个体化,同时需注意观察出血风险(无等级基于共识的声明)。
迄今,尚无明确的相关治疗指南,治疗建议来自以往的病例报道或回顾性研究。其中,在德国的一项回顾性队列研究中,共纳入52例心脏黏液瘤患者,其中13例分别合并TIA(23%)、缺血性卒中(61%)和视网膜缺血(15%)。46%的患者在抗血小板或抗凝治疗情况下发生脑血管事件(cerebrovascular events,CVE),23%的患者在心脏黏液瘤手术切除前的桥接抗栓治疗期间出现CVE复发。CVE和心脏黏液瘤手术之间的时间间隔延长与CVE复发显著相关(P=0.021)。
推荐意见:(1)肿瘤一旦诊断明确,建议尽早行心脏手术切除,尤其是那些合并TIA或视网膜缺血而无急性缺血性卒中者(无等级基于共识的声明)。(2)抗凝或抗血小板治疗不能替代心脏手术,应将其桥接至手术的间隔尽可能缩短(弱推荐,低质量证据)。
目前,有关抗栓治疗在AAA相关CES二级预防方面的数据相对较少,在一项法国关于卒中主动脉斑块的观察性研究中,抗血小板和抗凝治疗者有相似的复发事件。随后的ARCH(主动脉弓相关的脑危害)试验专门为研究主动脉栓塞设计,纳入了卒中、TIA或胸主动脉弓斑块(厚度>4 mm)所致周围动脉栓塞的患者(n=349),随机分为DAPT组(氯吡格雷和阿司匹林)和华法林组,平均随访3.4年,结果显示:卒中、心肌梗死、外周栓塞和血管死亡的发生率在DAPT组为7.6%,华法林组则为11.3%(P=0.2),但华法林组的血管性死亡更多。在SOCRATES试验事后分析中,患有主动脉弓疾病和(或)颈动脉狭窄<50%的亚组在接受替格瑞洛治疗后90 d内卒中、心肌梗死或死亡的发生率低于阿司匹林(3.7%比7.1%;HR=0.51,95%CI:0.29~0.90;P=0.020 8)[54]。近来,在法国和韩国进行的一项平行组试验中,共纳入2 860例缺血性卒中或TIA患者,均患有动脉粥样硬化性疾病[包括颅外或颅内动脉狭窄、主动脉弓粥样易损斑块(厚度≥4 mm)或者已知的冠状动脉病史],并接受他汀和(或)依折麦布,按降低LDL-C水平目标值分为低靶目标组(LDL-C<700 mg/L或1.8 mmol/L)、高靶目标组(LDL-C为900~1 100 mg/L或2.3~2.8 mmol/L)两组,平均随访3.5年,结果显示复合主要终点(缺血性卒中、心肌梗死、新症状所致紧急冠状动脉或颈动脉血运重建,或死于心血管疾病)在低靶目标组发生了121例(8.5%),高靶目标组156例(10.9%)(校正后HR=0.78,95%CI:0.61~0.98,P=0.04),而两组间颅内出血和新诊断糖尿病的发生率比较差异无统计学意义[55]。
推荐意见:目前无特殊治疗方法,建议控制动脉粥样硬化危险因素,并给予强化他汀调脂至LDL-C<700 mg/L(1.8 mmol/L)和抗血小板治疗(弱推荐,低质量证据)。
目前这部分的相关高等级研究证据较少,卒中急性期患者入住综合医院神经内科或卒中单元后,应立即给予全面的身体状况评估,成立由多学科组成的卒中康复治疗小组[56]。
推荐意见:在病情稳定的情况下应尽早开始康复治疗,对轻到中度神经功能障碍的缺血性卒中患者可在发病后24 h后进行床边康复、早期离床期的康复训练,包括坐、站、走等活动(无等级基于共识的声明),具体参照《中国卒中早期康复治疗指南》[56]。
本共识在制订过程中参考了最新研究进展及相关指南,并通过专家组多次讨论审阅而最终成稿,为临床医生提供心源性卒中治疗的规范化指导。另一方面,本共识内容仅系该领域的阶段性认识,临床实践过程中仍有诸多问题需要探索,如发病后抗凝治疗启动或重启时间、IE相关卒中的心脏手术时机等,期待未来开展相关临床研究提供进一步的证据,从而为CES患者带来更多临床获益。
执笔:刘广志(首都医科大学附属北京安贞医院神经内科);胡荣(首都医科大学附属北京安贞医院心脏中心);彭丹涛(中日友好医院神经内科)
顾问组成员(按姓氏拼音排序):董强(复旦大学附属华山医院神经内科);黄一宁(北京大学第一医院神经内科);吉训明(首都医科大学宣武医院神经外科);马长生(首都医科大学附属北京安贞医院心脏中心)
专家组成员(按姓氏拼音排序):丁文虹(首都医科大学附属北京安贞医院儿童心血管病中心);杜昕(首都医科大学附属北京安贞医院心脏中心);杜怡峰(山东省立医院神经内科);樊东升(北京大学第三医院神经内科);冯立群(首都医科大学附属北京安贞医院神经内科);郭秀海(首都医科大学宣武医院神经内科);何志义(中国医科大学附属第一医院神经内科);胡荣(首都医科大学附属北京安贞医院心脏中心);黄晓红(中国医学科学院阜外医院特需医疗诊治中心);纪勇(首都医科大学附属北京天坛医院神经中心);荆志成(中国医学科学院北京协和医院心内科);来永强(首都医科大学附属北京安贞医院心脏外科);李锐(陕西省人民医院神经内科);李淑娟(中国医学科学院阜外医院神经内科);刘广志(首都医科大学附属北京安贞医院神经内科);刘丽旭(中国康复研究中心北京博爱医院神经康复中心);陆正齐(中山大学附属第三医院神经内科);马欣(首都医科大学宣武医院神经内科);缪中荣(首都医科大学附属北京天坛医院神经介入科);彭丹涛(中日友好医院神经内科);任力杰(深圳市第二人民医院神经内科);任学军(首都医科大学附属北京安贞医院心脏中心);王辉(首都医科大学附属北京安贞医院放射科);王丽华(哈尔滨医科大学附属第二医院神经内科);文国强(海南省人民医院神经内科);武亮(北京小汤山医院康复中心);邢岩(航空总医院神经内科);徐俊(首都医科大学附属北京天坛医院神经中心);徐磊(首都医科大学附属北京安贞医院放射科);许予明(郑州大学第一附属医院神经内科);杨旗(首都医科大学附属北京朝阳医院放射科);杨新健(首都医科大学附属北京天坛医院神经外科-北京市神经外科研究所);章军建(武汉大学中南医院神经内科);张茁(首都医科大学附属北京安贞医院神经内科);张海波(首都医科大学附属北京安贞医院心脏外科);张玉顺(西安交通大学第一附属医院心脏内科);张占军(北京师范大学认知神经科学与学习国家重点实验室);赵冬(北京心肺血管疾病研究所-安贞医院流行病研究室);朱天刚(北京大学人民医院心脏中心)
所有作者均声明不存在利益冲突



























