
呼吸道合胞病毒(respiratory syncytial virus,RSV)是导致1岁以下婴儿罹患下呼吸道感染(lower respiratory tract infection,LRTI)的首要病毒病原,严重危害婴儿健康。大部分(约80%)RSV感染的LRTI住院婴儿是足月出生的健康婴儿。目前国内RSV预防和治疗领域,尚无有效药物或预防手段。新型全人源长效单克隆抗体Nirsevimab具有较强中和RSV能力、超长半衰期,通过单剂注射,即可为所有婴儿在第1个RSV流行季提供快速直接的免疫保护,预示预防婴儿RSV感染新时代即将来临。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
呼吸道合胞病毒(respiratory syncytial virus,RSV)是全球5岁以下儿童急性下呼吸道感染(lower respiratory tract infection,LRTI)最常见的病毒病原,也是导致1岁以下婴儿罹患LRTI住院的首要病毒病原[1]。目前尚无特异的抗RSV药物,临床仍然以对症支持治疗为主。迄今为止,尚无商品化疫苗可主动免疫预防RSV感染,唯一被美国食品与药品监督管理局(FDA)批准用于RSV被动免疫预防的帕利珠单抗(Palivizumab)尚未引进国内[2] 。2021年6月,世界卫生组织(WHO)制定了《世界卫生组织推荐用于呼吸道合胞病毒感染被动免疫理想的单克隆抗体的产品特性》,优先考虑使用被动免疫制剂长效单克隆抗体(以下简称单抗)保护婴儿免遭RSV危害[3]。2022年3月3日,《新英格兰医学杂志》发表了Nirsevimab 3期临床试验结果[4],显示对于健康的晚期早产儿和足月儿,新型长效单抗Nirsevimab预防RSV引起的LRTI具有良好安全性和有效性,预示预防婴儿RSV感染新时代即将来临。值此契机,现就婴儿RSV感染疾病负担以及Nirsevimab的临床研发进展进行阐述,以提升广大医务工作者对新型长效单抗预防婴儿RSV感染的认识。
基本再生指数(basic reproduction number,R0)是指在没有干预的情况下,全部是易感人群的环境中,平均1个患者可以传染的人数,是衡量病毒传播能力的最重要参数[5]。RSV是导致婴儿呼吸道感染最常见的病毒,具有明显的季节性,传染性较强,其R0为4.5(IQR:1.7~8.2)[6]。儿童普遍易感RSV,80%以上儿童在1岁前被感染,几乎所有儿童在2岁前均感染过RSV[7]。据估计,2015年全球约有3 310万5岁以下RSV相关LRTI新发病例,其中10%发展为重症,需要住院治疗,死亡病例约4.80万~7.45万[1]。在中国,每年约有61.9万~94.8万5岁以下儿童因RSV感染而住院,其中婴儿有21.5万~50.0万[8]。
RSV感染临床表现差异很大,可以表现为症状轻微的上呼吸道感染,也可表现为严重LRTI(毛细支气管炎或肺炎)[2]。既往认为早产儿或有基础疾病婴儿是患严重RSV感染的高风险人群,但国内外研究发现,大部分(美国79%、中国85.3%)因RSV感染住院的肺炎病例为足月出生的健康婴儿,因此,所有婴儿都面临着RSV的威胁[9,10]。此外,在生命早期感染RSV的儿童后续有发生反复喘息、气道高反应以及哮喘的风险[11]。RSV感染给医疗卫生系统的所有领域带来巨大负担,包括门诊、急诊和住院医疗资源消耗。据Meta分析估计,2017年全球用于管理5岁以下儿童RSV感染的直接医疗费用约为48.2亿欧元,其中约55%为住院费用[12]。RSV的急性感染以及长期并发症的管理都将对社会、医疗和家庭造成巨大的经济负担。
目前,尚无RSV疫苗及有效的抗病毒药物用于RSV感染的防治,RSV预防产品研发被WHO列为全球最优先开发产品之一[13,14]。RSV免疫预防分为被动预防(预防用单抗)和主动预防(疫苗接种)[15]。
被动免疫指注射同种或异种抗体获得免疫力。被动免疫预防感染性疾病历史悠久,早在1930年,我国现代儿科学之父诸福棠教授用胎盘球蛋白预防麻疹,开创了被动免疫预防感染性疾病的先河[16]。1998年,美国FDA批准可用于RSV预防的帕利珠单抗,为人鼠嵌合型单抗,仅用于具有高危因素特殊婴幼儿预防RSV感染,因半衰期短,需要每月注射,目前也尚未引进国内应用[2],因此亟需探索新型被动免疫制剂。长效、全人源预防RSV单抗一直是全球各国研发的热点。当前处于临床试验的RSV单抗共有3种,包含全人源单抗Nirsevimab、全人源单抗TNM001、全人源单抗MK-1654(表1),其中,Nirsevimab是首个完成3期临床试验的单抗,研发进展最快。
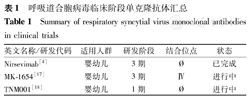
呼吸道合胞病毒临床阶段单克隆抗体汇总
Summary of respiratory syncytial virus monoclonal antibodies in clinical trials
2022年3月3日发表在《新英格兰医学杂志》的《Nirsevimab for Prevention of RSV in Healthy Late-Preterm and Term Infants》研究显示,长效、全人源单抗Nirsevimab预防婴儿RSV感染取得令人鼓舞的结果[4]。Nirsevimab的临床试验也被《自然医学》(Nature Medicine)列为"2022年将改变药物未来的十一大临床试验之一"[19]。根据新闻显示,Nirsevimab已于2022年2月在欧洲提交了注册上市申请(NDA)[20],提示长效单抗预防婴儿RSV感染新时代即将来临。
Nirsevimab靶向结合RSV融合(F)蛋白融合前构象上高度保守Ø表位,因此中和RSV能力大大提高。Nirsevimab是全人源单抗,识别融合前F蛋白(Pre-F)抗原表位Ø,阻止F蛋白介导病毒和细胞膜融合,对A、B两个亚型都有很强的中和作用。Pre-F特有抗原表位Ø诱导的中和抗体能力高于抗原表位Ⅱ(帕利珠结合位点)(图1)。Nirsevimab对RSV A2和RSV B9320毒株的半数抑制浓度(IC50)值分别为2.2 μg/L和1.8 μg/L,较帕利珠单抗的中和活性高50倍[21,22] 。
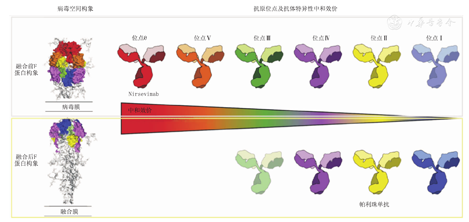

注:融合前F蛋白构象可诱导针对F蛋白上已识别的所有抗原位点(Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ和Ø)的抗体,但融合后F蛋白构象只有4种抗原表位(Ⅰ、Ⅱ、Ⅲ和Ⅳ)。融合前F蛋白特有的抗原表位Ø诱导中和抗体能力高于其他抗原表位
Antigenic sites Ⅰ-Ⅳ are shared between the prefusion F protein (pre-F) and post fusion F protein (post-F),but sites Ø and V are displayed exclusively on the pre-F conformation.Among all the sites,sites Ø has been shown to elicit antibodies with highest neutralizing activity
Nirsevimab采用M252Y/S254T/T256E (YTE)位点突变技术,因此获得超长半衰期。YTE位点突变技术是将IgG抗体的Fc结构域进行3种氨基酸替换,即252、254和256位的蛋氨酸(Met,M)、丝氨酸(Ser,S)和苏氨酸(Thr,T)分别被酪氨酸(Tyr,Y)、苏氨酸(Thr,T)和谷氨酸(Glu,E)替换,可以在较低pH值条件下提高IgG与新生儿Fc受体(FcRn)的亲和力。Nirsevimab通过pH依赖方式结合FcRn,避免其被细胞溶酶体降解,从而延长单抗的半衰期(图2)[23,24]。Nirsevimab的高中和能力及超长半衰期,为保护所有婴儿免遭RSV侵害奠定了基础。
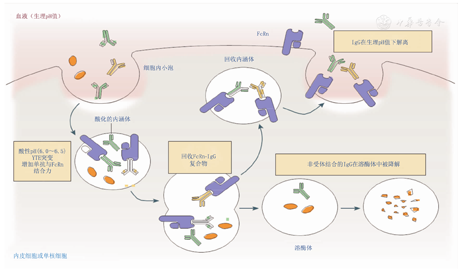
注:IgG的新生儿Fc受体(FcRn)由内皮细胞和循环单核细胞表达。这些细胞以胞吞作用摄取血液中的IgG,后者在酸化的内涵体与FcRn结合。与FcRn结合呈pH依赖性,在pH 7.4的生理条件下,FcRn与Fc不结合;在细胞内涵体pH 6.0~6.5的酸性条件下,两者结合,从而避免IgG在细胞内被溶酶体等快速降解。FcRn将IgG回收至血液循环中,从而延长其血清半衰期
The neonatal Fc receptor (FcRn) for IgG is expressed by endothelial cells and circulating monocytes.These cells internalize serum IgG,which binds to FcRn in an acidic endosomal compartment.The binding with FcRn was pH dependent.Under the physiological condition of pH 7.4,FcRn did not bind with Fc;Under the acidic condition of pH 6.0-6.5 of intracellular endosomes,the two combine to avoid the rapid degradation of IgG by lysosomes in cells.FcRn then recycles IgG back into circulation,thus extending its serum half-life
帕利珠单抗是目前唯一用于预防RSV感染的单抗,用于高危早产儿,这部分婴儿仅占整个出生婴儿的4%~6%[9,25,26]。2020年和2022年,2年内《新英格兰医学杂志》连续发表2项Nirsevimab随机双盲安慰剂对照临床试验结果和1项随机双盲对照试验,介绍全人源长效单抗Nirsevimab对婴儿RSV感染的预防效果和安全性。
第1篇《Single-Dose Nirsevimab for Prevention of RSV in Preterm Infants》介绍了Nirsevimab全球2b期研究,入组1 453例胎龄29~34周出生的健康早产儿,结果证明单剂注射Nirsevimab可在整个RSV流行季,给健康早产儿提供持续5个月的持久保护。Nirsevimab降低了70.1%的RSV-LRTI就诊率(95%CI:52.3%~81.2%,P<0.001)和78.4%的RSV-LRTI住院率(95%CI:51.9%~90.3%,P<0.001)。在不同地理区域以及RSV的A、B亚型中,在使用Nirsevimab后150 d内均观察到一致保护效果,提示其可同时中和多种A、B亚型RSV。给药后第91天,受试者中检测到抗药物抗体(ADAs) (Nirsevimab组为5.6%,安慰剂组为3.8%)。ADAs对Nirsevimab药物动力学、疗效和安全性均无影响。此外,在Nirsevimab接种后第151天,近98%的婴儿血清中和抗体滴度高于90%最大效应浓度(EC90),提示Nirsevimab保护时间至少可持续5个月[28]。
第2篇《Nirsevimab for Prevention of RSV in Healthy Late-Preterm and Term Infants》介绍了Nirsevimab全球3期研究,将受试者人群扩大到胎龄35周之后出生的晚期健康早产儿和足月儿。研究共入组1 490例进入第1个RSV流行季的足月婴儿或晚期早产儿(胎龄35周或以上),研究证明单次肌内注射Nirsevimab可在整个RSV流行季,给晚期健康早产儿及足月儿提供持续5个月保护。结果显示,Nirsevimab降低了74.5%的RSV-LRTI就诊率(95%CI:49.6%~87.1%,P<0.001),同时观察到RSV感染导致的住院患儿人数减少(62.1%,95%CI:8.6%~86.8%;P=0.07)。研究者还对3期及2b期试验中RSV导致住院情况进行预先设定的合并分析,结果发现在足月儿和早产儿(胎龄>28周)中,Nirsevimab降低了77.3%的RSV感染相关住院率(95%CI:50.3%~89.7%,P<0.001),两组安全性比较差异无统计学意义[4] 。
第3篇《Safety of Nirsevimab for RSV in Infants with Heart or Lung Disease or Prematurity》介绍了Nirsevimab全球2/3期研究,入组925例进入第1个和第2个RSV流行季且符合帕利珠单抗使用条件的高风险婴幼儿,证明在有显著血流动力学异常的先天性心脏病(CHD)及慢性肺疾病(CLD)婴儿和早产儿中,Nirsevimab的安全性与帕利珠单抗相似[29]。
综上,这3个基于早期早产儿(2b期)[28]、晚期早产儿及足月儿(3期)[4]和具有高危因素的早产儿(2/3期)[29]相关临床试验,证实长效单抗Nirsevimab只需单次肌内注射,即可在第1个RSV流行季为所有婴儿提供快速、持久、安全的免疫保护。
目前,Nirsevimab已获得全球多个权威监管机构的加速开发资格,其中包括中国国家药品监督管理局药品审评中心(NMPA)"突破性治疗药物程序";FDA"突破性疗法"认定;欧洲药品管理局(EMA)"优先药物计划";英国药品和保健品管理局(MHRA)"突破性创新药物"资格认定。此外,还被日本医学研究开发署(AMED)选为"促进儿科新药开发的药物遴选研究计划"中"优先开发药物"[30]。但需要同时关注以下几个问题。
制定合理的免疫策略。理解RSV疾病负担有利于帮助决策者确定免疫策略。有研究表明,住院的1岁以下婴儿中,51%是在RSV流行季节外出生[31],为尽可能避免严重的疾病和死亡,推荐对流行季节外出生婴儿在RSV流行季节开始前,在常规疫苗接种点接种预防用长效单抗。具体月份需根据各地RSV流行季节开始时间调整。搭建全国RSV监测系统,将有利于精确流行季节外出生婴儿单抗的最佳接种时间。因免疫系统尚未发育成熟,呼吸道黏膜分泌型抗体IgA(sIgA)产生缓慢,低月龄儿感染RSV重症比例明显更高,住院率最高人群为1月龄婴儿,病死率最高人群为2月龄以下婴儿,推荐RSV流行季节内出生婴儿,出生后尽早在产科接种预防用长效单抗[32]。未来具体接种场景和免疫策略,需结合国情进行更多政策、药物经济学等多维度评估。
监测RSV变异与Nirsevimab耐药。由于Nirsevimab针对F蛋白中最易变区域,Nirsevimab大量应用后可能会出现耐单抗毒株[33]。因此,要搭建RSV分子流行病学及Nirsevimab耐药性监测系统,及时监测RSV抗原漂移及Nirsevimab耐药发生情况。
评估Nirsevimab对RSV感染远期疾病负担的影响。在生命早期感染RSV的儿童后续有发生反复喘息、哮喘风险[11]、成人期慢性阻塞性肺疾病风险[34],从生命全周期管理角度出发,需评估Nirsevimab能否降低RSV感染远期疾病负担。
总之,Nirsevimab的成功研发将开拓长效单抗预防婴儿RSV感染的新时代。针对中国健康婴儿3期临床研究(NCT05110261)也已启动。政府、疾病预防控制和临床医疗机构需协同从免疫策略、流行病学监测、大规模疗效和安全性评估等方面继续开展研究,以提升RSV感染的防控水平,保护儿童生命健康。
所有作者均声明不存在利益冲突



























