2021年心力衰竭(心衰)临床研究领域出现了一些新进展和新认识,本文将从中国心衰防治水平的提升,心衰重大临床研究的突破,心衰新理念的出现,以及心衰药物治疗的现状和未来4个方面介绍2021年心衰临床研究领域的进展。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
2021年,心力衰竭(心衰)领域的新研究迭出,有的对未来临床实践影响较大或潜在应用价值较高。同时,3部有影响的国际心衰指南/专家共识颁布,提出的理念、建议和推荐,具有新意和一定借鉴应用价值。本文将从临床和实用的角度,搜集这些亮点,加以分析和解读。
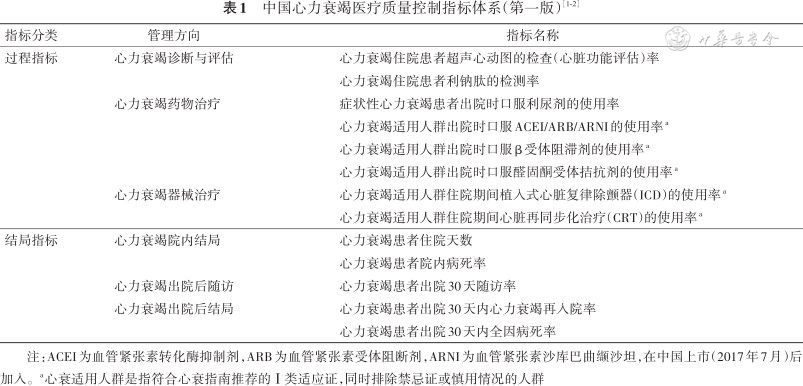
1. 中国心衰医疗质量控制报告首次发布:《2020年中国心力衰竭医疗质量控制报告》[1](报告)是我国首次发布的心衰医疗质量控制报告,既是对我国近几年心衰临床工作的总结,又为未来提高我国的心衰防治水平指明方向,值得重视和认真学习。(1)中国心衰医疗质量控制指标体系:报告中介绍的“中国心力衰竭医疗质量控制指标体系”(表1)是心衰管理的“地板”(基本要求),基层医院要遵循,三级医院也要遵循;全科医师应执行,心衰专家也应执行。实施过程中可以酌情“提高”水平,但不能降低标准。这些指标应该在心衰指南中列为Ⅰ类推荐。(2)我国心衰工作的现状、进步和差距:报告数据来源于2017年1月至2020年10月期间,全国27个省、直辖市和自治区的34 938例心衰住院患者。据报告分析,我国心衰病因主要为高血压(56.3%)和冠心病(52.8%),其次为瓣膜性心脏病(18.7%)和扩张型心肌病(16.3%)。合并症主要为糖尿病、肾功能不全和心房颤动(房颤)或心房扑动(房扑)。与美国心脏学会(American Heart Association,AHA)的“跟着指南走——心力衰竭”(Get With The Guideline-Heart Failure,GWTG-HF)项目的同期数据比较发现,我国住院心衰患者年龄较小、女性比例较低,收缩压水平较低;心衰病因中高血压的比例明显较低,冠心病和瓣膜性心脏病的比例也较低;合并症中糖尿病、房颤或房扑的比例也较低。与既往的“中国心力衰竭注册登记研究(China-HF)”(2012~2015年)[2, 3]结果比较,我国心衰患者超声心动图检查(心脏功能评估)率和利钠肽的检测率,心衰适用人群出院时肾素-血管紧张素系统(renin-angiotensin system,RAS)阻滞剂,包括血管紧张素转化酶抑制剂(angiotensin converting enzyme inhibitor,ACEI)/血管紧张素受体拮抗剂(angiotensin receptor blocker,ARB)/血管紧张素受体脑啡肽酶抑制剂(angiotensin receptor neprilysin inhibitor,ARNI,沙库巴曲缬沙坦),β受体阻滞剂及醛固酮受体拮抗剂(螺内酯)的使用率均有明显提高;但RAS阻滞剂应用的种类有所不同,其中,ACEI或ARB使用率明显下降,而ARNI使用率显著升高,提示我国心衰患者规范化诊疗水平有了明显提高。但是,与GWTG-HF项目比较,我国住院心衰患者中超声心动图检查率及心衰适用人群出院时RAS阻滞剂、β受体阻滞剂的使用率仍低于美国,而植入式心脏转复除颤起搏器(implantable cardioverter defibrillator,ICD)和心脏再同步化治疗(cardiac synchronization therapy,CRT)的使用率则更低,但我国心衰适用人群出院时醛固酮受体拮抗剂的使用率高于美国。(3)心衰不规范治疗情况值得关注:我国住院心衰合并低血压患者中应用RAS阻滞剂较多见,其中,出院收缩压<90 mmHg(1 mmHg=0.133 kPa)的心衰患者中ACEI的使用率为15.9%,出院收缩压<95 mmHg的心衰患者中ARNI的使用率为35.5%。合并严重肾功能不全的心衰患者中不恰当应用RAS阻滞剂的现象也较多见,其中,血肌酐>221 μmol/L的心衰患者中ACEI、ARB和ARNI的使用率分别为6.8%、10.8%和7.8%。此外,心衰患者不符合适应证应用CRT的现象也不少见,其中,CRT植入前左心室射血分数(left ventricular ejection fraction,LVEF)>35%患者占28.8%,植入前心电图QRS间期<130 ms患者占25.7%。治疗过度或不当:在我国射血分数降低的心力衰竭(heart failure with reduced ejection fraction,HFrEF)患者中ARNI的使用率明显高于美国,但是存在治疗过度或不当现象,在收缩压<95 mmHg的患者中使用率高达45.6%,在血肌酐>221 μmol/L的患者中使用率也达16.3%。在植入CRT的心衰患者中,符合Ⅰ类推荐的仅占47.2%,有禁忌证(Ⅲ类适应证)却有25.7%。
| 指标分类 | 管理方向 | 指标名称 |
|---|---|---|
| 过程指标 | 心力衰竭诊断与评估 | 心力衰竭住院患者超声心动图的检查(心脏功能评估)率 |
| 心力衰竭住院患者利钠肽的检测率 | ||
| 心力衰竭药物治疗 | 症状性心力衰竭患者出院时口服利尿剂的使用率 | |
| 心力衰竭适用人群出院时口服ACEI/ARB/ARNI的使用率a | ||
| 心力衰竭适用人群出院时口服β受体阻滞剂的使用率a | ||
| 心力衰竭适用人群出院时口服醛固酮受体拮抗剂的使用率a | ||
| 心力衰竭器械治疗 | 心力衰竭适用人群住院期间植入式心脏复律除颤器(ICD)的使用率a | |
| 心力衰竭适用人群住院期间心脏再同步化治疗(CRT)的使用率a | ||
| 结局指标 | 心力衰竭院内结局 | 心力衰竭患者住院天数 |
| 心力衰竭患者院内病死率 | ||
| 心力衰竭出院后随访 | 心力衰竭患者出院30天随访率 | |
| 心力衰竭出院后结局 | 心力衰竭患者出院30天内心力衰竭再入院率 | |
| 心力衰竭患者出院30天内全因病死率 |
注:ACEI为血管紧张素转化酶抑制剂,ARB为血管紧张素受体阻断剂,ARNI为血管紧张素沙库巴曲缬沙坦,在中国上市(2017年7月)后加入。a心衰适用人群是指符合心衰指南推荐的Ⅰ类适应证,同时排除禁忌证或慎用情况的人群
2. 中国心衰的管理体系和大样本研究队列已经形成:China-HF研究[3, 4]是首个全国范围的心衰注册登记研究,纳入了2012年1月至2015年9月期间全国132家医院13 687例有完整数据的成年心衰患者,详尽描述了我国住院心衰患者的临床特点。2018年3年建立了国家心血管病中心心力衰竭专病医联体(心衰医联体),承担心衰医疗质量控制(质控)工作,截至2020年10月,国家心衰医联体共纳入全国除西藏自治区及海南省外逾千家医院,涵盖了公立和民营医院,以及三级、二级和一级医院,这就为未来中国心衰工作奠定了坚实的基础。2018年5月,建立了心衰医联体质控数据库,截至2020年10月30日,共录入数据42 213例,为中国心衰医疗质控报告的形成和分析提供了客观、真实和可靠的依据。
3. 中国心衰临床研究正在走向世界:过去的一年,中国心衰团队成为国际心衰研究的主导和合作者。依司他沃(istaroxime)可抑制Na+/K+泵和激动肌浆网Ca2+泵,通过增强心肌收缩力,同时改善心脏的舒张功能。国家心血管病中心张健教授牵头的中国团队和欧洲团队共同设计和主持了该药的国际合作研究,结果己公布,受到国内外学术界的关注[5, 6]。标志着我国心衰新药研究已昂然进入国际多中心随机对照试验(randomized controlled trial,RCT)领域,不只是参与,也可以发挥主导作用。今后国内同行可以携手共同设计和开展这一类国际新药研究,以及心衰国际多中心、大样本RCT。
1. 钠葡萄糖协同转运蛋白-2(sodium glucose co-transporter-2,SGLT-2)抑制剂可用于不稳定HFrEF的研究。既往DAPA-HF研究[7]和EMPEROR-reduced研究[8]已经证实,SGLT-2抑制剂治疗慢性稳定性HFrEF患者有效,但是,对于不稳定心衰患者的疗效和安全性仍不清楚。索格列净(sotagliflozin)是一种新型的SGLT-1和SGLT-2双重抑制剂,SOLOIST-WHF试验[9](索格列净治疗糖尿病合并近期心衰恶化患者的研究)是一项国际多中心RCT。主要入选标准包括:年龄为18~85岁,由于出现心衰症状和/或体征恶化而住院并接受静脉利尿剂治疗,B型利钠肽(B type natriuretic peptide,BNP)≥150 pg/mL或N末端B型利钠肽原(N terminal-pro B type natriuretic peptide,NT-pro BNP)≥600 pg/mL(房颤时BNP≥450 pg/mL或NT-pro BNP ≥1800 pg/mL);主要排除标准包括:终末期心衰,近期急性冠状动脉综合征,经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)或冠状动脉旁路移植术(coronary artery bypass grafting,CABG),脑卒中,估算肾小球滤过率(estimated glomerular filtration rate,eGFR)<30mL·min-1·1.73m-2等。研究主要终点包括:心血管原因死亡、心衰住院或因心衰紧急就诊的临床事件。研究入选了1 222例患者,安慰剂组614例,索格列净组608例,结果表明,与安慰剂比较,索格列净治疗显著降低主要终点事件风险达33%(风险比HR 0.67,95%可信区间CI 0.52~0.85,P<0.001)。但是心血管死亡或全因死亡并未降低,提示获益主要来自因心衰住院或急诊就诊总数的减少。SOLOIST-WHF研究二次分析结果显示,索格列净减少心衰患者总住院量(包括首次和反复的),相应地增加了院外存活天数。在近期因心衰恶化住院2型糖尿病患者中减少随后的住院率,减少的住院量为每100人年29.0[10]。SCORED研究[11]也是一项国际多中心RCT,共纳入了10 584例糖尿病伴慢性肾脏病(chronic kidney disease,CKD)患者。主要复合终点为包括心血管死亡、心衰住院、因心衰紧急就诊的临床事件。主要入选标准包括:2型糖尿病(糖化血红蛋白HbA1c≥7%),eGFR 25~60 mL·min-1·1.73m-2(伴或不伴有大量或微量蛋白尿),有心血管危险因素。结果表明,与安慰剂相比,索格列净显著降低主要终点事件风险达26%。
2. 急性心肌梗死(acute myocardial infarction,AMI)后的治疗研究。AMI后的二级预防,RAS阻滞剂(ACEI或ARB)的应用没有争议。对于慢性心衰,ARNI优于ACEI或ARB亦有确凿证据,但AMI后患者应用ARNI是否也优于ACEI或ARB,则尚不清楚。PARADISE-MI试验(心肌梗死后ARNI沙库巴曲缬沙坦和ACEI雷米普利用于心力衰竭预防比较的研究)[12]回答了这个问题。该研究为大样本、双盲、阳性药物对照的试验,在41个国家和(或)地区的495个中心共纳入5 661例患者,临床特征为AMI后0.5~7天、LVEF≤40%,和(或)有短暂性肺淤血,伴有危险因素的患者。年龄为(64±12)岁,女性占24%,76%为ST段抬高型心肌梗死,87%接受了PCI,平均LVEF为37%,Killip心功能分级≥2级占58%。关键排除因素包括有心衰病史、随机前24h因为临床状况不稳定接受利尿剂治疗、eGFR<30 mL·min-1·1.73m-2和血管神经性水肿病史。中位数随访时间23个月。主要终点为心血管死亡、首次心衰住院或门诊心衰的复合終点。结果表明,与雷米普利(滴定至5 mg,2次/d的目标剂量)相比,ARNI(滴定至97/103 mg,2次/d的目标剂量)降低主要终点发生率10%,但未达到降低15%的统计学显著改善的阈值;次要终点风险下降16%,也未达到差异显著性的阈值(P=0.045)。两组不良事件发生率相当,血管性水肿、血钾异常、肾功能不全或肝脏异常的发生率方面均无没有显著差异,提示ARNI和雷米普利一样,在AMI患者的应用具有良好的耐受性和安全性。不过,ARNI组低血压发生率略高,而雷米普利患者出现咳嗽略高。显然,ACEI/ARB/ARNI,可同样应用于AMI后患者。
3. 晚期心衰患者不能从ARNI治疗中获益。晚期心衰(advanced HF)主要指纽约心脏协会(New York Heart Association,NYHA)心功能分级Ⅳ级患者,是临床试验的“盲区”,纳入的病例很少,又是治疗上的难题,前进一步就是平均寿命仅半年的终末期心衰(end-stage HF)。PARADIGM-HF研究[13]已经证实了ARNI治疗慢性HFrEF患者的有效性,但是该研究中入选的NYHA心功能Ⅳ级患者仅占<1%,无法明确ARNI在这类心衰患者中的治疗价值。LIFE研究[14](ARNI治疗晚期HFrEF患者的研究)正是为这一目的而设计和实施,由著名美国心脏病学和心衰专家Braunwald团队主持,美国国立卫生院(National Institutes of Health,NIH)给予资助。采用替代终点,旨在评估ARNI在晚期心衰患者中降低NT-proBNP水平是否优于缬沙坦。主要终点为治疗24周后测量的NT-proBNP与基线比较比值的曲线下面积(area under the curve,AUC)。二级终点包括:疗效终点为存活天数,院外和无心衰事件;药物耐受性评价包括低血压、肾功能恶化、高钾血症等。关键的三级临床结局包括心血管死亡或心衰住院,心衰住院,心血管死亡,全因死亡。研究共纳入335例患者,ARNI组和缬沙坦组分别纳入167例和168例患者,除缺血性心肌病ARNI组较多外,两组患者的基线特征具有可比性。患者的临床特点如下:(1)NYHA心功能分级Ⅳ级,此前3个月仍有症状;(2)6个月内使用过正性肌力药物;(3)遵循指南指导的药物治疗(guideline directed medical therapy,GDMT)已经3个月;(4)LVEF≤35%;(5)BNP≥250 pg/mL或NT-proBNP≥800pg/mL;(6)收缩压≥90 mmHg;(7)具有以下其他客观指标之一的晚期心衰患者:6个月内心衰住院≥1次,12个月内LVEF≤25%,12个月内峰值摄氧量降低,3个月内6分钟步行距离<300米。结果表明,ARNI与缬沙坦比较,两组主要终点NT-proBNP水平在治疗24周后均未降至基线以下,AUC亦无显著差异;二级终点和关键的三级临床结局未见降低;耐受性终点中非致命的高钾血症发生率ARNI组显著高于缬沙坦组(17%比9%,P=0.04)。提示晚期心衰应用ARNI并不优于缬沙坦,对于可以耐受RAS阻滞剂患者,ACEI/ARB和ARNI可同等应用,但ARNI引起的高钾血症需注意。总之,LIFE研究是一个小样本研究,设计上采用替代终点而非临床结局,具有局限性。但样本量是经计算而设计,其结果仍具可靠性和可信性。当然,也还需进一步研究证实。
4. GALACTIC-HF试验的二次分析或事后(post-hoc)分析。选择性心肌肌球蛋白激动剂——omecamtiv mecarbil(OM)是一种新型正性肌力药物,通过与心肌肌球蛋白ATP酶催化区结合,增加肌球蛋白与肌动蛋白的结合能力,从而增强心肌收缩力,但不影响心肌细胞内钙浓度或心肌耗氧量。GALACTIC-HF试验[15]已经证实OM可以改善HFrEF患者预后。二次分析结果显示,OM对主要复合终点(心衰事件或心血管原因死亡)的影响与LVEF有关(持续相互作用P=0.004),LVEF水平越低,OM降低主要复合终点的绝对值随着LVEF降低而升高。其中,对于基线LVEF≤28%患者,主要复合终点的风险较安慰剂组显著降低16%(HR 0.84,95%CI 0.77~0.92,P=0.003),但在基线LVEF>28%的患者没有显著差异(HR 1.04,95%CI 0.94~1.16,P=0.45)。与LVEF处于最高四分位数的患者比较,LVEF处于最低四分位数(≤22%)患者绝对风险降低(absolute risk reduction,ARR)为7.4事件/100人年,3年需治疗人数(number need-to-treat,NNT)为11.8,即治疗11.8例3年,可以预防发生一次心衰事件或心血管原因死亡事件[16]。另外一项事后分析将GALACTIC-HF试验的研究对象分为严重心衰(定义为满足以下所有标准:NYHA心功能分级Ⅲ~Ⅳ级,LVEF≤30%,过去6个月内因心衰住院)和非严重心衰两组,结果发现,与安慰剂比价,OM治疗可以使严重心衰患者的主要复合终点风险显著降低20%(HR 0.80,95%CI 0.71~0.90),但在非严重心衰中无显著差异(HR 0.99,95%CI 0.91~1.08)[17]。
1. EMPEROR-Preserved研究[18](恩格列净对HFpEF患者心血管死亡和心衰住院影响的研究)旨在评估恩格列净对HFpEF患者的疗效和安全性,纳入了5 988例NYHA心功能分级Ⅱ~Ⅳ级且LVEF>40%的患者。主要复合终点为心血管死亡和因心衰住院,中位数随访时间为26.2个月。结果证实了恩格列净(10 mg/d)的良好效果:与安慰剂比较,恩格列净显著降低主要终点的风险21%(HR 0.79,95%CI 0.69~0.90,P<0.001),包括有或无糖尿病的及其他预设的亚组,且在不同LVEF亚组的结果与整体研究一致。二级终点也获阳性结果:恩格列净与安慰剂比较,显著降低心衰住院风险27%(HR 0.73,95%CI 0.61~0.88,P<0.001),并使肾功能受损速率减慢。这是首个证实药物治疗可以改善HFpEF患者预后的临床研究。恩格列净的整体安全性与既往在HFrEF研究中所见具有可比性,证实该药在HFpEF中应用亦是安全的。
既往药物治疗HFpEF患者的临床研究,包括CHARM-Preserved研究[19](坎地沙坦,2003年)、PEP-CHF研究[20](培哚普利,2006年)、I-PRESERVE研究[21](厄贝沙坦,2008年)、J-DHF研究[22](卡维地洛,2013年)、TOPCAT研究[23](螺内酯,2014年)及PARAGON-HF研究[24](沙库巴曲缬沙坦,2019年)均不能降低HFpEF患者的死亡和改善预后。而EMPEROR-Preserved研究是HFpEF首次成功的研究,提示恩格列净已成为唯一可改善HFpEF患者预后的药物,不仅会使数百万患者受益,也为未来对该药有效的作用机理和HFpEF的基础与临床特征提供了广阔的研究空间。
2. SOLOIST-WHF研究和SCORED研究的汇总分析:一项汇总分析(pooled analysis)纳入两个研究的HFpEF患者发现,与安慰剂比较,索格列净可以显著降低HFpEF患者的主要复合终点达37%(HR 0.63,95%CI 0.45~0.89,P=0.009),ARR为每100人年11.6事件,据此估测治疗1年避免1例事件的NNT为9[25]。这是首个在预先设定的随机化研究数据分析中显示出药物治疗对HFpEF患者具有显著影响。提示该药对失代偿(恶化)性心衰的有效性,适应证有可能进一步扩展至不稳定心衰及HFpEF患者。
3. PIROUETTE研究(Pirfenidone in Heart Failure with Preserved Ejection Fraction,吡非尼酮治疗HFpEF患者的随机2期试验):吡非尼酮(pirfenidone)是一种无血流动力学作用的口服抗纤维化的新药物。心肌纤维化是HFpEF的重要病理生理学机制,逆转心肌纤维化有可能改善心脏结构和功能、血液动力学状态和生活质量,甚至改善不良临床结局。PIROUETTE研究[26]是一项随机2期试验,旨在评估该药对慢性HFpEF患者心肌纤维化的影响。研究纳入LVEF≥45%和利钠肽升高患者,接受心脏磁共振(cardiac magnetic resonance,CMR)检查,有心肌纤维化迹象,定义为CMR测量的细胞外体积(extracellular volume,ECV)≥27%,随机分组,接受吡非尼酮组(目标剂量2 403 mg/d)或安慰剂治疗52周。研究主要终点为从基线至治疗52周时ECV的变化,次要终点包括NT-proBNP、心室和心房结构及功能、6分钟步行距离,堪萨斯城心肌病生活质量问卷(the Kansas City Cardiomyopathy Questionnaire,KCCQ)评分。纳入患者的临床特点为平均年龄78岁,男性占54%,基线时LVEF64%,NT-proBNP中位数为1 104pg/mL,心肌ECV平均值为30.1%。结果表明,吡非尼酮与安慰剂相比,在52周内显著降低心肌ECV(变化值为-1.21%,95%CI-2.12~-0.31,P=0.009)。6分钟步行距离增加,但未达到统计学差异,未能显著改善左心室舒张功能、心房大小和功能,右室大小和功能,以及KCCQ评分。本研究提示,吡非尼酮的确可以显著降低HFpEF合并心肌纤维化患者的心肌纤维化程度。但是临床结局未改善,可以理解,因为这仅是2期试验,观察时间、临床结局并非研究目标。至少说明该药有前景,值得进一步研究。
1. EMPULSE研究(恩格列净治疗住院急性心衰的研究)[27]:研究纳入急性心衰住院患者530例,包括初发(de novo)的急性心衰或慢性心衰急性失代偿(acute decompensated heart failure,ADHF)患者。病情稳定后随机分组。主要终点为临床获益,定义为全因死亡、心衰事件数及首次心衰事件时间的分层复合终点,采用Win Ratio法评估。次要终点为KCCQ-总体症状评分(KCC-TSS)的改善。随访90天。结果表明,恩格列净(10 mg/d)与安慰剂比较,主要终点临床获益显著增加36%(分层win ratio:1.36,95%CI 1.09~1.68,P=0.0054)。无论是新发的急性心衰还是ADHF,无论LVEF水平及有无糖尿病患者同样获益。次要终点显著增加4.5分,提示心衰患者症状和生活质量改善。这是首次在急性心衰住院患者病情稳定后使用SGLT-2抑制剂——恩格列净口服,证实是安全的并有显著临床疗效。过去近30年研究显示,急性心衰的急性期(30天),患者的死亡率未见显著降低,故这一阶段的治疗主要着重于改善症状和血液动力学状态。同时,易损期(出院后90天)死亡率和再住院率亦高居不下,而传统的“金三角”药物却因不良反应而不能使用或只能应用小剂量,难以达到满意的疗效。这就使急性心衰成为心衰领域最难攻克的堡垒之一。该研究提示,SGLT-2抑制剂——恩格列净将可能是改变急性心衰早期治疗格局并使患者获益的良药。不过,该试验样本量较小,随访时间不够长,其结果有待进一步证实。
2. 依司他沃(istaroxime)治疗急性心衰研究:这项2期临床试验采用多中心、随机、双盲、安慰剂平行对照的方法,旨在评价依司他沃治疗LVEF降低的ADHF患者的安全性、耐受性和有效性[28]。药物组共两个剂量:依司他沃0.5 μg·kg-1·min-1和 1.0 μg·kg-1·min-1,均以24h持续静脉输注。主要疗效终点为基线到输注后24h的超声心动图测量的E/e′比值变化。次要终点为治疗24h与基线的其他超声心动图参数的改变、呼吸困难VAS评分和NT-proBNP变化、心衰恶化。结果显示,依司他沃的两个药物剂量组的主要研究终点均达到了设计要求的统计学显著性。次要终点也达到了要求,每搏输出量增加、收缩压有所升高、NT-proBNP降低。安全性和耐受性良好。提示该药具有治疗急性心衰的潜力。期待Ⅲ期试验的结果。
1. 心脏移植的重大进展。美国马里兰大学医学院的研究人员采用猪心脏为一例终末期心衰患者做了人体内异种心脏移植手术。患者未来的结局,尚难以预测,但这是全球首例此类心脏移植,开了先河,具有重要的里程碑意义。
2. 心衰的康复治疗。GUIDE-HF(有创血液动力学监测对心衰临床结局影响的研究)[29]是在CHAMPION研究[30]基础上的拓展研究。纳入NYHA心功能Ⅱ~Ⅳ级或伴有利钠肽水平升高但近期没有心衰住院史的患者,应用CardioMEMSTM系统监测肺动脉压力指导心衰治疗,与常规治疗比较,并没有降低12个月时全因死亡和总心衰事件(心衰恶化住院和因心衰紧急医院就诊)复合终点,提示现代心衰规范治疗有效。目前,老年心衰患者的康复干预仍有争议和未解问题。REHAB-HF研究(康复干预对老年住院心衰患者影响的研究)[31]纳入349例年龄≥60岁的ADHF住院患者,随机分到常规管理(对照组)和康复干预组,涉及身体功能的举措,以个体化、渐进过渡的方式进行。主要终点为3个月时简易体能状况量表(Short Physical Performance Battery,SPPB)评分(总分为0~12分,分数越低表示身体功能障碍越严重),次要终点为6个月时全因再住院率。结果显示,3个月时干预组SPPB评分高于对照组(平均相差1.5分,95%CI 0.9~2.0,P<0.001);但6个月时两组患者的全因再入院率及全因死亡率无显著差异。提示老年ADHF住院患者的康复干预可行和安全,早期做可改善身体功能。
3. 心衰伴缺铁性贫血:此种情况较常见,对患者不良预后有一定影响。口服铁剂治疗无效。既往研究已经证实,静脉新型铁剂——羧基麦芽糖铁(ferric carboxymaltosc,FCM)治疗可改善慢性心衰患者的功能和生活质量[32]。新近,AFFIRM-AHF研究[33]表明,对于LVEF<50%的急性心衰住院合并铁缺乏(定义为铁蛋白<100 μg/L或铁蛋白100~299 μg/L且转铁蛋白饱和度<20%)患者,稳定出院后应用FCM治疗,可以显著降低心衰再住院风险,而且是安全的。最新的《2021欧洲心脏病学会(European Society of Cardiology,ESC)急性和慢性心力衰竭诊断和治疗指南》[34]推荐,所有心衰患者应定期做血常规、血清铁蛋白和转铁蛋白饱和度(transferrin saturation,TAST)的检测,对于有症状的,LVEF<45%伴有铁缺乏的心衰患者,推荐静脉应用FCM,以缓解心衰症状,改善运动耐量和生活质量(Ⅱa类推荐,A级证据)。
4.口服钾结合剂:心衰患者高血钾发生率较高,风险也大。常用的心衰治疗药物如ACEI/ARB/ARNⅠ、醛固酮拮抗剂也可能诱发高血钾,反过来血钾偏高必定限制这些作为心衰治疗基石药物的应用。临床上的确需要一种有助于控制心衰患者血钾水平的药物。口服钾结合剂patiromer和锆环状硅酸钠(sodium zirconium cyclosilicate,ZS-9)初步研究表明有助于降低血钾,使之维持在理想范围。
5.氯苯唑酸(tafamidis):2021年ESC心衰指南[34]已经推荐,氯苯唑酸用于治疗转甲状腺素蛋白型淀粉样变心肌病、NYHA心功能分级Ⅰ~Ⅱ级的患者(Ⅰ类推荐,B级证据),用以降低心血管原因住院和病死率,并延缓活动能力及生活质量下降的速度。
6. 心衰特殊人群个体化和区别治疗的理念:(1)心衰伴糖尿病:2021年ESC心衰指南[34]推荐,2型糖尿病患者应使用SGLT-2抑制剂,以降低心衰住院、主要心血管事件、终末期肾衰及心血管死亡的风险(Ⅰ类推荐,A级证据);伴2型糖尿病的心衰患者应使用SGLT-2i以降低心衰住院及心血管死亡风险(Ⅰ类推荐,A级证据)。(2)心衰伴房颤:非瓣膜型房颤的心衰患者需应用直接口服抗凝剂利伐沙班,推荐级别从Ⅱa类提升到Ⅰ类(2021年ESC心衰指南)。(3)肿瘤患者:肿瘤的化学药物治疗和放射治疗均可能不同程度地损害心肌和心功能,有诱发和加重心衰的风险。因此,对于此类有发生心衰的高风险患者,在接受抗肿瘤治疗前应做心脏的结构和功能评估。已有左心功能障碍(如LVEF<50%或较治疗前降低>10%)而无心衰症状的患者,在抗肿瘤治疗前和治疗时需使用保护心功能和延缓心衰进展的药物,如ACEI和β受体阻滞剂(Ⅱa推荐,B级证据,2021年ESC心衰指南)。
《2021年美国心脏病学会(American College of Cardiology,ACC)优化心衰治疗决策路径专家共识》(ACC共识2021)是对2017版的修订[35],《2021年ESC急性和慢性心衰诊断和治疗指南》(ESC指南2021)出台,提出了一些新的观点和建议[34],《2021年共同心衰定义和分类》(心衰定义和分类共识2021)是多国组织协作制定的建议,涉及心衰最基本的定义和分类问题[36]。
1. 提出和解答10个心衰临床问题,旨在做好心衰的GDMT。这些问题包括:(1)如何基于证据和指南,启动和采用GDMT?(2)如何实现最佳治疗?(3)何时患者应转由心衰专家处理?(4)如何做好多学科协调?(5)如何提高患者的依从性?(6)如何个体化处理特定患者群体?(7)如何评估心衰治疗的成本和效益?(8)如何做好日益复杂的心衰管理?(9)如何管理心衰的共病?(10)如何进行姑息治疗和临终关怀。
2. 倡导做好GDMT的11条指导原则:这是有鉴于心衰治疗的复杂困难和GDMT的至关重要,这些原则可概述为:(1)GDMT是心衰管理的基础,应列为优先。(2)目标剂量与最佳结果相关。在无禁忌证和(或)可耐受时需达到目标剂量。(3)尽早启动GDMT。(4)优先排除GDMT的各种障碍,需由专业团队处理。(5)有效的容量负荷管理。(6)妥善处理伴有的肾功能损害、高血压及症状性低血压,以提高患者对GDMT药物的耐受性,减少副作用。(7)在GDMT达到最佳剂量3~6个月后,可考虑器械治疗(CRT或ICD)作为一级预防举措。(8)介入性三尖瓣瓣膜修复,用于伴慢性中度至重度三尖瓣关闭不全的有症状患者。(9)心衰的康复治疗。(10)考虑治疗的效价比,选择个体化最优方案。(11)综合管理有利于优化GDMT,包括规律随访、远程医疗和监控等。
3. 强调ARNI的优先地位和应用:依据新的证据,推荐HFrEF患者应用ARNI和SGLT-2抑制剂。在RAS阻滞剂适用时优选ARNI,因为临床研究证实在慢性稳定性心衰患者中,ARNI优于ACEI,还主张出院前后的尚不稳定的心衰患者也可以应用,从而将该药推到一个优选的新高度。
依据近几年的新证据,对心衰的分类、药物治疗、器械治疗、病因和(或)合并症的个体化处理,以及急性心衰的管理等提出了建议和推荐。
1. 将SGLT2抑制剂列为慢性稳定性心衰的基石药物,此为主要亮点。一般认为基石药物必须具备的条件,一是被指南确认为只要没有禁忌证就必须应用;二是有充分证据表明可显著降低心衰的死亡率(包括全因死亡、心血管死亡和心脏性猝死);三是在真实世界心衰人群中的应用,证实其疗效和安全性与前瞻性大样本RCT结果一致。RAS阻滞剂、β受体阻滞剂和醛固酮受体拮抗剂(即“金三角”)均完全符合上述条件。SGLT2抑制剂此前己在中国《慢性心力衰竭基层诊疗指南2019》[37]、加拿大心衰指南更新2020[38]及ACC共识2021[35]中得到推荐,但只有2021年ESC心衰指南才将其界定为基石,可与“金三角”相提并论。这是认识上前进的一大步,因为在现有的临床试验中,此类药物改善预后的作用主要依据复合终点(心血管死亡和因心衰住院)的显著降低,其组分中心血管死亡的降低并未达到统计学上的显著性差异,而且在随机前的基础治疗中均包括可耐受剂量的“金三角”药物。推荐级别“质”的提高,显然由于这两年SGLT2抑制剂新试验的成功,使其从众多心衰药物中脱颖而出,成为“广谱”的抗心衰药,适用于广泛的心衰人群,包括各种类型心衰(如HFrEF和HFpEF)以及心衰全程(如稳定性心衰和不稳定心衰)等。
2. HFmrEF的“正名”和药物治疗的推荐,此为又一亮点。2016年ESC心衰指南[39]中,HFmrEF名为“射血分数中间范围的心衰”,此次更名为“射血分数轻度降低的心衰”,英文缩写不变,而含义完全不同。新名称赋予此类心衰更“接近”HFrEF的新身份。因为分析一些临床研究,如 TOPCAT研究(螺内酯)、PARAGON研究(ARNI)试验、CHARM研究(坎地沙坦)等,发现这些药物对LVEF在40%~50%的患者,均有一定的有益疗效。因此,ESC指南2021终于使HFmrEF患者有了可推荐的药物,即“金三角”(均为Ⅱb类推荐,C级证据)。
3. 提出急性心衰治疗流程的新思路,为亮点之三。ESC新指南的建议,可以理解为对AHF患者做二次评估,第一次为“床边评估”,依据有无淤血和灌注不良,将患者区分为干暖、湿暖、干冷和湿冷4种类型(俗称“四格表分类”)。这是沿用近20年的传统方法。第二次依据临床表现和亚型特征进一步分类为ADHF、急性肺水肿、孤立性右心衰竭和心源性休克共4大类,后者中的每一种在机制、病因、血流动力学异常和临床表现上各具特点,需选择和采用相应的治疗方案(表2)。其中的“主要临床表现”呈现出“四格表分类”的亚型特征。这4大类确实是临床上,尤其心衰重症病房和监护室中常见的类型,有助于精准识别和治疗。这两种分类方法并不矛盾,而是各有侧重,临床医生可兼收并蓄,综合应用。

急性心力衰竭的临床表现和亚型特征分类
急性心力衰竭的临床表现和亚型特征分类
| 项目 | 急性失代偿性心力衰竭 | 急性肺水肿 | 孤立性右心衰竭 | 心源性休克 |
|---|---|---|---|---|
| 主要机制 | 左心室功能不全肾脏钠水潴留 | 后负荷增加和(或)明显左心室舒张功能不全心脏瓣膜病 | 右心室功能不全和(或)毛细血管前肺动脉高压 | 严重心功能不全 |
| 引起症状的主要原因 | 液体潴留心腔内压力增高 | 液体重新分布到肺和急性呼吸衰竭 | 中心静脉压升高通常全身低灌注 | 全身低灌注 |
| 发作 | 逐渐发生(天) | 快速发生(小时) | 逐渐或快速发生 | 逐渐或快速发生 |
| 主要血流动力学异常 | LVEDP和PCWP升高,心输出量降低或正常收缩压正常或降低 | LVEDP和PCWP升高,心输出量正常收缩压正常或升高 | RVEDP升高心输出量降低收缩压降低 | LVEDP和PCWP升高心输出量降低收缩压降低 |
| 主要临床表现 | 湿暖或湿冷 | 湿暖 | 干冷 | 湿冷 |
| 主要治疗 | 利尿剂正性肌力药/血管升压药(如果外周灌注不足或低血压)如果需要,可以短期MCS或RRT | 利尿剂血管扩张剂 | 利尿剂用于外周充血正性肌力药/血管升压药(如果外周灌注不足或低血压)如果需要,可以短期MCS或RRT | 正性肌力药/血管升压药如果需要,可以短期MCS或RRT |
LVEDP为左心室舒张末期压力;PCWP为肺毛细血管楔压;MCS为机械循环支持;RRT为肾脏替代治疗;RVEDP为右心室舒张末期压力
心衰的定义与既往并无变化,仍强调有症状和(或)体征才可以诊断为心衰,这是作为一种临时综合征必须具备的条件。共识建议的心衰分类标准,基本上与2021的ESC指南一致,即按LVEF为标准,分为HFrEF、HFmrEF和HFpEF,主要差异是单列了一种“射血分数改善的心衰”(heart failure with improved ejection fraction,HFimpEF),定义为LVEF原来≤40%,尔后升至>40%,且增幅≥10%的患者。HFimpEF实际上就是治疗后改善的HFrEF患者。
在心衰分类上美国和欧洲一直存在分歧,自2016年ESC指南[39]提出第三种心衰类型即“射血分数中间范围的心衰(HFmrEF)”后,一直并未得到全球尤其美国的认可,同期的美国心衰指南仍坚持原来的二种类型的分类方法,其原委可能认为HFmrEF的确缺乏“实质性”的内涵,欠缺可操作性,除了LVEF外,从病理生理学机制到治疗均无法与其他两种类型严格区分。不过,美国指南认为那些LVEF在这一区间的患者,可能来自HFpEF的“进展”或HFrEF 的“改善”。这种思考也有道理,与一些心衰患者的病情演变轨迹存在一定程度的契合。
心衰分类共识是由美欧日本专家联合制订的,似乎要弥合在心衰分类上欧美的争议,从内容看也是如此,将双方观点揉在一起,和了稀泥。这个共识由于得到包括中国在内的其他国家(如加拿大、印度、澳大利亚、新西兰等)专业学会的认可,故采用“universal”一词,该词的基本含义为“普适(或普遍)的”“通用的”“共同(或全体)的”“全世界的”等,本文采用“共同”一词,是认为这毕竟是全球的事情,这样的分类是否恰当,可以见仁见智,没有最好,只有更好,也可以进一步商榷。希望这个共识作为建议,引起各地学者关注这个心衰领域最基本的问题,推动心衰学术交流。当然,就现时而言,有一个共同接受的分类,对心衰的进一步研究和临床工作都有益处,值得推荐。
2021年是心衰的丰收年,临床试验带来的新进展,3部国际心衰新指南/共识传达的新理念和新推荐,均会引起我们的新思考,其中最重要和现实的问题,就是立足今天,如何做好心衰患者的治疗,合理应用心衰的各种药物,包括传统药物和新的药物。
1. 传统药物必不可少。“金三角”和利尿剂应成为HFrEF患者的初始和基本方案。“金三角”(包括ARNI)应努力达到目标剂量或耐受剂量。利尿剂应使患者处于“干重”状态,并以小剂量维持。
2. 新药作用如虎添翼。SGLT2抑制剂可以在HFrEF的全程应用,包括慢性稳定性心衰和失代偿的不稳定性心衰(SOLOIST-WHF试验)。主要推荐恩格列净或达格列净,因证据更多;由于对心衰的血流动力学、血压、电解质和肾功能影响小,可早期应用,如急性心衰出院的前后,以及“金三角”药物因不良反应而暂时不能用或仅用小剂量时;伴糖尿病患者可用作起始治疗,成为初始和基本方案成员之一;伴有糖尿病的心衰患者,该药应用后,原有降糖治疗宜作调整,以形成更适合的方案。
ARNI在HFrEF治疗中可以发挥重要作用。近几年的系列临床研究产生了宝贵的新信息和新证据,可以更加客观地评价其优势和局限,从而推荐用于心衰的适宜人群:(1)慢性稳定性HFrEF、心功能Ⅱ级和Ⅲ级的患者最为适用(PARADIGM-HF试验),优于ACEI和(或)ARB而列为优选。(2)不稳定性心衰包括出院前后患者的起始应用,或未曾用过ACEI和(或)ARB患者的初始应用(PIONEER-HF试验[40]和TRASITION试验[41]等),已得到ACC共识推荐。但ESC新指南持保留态度,推荐级别仅Ⅱb类。(3)ARNI的利尿作用值得重视,可协助消除液体潴留,明显改善症状,因而对于明显容量超负荷、无低血压的心衰患者,可考虑早期加用。(4)心功能Ⅳ级即晚期心衰,ARNI与ACEI和(或)ARB疗效不分伯仲(LIFE试验),可同等应用。(5)AMI后伴有心功能降低或障碍,或伴有初发肺淤血的患者,作为预防心衰、延缓进展和改善预后,ARNI也并不优于ACEI和(或)ARB(PARADISE-AMI试验),应一视同仁。
3. 其他药物仍有用武之地。伊伐布雷定适用于窦性心率≥70~75次/分的慢性HFrEF患者。心率增快是心衰进展和预后不良的危险因素,因此,降低心率可以改善心衰症状和降低再住院率(SHIFT试验[42])。地高辛适用于房颤伴有快速心室率的患者或伴明显低血压患者。
4. 将上市的新药可发挥辅助作用。维立西胍和肌球蛋白激动剂(OM)已在国外应用,中国尚未上市。维立西胍作为心肌代谢药物,其有益的临床疗效首次得到RCT证实,可显著降低HFrEF患者的心血管死亡或心衰住院(主要终点)的风险10%(VICTORIA试验[43]),ESC新指南推荐用于“金三角”后仍有症状的心功能Ⅱ~Ⅳ级的患者,包括急性心衰出院后的早期患者。肌球蛋白激动剂是新型的正性肌力药物,也得到了ESC新指南的推荐,可显著降低HFrEF患者的心血管死亡或心衰的风险(GALACTIC-HF试验[15])。
5. 未来的治疗构想。面对心衰的复杂性,又有众多的药物和器械治疗方法,怎么办?(1)HFrEF的处理:如上分析,药物治疗可采用如下步骤。首先采用利尿剂和“金三角”药物作为初始和基本方案,并达到优化。接着应在心衰全程包括早期尽早加用SGLT2抑制剂,伴糖尿病患者,可与初始方案同步。随后酌情应用伊伐布雷定和地高辛。将会上市的维利西胍和肌球蛋白激动剂宜在SGLT2抑制剂后用于仍有症状的心衰患者。经3~6个月标准和优化治疗后酌情考虑器械治疗的可能性和必要性。(2)HFpEF的处理:恩格列净优先应用。也推荐应用ARNI,试验中其与缬沙坦相比较,虽未能显著降低HFpEF(LVEF≥45%)患者的主要复合终点(因心衰住院和心血管原因死亡)的发生率,全因病死率两组也相似。然而,在因心衰住院发生率上,该药有一个小小的临界性地显著降低(RR 0.85,95%CI 0.72~1.00)(PARAGON-HF试验[24])。回顾性亚组扩展性分析提示,该药可能使LVEF低于中位数(≤57%)患者获益(类似TOPCAT基于LVEF的分析),也使女性患者获益,因而该药获批可用于HFpEF特定亚组人群。此类患者还可应用利尿剂、螺内酯、其他RAS阻滞剂等,以改善症状和(或)改善预后,尤其某些特定的亚组人群。其余的治疗原则一如既往。
所有作者均声明不存在利益冲突