
了解在全直肠系膜切除术(TME)直肠末端系膜游离过程中,神经血管束(NVB)前列腺部微出血的概率并探讨其临床意义;对NVB前列腺部的解剖学形态进行观察以探讨其保护策略。
采用描述性病例系列研究和尸体解剖研究的方法,对NVB前列腺部进行活体和尸体标本解剖学观察。活体标本的观察:从福建医科大学附属协和医院结直肠外科手术视频数据库中,选取2013年11月至2015年3月期间,行腹腔镜保留部分邓氏筋膜TME的38例非连续男性患者的手术录像。通过回顾性复习手术录像,盲法分别评估NVB前列腺部微出血以及泌尿和性功能情况,泌尿功能采用国际前列腺症状评分表(IPSS)评估,性功能采用勃起功能国际问卷(IIEF-5)评估,分析NVB前列腺部微出血与否与术后泌尿和性功能的关系。尸体标本解剖学观察:选择福建医科大学解剖学教研室的4例男性半盆腔尸体标本,采用两种方法进行尸体标本解剖,其一:2个半盆标本,模拟TME手术进行分离,观察NVB前列腺部;其二:另2个半盆标本,采用莱卡刀片从横断面进行连续横切(层厚约1 cm),将NVB前列腺部脂肪垫当做一个整体进行观察。最终将术中的活体解剖观察与相应尸体观察层面进行比对。计数资料组间比较采用Fisher精确概率法检验。偏态分布的计量资料用M(范围)表示,组间比较采用Mann-Whiteny U秩和检验。
38例患者中位年龄57(31~75)岁,肿瘤距肛缘中位距离6(1~8)cm。21例(55.3%)术中NVB前列腺部微出血(微出血组),17例(44.7%)未见出血(无出血组)。微出血组术后3个月和6个月IPSS评分高于无出血组[7(0~16)分比2(0~3)分,Z=-1.787,P=0.088;2(0~15)分比0(0~2)分,Z=-2.270,P=0.028],而术后12个月两组IPSS评分差异无统计学意义(P>0.05);性功能方面,有23例术前性活跃(IIEF-5≥18分)患者纳入分析,其中无出血组7/8例患者术后12个月性功能恢复至术前水平(定义为IIEF-5下降<3分、且患者主观性功能满意情况恢复至术前水平),而微出血组仅6/15的患者恢复至术前水平,差异有统计学意义(P=0.029)。模拟TME手术分离半盆尸体标本,见NVB前列腺部血管神经走行在直肠前外侧、前列腺后外侧和肛提肌前内侧所构成的狭小的三角空间内,血管神经组织缠绕成团,分支不易辨别。进一步将NVB前列腺部脂肪垫当做一个整体进行尸体和活体比对观察发现,在尸体的前列腺底和前列腺中部水平,NVB前列腺部脂肪垫与直肠系膜关系密切,两者投影线存在较大重叠,是术中NVB前列腺部微出血的高危区。手术视频观察发现,在对应的前列腺底和前列腺中部水平,术中因主刀医师和助手的对抗牵引,使该处NVB前列腺部脂肪垫呈横向走行。其转为纵向走行处为NVB发出的直肠支,张力最大,为易出血区。可清晰锚定数支NVB直肠支,需要采用超声刀紧靠直肠固有筋膜预先凝结。比对发现,该直肠支即为尸体投影线重叠区。
NVB前列腺部损伤是TME术后排尿和性功能障碍的原因之一,NVB前列腺部神经纤维细小,术中无法辨别其功能分区,需要将NVB血管神经组织和相应脂肪垫当做一个整体进行保护。术中充分理解NVB前列腺部形态,保持适当对抗牵引张力,采用超声刀及时凝结直肠支可保护NVB前列腺部。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
全直肠系膜切除术(total mesorectal excision,TME)术后泌尿和性功能障碍发生率高[1]。神经血管束(neurovascular bundle,NVB)的损伤,是TME术后排尿和性功能障碍的重要原因之一。NVB最早由Walsh等[2]描述,由来自盆丛的混合神经和来自髂内动脉的血管支混合而成,其末梢支支配阴茎海绵体,维持男性的性功能,特别是勃起功能。Walsh等[2]从泌尿外科角度出发,提出在前列腺癌根治术时应保留NVB主体,仅切断NVB分支。丛进春和张宏[3]将NVB分成3个部分:起始于精囊腺外上方为起始部、走行于前列腺后方为主干部和终止于阴茎海绵体的海绵体部。笔者则分别称之为精囊腺部、前列腺部和海绵体部。目前,在直肠癌手术方面,关于NVB的临床和解剖研究主要集中在NVB精囊腺部,例如其与邓氏筋膜的解剖学关系及邓氏筋膜的保留问题[4]。而关于NVB前列腺部的研究极少。TME经腹游离过程中,由于盆腔骨性结构的生理性弯曲和前列腺的遮盖,使NVB前列腺部位置背对主刀视野,且由于邻近直肠末端系膜而位置深在,术中容易损伤致出血。本研究旨在通过一系列活体和尸体解剖观察,对TME直肠末端系膜游离过程中NVB前列腺部微出血概率进行统计,探讨NVB前列腺部微出血的临床意义;并对NVB前列腺部的解剖学形态进行观察,探讨其保护策略。
采用描述性病例系列研究和尸体解剖研究的方法。本研究经福建医科大学附属协和医院伦理委员会批准(审批号:2020KY092)。
从福建医科大学附属协和医院结直肠外科手术视频数据库中,选取2013年11月至2015年3月期间,行腹腔镜保留部分邓氏筋膜TME[5]的38例非连续男性患者的手术录像进行回顾性观察。纳入的手术录像需记录完整无缺失,能清晰展示直肠的游离过程,视频质量合格,且临床基线和功能随访信息完整。38例患者的中位年龄为57(31~75)岁,肿瘤距肛缘中位距离6(1~8)cm。有34例(89.5%)行术前新辅助放化疗。术后病理TNM分期:0期(病理完全缓解)7例(18.4%),Ⅰ期8例(21.1%),Ⅱ期13例(34.2%),Ⅲ期10例(26.3%)。术后1例患者出现回肠造口旁疝,1例出现术后早期炎性肠梗阻,1例吻合口漏,2例肺部感染,1例切口感染;均经保守治疗治愈。术后住院时间为(7.9±4.2)d,
选择福建医科大学解剖学教研室的4具男性半盆腔尸体标本进行解剖观察。
观看手术视频时,将NVB前列腺部当做一个整体(包括NVB血管神经组织+脂肪垫),直肠前间隙分离过程中,在腹膜反折上1.0 cm处切开腹膜,沿邓氏筋膜前间隙向下分离,在距两侧精囊腺底部上0.5 cm相当于两侧NVB内侧水平,呈倒"U"形弧形切断邓氏筋膜,进入邓氏筋膜后间隙,从而保护NVB精囊腺部,并沿着邓氏筋膜后间隙向下分离至肛提肌水平。在直肠前壁游离过程中,观察不同高度NVB脂肪垫形态和走行,并与同高度水平的尸体研究结果进行比对。
采用盲法,由研究者甲回顾手术录像,记录NVB前列腺部微出血率和微出血部位;根据NVB的解剖学位置进行分类,精囊腺部定义为精囊腺尾部至前列腺上缘水平之间的NVB组织;前列腺部定义为前列腺上缘至前列腺尖部水平之间的NVB组织;海绵体部为前列腺尖部至阴茎海绵体的NVB组织。NVB的分段图示见图1。
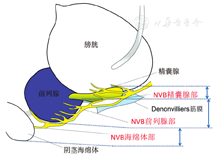

由研究者乙记录和随访患者术前以及术后3、6、12个月时的泌尿和性功能评分,其中泌尿功能以国际前列腺症状评分(international prostate symptom score,IPSS)评价,0~7分为轻度症状,8~19分为中度症状,20~35分为重度症状[6];术前及术后12个月的男性勃起功能以国际勃起功能指数(international index of erectile function 5,IIEF-5)评价[7]。
将研究者甲的观察结果与研究者乙的分析结果进行合并,分析比较全组38例患者NVB前列腺部微出血组与未出血组手术前后IPSS评分;纳入术前性活跃(定义为术前IIEF-5≥18分)的23例患者分析比较手术前后的IIEF-5评分,其中术后12个月性功能恢复至术前水平定义为术后12个月IIEF-5下降<3分、且患者主观性功能满意情况恢复至术前水平。
采用两种方法进行尸体标本解剖观察:(1)模拟TME手术对2个半盆标本进行分离,观察NVB前列腺部的相对位置关系,移除直肠,剔除NVB前列腺部脂肪垫组织,从尾侧向头侧观察NVB前列腺部的血管和神经走行。(2)采用莱卡刀片从横断面对2个半盆标本进行连续横切(层厚约1 cm),将NVB前列腺部脂肪垫当做一个整体,观察不同高度水平的NVB前列腺部脂肪垫和直肠系膜投影线的相对关系。
采用IBM SPSS 22统计软件进行统计学分析。计数资料采用例(%)表示,组间比较采用Fisher精确概率法进行。计量资料首先进行Shapiro-Wilk正态分布检验,服从正态分布的计量资料用 ±s表示;不符合正态分布的用M(范围)表示,组间比较采用Mann-Whiteny U秩和检验。P<0.05表示差异有统计学意义。
±s表示;不符合正态分布的用M(范围)表示,组间比较采用Mann-Whiteny U秩和检验。P<0.05表示差异有统计学意义。
38例患者中,21例(55.3%)术中NVB前列腺部微出血(微出血组),17例(44.7%)未见出血(无出血组)。微出血组有17例次(44.7%)出现左侧NVB前列腺部微出血,7例次(18.4%)出现右侧NVB前列腺部微出血,1例次(2.6%)出现正中NVB交通支微出血。
泌尿功能评估结果显示,微出血组术后3个月和6个月IPSS评分高于无出血组,但术后12个月时,两组IPSS评分差异无统计学意义(P>0.05)。本组术前性活跃的23例患者性功能评估结果显示,8例无出血组患者术后12个月时,有7例性功能恢复至术前水平,而15例微出血组患者仅6例恢复至术前水平,两组差异有统计学意义(P=0.029)。两组手术前后IPSS评分和IIEF-5评分比较见表1。
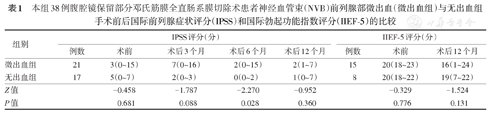
本组38例腹腔镜保留部分邓氏筋膜全直肠系膜切除术患者神经血管束(NVB)前列腺部微出血(微出血组)与无出血组手术前后国际前列腺症状评分(IPSS)和国际勃起功能指数评分(IIEF-5)的比较
本组38例腹腔镜保留部分邓氏筋膜全直肠系膜切除术患者神经血管束(NVB)前列腺部微出血(微出血组)与无出血组手术前后国际前列腺症状评分(IPSS)和国际勃起功能指数评分(IIEF-5)的比较
| 组别 | IPSS评分(分) | IIEF-5评分(分) | ||||||
|---|---|---|---|---|---|---|---|---|
| 例数 | 术前 | 术后3个月 | 术后6个月 | 术后12个月 | 例数 | 术前 | 术后12个月 | |
| 微出血组 | 21 | 3(0~15) | 7(0~16) | 2(0~15) | 2(1~7) | 15 | 20(18~23) | 16(1~24) |
| 无出血组 | 17 | 5(0~7) | 2(0~3) | 0(0~2) | 1(0~7) | 8 | 20(18~22) | 19(7~22) |
| Z值 | -0.458 | -1.787 | -2.270 | -0.952 | -0.329 | -1.524 | ||
| P值 | 0.681 | 0.088 | 0.028 | 0.360 | 0.776 | 0.131 | ||
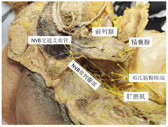
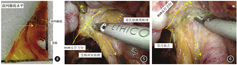
模拟TME手术分离半盆尸体标本,移除直肠,剥离NVB前列腺部脂肪组织后,见NVB前列腺部血管神经走行在直肠前外侧、前列腺后外侧和肛提肌前内侧所构成的狭小三角空间内,血管神经组织缠绕成团,分支不易辨别,在尿道膜部水平,直肠尿道肌后缘可见NVB的中央交通支血管。见图2。

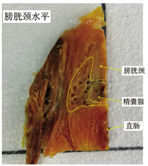
从头侧向尾侧活体和尸体解剖横断面观察所见,在膀胱颈水平,该处NVB精囊腺部脂肪垫较宽大,其边界与直肠前方系膜的直肠固有筋膜投影线存在轻微重叠,该水平为NVB精囊腺部的末端,向尾侧移行为NVB前列腺部。见图3。

从前列腺底、前列腺中部和前列腺尖3个水平,对NVB前列腺部进行活体和尸体观察比对。
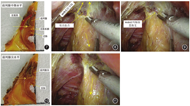
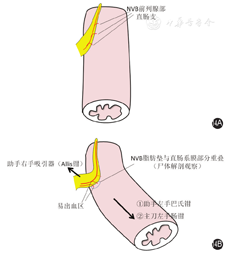
在尸体标本,该处NVB前列腺部脂肪垫和直肠系膜关系最为密切,两者投影线存在较大重叠,是术中NVB前列腺部微出血的高危区。见图4。在术中,因主刀医师和助手的对抗牵引,使该处NVB前列腺部脂肪垫呈横向走行。见图5。NVB前列腺部后方被灰白色致密的邓氏筋膜所覆盖,逐步向下分离,灰白色邓氏筋膜逐步变菲薄呈半透明状薄膜。NVB前列腺部脂肪垫逐步由横向转为纵向走行,其转折拐点处为NVB发出的直肠支,其张力最大,为易出血区。见图6。比对观察发现,该直肠支即为尸体解剖中NVB脂肪垫和直肠系膜的重叠部位。图4黄色虚线箭头所示。

该处NVB前列腺部脂肪垫呈狭长三角形,位于前列腺、直肠系膜、肛提肌之间的狭小空间内,其边界与直肠前方系膜的直肠固有筋膜投影线存在轻微重叠,其本质为NVB的直肠支供应直肠系膜。见图7。在活体中,见NVB前列腺部血管成团,可清晰锚定数支直肠支(对应于尸体的投影线重叠部位,图7黄色虚线箭头所示),需要采用超声刀预先凝结,以防止微出血后在止血过程中损伤NVB前列腺部。见图8和图9。

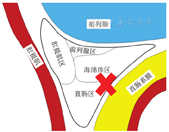
目前,关于NVB的临床和解剖研究主要集中在精囊腺部,例如邓氏筋膜保留问题,无论行完整、或行部分保留邓氏筋膜的TME,都能有效保护NVB精囊腺部[4,5]。作为NVB精囊腺部的延续——NVB前列腺部的TME相关临床研究尚未见报道。从解剖学角度考虑,Costello等[8]对12具尸体进行解剖,发现NVB前列腺部功能分区大致包括前列腺区、肛提肌区、直肠区和海绵体区。本研究发现,TME前壁游离过程中,NVB前列腺部微出血发生率高达55.3%,左侧损伤略常见;同时发现,NVB前列腺部微出血组术后短期排尿功能及术后长期性功能差于无出血组。虽然NVB前列腺部的微出血大多发生于直肠区(其分出直肠支的张力最大,且紧邻分离区),但在止血过程中,因出现跨分区的功能损伤,导致排尿和性功能障碍。损伤模式示意图见图12。

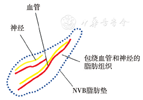
NVB前列腺部神经组织具有特殊的组织学特征。Nishimura等[9]的一项比较横断面NVB精囊腺部和前列腺部的神经纤维数目和面积的组织学研究发现,NVB前列腺部和精囊腺部的神经纤维数目相近;但NVB前列腺部神经纤维直径更细小,这是NVB前列腺部在术中更易损伤的组织学因素。本研究的尸体标本观察亦发现,NVB前列腺部血管神经组织走行在直肠前外侧、前列腺后外侧和肛提肌前内侧所构成的狭小的三角空间内,血管神经组织缠绕成团,分支不易辨别,亦无法辨别其分区。因此,NVB前列腺部无法于TME术中游离暴露进行保护。从保护策略上说,应从整体的角度出发,将神经血管组织和包饶的脂肪组织当作一个整体,即对位于直肠两边固有筋膜前外侧、精囊腺下方、前列腺外侧的由"脂肪垫包绕神经血管束形成的卵圆形的组织块"进行整体保护,避免出血。见图13。

本研究通过尸体标本的横断面和活体解剖进行同步比对,有助于将NVB前列腺部脂肪垫当做一个整体进行观察。在前列腺底和前列腺中部水平,NVB前列腺部脂肪垫和直肠系膜关系最为密切,两者投影线存在较大重叠,其本质上是NVB发出的直肠支,该区域是术中NVB前列腺部微出血的高危区。从功能上说,Stelzner等[10]的解剖学研究发现,NVB发出的直肠支沿着肛提肌上缘,从直肠两侧前壁穿过直肠壁纵肌,移行为内括约肌神经,支配肛门内括约肌,该神经参与维持肛门功能。从头侧向尾侧观察,NVB前列腺部在不同水平均发出直肠支供应直肠,为TME前侧壁分离时的易出血区。见图14A。直肠前侧壁游离过程中,在主刀和助手的对抗牵引作用下,NVB的直肠支为张力最高的区域,容易直接拉断出血。此外,助手将NVB向前外侧推挡,亦使NVB更改原有形态,呈"S"型,容易误导切割方向而致出血。见图14B。对不同力学牵拉作用下的NVB前列腺部脂肪垫形态的充分理解,保持适当张力,并采用超声刀及时紧靠直肠固有筋膜凝结直肠支,有助于NVB前列腺部的保护。

至前列腺尖水平,NVB脂肪垫组织向前移行,更靠近前列腺,与直肠系膜之间较疏松。McLaughlin等[11]在一项综述中展示了尿道膜部和海绵体神经的三维关系,发现该区域海绵体神经(相当于NVB前列腺部的延续)从尿道外侧穿过尿生殖膈上筋膜,向前移行,即从尿道的截石位5点和7点方向,跨越至尿道的3点和9点方向,向11点和1点走行并支配海绵体。该区域并非NVB前列腺部出血的高危区。
关于邓氏筋膜与NVB的关系,目前尚无定论。目前观点认为,邓氏筋膜向两侧移行,包饶两侧的NVB并逐渐消失,其间有大量细小的神经纤维穿过该筋膜[12,13]。笔者认为,邓氏筋膜在TME术中具有屏障作用,邓氏筋膜在NVB精囊腺部水平呈灰白色,较为致密,将NVB精囊腺部覆盖于前外侧,如在双侧精囊腺底部上方0.5 cm处离断,进入邓氏筋膜后间隙游离,即可保护NVB精囊腺部。而随着分离深入,NVB前列腺部位于直肠两前外侧、精囊腺下方、前列腺外侧,由离断后的邓氏筋膜下切端翻转覆盖,透过其灰白色薄膜,可见其内为由黄色的脂肪垫包绕神经血管束形成的卵圆形的组织块。此时,需准确识别其与直肠固有筋膜间的间隙,直至终点线的显露。我们的前期研究结果证实,保留部分邓氏筋膜TME术后12个月随访时,机器人手术和腹腔镜手术直肠癌患者均未出现严重的泌尿功能障碍,优良率分别达97.6%及98.4%,勃起功能优良率(包含正常及轻度障碍)分别为92.2%和92.6%[5]。
综上,NVB前列腺部损伤是TME术后排尿和性功能障碍的原因之一,NVB前列腺部神经纤维细小,无法解剖游离进行保护。术中无法辨别其功能分区,需要将NVB血管神经组织和相应脂肪垫当做一个整体进行保护。在前列腺底和前列腺中部水平,NVB前列腺部与直肠系膜关系最为密切,预防NVB微出血是保护的主要策略。充分理解NVB前列腺部形态,保持适当对抗牵引张力,采用超声刀及时凝结直肠支,可保护NVB前列腺部。
所有作者均声明不存在利益冲突



























