
11岁患儿因“发现肺部影像学异常1年余”入院。完善基因检测提示SLC34A2基因存在复合杂合变异c.286C>T(exon4)、c.910A>T(exon8),变异分别来源于患儿父亲和母亲,诊断为SLC34A2复合杂合变异致肺泡微石症。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患儿 男,11岁,因“发现肺部影像学异常1年余,无伴随症状”于2020年8月至复旦大学附属儿科医院呼吸科就诊。患儿1年前因发热咳嗽于当地医院完善胸部增强CT提示双肺弥漫性间质改变,检查提示烟曲霉菌IgM抗体>500 kAU/L,予抗感染治疗好转后出院,出院后无明显症状。患儿既往健康,系其母第1胎第1产,因胎膜早破足月剖宫产出生,出生体重3 200 g。患儿有一弟弟(4岁),体健,父母非近亲婚配,否认家族遗传史,家族中无类似疾病。
入院体格检查:身高147 cm,体重31.9 kg。生长发育正常,神志清,精神反应可,口唇无发绀,浅表淋巴结未触及肿大,呼吸平稳,双肺呼吸音粗,未闻及干湿性啰音,四肢骨骼未见畸形,无杵状指及杵状趾。
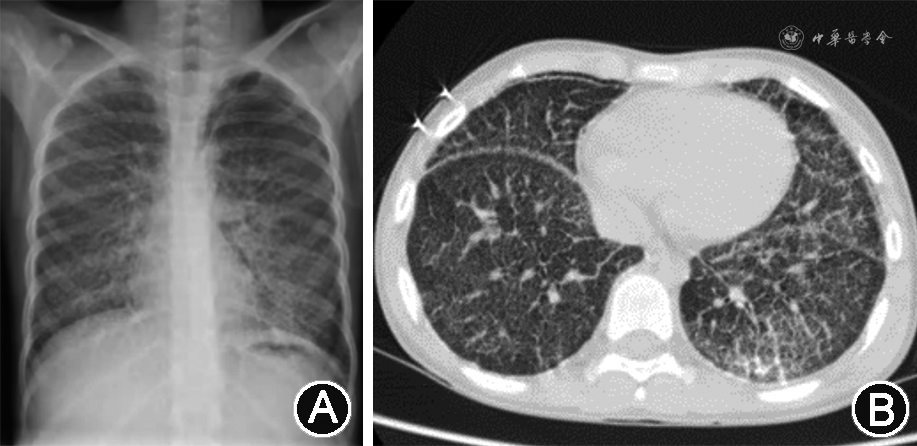
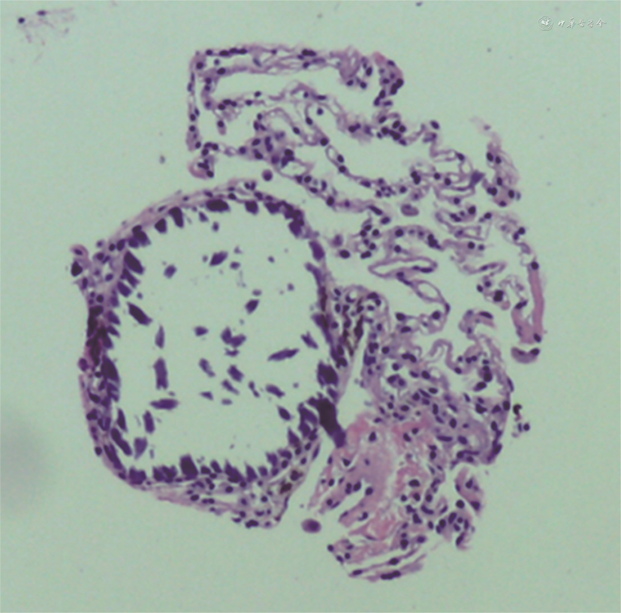
辅助检查:血常规,动脉血气分析,肝、肾功能均未见异常,结核分枝杆菌特异性细胞免疫反应检测、结核菌素试验、痰培养、痰涂片抗酸染色、肺泡灌洗液培养、肺泡灌洗液抗酸染色、血清结核抗体均为阴性,涎液化糖链抗原6 211 kU/L(参考值<500 kU/L),烟曲霉IgM抗体256.97 kAU/L(参考值 0~79.99 kAU/L)。胸X线片检查提示肺部间质性病变(图1A)。肺功能检查提示轻度阻塞性通气功能障碍,心脏超声未见异常,胸腹部增强磁共振成像见明显异常,胸部增强CT提示两肺弥漫间质病变,两侧胸膜钙化(图1B)。术后病理示肺泡腔内见多发破碎钙化结节,部分呈同心圆样改变,符合肺泡微石症表现(图2)。


基因检测:采集患儿及其父母静脉血2 ml(乙二胺四乙酸抗凝)送至复旦大学附属儿科医院分子医学中心,提取外周血基因组DNA,构建文库后利用xGen Exome V2进行外显子靶向测序,使用Illumina HiSeq平台进行全外显子测序,与人类参考基因组序列对比。基因检测结果发现患儿SLC34A2基因存在复合杂合变异,即c.286C>T(p.Q96X),c.910A>T(p.K304X)分别来自表型正常的父亲及母亲(图3)。经生物信息学分析有致病意义。经过一代测序验证,患儿结果与二代测序相符合,诊断为SLC34A2基因复合杂合变异所致肺泡微石症(pulmonary alveolar microlithiasis,PAM)。患儿完善检查提示曲霉菌IgM水平明显升高,考虑合并曲霉菌感染,予以伏立康唑口服治疗2个月后症状好转,未再出现咳嗽等呼吸道症状。患儿出院后未予特殊处理,随访6个月病情无明显进展。
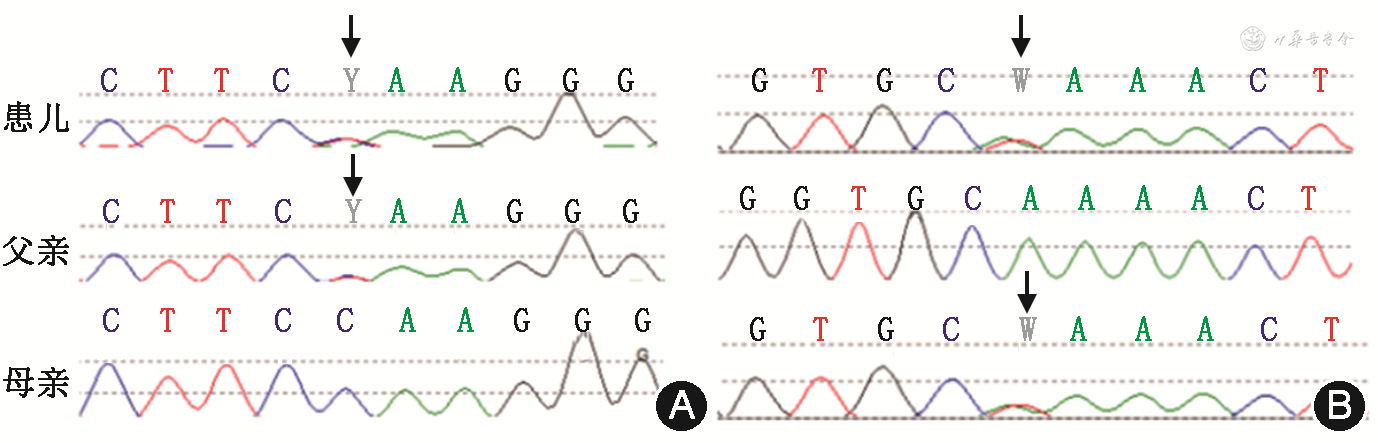

注:箭头所示为变异位点
PAM是以钙磷代谢紊乱,肺部微结石逐渐沉积为特征的一种罕见疾病[1]。近年来研究证实,PAM是由于SLC34A2基因变异导致的一种常染色体隐性遗传病,该基因定位于4p15.1-p15.3[2, 3]。国内报道大多为成人病例,儿童病例较少见。PAM是一种慢性进展的肺部间质性病变,大多于成年期发病,具有家族聚集性发病倾向,男性发病率高于女性[2,4]。PAM是由于编码Na+依赖的Pi转运蛋白的SLC34A2基因发生变异致病,影响肺泡液中无机磷的吸收,引起肺泡内无机磷的积累,从而导致磷酸钙在肺内的沉积[3]。SLC34A2的变异类型超过15种。PAM多发生于亚洲与欧洲地区,中国PAM患者大多数为外显子8发生变异,有1例外显子6发生变异,特别是8号外显子C.910A>T的变异具有高度重复性,本例患儿存在外显子8及外显子4的复合杂合变异,其中外显子8的变异类型与之前的报道一致[4, 5]。本例患儿具有典型的PAM表型,进一步丰富了SLC34A2的基因型。PAM的诊断主要通过影像学或病理学检查[2,4, 5, 6]。影像学检查结果会随着疾病进展逐渐加重,疾病早期可表现为散在微小钙化结节,结节会逐渐增大增多,主要集中在中下肺野,疾病较重时,可以出现“白描征”“暴风雪征”“沙暴征”或“火焰征”,具有确诊意义。PAM典型的病理改变是肺泡腔内不规则分布的同心圆样层状结石。镜下可见结石沿支气管、血管分布,大多位于肺泡腔内,也可见于肺泡壁,并向肺泡腔内突入。部分患儿的肺泡灌洗液或痰液中可检出微结石,对诊断也有帮助[2]。PAM部分患儿症状轻微或无明显症状,随着年龄进展,可出现气促、胸闷、喘息、乏力劳力性呼吸困难等症状[2]。PAM的症状与年龄相关,在儿童期症状多不典型,本例患儿无明显临床症状,胸部影像学存在间质性改变,胸膜钙化等特点,肺组织病理学可见同心圆样钙化结节,在基因诊断前已经可以临床确诊[1]。但由于儿童PAM比较罕见,对于患儿胸部影像学的“白描征”认识不足,故诊断需依赖病理学或基因检查相关结果。PAM尚没有有效的治疗手段[2, 3, 4]。应用羟乙磷酸钠治疗PAM的报道,但其疗效尚不能肯定。肺移植是终末期PAM患者的有效治疗手段,国内外均有移植成功的报道,移植后的远期疗效仍需要进一步观察研究[6]。SLC34A2基因相关性PAM在儿童中是一种罕见的肺部间质性疾病,进展缓慢,部分患儿无明显临床表现或仅有轻微咳嗽症状。对于肺部弥漫性间质性改变,广泛异常钙化的患儿,应考虑到PAM的可能,建议可完善肺泡灌洗术、肺活检等相关检查明确病因。根据患儿的典型的影像学表现,病理结果或基因检测结果可以明确诊断。
所有作者声明无利益冲突



























