
本版指南明确了肺纤维化的胸部高分辨率(HR)CT特征,建议将影像表现为可能寻常型间质性肺炎(UIP)型与UIP型等同对待,影像表现非UIP型患者若病理为可能UIP型,则诊断为不确定的IPF(过去诊断为非IPF);有操作和病理解读经验的机构开展的经支气管冷冻肺活检可能替代外科肺活检来诊断病理UIP型;不推荐抑酸药物、抗胃-食管反流的外科手术作为治疗IPF的措施。此外,首次明确了进展性肺纤维化(PPF)的诊断标准、临床疾病谱和治疗药物推荐,并展望了未来在PPF的临床和科研中的研究内容、以推进对PPF的诊疗。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
自2011、2015、2018年特发性肺纤维化(IPF)的诊断和治疗指南颁布、实施以来,经临床实践后发现了一些需要重新评价、达成共识的地方:影像学UIP型特征、病理学UIP型的特征、IPF的诊断措施、IPF的诊断标准和治疗推荐,以及尚无循证证据支持的诊断和治疗措施,如抗酸药物治疗或外科手术、经支气管镜冷冻肺活检(TBLC)以及基因分型等。故而,专家组[来自美国胸科协会(ATS)、欧洲呼吸病学会(ERS)、日本呼吸病学会(JRS)以及拉丁美洲胸科联盟(ALAT)]更新了IPF的临床诊疗指南[1]。另外,近年来,随着抗纤维化药物临床试验证实其在非IPF的间质性肺疾病(ILD)中的疗效,呈现抗纤维化药物在多种纤维化型ILD(FILD)中有效的局面。为了能更好地认识这些非IPF-FILD,专家组在本共识中,还就进展性肺纤维化(progressive pulmonary fibrosis,PPF)的定义、抗纤维化药物的使用策略等内容深入讨论,达成共识后形成PPF临床诊疗指南。
IPF的胸部高分辨率CT(HRCT)特征(表1):在胸部HRCT中出现牵张性支气管扩张/细支气管扩张和(或)蜂窝影是影像学提示存在明确肺纤维化的特征。其中,蜂窝影一定要与旁间隔肺气肿、气腔扩张并肺纤维化(airspace enlargement with fibrosis,AEF)相鉴别。蜂窝影中的囊泡是由近胸膜的肺组织中的肺泡间隔纤维化后引起附近的肺泡扩张和(或)支气管/细支气管扩张形成。HRCT提示的典型UIP型和蜂窝影,在肺组织病理中表现为牵张性支气管扩张。牵张性支气管扩张可发展为蜂窝影,两者密不可分。

IPF患者高分辨率(HR)CT的特征
IPF患者高分辨率(HR)CT的特征
| 特征 | HRCT的类型 | |||
|---|---|---|---|---|
| UIP型 | 可能UIP型 | 不确定UIP型 | CT表现提示其他诊断 | |
| 病理UIP型的可能性 | 确定(>90%) | 很可能(70%~89%) | 可能(51%~69%) | 不大可能(<50%) |
| 病变分布特征 | ·下肺近胸膜分布为主 ·病变常常不规则分布(正常肺 之间穿插着纤维化性病变) ·常常累及全肺 ·双肺病变可能不对称 | ·下肺近胸膜分布为主 ·病变常常常不规则分布(正常肺 之间穿插着网格影、牵张性支气 管扩张/细支气管扩张) | ·病变弥漫性分布,并 非胸膜下分布为著 | ·沿着气管-血管束走形为主, 一般远离胸膜分布(NSIP型) ·淋巴管周边分布(考虑结节病) ·上肺或中肺野分布(考虑纤 维化型HP、CTD-ILD、结节病) ·远离胸膜分布(考虑NSIP或吸烟相关性IP) |
| 高分辨率CT中肺部阴影的特征 | ·蜂窝影,可伴/不伴牵张性支气 管扩张/细支气管扩张 ·可见不规则的小叶间隔增厚 ·常常可见网格影,少量GGO ·可能伴有肺骨化 | ·网格影,可伴或不伴牵张性支气 管扩张/细支气管扩张 ·可有少量GGO ·病变一般不远离胸膜分布 | ·CT所示的肺纤维化 阴影无特异性 | ·肺窗阴影 囊泡影(考虑LAM、PLCH、LIP及DIP等) 马赛克征或三重密度征(考 虑HP) GGO为主(考虑HP、吸烟相 关性疾病、药物性肺病、肺纤维化急性加重) 明显的小叶中心型小结节 影(考虑HP、吸烟相关性疾病) 小结节结节影(考虑结节病) 实变影(考虑机化性肺炎) ·纵隔窗 胸膜斑(考虑石棉肺) 食管扩张(考虑CTD) |
注:CT为计算机体层扫描;CTD为结缔组织病;DIP为脱屑性间质性肺炎;GGO为磨玻璃影;HP为过敏性肺炎;HRCT为高分辨CT;ILD为间质性肺疾病;IP为间质性肺炎;LAM为淋巴管肌瘤病;LIP为淋巴细胞性间质性肺炎;NSIP为非特异性间质性肺炎;PLCH为肺朗格罕斯组织细胞增生症;UIP为寻常型间质性肺炎
需要强调的是,UIP型HRCT表现可以出现在IPF中,也可以出现其他非IPF的FILD中,其中以纤维化型过敏性肺炎(FHP)、某些结缔组织疾病相关性间质性肺疾病(CTD-ILD)和职业暴露相关性ILD多见。不过不同病因的UIP型ILD与IPF之间存在细微差异,比如FHP以上肺分布为著,常伴有马赛克征;但IPF的纤维化则以下肺近胸膜分布为著,且病灶分布不均一。此外,6%~10%左右的IPF患者可以伴有胸膜肺弹力纤维增生症样的胸膜病变,此时需要与职业暴露相关性ILD鉴别。
虽然不少研究认为,UIP型和可能UIP型ILD的疾病行为学和预后特征类似,且若有某些IPF的临床特征(比如老年男性,有吸烟史,无其他疾病的证据等)时,可能UIP型的患者也可以不借助肺活检来诊断IPF。但鉴于如下因素,更新版的指南仍建议把胸部HRCT的类型分为UIP型、可能UIP型、不确定UIP型和其他类型4种:可能UIP型的患者预后可能稍优于UIP型患者;HRCT的可能UIP型与肺组织病理UIP型的相关性逊于HRCT的UIP型与病理UIP型的相关性,可能UIP型还可见于FHP等其他FILD。不过,更新版指南仍建议在IPF的诊断流程中,将胸部HRCT的可能UIP型与UIP型等同对待。此外,本版指南中,删去“早期UIP”,以避免与“肺间质异常”混淆;保留“不确定UIP型”来描述那些不符合UIP型、可能UIP型且也没有特征性的其他非UIP型的表现。
病理学UIP型的特点包括以下4点:(1)肺结构的扭曲变形(瘢痕、蜂窝)伴有片状分布的致密性纤维化;(2)病变以胸膜下和间隔旁的肺实质分布为主;(3)成纤维母细胞灶;(4)无提示其他疾病的病变。而可能UIP型则指缺少前3项特征中的至少1项。
近胸膜分布为主的病变很难经TBLC获得;故而,相比SLB,经TBLC获取的肺组织更易于诊断可能UIP型。
1. 由有经验的专家操作TBLC获取肺组织、并请有经验的病理专家解读时,TBLC可替代SLB用于形态学表型未明的ILD是否为UIP的鉴别诊断中(有条件的推荐,证据级别非常低)。
2. 尚无足够的证据来支持或反对通过基因组学检测协助经支气管镜钳取活检后、形态学表型仍未明的ILD是否为UIP的鉴别诊断。
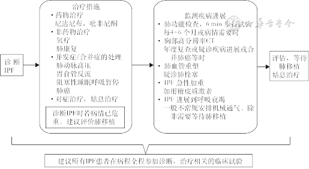
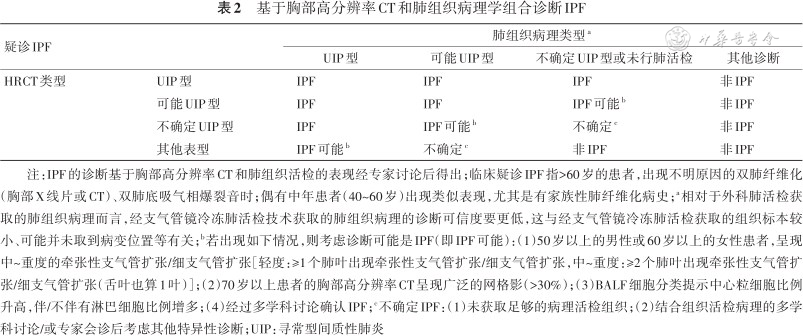
更新版的指南中(图1、2),诊断IPF有两处比较大的变动:第一,在IPF诊断流程中:将HRCT的可能UIP型等同于UIP型对待,即可能UIP型的也未必要安排肺活检,综合临床特征、化验等资料经MDD后诊断IPF。第二,综合HRCT表型和肺组织活检病理表型时:非UIP型的HRCT患者,若经肺组织活检,病理提示可能UIP型则诊断不确定的IPF;但在2018年版的指南中则认为是非IPF(表2)。


注:a胸部CT表现为可能UIP型的患者,若具有某些IPF的临床特征(如60岁、男性、吸烟),即便未进行开胸肺活检,也可能经多学科讨论(MDD)后诊断IPF;可给某些可能UIP型的患者安排BAL检查;b有经验的医疗中心可以在MDD前安排BAL;c在有经验的医疗中心,专家操作或针对某些疾病(详见文中描述),经气管镜冷冻肺活检(TBLC)可能优于外科肺活检(SLB);若TBLC后未能明确诊断,某些患者可能需要安排SLB

基于胸部高分辨率CT和肺组织病理学组合诊断IPF
基于胸部高分辨率CT和肺组织病理学组合诊断IPF
| 疑诊IPF | 肺组织病理类型a | ||||
|---|---|---|---|---|---|
| UIP型 | 可能UIP型 | 不确定UIP型或未行肺活检 | 其他诊断 | ||
| HRCT类型 | UIP型 | IPF | IPF | IPF | 非IPF |
| 可能UIP型 | IPF | IPF | IPF可能b | 非IPF | |
| 不确定UIP型 | IPF | IPF可能b | 不确定c | 非IPF | |
| 其他表型 | IPF可能b | 不确定c | 非IPF | 非IPF | |
注:IPF的诊断基于胸部高分辨率CT和肺组织活检的表现经专家讨论后得出;临床疑诊IPF指>60岁的患者,出现不明原因的双肺纤维化(胸部X线片或CT)、双肺底吸气相爆裂音时;偶有中年患者(40~60岁)出现类似表现,尤其是有家族性肺纤维化病史;a相对于外科肺活检获取的肺组织病理而言,经支气管镜冷冻肺活检技术获取的肺组织病理的诊断可信度要更低,这与经支气管镜冷冻肺活检获取的组织标本较小、可能并未取到病变位置等有关;b若出现如下情况,则考虑诊断可能是IPF(即IPF可能):(1)50岁以上的男性或60岁以上的女性患者,呈现中~重度的牵张性支气管扩张/细支气管扩张[轻度:≥1个肺叶出现牵张性支气管扩张/细支气管扩张,中~重度:≥2个肺叶出现牵张性支气管扩张/细支气管扩张(舌叶也算1叶)];(2)70岁以上患者的胸部高分辨率CT呈现广泛的网格影(>30%);(3)BALF细胞分类提示中心粒细胞比例升高,伴/不伴有淋巴细胞比例增多;(4)经过多学科讨论确认IPF;c不确定IPF:(1)未获取足够的病理活检组织;(2)结合组织活检病理的多学科讨论/或专家会诊后考虑其他特异性诊断;UIP:寻常型间质性肺炎
1. 不推荐将抑酸药物作为改善IPF预后的治疗措施(有条件推荐,证据级别非常低)。
2. 不推荐将抗胃-食管反流的外科手术作为改善IPF预后的治疗措施(有条件推荐,证据级别非常低)。
IPF的治疗策略包括药物(吡非尼酮、尼达尼布)和非药物治疗(详见图2),兼顾患者的合并症、并发症的治疗。推荐处于不同病程阶段和不同严重程度的IPF患者参加可能的临床试验。IPF患者出现呼吸衰竭时,一般不推荐机械通气,除非即将接受肺移植。在IPF急性加重期时可加用糖皮质激素。
未来,在IPF的诊疗流程中,可在MDD时整合家族史、基因分析结果,以期减少有创操作。进一步评价联合治疗的疗效;关注患者的生活质量,包括治疗合并症、提升体能、改善情绪和减轻症状。
PPF是指一大类病因已知或未知的、胸CT上有明确的肺纤维化,在近1年内出现≥2项如下表现的非IPF-FILD患者:(1)咳嗽、气短等呼吸系统症状恶化;(2)肺功能下降:1年内FVC占预计值%下降>5%,和(或)1年内DLCO(经血色素校正后)占预计值%下降>10%;(3)胸部影像学进展(≥1项):牵张性支气管扩张/细支气管扩张范围增大或程度加剧;新发磨玻璃影伴有牵张性细支气管扩张;新发细网格影;粗网格影范围增大或程度加剧;新发蜂窝影或原有蜂窝影加剧;肺容积进一步缩小。
PPF可以出现在一系列FILD中:(1)特发性间质性肺炎(IIP):几乎所有的非IPF-IIP都可能出现PPF,包括纤维化型非特异性间质性肺炎(FNSIP)、特发性肺胸膜弹力纤维增生症、纤维化性机化性肺炎(FOP)、脱屑性间质性肺炎、急性间质性肺炎、未能分类的间质性肺炎等;(2)CTD-ILD:尤其是类风湿关节炎相关性ILD(RA-ILD)、系统性硬化症相关性ILD(SSc-ILD)、混合结缔组织病相关性ILD(MCTD-ILD)、血管炎相关性ILD等;(3)职业-环境暴露相关性ILD:包括FHP、各种纤维化性职业性肺病、药物性肺病等;(4)弥漫性囊性病变和肺泡充填性病变:包括PLCH、LAM、肺泡蛋白沉积症等;(5)纤维化性肺结节病。
本指南特别强调:PPF中不包括IPF,PPF不是一种特定的疾病,其中包括了一大类具有类似的临床表现和胸部影像学、呼吸生理变化的疾病。更为重要的是,PPF与疾病预后相关,而并非强调达到PPF标准就需要抗纤维化药物治疗。
至于本指南用PPF代替之前临床研究中的具有进展性表型的纤维化型间质性肺疾病(PF-ILD),专家们解释如下:FILD疾病进展导致PPF而非单纯是肺间质病变的加剧,且疾病进展后的临床过程类似于IPF,PPF的称谓(进展性肺纤维化)更顺口。
1.吡非尼酮:推荐开展临床试验来进一步评价吡非尼酮治疗所有的非IPF-PPF、特定疾病相关的非IPF-PPF的有效性、安全性。
2.尼达尼布:(1)在非IPF-FILD患者经标准治疗失败、呈现为PPF时,推荐使用尼达尼布(有条件的推荐,低证据级别);(2)推荐开展临床试验来进一步评价尼达尼布治疗特定疾病相关的非IPF-PPF的有效性、安全性。
该指南从发病机制的探索、诊疗措施及治疗方案等方面提出了对于PPF的展望:建议探究FILD患者接受初始治疗后仍出现进展性、不可逆的纤维化表型的触发因素、基因易感性以及血管重建在其中的作用;可进一步通过外周血或BALF的蛋白组组学分析、转录组学分析,寻找进展为PPF的危险因素的生物标志物;开发卷积神经网络技术等人工智能技术来智能化识别ILD的表型、判断预后、提示疾病进展以及识别偶然发现的ILAs;优化可能引起PPF的FILD患者的药物治疗方案,即抗纤维化药物和抗炎治疗药物[糖皮质激素和(或)免疫抑制剂]的使用时机、顺序。
所有作者声明无利益冲突



























