
本文报道1例咽旁间隙血管周上皮样细胞肿瘤(perivascular epithelioid cell tumor,PEComa)合并甲状腺乳头状癌双原发恶性肿瘤的病例。患者女,54岁,因“发现左侧耳前肿物半年”入院。入院后完善穿刺活检诊断为:左侧咽旁间隙PEComa合并甲状腺乳头状癌双原发恶性肿瘤,其咽旁间隙PEComa已侵犯左侧下颌骨,经过手术治疗后病情好转出院。出院后耳鼻咽喉头颈外科及肿瘤科定期复查,现患者术后1年,恢复良好,未见明显复发征象。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
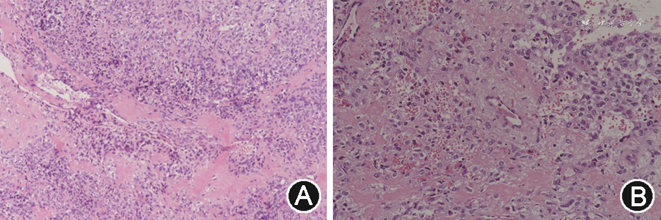
患者女,54岁,因“发现左侧耳前肿物半年”于2021年4月14日就诊于湖南省人民医院耳鼻咽喉头颈外科。半年前肿块大小约2.0 cm×2.0 cm×1.5 cm,患者无不适症状,未予诊治。2021年4月5日患者在当地县人民医院行CT检查示左侧咽旁间隙团块状软组织肿块可疑恶性。4月8日就诊于长沙市某医院,行MRI检查示左侧咽旁间隙肿块恶性可能性大。为求进一步诊治就诊于我院。患者既往无特殊病史。专科查体:左侧耳前可触及一大小约4 cm×4 cm×3 cm肿物,质硬,活动欠佳,边界不清,无明显触痛及压痛,张口无明显受限,舌体活动可。颈软,气管居中,甲状腺不大,未扪及明显结节,无颈静脉充盈,颈部未扪及明显浅表淋巴结。血生化检查无明显异常。影像学检查:全身骨扫描示左侧面颊区代谢异常增高;甲状腺彩超示甲状腺左侧叶低回声结节并钙化甲状腺影像报告和数据系统(TI-RADS)4b类,甲状腺左侧叶低回声结节TI-RADS 4a类,甲状腺双侧叶混和回声结节TI-RADS 3类;腮腺增强CT示左侧咽旁间隙占位伴左侧下颌骨破坏、甲状腺左侧叶病灶(图1);头颈部CT血管成像(CTA)示左侧咽旁间隙肿块由左侧颈外动脉分支供血,引流静脉为颈外静脉(图2)。患者于超声下行甲状腺左侧叶结节及左侧咽旁间隙肿物穿刺活检,病理结果提示甲状腺乳头状癌、左侧咽旁间隙肿物倾向具有血管周上皮样细胞分化的肿瘤。遂于2021年5月6日在全身麻醉下行颈外进路咽旁间隙肿物摘除术+下颌骨部分切除术+面神经松解减压术+甲状腺全切术+左侧Ⅵ区淋巴清扫术。针对咽旁间隙肿物,于左侧耳部做S形切口,术中见质硬肿物位于腮腺深叶深面,侵犯左侧下颌骨升支达髁状突,保护好面神经,从左侧下颌角处截断下颌骨,将肿物与左侧下颌骨升支及髁状突一同切除取出。术后病理回报:左侧咽旁间隙肿块为间叶源性肿瘤,符合恶性血管周上皮样细胞肿瘤(perivascular epithelioid cell tumor,PEComa),侵犯破坏骨质,未见血管及神经侵犯。免疫组织化学:CK(pan)(-)、EMA(-)、SATB2(-)、S-100(-)、Ki67(+2%)、Vimentin(灶+)、SMA(灶+)、Melan-A(灶+)、Melanoma(-)、p53(+1%)、TFE-3(-)、CD56(-)、Desmin(-)、CD34(血管及少数细胞+)、STAT6(-)、Calponin(-)、MyoD1(-),见图3。甲状腺左侧叶肿物为甲状腺乳头状癌,可见两处癌灶,直径0.6~0.7 cm,可见被膜侵犯;甲状腺右侧叶为结节性甲状腺肿。术后予以头孢哌酮舒巴坦钠注射液预防感染以及消肿、补液等对症治疗后,患者伤口愈合佳,伴有中度面瘫,House-Brackmann分级为Ⅲ级。于2021年5月18日出院,出院后我科及肿瘤科门诊定期复查,现患者恢复良好,无明显面瘫症状,随访1年未见明显复发征象。
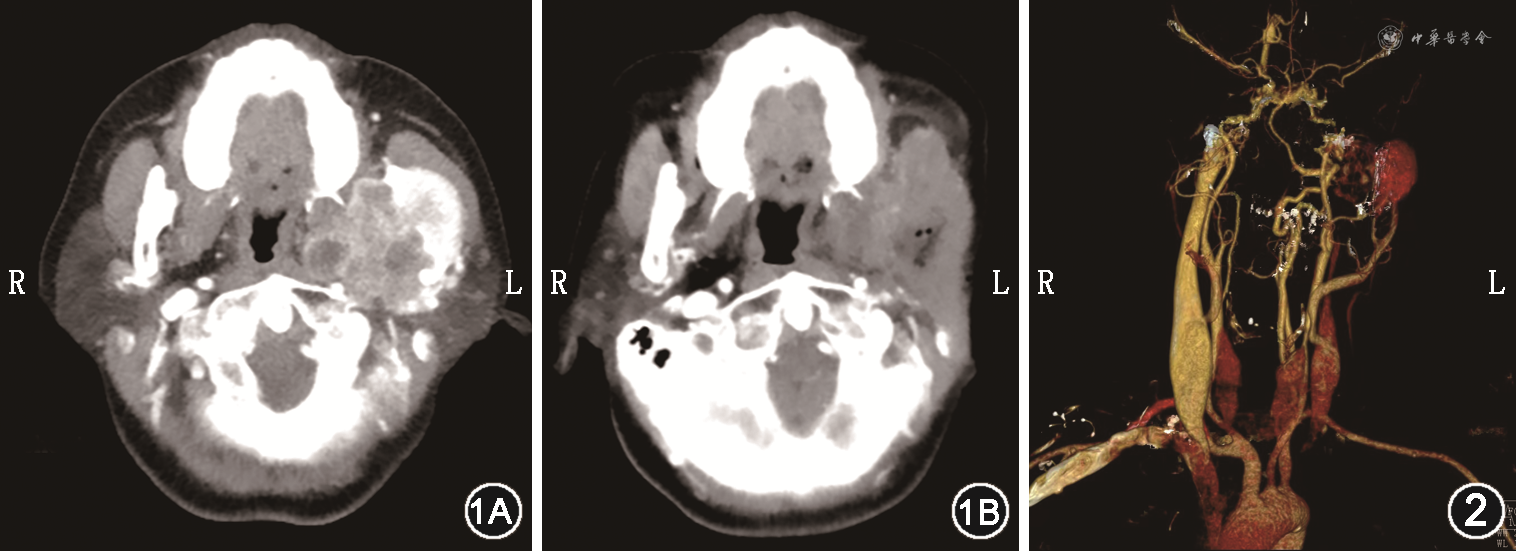


血管周上皮样细胞(perivascular epithelioid cell,PEC)是位于血管周围,通常在血管腔周围呈放射状排列的细胞。世界卫生组织将PEComa定义为一组在组织学和免疫表型上具有PEC特征的间叶性肿瘤[1]。该病在临床上较罕见,PEComa最常见的起源部位是腹膜后器官(如肾脏、胰腺),其次为子宫[2],眼眶、肺部、消化道、肝脏、膀胱均有PEComa的报道,咽旁间隙罕见。本病例合并甲状腺乳头状癌,易误诊及漏诊,目前尚未发现文献报道这2种肿瘤的关联性。关于PEComa的临床表现,妇科PEComa因肿瘤的大小、位置和扩散而不同,小的肿瘤大多无症状,症状明显的病例常表现为异常的阴道或腹膜出血、腹痛、子宫破裂和腹腔积血等[3]。大部分肾PEComa临床表现也缺乏特异性,肿块较大时可出现腰腹部疼痛、包块及血尿等[4]。许多PEComa患者无特异性症状,有症状者可能是合并其他疾病或肿块增大引起的压迫症状。本病例中,患者无明显临床不适,导致就医延误,加重病情。
诊断方面,影像学检查难以诊断PEComa,但CT、MRI等可以帮助诊断肿瘤的位置、大小及与周围组织的关系,有助于评估良恶性及判断转移情况[5]。明确诊断需组织病理切片及免疫组织化学检查。PEComa病理组织形态:以瘤体内含有丰富、纤细的血管网,血管周围或血管间成片、成巢或器官样排列的上皮样或梭形透明细胞,类似肾透明细胞癌或副神经节瘤样形态为特征。恶性PEComa病理表现:浸润生长,核大且深染,核分裂象增多,不典型性核分裂象及凝固性坏死[6, 7]。Folpe等[8]认为软组织和妇科来源的PEComa可归类为“良性”“恶性潜能未定”或“恶性”,提出恶性PEComa须具有2个或以上的特点:包括肿瘤直径>5 cm,呈浸润性生长,高级别核分级和细胞丰富度,核分裂象≥1/50 HP,凝固性坏死,血管侵犯;恶性潜能未定的PEComa为核多形性(仅见于多核巨细胞),或直径>5 cm;良性PEComa为肿瘤直径<5 cm且无其他组织学异常[8]。Bleeker等[9]认为肿瘤体积≥5 cm和高核分裂象指数为PEComa高风险指标,研究发现这2条组织学特征与肿瘤复发显著相关。免疫组织化学检测方面,肿瘤细胞可双重表达肌源性标志物平滑肌肌动蛋白及黑色素细胞源性标志物HMB-45、Melan-A[3,8]。
研究表明,大多数PEComa对放疗和传统细胞毒性药物有抵抗力,因此,手术切除已成为主要治疗方法。非手术治疗方面:(1)部分PEComa与结节性硬化症(tuberous sclerosis complex,TSC)这种常染色体显性遗传疾病相关,涉及基因9q34中的TSC1或基因16p13.3中的TSC2突变,导致异常激活mTOR通路,促进细胞增殖和血管生成。在与TSC无关的PEComa中也发现了这一过程,并且使用mTOR抑制剂治疗有效。因此,PEComa患者可能从mTOR抑制剂治疗中受益。(2)对于TFE3基因融合的PEComa,MET信号通路抑制剂是一种合理的治疗选择。(3)当标准治疗方法不可用或未发现特定靶基因时,也可以应用抗血管生成药物。因为从病理形态学上看,放射状分布于血管周围的肿瘤对抗血管生成治疗敏感。其中酪氨酸激酶抑制剂被用于治疗PEComa,并显示出一定效果,相关临床研究正在进行。总之,本病以手术治疗为主,预后良好。mTOR抑制剂、MET抑制剂、抗血管生成药物相关确切疗效正在研究中[9, 10]。本例患者予以手术治疗,术后暂未行靶向治疗或其他进一步治疗,至今已随访1年,尚未见肿瘤复发及转移。
综上所述,位于咽旁间隙的PEComa罕见,医务工作者应提高对该疾病的认识,合并甲状腺乳头状癌者更为罕见,诊断过程中避免漏诊误诊极为重要,而咽旁间隙PEComa与甲状腺乳头状癌是否有关联性也值得探索。PEComa在影像学上无特征性表现,但影像学检查可协助诊断肿瘤的位置、大小、良恶性以及与周围组织的关系,用以完善检查必不可少;病理检查为诊断金标准,发现多个肿物的情况下可采取穿刺活检明确性质后决定治疗方式;手术是PEComa主要治疗方式,若发现特定靶基因可辅以靶向治疗或使用抗血管生成药物,术后随访、定期复查必不可少。咽旁间隙PEComa的表现及治疗值得继续探索,且需病例的进一步积累。
所有作者声明无利益冲突



























