
超过80%的临床决策会涉及临床实验室化验结果,化验结果的正确解读将直接影响临床诊疗决策,而参考区间(RI)和临床决定值(CDL)是用于支持化验结果解释的重要标准。RI描述了某一化验指标测量值在健康参考人群中的分布,而CDL则涉及特定疾病的诊断,或与不良临床结局的风险相关。由于临床实践中常常会混淆这两个概念,如错误地将高于RI上限值作为临床决策阈值等,因此有必要澄清RI与CDL的区别。值得注意的是:RI是基于健康人群参考值分布范围建立的,因此化验结果不在RI范围内时,大多数情况下只是提示异常,而不一定意味着患病,是否患病或需要临床干预,常常需要额外的医学随访和综合评估。相比之下,CDL则与特定不良临床结局的发生风险相关,CDL是基于临床患者和疑似患者,对比金标准诊断结果或临床结局建立的,患者化验结果超过CDL阈值时,可以支持诊断或治疗等临床决策的制定。过去20年,国际临床实验室主要关注RI的建立,发布了RI建立与验证的方法学流程,很多国家在此基础上开展多中心研究针对临床常规化验指标建立了RI。如何建立适用的CDL,尚无达成共识的方法学流程,但基于临床结局的真实世界数据挖掘可以推动CDL的制定。本文一方面描述了RI和CDL这两种重要的实验室医学标准的异同,清楚地解释了其定义及制定过程,一方面希望推动我国临床科研工作者积极开展CDL相关研究。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
经全国继续医学教育委员会批准,本刊开设继教专栏,每年从第1期至第10期共刊发6篇继教文章,文后附5道单选题,读者阅读后可扫描标签二维码答题,每篇可免费获得Ⅱ类继教学分0.5分,全年最多可获3分。
超过80%的临床决策会涉及临床实验室化验结果(以下简称化验结果),化验结果的正确解读直接影响临床诊疗决策,如健康体检人群是否需要进一步检查,就诊患者是否需要进行有创检查,是否需要服药或手术等。化验结果的解读常依赖于两个标准,即参考区间(reference interval,RI)和临床决定值(clinical decision limit,CDL),这两个标准的定义、制定方法学程序以及临床意义均存在重要差异。笔者在2016—2021年间致力于建立我国儿童血细胞分析与常规生化检测指标参考区间的研究[1, 2, 3, 4],发现临床医护人员并不熟悉RI与CDL制定的方法学程序,从而影响了这两个标准的正确理解与应用。本文将详细阐述RI与CDL的定义、制定流程及其临床意义,以提高临床医护对化验结果的解读能力与临床决策水平。
在介绍RI与CDL与定义之前,我们需要从个体水平、群体水平了解影响化验结果的变异来源(表1),以帮助大家理解RI与CDL的临床意义。如表1所示,每个被检测个体存在个体水平的变异,即个体内变异,如每个人的血糖会随着时间变化而变化,血压会因体位不同而发生变异,血清肌酐、丙氨酸转氨酶、碱性磷酸酶等会受运动的影响发生变异,这些变异都是客观存在的。我们在建立诊断标准时,更多的考量是群体水平的变异,即个体间变异,如身高等由遗传因素决定的个体间变异,以及血红蛋白等由海拔这一环境因素引起的个体间变异。实际研究往往借助样本的测量结果来推断总体,但不同的抽样方法以及样本量大小均会影响样本与总体之间的差异。此外,无论是哪一水平的测量值,都无法完全消除测量本身存在的随机误差,因此,在制定RI与CDL的研究中,要设计严格的分析前、分析中与分析后质量控制策略,以减少随机误差对检测结果的影响。

不同水平的化验结果变异来源
不同水平的化验结果变异来源
| 变异水平 | 变异来源 | 举例 |
|---|---|---|
| 个体水平 | 个体内变异 | 研究对象的生理、生化指标会随时间、体位、温度等客观环境的改变而发生改变,这种变异是客观存在的 |
| 测量方法本身的随机变异 | 由于测量仪器的精密度不足而导致测量结果发生随机误差 | |
| 群体水平 | 遗传因素决定的个体间变异 | 研究对象的身高、体重、白细胞计数、各种酶学指标等生物学特征在个体间存在差异 |
| 环境因素引起的个体间变异 | 不同海拔地区导致的血红蛋白含量差异,地区饮食习惯引起的血肌酐浓度变异 | |
| 测量方法本身的随机变异 | 由于测量仪器的精密度不足而导致测量结果发生随机误差 | |
| 样本 | 抽样方法 | 不同的抽样方法导致样本与总体之间的差异大小不同 |
| 测量方法本身的随机变异 | 由于测量仪器的精密度不足而导致测量结果发生随机误差 |
1. RI定义:RI指在健康人群中,95%的健康参考个体某一检测指标测量值所在的分布区间[5]。采用临床实验室标准委员会(clinical laboratory standards institute,CLSI)推荐的非参数法来计算参考区间限值时,RI可表达为:下限值(2.5%分位数)~上限值(97.5%分位数)。当某些检测指标明确只有一侧有临床意义时,可以表达为单侧参考区间,即下限值(0)~上限值(95.0%分位数)或下限值(5%分位数)~上限值(最大值)[5]。制定参考区间旨在为回答“此人是健康的还是不健康的?”这一问题提供参考标准,但从RI的定义不难理解,在建立RI时,参考上限或下限外5%的参考个体其实也是健康参考个体,因此,当某个体的化验值超出RI限值时,并不意味着该个体一定患有某种疾病。正是为了避免大家对RI的误解,国际范围内近20年来倡导采用“参考区间”,而避免用“正常值范围”[6]。
2. RI制定的方法学流程:一般情况下,大家会遵循CLSI发布的参考区间制定流程[5]来建立适用于本地区人群的参考区间,我们完成的中国儿童参考区间研究也严格遵循了该方法学流程,包括:(1)定义健康参考个体:健康参考个体(尤其是儿童或老年人)的定义与测量并没有达成共识的标准,在设计参考个体的纳入与排除标准时,一般考虑将明确影响临床实验室检测结果的因素和生物学变异来源作为参考个体的排除标准,排除有明确影响因素(如1周内有服药史、手术史或输血史等)和生物学变异来源(如患有先天遗传代谢疾病)的个体后,获得相对的表观健康个体作为参考个体。(2)确定是要制定全国范围内通用的参考区间,还是为某地区的临床实验室建立参考区间,如果是前者,需要考虑通过多中心招募参考个体。(3)计算样本量:CLSI建议每个分组内建立参考区间的样本量不少于120例。在针对具体的临床实验室化验指标制定参考区间时,需要事先判断这些指标是否存在年龄依赖趋势、性别差异、地区差异等,如果存在,需要明确是否需要划分不同亚组制定参考区间。然后采用以下公式估算最小样本量:n=120×2(2个性别分组)×m(m个年龄分组)×o(o个地区分组)。(4)设计健康参考个体的筛查流程:一般会通过问卷调查(主要针对影响因素)、健康体检以及临床实验室检查来逐步筛出表观健康的参考个体。(5)制定标准操作规程(standard operating procedure,SOP):包括健康个体筛查,血标本采集、处理及转运,实验室分析,数据管理及统计分析等关键实施环节的SOP,以及针对参考个体的分析前、分析中及分析后质量控制手册。(6)基于SOP培训相关研究人员,保证研究人员参照SOP标准化实施研究,确保数据真实、可溯源。(7)数据清洗与统计分析:获得参考值后,进行数据清洗,然后实施统计分析。详细步骤包括:确定是否需要按年龄、性别划分亚组[7];在划分好的亚组内采用统计学方法识别离群值,对离群值产生原因进行分析,然后确定是否保留离群值;绘制频数分布图,采用非参数法估计RI上限值和下限值及其90%CI,(下限值,上限值)即为RI(图1)。(8)RI适用性验证:RI区间建立后,需要对其在其他临床实验室的适用性进行评价,一般按照制定RI时设计的研究对象纳入标准筛选年龄与性别匹配的研究对象,≥20例,将其化验值与RI进行比对,如果落在RI外的化验值所占比例≤10%,则视为适用,否则不适用。如果不是由于人群差异导致的,则需要进一步评估临床实验室质量,改进后再次开展评估。反之,需要考虑制定适用于本实验室覆盖人群的RI。
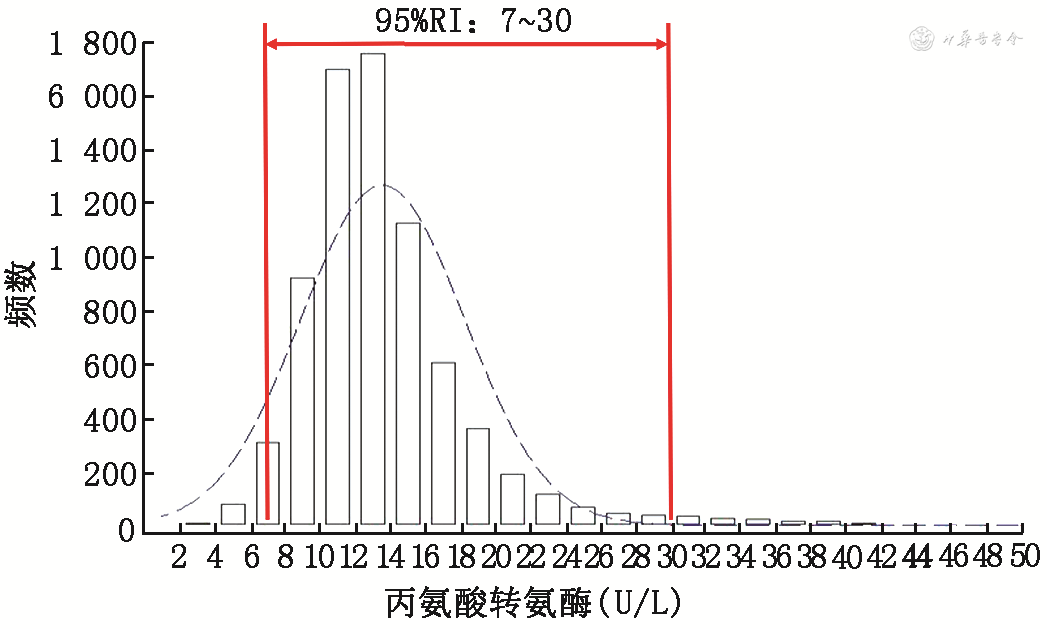

注:虚线为拟合正态曲线,红色实线为RI下限值与上限值之间的区域;RI为参考区间
1. CDL定义:CDL指在疑似患者或确诊患者人群中,当某一检测指标测量值高于或低于特定“阈值”时,可以对特定疾病进行明确诊断,或与不良临床结局发生风险显著相关,这一阈值即为CDL[8]。如果一个个体的某指标化验结果高于或低于RI的上、下限值,仅仅提示健康状态出现异常,而不一定需要临床处理。CDL的临床意义则显然不同于RI,如果一个个体的某指标化验结果高于或低于CDL,意味着该个体已患某种疾病,或该患者的病情发生恶化,如果不及时采取临床处理的话,发生不良临床结局的风险会显著升高,因此,CDL也被称为医学决定水平。一个临床实验室检测指标,在特定人群中建立唯一的RI,但CDL可能有多个,因为不同的临床决策需要相应的CDL。例如,成人空腹血糖的RI为3.9~6.1 mmol/L;<3.9 mmol/L时,可以诊断低血糖;<2.2 mmol/L时,即为致命性低血糖;6.1~<7.0 mmol/L时,为糖尿病前期;≥7.0 mmol/L时,可诊断糖尿病[9]。
2. 医学决定值制定的方法学流程:根据不同的临床决策目的,CDL主要包括诊断截点值(diagnostic cutoff)和危急值(critical value),顾名思义,诊断截点值是用于诊断的阈值,而危急值是实施临床干预的阈值。
(1)诊断截点值的建立:如何确定诊断截点值,取决于该诊断截点值对应的结局指标。针对类似肿瘤标志物诊断截点值的相关研究,常常遵循以下步骤[10]:①以明确诊断肿瘤患者为病例组,基线可比的健康人为对照组,比较两组人群的肿瘤标志物表达水平是否存在差异,尤其是病例组测量值分布范围与对照组无重叠时,高度提示该标志物有潜在诊断价值;②在临床门诊连续纳入疑似患者,测量肿瘤标志物,同时随访每一位患者的金标准诊断结果,然后通过绘制受试者工作特征(receiver operating characteristic,ROC)曲线确定诊断截点值,如果在该诊断截点值下获得的灵敏度与特异度有临床意义,则开展下一步研究对其诊断准确性进行评估;③依然在临床门诊连续纳入疑似患者,测量肿瘤标志物,采用上一步建立的诊断截点值进行诊断,将基于肿瘤标志物的诊断结果与金标准诊断结果进行对比,计算灵敏度、特异度、阳性和阴性预测值等指标,对该肿瘤标志物的诊断准确性及其诊断截点值的适用性进行评价。诊断截点值一般会权衡灵敏度与特异度的临床意义,取患病人群与非患病人群的频数分布图的交叉点(图2)。
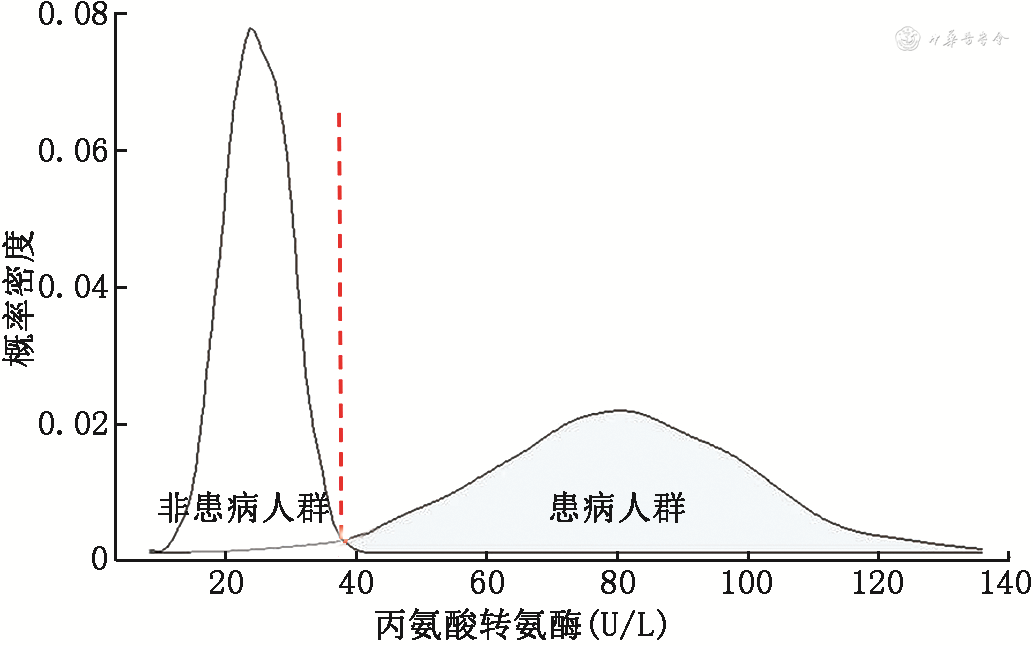

注:虚线为诊断截点值所在位置
针对类似将糖化血红蛋白控制在什么水平可以降低心血管风险的CDL制定,常常需要开展流行病学研究。例如:一项基于社区的前瞻性队列研究从美国4个社区共招募15 792例未患糖尿病的中年成人,1987—1989年完成基线调查,之后每3年进行一次随访,1990—1992年有14 348例参与者完成了第2次随访,此次随访中测量了糖化血红蛋白。排除第1次及第2次随访期间有糖尿病与心血管疾病诊断记录的人,最终纳入11 092例进行统计分析。结果发现基线时糖化血红蛋白水平与糖尿病和心血管发病存在关联。将研究对象按糖化血红蛋白值<5.0%、5.0%~<5.5%、5.5%~<6.0%、6.0%~<6.5%和≥6.5%分组,多因素调整的糖尿病风险比及其95%CI分别为0.52(0.40,0.69)、1.00(对照)、1.86(1.67,2.08)、4.48(3.92,5.13)和16.47(14.22,19.08);冠心病风险比分别为0.96(0.74,1.24)、1.00(对照)、1.23(1.07,1.41)、1.78(1.48,2.15)和1.95(1.53,2.48);卒中的发生风险比与冠心病相似[11]。据此成果,美国糖尿病协会将糖尿病诊断标准更新为:糖化血红蛋白<5.7%为健康,5.7%~<6.5%诊断为糖尿病前期,≥6.5%诊断为糖尿病。
(2)危急值的建立:危急值,也称为预警值,指某一个体的实验室检查结果一旦达到危急值水平,提示该个体健康状态不同于正常的病生理状态,如果不立即进行干预,将会对患者的生命构成威胁[12]。当某一指标的实验室检测结果达到或超过危急值水平时,代表患者已丧失体内稳态,存在失代偿风险,从而导致死亡。危急值的定义是通过预测某实验室检查结果显著变化,高于或低于某一界值可能与患者90%死亡概率关联时,将此界值定义为危急值[13]。
危急值多采用基于医院患者结局的大数据分析来建立[14],具体步骤如下:①提取某时间范围内某医院来源的病例数据,包括不良临床结局(如死亡、住院期间转入重症监护室等)、住院期间特定指标的所有实验室化验数据以及人口学信息等;②充分考虑影响实验室检测结果的影响因素,设计数据的纳入与排除标准,筛选符合要求的数据构建分析数据集;③清洗数据,如识别离群值,对离群值产生原因进行分析等;④基于贝叶斯定理,计算每个实验室检测水平下的不良临床结局发生概率;⑤以实验室检测结果为横坐标,不良临床结局发生概率为纵坐标,绘制散点图及拟合多项式概率趋势曲线(图3);⑥将与90%不良临床结局概率趋势线相交的实验室检测值定义为危急值。
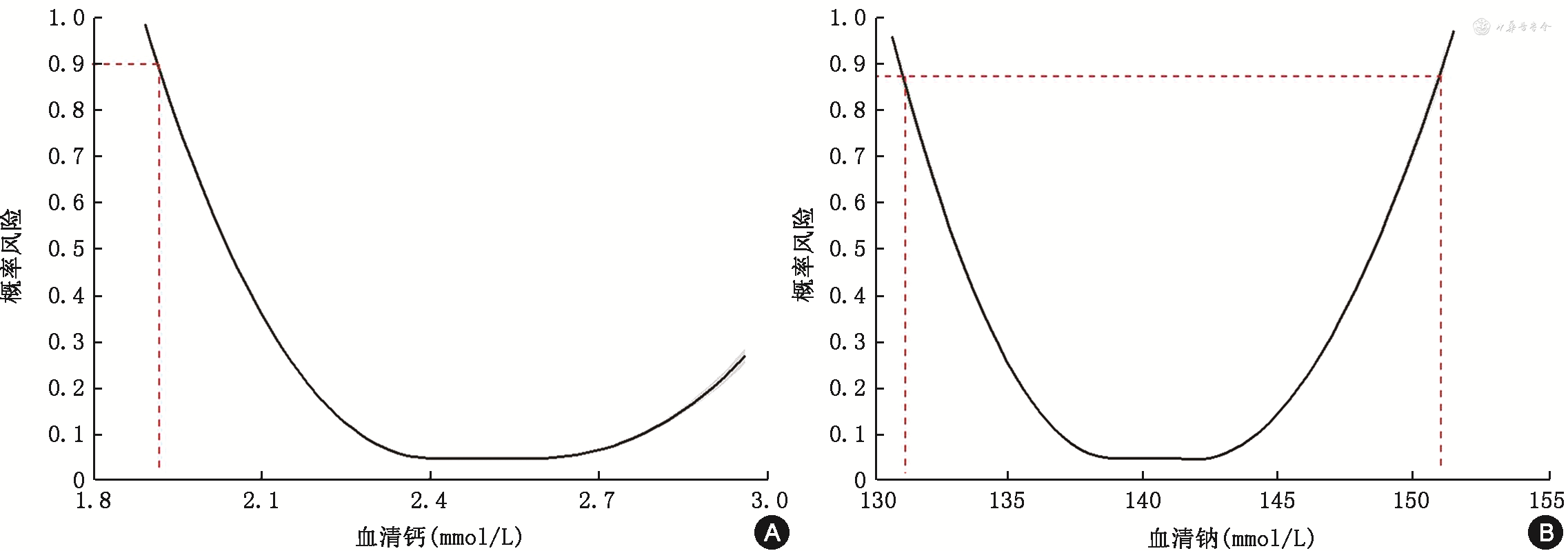

注:虚线为血清钙和血清钠水平对应的不良临床结局发生风险
近年来,ISO 15189[15]将RI和CDL的报告纳入临床实验室报告质量,正确地解读临床实验室化验结果对提高临床决策能力有重要意义。疾病诊断和治疗时机判断使用的应为CDL,而不是RI的上限值,但很多临床指南采用n倍上限值或下限值来表示诊断阈值或危急值,从而在一定程度上造成了RI上限与CDL的混淆。例如,尿酸的RI上限值,与预测痛风的CDL并不相同;仅依据丙氨酸转氨酶高于RI上限也不足以支持启动慢性乙型肝炎治疗,还需结合肝硬化是否代偿及乙肝病毒的DNA拷贝数等多种因素,经过综合评估后才能制定临床治疗决策。为了避免大家的困惑,将RI与CDL的区别汇总于表2。
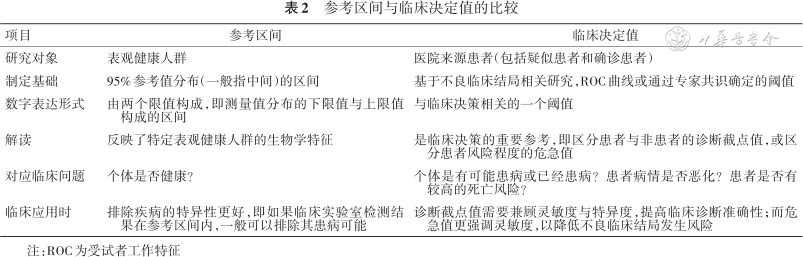
参考区间与临床决定值的比较
参考区间与临床决定值的比较
| 项目 | 参考区间 | 临床决定值 |
|---|---|---|
| 研究对象 | 表观健康人群 | 医院来源患者(包括疑似患者和确诊患者) |
| 制定基础 | 95%参考值分布(一般指中间)的区间 | 基于不良临床结局相关研究,ROC曲线或通过专家共识确定的阈值 |
| 数字表达形式 | 由两个限值构成,即测量值分布的下限值与上限值构成的区间 | 与临床决策相关的一个阈值 |
| 解读 | 反映了特定表观健康人群的生物学特征 | 是临床决策的重要参考,即区分患者与非患者的诊断截点值,或区分患者风险程度的危急值 |
| 对应临床问题 | 个体是否健康? | 个体是有可能患病或已经患病?患者病情是否恶化?患者是否有较高的死亡风险? |
| 临床应用时 | 排除疾病的特异性更好,即如果临床实验室检测结果在参考区间内,一般可以排除其患病可能 | 诊断截点值需要兼顾灵敏度与特异度,提高临床诊断准确性;而危急值更强调灵敏度,以降低不良临床结局发生风险 |
注:ROC为受试者工作特征
ISO 15189要求临床实验室根据适用条件报告RI或CDL,因为孤立的实验室检测结果需要与RI或CDL进行比较,才能准确判断患者病情进展及可能的预后,因此,RI和CDL的真实性与人群适用性将影响患者的临床结局。为了提高临床实验室报告质量,过去20年间,我国针对临床重要且常规检测的指标开展了RI建立与验证相关研究,在更新成人参考区间后,于2021年首次发布了儿童参考区间[3, 4]。但采用基于表观健康人群的多中心横断面研究(也称直接法)建立RI面临巨大挑战:(1)建立通用的RI,目前仅适用于实验室检测数据溯源性较高的指标;(2)为了解决多个分析系统之间的可比性,需要采集1~15 ml甚至更多的血标本,现场流调时会影响可行性;(3)针对特殊人群,如新生儿、高龄老人,往往无法采集足够的生物标本;(4)需要有非常严格的分析前、分析中与分析后质量控制系统;(5)RI建立研究往往需要巨额经费支持,耗时3~5年。针对以上挑战,近10年来,大家尝试采用临床实验室在日常诊疗中测量并保存下来的真实世界数据(也称间接法)来建立RI,笔者所在团队也正在对间接法的方法学进行研究[16, 17],但对其中的关键技术,即如何从医院来源的数据中分离出近似健康参考个体的数据集,尚未形成共识。
CDL,尤其是危急值与患者安全息息相关,因此,全球范围都非常关注CDL的制定及其标准化问题,但制定适用的CDL,在方法学方面存在以下挑战:(1)为正确定义CDL,原则上应在无任何医疗干预的情况下观察实验室结果异常患者的相关临床结局,以便在没有混杂或偏倚的情况下客观评估其临床影响,但是,这在当今的研究和医疗实践中显然是不可接受的;(2)不同实验室检查项目,对应的不良临床结局也不相同,因此,CDL的建立需要由多学科团队(包括临床专业、检验专业、病理专业与统计学专业等)共同完成;(3)同RI一样,许多实验室检查项目的CDL也存在性别差异或年龄依赖趋势,与儿童生长发育过程中生化特征的持续变化有关,这时需要考虑分性别、分年龄组建立CDL,当不良结局事件发生率较低时,需要极大的样本量;(4)虽然有专家提出使用数据挖掘技术来建立CDL,但是尚未达成共识的方法学流程及关键技术的解决方案。
综上所述,过去20年,各国逐步建立RI,并完善了RI相关实验室质量,但未来更应该重视CDL的制定,以通过提高临床实验室报告质量及实验室与临床医护的信息沟通质量来改善临床结局[18]。
作者声明无利益冲突
1.建立参考区间的研究对象是基于()
A.疑似患者
B.健康人群
C.确诊病例
D.以上都不对
2.建立诊断截点值的研究对象是基于()
A.疑似患者
B.确诊病例和健康对照人群
C.确诊病例
D.以上都不对
3.建立临床危急值是否必须以死亡为结局?()
A.是
B.否
4.对于体检人群的健康状态评估而言,最常用的标准是()
A.诊断截点值
B.危急值
C.参考区间
D.风险比值
5.确定参考区间的参考限值常用的统计方法是()
A.
B.P2.5~P97.5
C.
D.



























