
报道1例2型糖尿病(T2DM)合并非酒精性脂肪性肝病患者使用司美格鲁肽的诊疗过程。患者为37岁男性,因“发现血糖升高1年”就诊,既往合并脂肪肝、肝功能异常、肥厚型梗阻性心肌病,结合实验室检查明确诊断为T2DM。考虑患者合并疾病情况,及减少用药频次需求,更改原有降糖方案为司美格鲁肽皮下注射治疗,患者血糖控制更加理想,脂肪肝程度减轻,肝功能恢复正常,用药频次较前明显减少,患者依从性和满意度均提高。有研究表明,胰高糖素样肽-1受体激动剂(GLP-1RA)可以改善T2DM患者的肝脏脂肪含量,司美格鲁肽作为最新的GLP-1RA周制剂,可考虑应用于合并脂肪肝的T2DM患者,改善血糖控制的同时也改善脂肪肝和肝功能。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)在普通成年人群中患病率为30%,在糖尿病及肥胖患者中高达60%~70%[1, 2]。胰高糖素样肽-1受体激动剂(glucagon-like peptide-1 receptor agonist,GLP-1RA)作为近年应用越来越广的新型降糖制剂,除了有效降低血糖,还具有改善多种心血管危险因素的作用[3],同时也有研究表明GLP-1RA可以改善2型糖尿病(type 2 diabetes mellitus,T2DM)患者的肝脏脂肪含量[4],因此可能具有改善脂肪肝的作用。现将就诊于我科门诊的1例T2DM合并脂肪肝患者应用司美格鲁肽的诊疗经过报道如下,以期为类似患者的治疗提供参考。
患者 男,37岁,主因“发现血糖升高1年”就诊我科门诊。患者1年前因肥厚型梗阻性心肌病就诊外院时发现血糖升高,多次静脉空腹血糖大于7.0 mmol/L(参考值3.9~6.1 mmol/L),糖化血红蛋白(glycosylated hemoglobin,type A1c,HbA1c)6.6%(参考值4%~6%),空腹C肽3.57 ng/ml(参考值1.1~4.4 ng/ml),无明显口干、多尿、多饮、多食、体重下降,无尿中泡沫增多、下肢水肿,无视物模糊、视力下降,无手足麻木、发凉、针刺样感觉,无下肢疼痛、间歇跛行等不适,诊断T2DM。给予西格列汀(100 mg,1次/d)联合二甲双胍(0.5 g,3次/d)降糖,控制饮食,规律锻炼,每顿主食1~2两,每周锻炼3~4次,每次40~60 min,自测空腹血糖6.0~7.2 mmol/L,餐后2 h血糖6.0~8.5 mmol/L,无心悸、手抖、出汗等不适。8个月前就诊我科门诊,要求简化降糖方案,减少用药次数,外院查HbA1c 6.4%。
既往史:肝功能异常10余年,长期口服双环醇等保肝药物治疗,多次复查肝功能仍异常,8个月前就诊北京地坛医院,诊断考虑脂肪肝,予长期口服药物保肝治疗。另患者合并“肥厚型梗阻性心肌病”1年,口服比索洛尔(10 mg,1次/d),近期无心悸、胸闷等不适。否认高血压、脑血管病病史,否认肝炎、结核史,否认手术、外伤病史,否认药物过敏史。个人史:否认吸烟、饮酒史。家族史:父亲因心脏病去世,具体病因未确诊,否认其他家族遗传性疾病史。
查体:神志清楚,精神好,体型中等,无满月脸、水牛背,身高178 cm,体重85 kg,体重指数26.8 kg/m2,血压122/70 mm Hg(1 mmHg=0.133 kPa),甲状腺未触及明显肿大,双肺呼吸音清,未闻及明显干湿啰音,心率72 次/min,律齐,腹软,无压痛,双下肢无水肿。
实验室检查(使用司美格鲁肽之前):2021年6月于外院进行肥厚型梗阻性心肌病单基因遗传病基因检测(高通量测序法),结果显示心肌肌球蛋白结合蛋白-C3基因突变阳性,杂合突变;2021年7月外院查空腹静脉血糖7.43 mmol/L,丙氨酸转氨酶(glutamic pyruvic transaminase,ALT)154 U/L(0~50 U/L),天冬氨酸转氨酶(glutamic oxaloacetic transaminase,AST)68 U/L(0~50 U/L),γ-谷氨酰转移酶(γ-glutamyltransferase,GGT)70 U/L(0~50 U/L),HbA1c 6.6 %,空腹C肽3.66 ng/ml(参考值1.1~4.4 ng/ml)。2021年9月于外院查空腹静脉血糖7.27 mmol/L,ALT 195 U/L,AST 79 U/L,GGT 70 U/L;2021年11月于外院查HbA1c 6.4 %,病毒性肝炎系列、甲功五项、免疫球蛋白、肿瘤系列、自身免疫性肝炎系列均正常,腹部超声提示肝大,右叶最大斜径14.5 cm,中-重度脂肪肝,脾大,胆囊壁毛糙,胆囊多发息肉样病变,大者0.5 cm。
结合病史、查体及空腹胰岛素C肽等化验检查,T2DM诊断明确,同时合并有非酒精性脂肪肝、肝功能异常、肥厚型梗阻性心肌病、胆囊多发息肉。患者平时生活方式已较规律,控制饮食、锻炼,应用西格列汀联合二甲双胍治疗后血糖较前有所下降,但仍未达到理想水平,考虑患者合并有多年脂肪肝病史、并有减少用药频次的需求,更换为司美格鲁肽治疗,起始剂量0.25 mg,1次/周,患者用药后无恶心、呕吐、腹泻等胃肠道反应,食欲轻度抑制,4周后加量至0.5 mg,1次/周至今,自测血糖较前下降(表1),体重共下降约2 kg。3个月前外院查HbA1c 6.3%,1个月前我院复查HbA1c 6.0%,尿白蛋白/肌酐比值6.91 mg/g(参考值0~20 mg/g),空腹胰岛素37.05 mU/L(参考值2.6~24.9 mU/L),空腹C肽3.66 ng/ml。
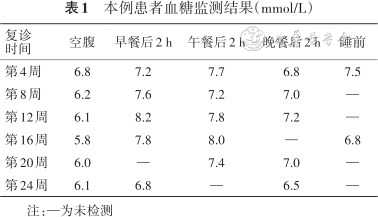
本例患者血糖监测结果(mmol/L)
本例患者血糖监测结果(mmol/L)
复诊 时间 | 空腹 | 早餐后2 h | 午餐后2 h | 晚餐后2 h | 睡前 |
|---|---|---|---|---|---|
| 第4周 | 6.8 | 7.2 | 7.7 | 6.8 | 7.5 |
| 第8周 | 6.2 | 7.6 | 7.2 | 7.0 | — |
| 第12周 | 6.1 | 8.2 | 7.8 | 7.2 | — |
| 第16周 | 5.8 | 7.8 | 8.0 | — | 6.8 |
| 第20周 | 6.0 | — | 7.4 | 7.0 | — |
| 第24周 | 6.1 | 6.8 | — | 6.5 | — |
注:—为未检测
患者脂肪肝随访情况如下。使用司美格鲁肽4个月后复查肝功能降至正常,ALT 23 U/L,AST 32 U/L,GGT 49 U/L,2个月前嘱患者停用保肝药,并于1个月前就诊我科门诊,复查肝功仍维持正常,ALT 42 U/L,AST 27 U/L,GGT 39 U/L。同时复查腹部超声,结果示肝脏饱满,右叶最大斜径13.3 cm,左叶前后径6.5 cm,轻-中度脂肪肝,脾脏大小正常,胆囊壁多发隆起样病变,大者0.5 cm×0.5 cm(息肉可能性大),提示患者肝脏增大较前好转,脂肪肝程度较前减轻。同时患者由既往的每日多次服药减少至每周1次用药,用药频次较前明显减少,且无明显的胃肠道反应,自觉生活质量较前提升,治疗依从性和满意度均较前提高。
T2DM的患病率近年逐年提升,最新流调数据显示,我国T2DM患病率已达11.2%[5]。NAFLD在普通成年人群,尤其中青年男性患者中患病率很高,在糖尿病及肥胖患者中更是高达60%~70%[1, 2]。T2DM和NAFLD互相影响,存在共同的病理生理机制,如胰岛素抵抗、脂代谢受损、遗传易感性、环境因素等[6, 7],且NAFLD可能是T2DM的早期表现[1, 2]。T2DM合并NAFLD的患者,尤其男性患者,心血管风险及冠心病患病率显著增加[8, 9, 10]。因此对于此类患者,是否优先选择某些既能控制血糖,又能改善脂肪肝情况的降糖药物?既往研究显示,在T2DM合并NAFLD的患者中,GLP-1RA可以明确改善转氨酶水平,减轻肝脏中脂肪含量;钠-葡萄糖共转运蛋白2抑制剂可能通过减少肝脏脂质负担、减轻体重从而对NAFLD有潜在获益;二甲双胍可以改善肝脏胰岛素敏感性,对是否能改善NAFLD疾病活动及肝纤维化情况,目前尚无明确临床证据;二肽基肽酶Ⅳ抑制剂可能对NAFLD有潜在获益,但结果尚未在大型随机对照研究(randomized controlled trial,RCT)中验证;胰岛素可以减少肝脏脂肪变性,但目前尚无肝活检研究评估其对肝脏组织学的影响[11]。因此结合本例患者,既往肝功能异常多年,NAFLD诊断明确,血糖长期控制不达标,空腹血糖持续大于6.0 mmol/L,且患者有减少用药频次、提高生活水平的意愿,综合考虑,调整降糖方案为司美格鲁肽每周1次注射。调整方案后,患者的肝功能、脂肪肝情况均较前明显改善,血糖水平进一步下降,同时患者的生活质量和治疗依从性也明显提升。
GLP-1RA具有治疗NAFLD的应用前景。研究证实,肝脏细胞上存在GLP-1受体[12],NAFLD患者的GLP-1分泌明显减低[11]。GLP-1RA可能直接调节肝脏脂质代谢,并抑制氧化应激和内质网应激产生炎性反应,从而达到保护肝细胞、改善NAFLD的作用。研究显示,GLP-1RA中的代表药物利拉鲁肽可以显著改善肝酶异常的T2DM患者的肝酶水平,并可改善肝脏脂肪变性,延缓肝脏纤维化进展[13]。本例患者的治疗过程提示,司美格鲁肽作为新型GLP-1RA周制剂,可能存在与利拉鲁肽相似、甚至更强的改善T2DM患者肝酶和NAFLD的作用。后续需要大型的RCT研究证据来进一步证实,并探索其可能的作用机制。
在降糖方面,由于司美格鲁肽独特的分子结构,使其半衰期可以长达7 d左右,并在体内维持稳定的血药浓度,因此在减少注射频次的同时,也能保证良好的降糖效果。在司美格鲁肽和西格列汀降糖效果和安全性比较的RCT研究当中,各组基线特征类似,但司美格鲁肽组在降糖疗效,如HbA1c的达标率和达标人群比例中,均显著优于西格列汀组,且在降低体重方面也具有明显优势。其中在我国的T2DM人群研究数据显示,司美格鲁肽可以降低HbA1c达1.8%,HbA1c达标人群比例高达86.1%,且其具有改善血压、血脂、体重、腰围等多种获益,也具有良好的安全性[14]。同时其还可以显著降低主要心血管不良事件的风险达26%,且该获益不受基线HbA1c、年龄、性别等因素的影响[15]。对于本例患者,其同时合并有肥厚型梗阻性心肌病,除了血糖、脂肪肝、体重等方面的获益,可能也会有心血管方面的长远获益。
因此,对于同时合并有T2DM和NAFLD的患者,尤其超重或肥胖患者,可以考虑起始司美格鲁肽治疗。其在控制血糖、减轻体重的同时,可能也能改善脂肪肝和肝脏代谢,从而改善肝功能,并且提高患者的依从性、治疗满意度和生活质量。
所有作者声明无利益冲突



























