
心力衰竭(心衰)是一种儿科常见的急危重症,通常表现为液体超负荷,但部分情况下也存在容量不足的现象。容量管理是心衰患儿重要的治疗措施之一,其目的是使心衰患儿达到个体化的最佳容量平衡状态,而容量评估则是容量管理的前提和基础。如何全面地对心衰患儿进行容量评估并进行有效的容量管理,对临床医师具有一定的挑战性。本文结合国内外文献,对容量评估的方法和处理措施进行了详细阐述,以期为临床工作提供参考。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
心力衰竭(简称心衰)是儿科常见的急危重症之一,也是导致儿童死亡的重要原因。虽然引起心衰的病因复杂,但其主要的病理生理变化相似,均因心输出量降低,导致交感神经以及肾素-血管紧张素-醛固酮系统等一系列神经内分泌系统激活,继而水钠潴留,液体过负荷。因此,容量管理对心衰患儿非常重要,同时亦是治疗的难点。
如前所述,心衰患儿绝大多数情况下,主要面临液体超负荷,但少数情况下也会出现容量不足的情况,其容量状态是复杂且是动态变化的,故应在容量状态的连续监测和动态评估下进行心衰患儿的容量管理,目的是使心衰患儿达到个体化的最佳容量平衡状态。
评估是管理的基础。心衰患儿的疾病状态以及合并症不同,均会影响其容量状态,故应从多角度、分层次进行容量状态的评估。评估方法包括容量相关病史的询问、临床表现的观察和血流动力学的监测等。
详细地询问病史,有助于患儿容量状态的判断。询问患儿近期有无失血、腹泻、多尿、大汗等体液大量丢失的病史,有无严重摄入不足的情况,以及基础肾功能的情况,以明确患儿近期液体出入量的总体情况。短期内体重明显增加提示液体超负荷。
容量过负荷的症状包括左心功能不全导致的肺淤血症状(呼吸困难等)和右心功能不全导致的体循环淤血症状(水肿、腹胀、纳差等消化道症状)。存在上述症状时,提示容量超负荷;完全没有上述淤血症状,提示容量状态正常;无淤血症状,同时出现低血压等血流动力学不稳定的表现,可能存在容量不足,需结合其他指标进行综合判断。
应进行针对性地体格检查,重点评估以下体征:如颈静脉怒张、肝颈静脉回流征、肺部啰音、浆膜腔积液、肝脏肿大及水肿等。如存在上述体征,提示体内容量超负荷。如果无上述体征,同时存在低血压、皮肤弹性差、干燥、眼窝凹陷等表现,提示容量不足。其中,水肿是最直观的提示容量超负荷的体征,多为双下肢或身体低垂部位的水肿,多浆膜腔积液(如胸腔积液、腹腔积液)也提示容量过负荷。另外,体重、尿量及液体出入量的情况也均可反映体内的容量状态,如短时间内体重增加、尿量减少、入量大于出量,均提示体内液体潴留。
需强调的是,血压下降、心率加快可由于容量超负荷使心衰加重引起,也可因有效循环血量不足所致,此时需结合辅助检查进一步明确。
X线胸片上如出现肺上叶血管扩张、肺淤血、肺间质水肿、胸腔积液、克氏线等征象,均提示容量超负荷。
容量超负荷时,会引起血清或血浆中的利钠肽水平升高。但容量超负荷不是利钠肽升高的唯一原因,故利钠肽水平升高并不等同于容量超负荷。另外,因个体间存在差异,不能采用利钠肽的绝对数值作为确定容量状态的阈值,需要动态监测其水平。
在治疗过程中,可动态观察红细胞压积、血红蛋白浓度、白蛋白和血钠的水平,如上述指标进行性升高,提示体内容量超负荷的状态逐渐被纠正,甚至出现容量不足的情况[4,5]。需强调的是,上述指标的绝对值对于容量评估的意义不大,需进行连续的动态观察。
利用超声进行检测,如出现下腔静脉塌陷指数下降、下腔静脉直径增宽、肺部B线等均提示容量超负荷。平均的舒张早期二尖瓣血流速度峰值/二尖瓣瓣环速度峰值(E/e′)>14提示左房压升高,也提示容量过多[6]。
血流动力学监测技术是急危重症患者监护的一项重要手段,已经有多种血流动力学监测技术应用于临床,包括有创监测方法如中心静脉压(central venous pressure,CVP)监测、肺动脉导管(pulmonary artery catheteri-zation,PAC)监测、脉搏指示剂连续心输出量(pulse-indicated continuous cardiac output,PiCCO)监测等,以及近些年新兴的无创血流动力学监测方法如无创心排量监测(noninvasive cardiac output monitor,NICOM)和多普勒超声无创心功能监测(ultrasonic cardiac output monitor,USCOM)等。
是将动脉导管置入动脉内直接测量动脉内血压,与无创血压监测相比更加准确可靠,且可实时获得患者的收缩压、舒张压和平均动脉压,进行动态化持续测量。
用于评估右心前负荷状态,正常值6~10 mmHg(1 mmHg=0.133 kPa)。<4 mmHg通常提示心脏充盈欠佳或容量不足,>12 mmHg通常表示右心功能不全或液体超负荷[7]。但CVP的影响因素较多,包括循环血容量、心肌收缩力、胸腔内压力、肺循环阻力和心脏周围压力(如心包疾病)等,故不建议单纯依据CVP的测定值作为容量管理的依据[8],可联合有创血压监测的结果进行综合判断,具体见表1[9]。
PAC又称Swan-Ganz导管或肺动脉漂浮导管,可测量肺动脉压和肺毛细血管楔压(pulmonary capillary wedge pressure,PCWP)等指标,其中PCWP用于评估左心前负荷状态,正常范围6~12 mmHg。若每搏输出量指数降低,PCWP<6 mmHg提示可能存在容量不足,PCWP>12 mmHg提示左心功能衰竭,PCWP>25 mmHg提示可能存在急性肺淤血[7]。作为一项有创检测,PAC的临床应用有一定的争议性,目前国内外儿科临床应用较少。美国国立心肺血液研究所2000年的一项声明提出,儿科明确的PAC适应证是对于液体复苏和中小剂量血管活性药物无效的难治性休克患者[10]。
也称容量负荷试验,根据Frank-Starling原理,心室功能曲线处于上升期时,扩容可通过增加心脏前负荷从而提高每搏输出量,即容量反应性好;若心室功能曲线趋于平坦,补液对每搏输出量影响不大,即容量反应性差。通常选用晶体液,5~10 mL/(kg·次),静脉输入,具体输注速度需根据患者的具体情况。若补液后,患者心率下降,血压上升,每搏输出量或心输出量升高超过15%~20%可判断患者具有容量反应性[15]。但若补液后,患者心率增加,肝脏增大,肺部啰音增多,则提示体内容量过负荷,需停止补液。
是一种非侵入性的评估方法,通过抬高下肢,快速、短暂地增加静脉回流,增加左心前负荷及每搏输出量,起到快速扩容作用。适应证:患者不明原因心率加快,怀疑血容量不足时。禁忌证:患者存在严重的心功能不全、肺水肿、腹腔高压等。具体操作步骤为:首先评估患者病情及意识状态,将患者床头抬高45°,使患者处于半坐卧位2~3 min,观察并记录患者的心率;再将患者床头摇平,使患者置于平卧位,被动抬高患者双下肢45°,观察并记录患者心率。若患者心率明显下降,则说明存在血容量不足,应给予充分补液。若心率未见明显变化,则提示患者心率快可能不是容量不足所致,应积极寻找其他原因。若患者心率明显增加,则说明患者可能存在心功能不良或容量相对过多,应立即给予抬高床头,置于半坐卧位,并采取其他相应处置。该方法若同时结合食管多普勒超声、PiCCO、经胸超声心动图或USCOM等实时血流动力学监测技术,可更精准地预测容量反应性。若监测发现,每搏输出量增加≥15%,提示存在容量反应性,可能存在容量不足,反之,容量反应性差[16]。
上述不同的容量评估方法各有优缺点,任何一种单一的容量评估方法都存在局限性。临床上需要结合多种评估方法,并根据临床指标的动态变化进行综合分析。
遵循由简单到复杂,由无创到有创的原则。首先,根据病史和临床表现,初步判断患儿体内的容量状态;其次结合X线胸片、心脏超声及血常规、血生化、利钠肽等易得的实验室检查进一步评估,对于容量判断困难者,可结合被动抬腿试验、快速补液试验以及有创性血流动力学监测,进行精确评估。具体容量评估流程见图1。
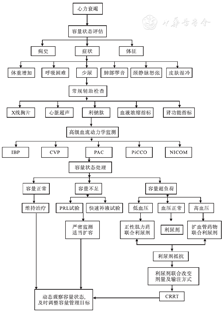

IBP:有创血压监测;CVP:中心静脉压;PAC:肺动脉导管;PiCCO:脉搏指示剂连续心输出量;NICOM:无创心排量监测;CRRT:连续性肾脏替代治疗;PRL:被动抬腿。
稳定期和轻度心衰患儿多可维持正常血容量,无需限钠和限水,其重点在于积极控制原发病,定期监测体重变化,避免出现液体失衡。
心衰患儿同时合并低血容量时,首要处理原则仍是给予扩容补液,补充循环血量。但补液速度不宜过快,补液量也需酌情减少,必须结合患儿的心功能和原发病状况,采取个体化的补液策略。补液期间密切监测心率、血压、肺部啰音、肝脏大小,如出现肝大和肺部啰音增多,则提示容量超负荷,需停止补液。
急性心衰患儿应严格控制液体入量,尤其淤血及水肿明显时,在排除低血容量且血压维持正常范围的情况下,建议液体摄入量减为生理需要量的80%[17]。对利尿治疗无反应或低钠血症的水肿患儿应限制饮水,可用高热卡液体食物来代替纯水。
利尿剂是心衰治疗取得成功的关键和基础,可有效减轻全身、肺部和静脉充血。有液体潴留证据的心衰患儿均应使用利尿剂,慢性心衰患儿多长期口服最小有效量利尿剂,急性心衰或慢性心衰急性失代偿期的患儿需静脉给予更高剂量的利尿剂。应用利尿剂的并发症包括电解质异常(低钠血症、低或高钾血症和低氯血症)和代谢性碱中毒。心衰患儿临床常用的利尿剂用法及剂量见表2。

心衰患儿常用利尿剂的用法及剂量
心衰患儿常用利尿剂的用法及剂量
| 药物 | 用法及剂量 |
|---|---|
| 呋塞米 | 口服或静脉推注:每次0.5~2.0 mg/kg,每6~24小时1次;最大剂量6 mg/(kg·d);静脉持续滴注:0.05~0.2 mg/(kg·h),最大量1 mg/(kg·h); |
| 布美他尼a | 静脉推注:0.015~0.1 mg/(kg·次),1~4次/d; |
| 托拉塞米 | 静脉推注:每次1~2 mg/kg,单次最大剂量不超过20 mg; |
| 氢氯噻嗪 | 口服:<6月龄,1~3 mg/(kg·d),1~2次/d;6月龄~2岁,1~2 mg/(kg·d),1~2次/d,最大剂量为37.5 mg/d;>2岁,1~2 mg/(kg·d),1~2次/d,最大剂量为100 mg/d; |
| 美托拉宗 | 口服,0.2~0.4 mg/(kg·d),1次/d; |
| 螺内酯 | 口服:< 32周早产儿,1 mg/(kg·d),每日1次;足月新生儿,1~2 mg/(kg·d),2次/d;婴儿和儿童,1~3 mg/(kg·d),2~4次/d;最大剂量为100 mg/d; |
| 托伐普坦a | 口服,0.3~0.5 mg/(kg·d),1次/d。 |
注:aFDA未批准用于18岁以下儿童。
襻利尿剂是通过抑制髓襻升支粗段Na离子、Cl离子重吸收而发挥利尿作用,通常被用作儿科利尿的一线用药[18]。临床可用的襻利尿剂包括呋塞米、托拉塞米、布美他尼等,其中呋塞米为儿科的常用利尿剂,药代动力学模型已经证明呋塞米存在明显的剂量-效应关系[19]。呋塞米持续输注是否比间断给药更安全、有效,目前尚无普遍共识。理论上来说,持续输注可以保证对肾单位的持续作用、减少血管内容积的波动、根据患儿出入量对尿量进行滴定[20]。有研究指出,持续输注患者的血流动力学参数、CVP、血氧饱和度和心率波动更小[21],并可处于长期的液体负平衡状态,减少对输液的需求。多数成人研究倾向于呋塞米持续输注有更好的利尿效果,但两者在病死率、电解质紊乱和肾功能方面差异无统计学意义[20,22],儿童研究未发现二者的显著差异。推荐的静脉滴注剂量为0.05~0.20 mg/(kg·h),最大量1.0 mg/(kg·h)。需要警惕呋塞米对新生儿尤其是早产儿的不良反应,包括耳毒性、肾钙质沉着症,与出生体重和日剂量密切相关[23]。
与呋塞米相比,其他的襻利尿剂利尿效果更强。如托拉塞米的利尿效果是呋塞米的2倍,但目前未获准应用于儿童,故缺乏临床研究数据。布美他尼利尿效果是呋塞米的40倍,同样FDA未批准其用于18岁以下儿童,但已有关于儿童的临床研究,静注剂量波动范围较大,每次0.015~0.1 mg/kg,1~4次/d[24]。
该类利尿剂的作用是抑制远端肾小管钠的重吸收,从而发挥利尿的作用。虽然噻嗪类药物可以作为单药治疗,但经常与襻利尿剂联用,以提供协同效应,克服对襻利尿剂的耐药性。常用药物为氢氯噻嗪,口服给药,不同年龄的儿童用量不同,具体为:<6月龄,1~3 mg/(kg·d),分1~2次,最大剂量为37.5 mg/d;6月龄~2岁,1~2 mg/(kg·d),分1~2次,最大剂量为37.5 mg/d;>2岁,1~2 mg/(kg·d),分1~2次,最大剂量为100 mg/d。美托拉宗是另外一种强效的类噻嗪类利尿剂,通过阻断肾小管近端和远端区域的钠重吸收起作用,持续时间为12~24 h,口服给药,用药剂量为0.2~0.4 mg/(kg·d),每日1次,通常作为二线或三线药物,与襻利尿剂和噻嗪类利尿剂组合,用于可耐受肠内给药的难治性液体超负荷患者[25]。
常用药物为螺内酯,是一种合成类固醇,竞争性地抑制醛固酮与远端肾小管受体的结合,保钾排钠。单独使用时利尿作用弱,临床上常作为利尿方案的辅助药物,以预防或治疗低钾血症。螺内酯在成人和儿童慢性心衰的治疗中起着核心作用,可以预防心肌纤维化[26],并可以提高心衰患者的存活率[27]。口服给药,不同年龄的儿童用量不同,具体为:< 32周的早产儿,1 mg/(kg·d),每日1次;足月新生儿,1~2 mg/(kg·d),2次/d;婴儿和儿童,1~3 mg/(kg·d),2~4次/d;最大剂量为100 mg/d。
代表药物为托伐普坦,作为选择性的血管加压素V2受体拮抗剂,通过拮抗肾集合管中的水通道蛋白-2通道以减少水分吸收,尤其适用于低钠血症患者。心衰患者血管加压素水平升高,血管加压素通过作用于肾脏集合管主细胞基底外侧表面的V2受体引起水潴留以维持血压,可导致水肿、呼吸困难和淤血等症状[28]。ACTIV、EVEREST、AVCAM、SALT-1和SALT-2等全球范围内的多中心成人临床试验已经证明,在常规心衰治疗方案的基础上加用托伐普坦,可增加液体负平衡、减轻体重和减缓心衰恶化速度,且不会导致电解质紊乱、低血压、肾功能恶化[29,30,31,32]。日本儿科循环和血流动力学学会(J-SPECH)研究证明,托伐普坦能有效、安全地用于儿科患者,但由于新生儿和婴儿的肾脏对血管加压素具有耐药性,疗效可能不如年龄较大的儿童[33]。一项单中心回顾性研究,纳入了25例心脏病术后出现容量超载合并毛细血管渗漏的婴儿(包括新生儿),结果显示,68%的患儿使用托伐普坦后利尿剂反应增加、气管插管和ICU住院时间缩短[34]。但托伐普坦儿童用药方面的临床研究资料仍较少,目前推荐剂量为0.3~0.5 mg/kg,每日1次口服[35]。
适用于血流动力学明显受损的心衰患儿[36]。米力农和(或)多巴酚丁胺可作为一线抢救治疗,肾上腺素可在顽固性低血压和器官灌注不良的情况下使用。但该类药物有导致心律失常的风险和快速减效反应,通常为急性期缓解症状时短期应用,以期提高心输出量,改善肾脏灌注,增加尿量。如用药后无明显的临床改善,则应及时给予机械循环支持和(或)心脏移植[37]。
(1)作用机制:体外超滤通过模仿肾小球滤过的原理,利用滤器半透膜两侧的压力梯度,滤出水分和小于半透膜孔径的中小分子物质。超滤滤出的液体为等张液,与血浆渗透压相同,排钠能力强于利尿剂,且不会产生类似于使用利尿剂的低钾血症或低镁血症。(2)临床证据和适应证/禁忌证:难治性尤其是终末期心衰患者通常有明显的水钠潴留和电解质紊乱,容易合并利尿剂抵抗。Kazory[38]对2007至2016年针对超滤和传统利尿药治疗效果比较的四个临床研究(UNLOAD、CARRESS-HF、CUORE、AVOID-HF)进行分析,其中UNLOAD、CUORE、AVOID-HF均倾向于超滤治疗,超滤能可控地减低容量超负荷,减轻神经内分泌激活,并可恢复利尿剂疗效,还可改善中期预后、减少数周至数月内心衰的再住院率,但未能改善长期存活率。中国2018年心衰指南亦推荐高容量负荷如肺水肿或严重外周水肿,且存在利尿剂抵抗的患者均推荐超滤治疗[39]。有学者建议将血液超滤作为失代偿性心衰患者清除水钠潴留和改善预后的金标准[40],但缺乏足够的循证医学证据来证实这一观点,目前临床上仍未将血液净化作为心衰的常规治疗手段。
结合国内外指南[39,41],心衰患儿血液超滤的适应证为[42]:(1)顽固性容量超负荷且对标准利尿治疗无反应;(2)严重电解质紊乱,如低钠血症、高钾血症;(3)进行性肾损伤;符合上述任一条均可考虑应用。相对禁忌证为:(1)低血压;(2)严重出血倾向,如血小板减少、凝血功能障碍等;(3)严重二尖瓣或主动脉瓣狭窄;(4)全身性感染者。
综上所述,心衰是一种复杂的临床综合征,容量状态复杂多变,临床医师需根据患儿的临床症状,实验室、影像学及血流动力学检查动态评估其容量状态,按照个体化原则进行容量管理。容量不足的心衰患儿需在严密监测下适当补液,容量过负荷的心衰患儿则需积极利尿,对于血流动力学不稳定的患儿可加用正性肌力药物,对于利尿剂反应不佳的顽固性心衰患儿,可考虑加用超滤治疗。
所有作者均声明不存在利益冲突




























