
子宫颈癌是最常见的女性恶性肿瘤之一,早期宫颈癌的治疗以手术为主。其中,保留盆腔自主神经功能的广泛子宫切除术可在达到相同肿瘤结局的同时改善术后控尿功能,提高患者生存质量。本文就广泛子宫切除术术式演进、腔室解剖理论及其术中实践、保留盆腔自主神经功能的腹腔镜术式及后子宫颈癌开腹与微创手术非劣效随机对照研究(LACC)时代的术式改良进行探讨。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
经全国继续医学教育委员会批准,本刊开设继教专栏,文后附5道单选题,读者阅读后可扫描标签二维码答题,每篇可免费获得Ⅱ类继教学分0.5分,全年最多可获5分
子宫颈癌是最常见的妇科恶性肿瘤之一,目前发病有年轻化趋势,其治疗是以手术、放疗为主,化疗为辅的综合治疗。广泛子宫切除作为早期子宫颈癌治疗的主要方式,可在取得病理学证据准确分期的同时,保留女性患者卵巢及部分阴道功能,提高患者生存质量。在强调手术切缘距离的肿瘤外科学理念影响下,广泛子宫切除术逐步演进,术中通过建立各个解剖间隙,充分游离周围组织,增加了手术可切除范围。而随着宫旁、阴道旁组织的大范围切除,术后排尿、排便功能障碍等并发症成为手术治疗中改善生存质量的阻碍。随着传统手术解剖学的进一步发展,日本学者率先提出并完善了宫旁组织的选择性切除,在切除宫骶韧带、主韧带的同时,选择性保留盆腔自主神经,实现了达到相同肿瘤结局并改善生存质量的目的。2008年子宫颈癌国际手术分型(Q-M分型)中将保留自主神经功能的广泛子宫切除术(NSRH)归为C1型,2017年Q-M分型将NSRH作为主要术式广泛推行[1, 2]。此外,2003年德国学者Höckel等[3]提出基于腔室解剖理论(ontogenetic compartment theory)的全系膜子宫切除术(TMMR),该术式强调完整切除宫颈肿瘤所在的苗勒管腔室(Müllerian compartment),对周围尿生殖窦腔室(urogenital sinus compartment)及直肠腔室的保护同样可达到保留盆腔自主神经,改善术后膀胱功能的效果。
腔室解剖理论是基于胚胎发育理论建立的解剖学。区别于传统解剖的功能单位(器官),腔室解剖强调在个体发育过程中,即使伴随大量原始细胞增殖与迁移,不同发育来源的腔室间边界在发育过程中持续存在[4]。在成人个体中,这种自然存在的腔室边界可借由其包绕的系膜区分。该理论指出,基于胚胎发育过程中同腔室组织固有的组织学特性,恶性实体瘤在初发的较长一段时间内的生物学行为表现为腔室局限性生长,瘤细胞通过侵袭腔室内组织间质、淋巴系统、静脉系统及神经周围组织扩散。而跨越腔室边界的扩散种植要求瘤细胞在突变中获得足够大的表型差异,通常发生在肿瘤进展晚期[5]。Höckel等[6]发现,宫颈肿瘤的腔室边界效应在高分辨MRI中可见。因此,传统意义上以实体瘤为中心确定手术切缘范围的广泛切除术在病理切缘阴性的情况下亦可能存在同腔室未切除部位的镜下转移,并可以此解释术中完全切净后仍伴术后局灶复发可能及扩大瘤周切缘宽度与降低局灶复发率无明确关联的现象[7]。
全直肠系膜切除(TME)是腔室解剖理论在肿瘤外科中的首次成功实践。1988年英国学者Heald基于直肠解剖腔室概念提出了TME手术范围,较传统直肠癌根治术降低了术后局部复发率、提高了生存率,成为直肠癌治疗的标准术式[8]。随后,德国学者Höckel提出了基于腔室解剖的TMMR及腔室引流的治疗性淋巴切除(tLNE)的结合术式,旨在达到早期宫颈癌的完全切净,避免术后复发高危人群辅助治疗不良反应的二次打击[3]。TMMR手术范围包含子宫、输卵管、阴道近段、血管系膜(vascular mesometria)及纤维脂肪系膜(fibrofatty mesometria),其中血管系膜对应腹侧宫旁组织、子宫血管及其膀胱血管吻合支;纤维脂肪系膜对应宫颈背侧宫骶韧带、直肠子宫/阴道韧带。tLNE切除全部苗勒管腔室引流淋巴结,包含髂血管淋巴结及骶前淋巴结。相较传统的C1型宫颈癌根治术(Q-M分型),TMMR术式强调锐性分离腔室间隙、保留尿生殖窦腔室结构(输尿管板及膀胱血供)及完全切除肛提肌以上的纤维脂肪系膜和回流腔室淋巴组织。Höckel等[6]报道在未接受术后辅助放疗的212例ⅠB~ⅡB期[国际妇产科联盟(FIGO)分期2009]宫颈癌TMMR手术患者中,总生存率可达96%,5年无瘤生存率可达到94%。该术式预后结局理想,但术中深度广泛淋巴清扫对术者解剖储备及手术技巧提出较高要求,纳入研究的各期别患者对TMMR术式获益是否相似仍待进一步研究。
早期宫颈癌广泛子宫切除术淋巴清扫上界至髂总动脉分叉上方,下界至旋髂深静脉,外侧至髂腰肌表面,内侧至输尿管外侧,底至闭孔神经。对于恶性肿瘤盆腔淋巴结清扫,笔者建议遵循“自上而下、由外向内、从浅到深、连续整片切除”原则。术中剥离髂外动脉上方淋巴结时应尽可能保留生殖股神经的完整,分离髂外血管外侧淋巴结时注意避免损伤闭孔神经、闭孔静脉及其下方的髂腰静脉和腰骶干。此外,术中应避免对淋巴结组织过度撕拉,及时使用能量器械凝闭可能开放淋巴管。探查肿大的淋巴结时尽量避免挤压,且在标本离体后及时装入标本袋封存。
1. 暴露宫旁间隙、处理主韧带:主韧带横行于宫颈两侧及骨盆壁之间,其上部为血管部,由血管及疏松结缔组织组成,下部为索状部,盆腔自主神经穿行其中。主韧带上部将宫旁间隙一分为二,腹侧为膀胱侧间隙,前界为侧脐韧带,外界为髂内血管,内侧为膀胱宫颈韧带;主韧带背侧为直肠侧间隙,下界为肛提肌,内界为宫骶韧带;直肠侧间隙又被输尿管分为内侧的Okabayashi直肠侧间隙和外侧的Latzko直肠侧间隙(图1A)。沿髂内动脉内侧钝锐性分离膀胱侧间隙;沿输尿管外侧缘向髂内血管分离疏松的结缔组织,打开Latzko直肠侧间隙。找到子宫动脉、子宫浅静脉及子宫深静脉所在平面,进一步裸化子宫血管。术中需仔细辨识子宫深静脉及汇入的膀胱中下静脉,该静脉丛存在多支多向等解剖变异(图1B),夹凝不全可导致一定量的术中出血,影响术野,引发副损伤。术中可选择Hem-o-lok钳充分夹闭粗壮静脉,以避免双极电凝止血时导致其下方的神经束热损伤。
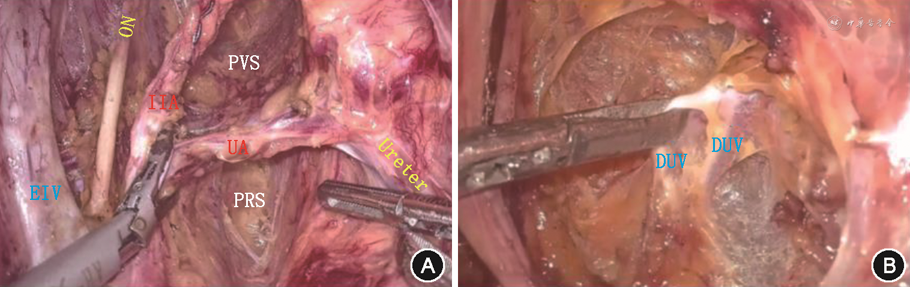

注:PRS为直肠侧间隙;UA为子宫动脉;DUV为子宫深静脉;EIV为髂外静脉;IIA为髂内动脉;Ureter输尿管;ON为闭孔神经;PVS为膀胱侧间隙
2. 游离膀胱、松解输尿管板、处理膀胱宫颈韧带:打开子宫膀胱腹膜反折,从中央向两侧下推膀胱直至膀胱宫颈韧带后叶水平。以“打坎儿井”的方式下推子宫下段两侧稍致密的结缔组织,沿苗勒管腔室及尿生殖窦腔室间白色的无血管区,通过刀头下推探查下方组织后再行切断,采用该方式可有效避免输尿管膝部和膀胱后壁损伤(图2A)[9]。
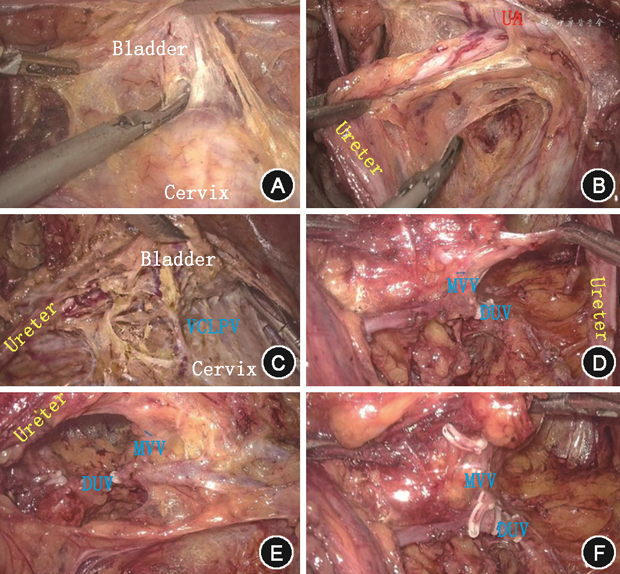

注:Bladder为膀胱Ureter为输尿管;Cervix为宫颈;VCLPV为膀胱宫颈韧带后叶血管;DUV为子宫深静脉;MVV为膀胱中静脉
充分裸化子宫动脉,沿阔韧带后叶疏松处剥离输尿管及其下方系膜(又称输尿管板)(图2B)。上提子宫动脉同时下压输尿管,显露子宫动脉输尿管营养支后离断(2~4支)。上翻子宫动脉断端。分离膀胱宫颈韧带前叶周围结缔组织,离断膀胱宫颈韧带前叶的膀胱上静脉,进一步游离下推输尿管。此过程应精细操作,注意离断输尿管宫颈走向的细小静脉,尽可能寻找疏松的无血管区,避免术中出血影响术野。必要时可尝试腔镜纱条压迫止血或腔镜下缝扎止血,需警惕双极电凝导致的输尿管热损伤。继续向下游离输尿管,凝/夹闭并切断膀胱中静脉和膀胱下静脉以离断膀胱子宫颈韧带后叶,切开膀胱阴道间结缔组织,彻底游离膀胱和双侧输尿管(图2C~F)。
基于腔室解剖理论,尿生殖窦腔室与苗勒管腔室交界由疏松系膜分隔开,在输尿管穿行处形成较为致密的间隙,即为手术解剖学中的“输尿管隧道”。笔者认为,输尿管隧道实为膀胱宫颈韧带前后叶包绕输尿管形成,在保持输尿管张力的情况下可找到膀胱宫颈韧带前叶下方间隙(输尿管隧道入口)。在找到正确系膜间隙平面后,依次离断膀胱宫颈韧带穿行血管,可实现输尿管的“无血”分离。
3. 处理直肠阴道间隙、分离阴道旁组织:分离直肠侧间隙内侧腹膜,离断宫骶韧带,向下打开直肠阴道间隙,游离直肠。沿间隙向两侧游离阴道旁组织。该过程应避免过于贴近阴道组织导致阴道壁静脉丛汹涌出血,同时需注意盆腔内脏神经走行,保留腹下神经及下腹下丛除子宫走向以外的分支。
盆腔自主神经由腹下神经(交感神经)、盆腔内脏神经(副交感神经)及两者交汇后形成的下腹下神经丛(又称盆丛)组成。起自胸12至腰2的交感神经的上腹下神经,于骶岬处汇聚成束形成腹下神经丛,包绕直肠系膜,于宫骶韧带外侧缘沿输尿管下潜行,直至与来自第2~4对骶神经的盆腔内脏神经汇合形成下腹下丛。下腹下丛又分为直肠丛、膀胱丛、输尿管丛及子宫阴道丛,膀胱支中的交感神经和副交感神经分别支配膀胱括约肌和逼尿肌,起到控尿作用。副交感神经的损伤可引起膀胱压力敏感性下降,导致尿潴留;交感神经损伤可使膀胱顺应性降低、膀胱颈关闭功能不全,进而导致尿失禁。
腔镜手术为盆腔自主神经的辨识提供了良好的手术视野,术中正确识别解剖标志和精细解剖为自主神经的保留起到至关重要的作用:(1)在分离输尿管板及游离宫骶韧带时注意保留外侧腹下神经丛;(2)凝断子宫深静脉根部时警惕下方盆腔内脏神经损伤;(3)凝断膀胱子宫颈韧带后叶膀胱中下静脉,进一步推离膀胱及分离阴道旁组织时应避免损伤下腹下丛膀胱支,以达仅切断“十”字交叉内侧子宫支、保留“T”字盆腔自主神经的效果(图3)。对于术中可疑单侧宫旁浸润的情况,保留对侧自主神经亦可达到保护膀胱功能的效果。
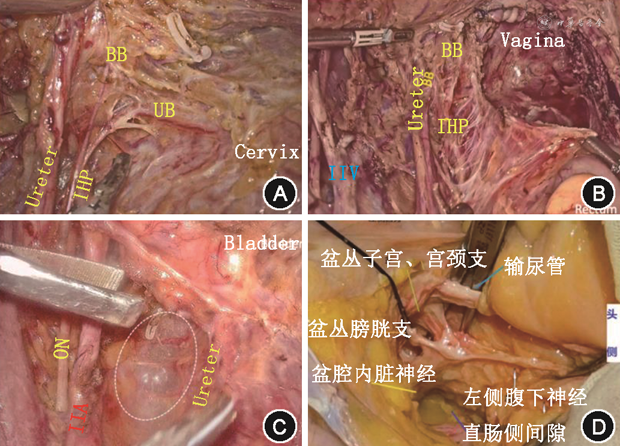

注:Ureter为输尿管;Bladder为膀胱;Cervix为宫颈;Vagina为阴道;Rectum为直肠;IHP为下腹下丛;BB为膀胱支;UB为子宫支;ON为闭孔神经,椭圆来自第2~4对骶神经的盆腔内脏神经;IIA为髂内动脉;IIV为髂内静脉
一项荟萃分析指出,保留盆腔自主神经的腹腔镜术式较传统腹腔镜术式肿瘤预后差异无统计学意义,同时具有术后排尿功能恢复快、住院时间短等优势[10]。另一项系统分析研究指出,保留盆腔自主神经的宫颈癌根治术式虽手术时间较传统术式有所延长,术后的排尿功能、留置导尿管时间、残余尿恢复正常所需时间均优于传统术式,泌尿系并发症(如尿潴留、尿失禁)较传统术式发生更少[11]。值得注意的是,目前对于保留自主神经术式研究以回顾性分析为主,研究多聚焦于围手术期排尿排便并发症的改善,对远期生活质量研究较少。
为避免术中肿瘤播散,肿瘤外科操作需遵循“无瘤”原则。传统的“无瘤”原则要求手术操作在正常组织中进行;术中避免破坏瘤体,污染手术野;防止挤压肿瘤组织,避免播散;强调肿瘤的整块切除。我们在传统开腹广泛子宫切除术中“无瘤”操作主要体现在术中避免宫颈挤压;闭合式离断阴道,应用单把心耳钳封闭阴道上段,双侧直角钳钳夹封闭阴道末端,以避免宫颈肿瘤及阴道残端的术也暴露;术毕使用足量蒸馏水冲洗手术野。
随着腔镜技术的成熟,腹腔镜手术已被应用于NSRH中。多项回顾性研究指出,早期子宫颈癌腔镜手术具有减少术中出血、缩短住院时间、降低术后并发症等优势。然而2018年多中心随机对照研究(LACC研究)结果显示,早期子宫颈癌微创手术患者的复发和死亡风险均高于开腹手术患者(3年总生存率93.8%比99.0%,全因死亡风险比为6.0,95%CI:1.77~20.30)[12]。部分国内外学者对LACC研究的结果提出了异议,亦有多项回顾性分析的结果显示ⅠB1期子宫颈癌(肿瘤直径≤2 cm)患者的腔镜肿瘤结局并不亚于开腹手术[13]。基于各项临床研究结果,目前多数观点认为临床分期为ⅠB1期、肿瘤直径≤2 cm的子宫颈癌在严格无瘤原则下可以实施腹腔镜手术治疗,术者应严格把握腔镜手术的适应证、坚持无瘤原则、保证患者的知情选择权,并进一步完善以中国经验为主的临床研究[14]。
回顾腹腔镜广泛子宫切除术的过程,腹腔镜手术“无瘤”操作不当可能与预后不良相关,如术中举宫杯机械性压力相关性瘤细胞外溢。腔镜手术中长器械远距离操作特点对“无瘤”手术提出了新的要求。因此,我们在腹腔镜术式中采取一系列举措,以沿袭开腹手术中的“无瘤”原则。(1)手术之初电凝双侧输卵管根部,防止子宫腔内容物在术中流入腹腔;(2)术中子宫底悬吊替代举宫器,在提供一定张力的同时避免挤压宫颈病灶(图4A);(3)离断阴道前使用套扎环封闭子宫颈远端,避免宫颈病灶经阴道取出时的体内暴露(图4B);(4)术毕蒸馏水冲洗术野。
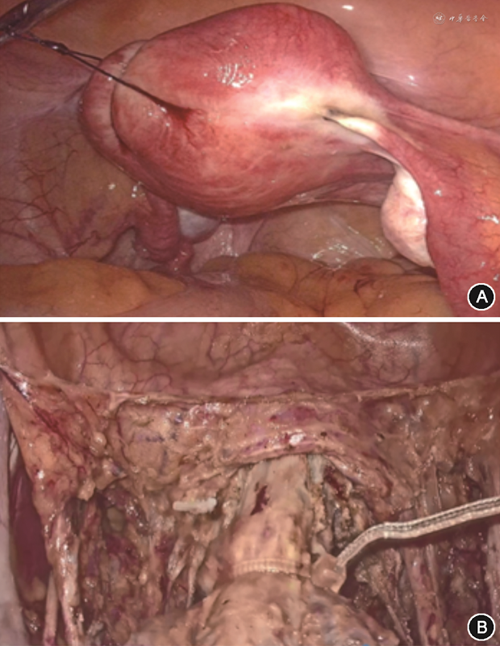

综上所述,对于早期宫颈癌的手术治疗,我们的经验是在保证手术切除范围的同时保留周围重要功能结构,改善生活质量而不降低生存结局。通过术前充分评估患者个体情况,做出最优的术式选择。手术操作融合腔室解剖理念,锐性分离、切除宫颈肿瘤所在苗勒管腔室,保护其他腔室来源组织,利用手术解剖学中各盆腔间隙达到组织的精准分离、切除与保留,减少术中出血及手术副损伤,术中操作遵循“无瘤”原则,在不影响肿瘤预后的前提下改善患者术后排尿排便功能,提高生存质量。
丁雪松, 杨隽钧, 向阳. 基于腔室解剖的宫颈癌广泛子宫切除手术应用[J]. 中华医学杂志, 2023, 103(6): 452-456. DOI: 10.3760/cma.j.cn112137-20220720-01586.
所有作者均声明不存在利益冲突
1、全系膜子宫切除术(TMMR)最先由哪位学者提出()
A. Denis Querleu
B. David Cibula
C. Shingo Fujii
D. Michael Höckel
2、广泛子宫切除术中常见存在解剖变异的结构为()
A.膀胱中静脉
B.子宫动脉
C.输尿管
D.闭孔神经
3、分离髂血管外侧淋巴结时需注意的解剖结构不包括()
A.腹下神经
B.闭孔神经
C.髂腰静脉
D.腰骶干
4、以下不属于C1型广泛子宫切除手术要点的是()
A.分离输尿管板及游离宫骶韧带时注意保留外侧腹下神经丛
B.于输尿管隧道上端切开阴道壁
C.凝断子宫深静脉根部时警惕下方盆腔内脏神经损伤
D.离阴道旁组织时应避免损伤下腹下丛膀胱支
5、列操作中不符合“无瘤”原则的是()
A.手术之初电凝双侧输卵管根部
B.术中子宫底悬吊
C.经TROCAR孔直接取出淋巴组织
D.离断阴道前使用套扎环封闭子宫颈远端
E.术毕蒸馏水冲洗术野



























