儿童支气管哮喘(简称哮喘)是一种常见的慢性呼吸道疾病,严重影响儿童的身心健康。目前我国儿童哮喘的规范化诊治水平有了显著提高,但儿童哮喘的诊断和控制仍面临诸多挑战。本文从流行病学、诊断现状、诊治及管理策略、基础研究、未来展望等几个方面全面综述了中国儿童哮喘的流行状况和诊治现状,并提出了未来发展的策略和目标,旨在加强儿童哮喘的控制并改善预后,并为提高规范化诊治和管理提供参考。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
支气管哮喘(简称哮喘)是儿童最为常见的慢性呼吸道疾病,严重影响儿童的身心健康,给家庭、社会带来巨大的经济负担,消耗了大量的医疗卫生资源。近年来,包括我国在内的世界各国儿童哮喘患病率总体仍呈上升趋势,尤其是年幼儿童。我国经过几代儿科医师的不断努力,儿童哮喘的规范化诊治水平虽有了显著提高,但儿童哮喘的诊断率和控制率尚不理想,仍面临诸多挑战。此外,我国医院-社会-家庭医师-互联网-患儿家长的体系有待进一步完善,以增强针对每个儿童独特需求的个性化治疗方案,使患儿得到全程有效管理。我国整体医疗服务体系起步晚,目前仍然处于一个探索阶段,发展还不成熟,服务尚不够完善。临床实践证明,儿童哮喘的早期干预和规范化管理有利于控制疾病,提高生活质量、改善预后。为提高儿科医师儿童哮喘诊断和规范化管理水平,增强疾病早期管理意识,本文总结了近年来我国儿童哮喘规范化诊治和管理现状,提出规范化诊治及管理的策略以及未来发展的目标,旨在提高我国儿童哮喘的临床规范化诊治和管理水平,为制定儿童哮喘规范化诊治和管理的未来发展规划和卫生政策等提供参考。
哮喘是一种以慢性气道炎症和气道高反应性为特征的异质性疾病,以反复发作的喘息、咳嗽、气促、胸闷为主要临床表现,常在夜间和/或凌晨发作或加剧。呼吸道症状的具体表现形式和严重程度具有随时间而变化的特点,并常伴有可变的呼气气流受限[1]。
哮喘定义中的喘息、咳嗽、气促、胸闷等临床表现为儿童期非特异性的呼吸道症状,亦可见于非哮喘性疾病,应注意与之鉴别。儿童典型哮喘的呼吸道症状具有以下特征[1]:(1)诱因多样性:常有上呼吸道感染、变应原暴露、剧烈运动、大笑、哭闹、气候变化等诱因;(2)反复发作性:当遇到诱因时突然发作或呈发作性加重;(3)时间节律性:常在夜间及凌晨发作或加重;(4)季节性:常在秋冬季节或换季时发作或加重;(5)可逆性:平喘药通常能够缓解症状,哮喘症状也可以自然缓解。根据临床表现是否典型,儿童哮喘可分为典型哮喘和不典型哮喘。
患儿以反复发作的喘息、咳嗽、气促、胸闷为主要表现,多与接触变应原、冷空气、物理或化学性刺激、呼吸道感染及运动等有关,常在夜间或清晨发作。
(1)咳嗽变异性哮喘(cough variant asthma,CVA):CVA是哮喘的一种特殊类型,以咳嗽为唯一或主要的临床表现,无明显喘息、气促等症状,咳嗽持续时间>4周,以干咳为主,常在夜间和/或清晨发作或加重,抗生素治疗无效,抗哮喘药物治疗有效[2]。患儿肺通气功能基本正常,但肺功能气道激发试验检测显示气道高反应性。(2)胸闷变异性哮喘(chest tightness variant asthma,CTVA):临床表现为胸闷持续或反复发作,且以胸闷为唯一或主要临床表现[2]。儿童CTVA起病较为隐匿、无咳嗽、喘息、气促等典型哮喘表现[2,3],肺功能气道激发试验检测显示存在气道高反应性,抗哮喘药物治疗有效。
为了解我国0~14岁儿童哮喘的患病率、发病规律及诊治情况,全国儿童哮喘协作组分别在1990年、2000年和2010年进行了3次城市大规模的抽样调查:第1次调查了全国27个省市952 240名儿童[4];第2次调查了31个省43个城市437 837名儿童[5];第3次调查了全国27个省市或自治区,4个直辖市,43个城市共463 982名儿童[6]。以下为这3次全国城市儿童哮喘流行病学调查结果概况总结。
1990年、2000年和2010年3次城市儿童哮喘流行病学调查显示,累积患病率分别为1.00%[4]、1.97%[5]、3.02%[6],呈现明显增长趋势。
(1)不同地区儿童哮喘患病率存在地域差异。第3次全国流行病学调查显示,华东地区患病率最高(4.23%),现患率亦最高(3.24%);东北地区的患病率和现患率均最低(2.00%、1.40%)[6]。总体来说东北地区和西北地区患病率偏低,南方儿童患病率高于北方。不同地区的患病率见表1。
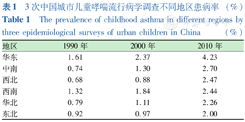
3次中国城市儿童哮喘流行病学调查不同地区患病率 (%)
The prevalence of childhood asthma in different regions by three epidemiological surveys of urban children in China (%)
3次中国城市儿童哮喘流行病学调查不同地区患病率 (%)
The prevalence of childhood asthma in different regions by three epidemiological surveys of urban children in China (%)
| 地区 | 1990年 | 2000年 | 2010年 |
|---|---|---|---|
| 华东 | 1.61 | 2.37 | 4.23 |
| 中南 | 0.74 | 1.30 | 2.70 |
| 西北 | 0.68 | 0.88 | 2.47 |
| 西南 | 1.32 | 1.84 | 2.44 |
| 华北 | 0.79 | 1.11 | 2.26 |
| 东北 | 0.92 | 0.97 | 2.00 |
(2)不同省市儿童哮喘患病率不同。第3次全国流行病学调查显示,上海患病率最高(7.57%),现患率亦最高(5.73%);拉萨最低(0.48%),现患率为0.42%。大多省市呈现上升趋势[6]。3次中国城市儿童哮喘流行病学调查不同省市的患病率见表2。
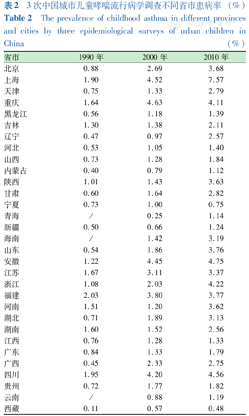
3次中国城市儿童哮喘流行病学调查不同省市患病率 (%)
The prevalence of childhood asthma in different provinces and cities by three epidemiological surveys of urban children in China (%)
3次中国城市儿童哮喘流行病学调查不同省市患病率 (%)
The prevalence of childhood asthma in different provinces and cities by three epidemiological surveys of urban children in China (%)
| 省市 | 1990年 | 2000年 | 2010年 |
|---|---|---|---|
| 北京 | 0.88 | 2.69 | 3.68 |
| 上海 | 1.90 | 4.52 | 7.57 |
| 天津 | 0.75 | 1.33 | 2.79 |
| 重庆 | 1.64 | 4.63 | 4.11 |
| 黑龙江 | 0.56 | 1.18 | 1.39 |
| 吉林 | 1.30 | 1.38 | 2.11 |
| 辽宁 | 0.47 | 0.97 | 2.57 |
| 河北 | 0.53 | 1.05 | 1.40 |
| 山西 | 0.73 | 1.28 | 1.84 |
| 内蒙古 | 0.40 | 0.79 | 1.12 |
| 陕西 | 1.01 | 1.43 | 3.63 |
| 甘肃 | 0.60 | 1.64 | 2.82 |
| 宁夏 | 0.73 | 1.00 | 0.75 |
| 青海 | / | 0.25 | 1.14 |
| 新疆 | 0.50 | 0.66 | 1.24 |
| 海南 | / | 1.42 | 3.19 |
| 山东 | 0.54 | 1.86 | 3.76 |
| 安徽 | 1.22 | 4.45 | 4.75 |
| 江苏 | 1.67 | 3.11 | 3.37 |
| 浙江 | 1.08 | 2.03 | 4.22 |
| 福建 | 2.03 | 3.80 | 3.77 |
| 河南 | 1.51 | 1.20 | 3.62 |
| 湖北 | 0.71 | 1.89 | 3.13 |
| 湖南 | 1.60 | 1.52 | 2.56 |
| 江西 | 0.76 | 1.28 | 1.33 |
| 广东 | 0.84 | 1.33 | 1.79 |
| 广西 | 0.45 | 2.33 | 2.75 |
| 四川 | 1.95 | 4.20 | 4.56 |
| 贵州 | 0.72 | 1.77 | 1.82 |
| 云南 | / | 0.88 | 1.19 |
| 西藏 | 0.11 | 0.57 | 0.48 |
(3)城市儿童患病率高于农村。3次全国流行病学调查所调查的主要人群为城市儿童,针对农村地区儿童哮喘患病率的研究仍相对不足。一项针对农村地区儿童哮喘患病率的荟萃分析显示[7],1990年至2015年我国农村儿童哮喘的总体患病率为2.02%,低于城市(3.02%)[6]。不同地区也存在差异,患病率从高到低依次为华南(3.15%)、华东(2.31%)、西南(2.15%)、华北(1.19%)、华中(1.12%)[7]。
(1)第3次全国儿童哮喘流行病学调查显示,3~9岁年龄段儿童哮喘患病率超过3.0%[5,6],见表3。
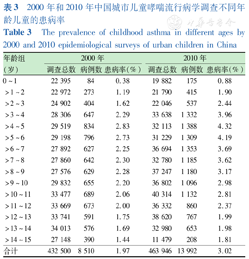
2000年和2010年中国城市儿童哮喘流行病学调查不同年龄儿童的患病率
The prevalence of childhood asthma in different ages by 2000 and 2010 epidemiological surveys of urban children in China
2000年和2010年中国城市儿童哮喘流行病学调查不同年龄儿童的患病率
The prevalence of childhood asthma in different ages by 2000 and 2010 epidemiological surveys of urban children in China
| 年龄组(岁) | 2000年 | 2010年 | ||||
|---|---|---|---|---|---|---|
| 调查总数 | 病例数 | 患病率(%) | 调查总数 | 病例数 | 患病率(%) | |
| 0~1 | 22 395 | 84 | 0.38 | 19 882 | 175 | 0.88 |
| >1~2 | 22 972 | 273 | 1.19 | 21 790 | 415 | 1.90 |
| >2~3 | 24 902 | 404 | 1.62 | 22 046 | 537 | 2.44 |
| >3~4 | 28 306 | 647 | 2.29 | 33 638 | 1 332 | 3.96 |
| >4~5 | 29 519 | 834 | 2.83 | 32 113 | 1 388 | 4.32 |
| >5~6 | 29 198 | 796 | 2.73 | 31 229 | 1 309 | 4.19 |
| >6~7 | 27 892 | 627 | 2.25 | 36 694 | 1 353 | 3.69 |
| >7~8 | 27 860 | 642 | 2.30 | 32 780 | 1 185 | 3.62 |
| >8~9 | 27 576 | 629 | 2.28 | 37 247 | 1 180 | 3.17 |
| >9~10 | 29 832 | 655 | 2.20 | 36 802 | 1 096 | 2.98 |
| >10~11 | 33 477 | 689 | 2.06 | 40 314 | 1 132 | 2.81 |
| >11~12 | 33 669 | 673 | 2.00 | 36 332 | 860 | 2.37 |
| >12~13 | 33 741 | 591 | 1.75 | 38 620 | 767 | 1.99 |
| >13~14 | 34 013 | 576 | 1.69 | 32 980 | 653 | 1.98 |
| >14~15 | 27 148 | 390 | 1.44 | 11 479 | 208 | 1.81 |
| 合计 | 432 500 | 8 510 | 1.97 | 463 946 | 13 992 | 3.02 |
(2)3~6岁是儿童哮喘的高发年龄段。2000年儿童哮喘患病率最高年龄组为3~6岁,其现患率为2.43%,高于3岁以下年龄组(1.11%)及6岁以上年龄组(1.43%);2010年调查结果显示,3~6岁仍是儿童哮喘患病率最高的年龄组,其现患率上升至3.49%,仍显著高于3岁以下年龄组(1.55%)及6岁以上年龄组(1.67%)(P<0.01)。2010年与2000年相比,婴幼儿期的患病率较前下降,而学龄前期和学龄期患病率呈现上升趋势[8],见表4。
2000年和2010年中国城市儿童哮喘流行病学调查不同年龄段患病率
The prevalence of childhood asthma in different age groups by 2000 and 2010 epidemiological surveys of urban children in China
2000年和2010年中国城市儿童哮喘流行病学调查不同年龄段患病率
The prevalence of childhood asthma in different age groups by 2000 and 2010 epidemiological surveys of urban children in China
| 年龄组(岁) | 2000年 | 2010年 | ||||
|---|---|---|---|---|---|---|
| 调查人数 | 现患人数 | 患病率(%) | 调查人数 | 现患人数 | 患病率(%) | |
| <3 | 54 767 | 609 | 1.11 | 48 653 | 754 | 1.55 |
| 3~6 | 69 490 | 1 692 | 2.43 | 73 931 | 2 577 | 3.49 |
| >6 | 210 728 | 3 014 | 1.43 | 227 732 | 3 797 | 1.67 |
2010年第3次全国儿童哮喘流行病学调查结果显示,儿童CVA患病率为0.29%[6]。北京地区儿童CVA患病率调查结果表明,北京城区和农村分别为0.34%和0.42%,二者比较差异无统计学意义[10]。另一项调研显示,我国儿科医师对CVA的知晓率为98.92%[11]。
目前有关儿童CTVA的研究仍较少,仅有数篇研究报道以胸闷为主诉的不典型哮喘患儿的临床及肺功能特点[12,13,14,15,16],关于我国儿童CTVA患病率仍不明确。调研显示,我国儿科医师对CTVA的知晓率为77.83%,三级医院儿科医师对CTVA的知晓率高于二级医院(81.86%比66.41%)[11]。
距上一次全国大规模的流行病学调研已经过去了13年,我国城市化进程、生活习惯、室外与家居环境以及儿童营养状况都发生了很大变化,会影响到儿童哮喘的患病率。经过医护人员多年的努力,我国儿童哮喘的患病率和诊治情况也均有所变化,但均缺乏相关的调研数据。建议定期开展全国大规模的调研,以明确目前我国儿童哮喘的患病情况。
儿童哮喘严重性发作可导致死亡,世界卫生组织(World Health Organization,WHO)公布5~14岁儿童哮喘死亡率为0~0.7/10万[17]。我国2008年至2018年0~19岁人群哮喘死亡率及变化趋势如下[18]:(1)哮喘死亡率为0.023/10万~0.046/10万,估算全国共有1 158名患儿因哮喘死亡。2009年和2012年哮喘死亡率最高(0.046/10万),2018年最低(0.023/10万),与2008年相比,2018年的死亡率降低了42.5%。(2)我国哮喘死亡率总体呈下降趋势,与全球变化趋势一致。与其他国家相比,我国儿童哮喘死亡率较低。2008年至2017年美国0~17岁人群哮喘死亡率为0.244/10万~0.297/10万,其中2017年为0.25/10万,约为中国死亡率的10倍。(3)女性死亡率整体低于男性,且下降幅度高于男性[18],见图1。


2008年至2018年中国城市与农村0~19岁人群哮喘死亡率现状:(1)城市人群哮喘死亡率整体高于农村,仅在2008年、2013年、2018年低于农村;(2)城市和农村儿童哮喘死亡率均呈下降趋势,与2008年相比,2018年城市哮喘死亡率降低了37.14%,农村降低了42.86%[18],见图2。


2008年至2018年中国不同区域0~19岁人群哮喘死亡率现状:(1)西部地区死亡率整体高于东部和中部;(2)与2008年相比,2018年东部地区死亡率增高了28.57%,中部地区降低了83.93%,西部地区降低了4.08%;(3)按地理区域分组显示,中部地区死亡率呈逐年降低趋势[18],见图3。
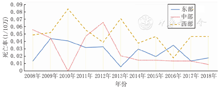

尽管我国儿童哮喘死亡率较低,但由于人口基数大,死亡数仍高于其他国家,2008年至2018年我国0~19岁人群每年的哮喘死亡人数为70~148例[18],而2001年至2016年,英国0~14岁人群每年哮喘死亡人数仅为12~38例[19],1999年至2015年,芬兰仅有4名儿童死于哮喘[20]。
哮喘是由遗传和环境因素共同作用的疾病。哮喘患病有家族聚集倾向,双方父母有一方罹患哮喘,其子女哮喘的发病率较正常儿童高2~5倍。双方父母均罹患哮喘,其子女哮喘的发病率较正常儿童高10倍[21]。母亲孕期的营养、健康状态、生活方式和压力等也可能通过影响胎儿的基因表达而与哮喘发病相关联[22,23]。此外,父母过敏可增加子女发生哮喘的风险,哮喘患儿有家族特应性病史者占32.6%[24]。
特应性也是引起哮喘发病重要的宿主因素。特应性是一种易患变应性疾病的体质或全身状态,称为过敏体质。在0~17岁儿童中,患过敏性疾病使哮喘发病风险的危险增加30%[21],过敏性哮喘是儿童哮喘的主要类型或表型,尤其在学龄儿童,占哮喘的60%~80%[25]。
室内外环境因素是影响儿童哮喘发生和发展的重要因素[26]。生命早期的不良环境因素与儿童期哮喘等过敏性疾病的发生存在关联性[27]。早期生活和长期暴露于空气污染会促进哮喘的发展,如以煤为家庭燃料的家庭,更容易暴露在室内空气污染中,家居霉菌暴露也是哮喘发病的重要危险因素[28]。环境因素中的空气工业污染、秸秆焚烧、汽车尾气、家中养有宠物、被动吸烟、居住环境潮湿、通风不良、家庭霉菌、尘螨环境、花粉环境、取暖方式、食品添加剂等,均可能是诱发儿童哮喘发病的危险因素[29,30,31,32]。欧洲研究揭示,如果大气中PM2.5的水平能够达到WHO制定的标准,每年可以预防66 567例儿童哮喘的发生(占总哮喘患儿的11%)[33]。1993年至2014年美国南加州通过改善大气质量降低了大气中二氧化氮(NO2)和PM2.5的水平,使得儿童哮喘的患病率显著下降[34]。
早年呼吸道感染史也是引发儿童哮喘的主要因素[35]。有研究认为,呼吸道合胞病毒(respiratory syncytial virus,RSV)和鼻病毒(rhinovirus,RV)是儿童哮喘的主要原因[36]。加拿大对5~14岁儿童的调研认为父母哮喘史、早期呼吸道感染史和过敏史不仅可能影响儿童哮喘发病,而且可能与哮喘持续时间有关[37]。荷兰的一项研究发现从出生至4岁前,每年至少发生1次呼吸道感染的患儿,在7~8岁时患哮喘的风险增加近1倍[38]。生命早期气道微生物的组成、细菌-病毒相互作用是儿童哮喘发生的重要因素,预防早期呼吸道感染的干预措施可能有助于帮助预防儿童哮喘。
食物过敏或吸入变应原均与哮喘加重相关。花粉季节的雷暴天气可引起严重的哮喘发作,因为强烈的电离作用可以使空气中可吸入的微颗粒、花粉、霉菌、孢子等大量增加[39]。链格孢属、枝孢属及烟曲霉菌等霉菌也与严重的哮喘急性发作有关,与其他变应原比较,霉菌具有主动出芽的能力,可感染宿主的皮肤,并定植在呼吸道[40]。
环境不但与儿童哮喘的发生密切相关,也可影响儿童哮喘的控制[41]。儿童哮喘的急性发作与大气中的污染物密切相关,短期接触空气污染物[PM2.5、NO2、二氧化硫(SO2)和臭氧(O3)]与儿童哮喘每日急诊就诊呈正相关[42]。对于哮喘个体而言,室内环境的干预更具有重要性和可操作性,最近多项国际哮喘防治指南都强调改善室内环境,包括降低室内变应原和有害物质水平对儿童哮喘控制的重要性[43]。国内有研究应用普通室内空气净化器对哮喘儿童的家庭进行了空气净化,通过降低室内PM2.5水平,减轻气道炎症,改善了哮喘儿童小气道功能[44,45]。
呼吸道感染是导致儿童哮喘加重或急性发作的主要因素。呼吸道病毒(尤其是RV)能与其他致病因素共同作用导致儿童哮喘的加重,呼吸道其他病毒以及不典型病原,如肺炎支原体、衣原体等感染也可导致儿童哮喘急性发作[46]。
ICS吸入量不足包括用药依从性差,ICS处方剂量不足及吸入技术不正确。瑞典的研究显示,1994年至2003年10年间,共有12例哮喘死亡儿童,其中6例存在治疗不足,包括用药依从性差(3/6例)和治疗方案处方剂量不足(3/6例)[47]。哮喘儿童ICS控制治疗中由于剂量不足,降低了哮喘控制水平,导致儿童哮喘急性发作[46]。
哮喘儿童药物控制治疗依从性对疗效至关重要,依从性差是控制不良的危险因素[48]。由于过度担心长期用药可能出现的不良反应,不少家长与患儿常在病情略有改善时,就自行减少药物剂量,甚至擅自停药,导致哮喘症状反复。
心理/精神状态与哮喘的症状反复关系密切。哮喘儿童家长和/或患儿过度焦虑、紧张、唠叨、烦恼等不良心理/精神状态,将直接影响儿童哮喘的治疗和康复,使疾病难以控制[49]。
儿童哮喘死亡多与哮喘控制不良及急性发作的识别和/或处理不当相关[46]。全球哮喘防治创议(GINA)2022指出,哮喘相关死亡的危险因素包括:既往有需要插管和机械通气的哮喘史、近一年内有哮喘住院史或急诊就诊史、正在使用或近期刚停用口服糖皮质激素、目前未使用ICS、过度使用短效β2受体激动剂(short-acting β2 agonist,SABA)、既往有精神病史或心理社会问题史、对哮喘药物治疗和哮喘行动计划(asthma action plan,AAP)的依从性差、哮喘患儿有食物过敏等[50,51]。与儿童哮喘死亡相关的确切危险因素还需要更多的个案分析和进一步研究,目前我国已启动相关的研究和工作。
哮喘控制不良明显增加了哮喘发作的可能性,与哮喘死亡密切相关。
研究发现,SABA可增加气道高反应性,并诱导气道对其产生耐受,过度使用SABA是哮喘相关死亡的独立危险因素,过度使用SABA会增加嗜酸性细胞,并提高气道反应性,可能会诱发危及生命的急性发作[51]。儿童和青少年哮喘每年应用SABA超过3支(600喷)会显著增加住院风险[52]。研究发现,过度使用经定量气雾剂(MDI)吸入SABA,特别是沙丁胺醇用量超过1支/月(100 μg/喷,200喷)是哮喘相关死亡的独立危险因素[51]。20世纪80年代中期,哮喘死亡人数增加38%,与非诺特罗的单独应用有关[53]。目前,GINA不再推荐单用SABA治疗成人及青少年哮喘。
食物过敏或吸入变应原均与哮喘死亡相关。大多数重症哮喘患儿为过敏性哮喘[54],95%的重症哮喘患儿有变应原致敏[55]。澳大利亚分析2004年至2013年死亡的20例哮喘患儿,发现其中90%的患儿具有过敏性体质、1/3有食物过敏史、3例有全身严重过敏反应史[48]。严重过敏反应是引起哮喘死亡的重要危险因素[56]。严重过敏反应的终身患病率为0.05%~2.00%[57],约1/4的严重过敏反应发生在<18岁的儿童和青少年[58],国内一项回顾性研究显示,我国严重过敏反应的患者中21.6%为18岁以下儿童[59]。儿童严重过敏反应的发病率为1/10万人年~761/10万人年[60],且近年来发病率呈上升趋势[61],尤其是低龄儿童。研究发现,70%的严重过敏反应发生在呼吸系统,支气管阻塞是危及生命的首要原因,特别是对于哮喘者更易出现[62,63]。
儿童哮喘不仅严重影响儿童的身心健康,还给家庭和社会带来沉重的经济负担。2015年我国哮喘儿童人均直接医疗费用约为525元人民币(75美元),占我国当年人均GDP的1.06%[68]。2013年对2 960名哮喘儿童的问卷调查显示,治疗年花费在2 000元及以下的患儿占54.6%,2 000~3 500元的患儿占14.6%,3 500~5 000元的患儿占12.7%,5 000~8 000元的患儿占7.5%,8 000~10 000元的患儿占4.5%,超过10 000元的患儿占5.8%。63.3%哮喘未得到控制的患儿年总花费在2 000元以上,而哮喘控制良好的患儿中仅有10.48%年总花费在2 000元以上。36.8%的家长因为儿童哮喘发作而缺勤,38.3%的患儿缺课[69]。
2010年我国14岁以下儿童因哮喘缺课天数较2000年显著减少,缺课<10 d/年的患儿比例显著增加,每年缺课超过10 d以及长期缺课(30 d以上)患儿比例均显著下降,因病留级或停学者较少(表5)。2010年曾因喘息发作而住院治疗的患儿占比为47.3%,较10年前明显下降。虽然我国儿童哮喘防治工作取得了可喜的成绩,但出现急性发作和需要住院治疗的患儿仍占较大比例,因此,降低急性发作和住院率仍是今后工作的重点[70]。

经过几十年的不懈努力,我国儿童哮喘规范化诊治水平有了显著提高,但仍然面临很多困难[70]。中华医学会儿科学分会呼吸学组1987年正式成立了"儿童哮喘协作组"。儿童哮喘协助组牵头制定、修订儿童哮喘诊治指南已经历时30余年,在《中华儿科杂志》上发表的儿童疾病诊治指南中,是历时最长、更新频率和被引频次较高的指南之一。
1988年,首次在《中华儿科杂志》发表了我国儿童哮喘的诊断及分型标准。该标准的制定也为随后在全国范围内开展的儿童哮喘流行病学调查打下了坚实的基础[71]。
1992年,儿童哮喘协作组对儿童哮喘诊断标准进行了较大幅度的修订。提出儿童哮喘早诊、早治、早防的诊治原则,强调了哮喘的炎症本质,在治疗中明确提出"吸入治疗在任何时候都是最好方法"的观点,对在我国儿科领域推广吸入治疗起到了关键性作用。
1998年,儿童哮喘协作组对儿童哮喘诊治常规又进行了一次修订。明确了哮喘病情分期和严重度的判断标准,并根据不同年龄组,分别列出了详细的长期控制方案和急性哮喘的处理方案。并以附件形式对常用哮喘药物进行了详细介绍,有利于哮喘规范用药的临床推广。
2003年,完成了新版《儿童支气管哮喘防治常规(试行)》。针对当时儿童哮喘急性发作治疗中存在的问题,将"哮喘危重状态的诊断和治疗"单独成文刊出,对儿童重症哮喘发作诊治水平的提高起到了重要促进作用[72,73]。
2008年,完成《儿童支气管哮喘诊断与防治指南(2008年修订)》。参照国内外发表的哮喘防治指南和循证医学证据,结合我国儿科临床实践的特点,在儿童哮喘的诊断和分型、临床评估、监测及治疗策略等方面进行重点修改[74]。
2016年,完成《儿童支气管哮喘诊断与防治指南(2016年版)》的再次修订。有别于多数国际指南中倡导的闭环管理模式,该版指南根据儿童生长发育的特点和我国儿童哮喘的诊治实践,首次提出了"开放式"儿童哮喘管理流程,该模式已逐渐被学界所接受,指南的英文版也已在国际专业期刊发表,引起了高度关注与肯定[1,75]。
2020年,完成了《儿童支气管哮喘规范化诊治建议(2020版)》。参照近年来国内外最新发表的指南及共识,纳入近期循证医学证据,对儿童哮喘规范化诊治提出了建设性意见,增加了难治性和重症哮喘的诊治流程,细化了哮喘分级治疗方案的选择和降级治疗的具体路径[76]。除此之外,我国许多专家,如陈育智教授等,也作为专家组成员参与GINA的编写和修订工作,积极参与各种国际交流。
虽然我国儿童哮喘的诊治已取得较大进展,但仍存在诊断不足和诊断过度的现象。2010年第3次全国城市儿童哮喘流行病学调查显示,诊断为哮喘的患儿,其既往诊断正确的符合率为70.7%,较2000年有显著改善,但仍有14.2%的患儿曾疑诊哮喘,11.8%的患儿误诊为下呼吸道感染,3.3%的患儿未获诊断。在确定为典型哮喘的患儿中,69.9%的患儿既往已正确诊断,确定为CVA的患儿仅56.8%既往已正确诊断,21.0%的患儿被诊断为支气管炎。诊断不足是我国儿童哮喘诊治管理中存在的一个重要问题[6]。为此,在2020年发表的儿童哮喘规范化诊治建议中,进一步强调了抗哮喘药物治疗效应评估在儿童哮喘诊断中的重要性,列出了儿童哮喘临床实践诊断流程图,提出了对于严重和反复喘息的高危儿童可以采用1~2个月的尝试性抗哮喘治疗和评估策略,以提高儿童哮喘的诊断率[76]。
存在儿童哮喘诊断不足的同时,也存在诊断过度的问题。对于喘息的患儿,未进行详细的诊断评估与鉴别诊断,即诊断为哮喘并按哮喘进行长期治疗,类似情况在临床中并不少见。
导致儿童哮喘诊断不足和诊断过度的原因主要包括以下几个方面:(1)目前对于儿童哮喘的定义在理解与认知上存在一定的差异,临床医师关于儿童哮喘的规范化诊治水平参差不齐;(2)儿童哮喘的诊断主要依赖于临床症状,对于<6岁儿童,尤其是婴幼儿缺乏可靠的、可量化的客观诊断指标,其诊断与鉴别诊断困难;(3)儿童喘息原因众多,非哮喘儿童也可以出现反复喘息症状;(4)临床常应用的儿童哮喘预测模型对喘息儿童发生哮喘的阳性概率预测价值不高;(5)对儿童肺功能检查重视不足。针对目前<6岁儿童哮喘诊断存在的诸多问题,中华医学会儿科学分会呼吸学组哮喘协作组已经启动了该年龄段哮喘诊断标准建立的研究。提出了6岁以下儿童哮喘诊断评分系统,并进行了初步探索[17,77,78],以喘息发作频率和可逆性气流受限为主要指标[79,80]。但尚需通过多中心、大样本量的前瞻性研究,对该诊断评分系统进一步验证和优化。只要能掌握"喘息发作的反复性、呼气气流受限的可逆性"哮喘诊断的正确性就会明显提高。
难治性哮喘是指采用包括吸入中高剂量糖皮质激素和长效β2受体激动剂(long-acting β2 agonist,LABA)2种或更多种的控制药物规范治疗至少3~6个月仍不能达到良好控制的哮喘[1]。重症哮喘是指虽然使用了最佳治疗方案,并关注到排除难以控制的相关因素,但是哮喘仍不能得到控制,或者高剂量药物治疗降级后哮喘症状加重[81,82]。虽然儿童重症哮喘占哮喘患者总数的比例不足5%,但其医疗费用却占哮喘总医疗费用的30%以上,社会负担更重[82,83,84],应引起临床医师的重视。因重症哮喘而转诊的患儿中,高达30%诊断有误[85],这说明对于重症哮喘和难治性哮喘仍存在认识不足的情况。因此,哮喘患儿经过适当的控制治疗后,症状未能达到良好控制时,临床医师应该重新审视哮喘的诊断。
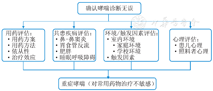
为此,我国儿童哮喘防治指南明确指出,在临床实践中要注意识别导致儿童哮喘难以控制的不利因素,通过治疗调整,再评估临床治疗效应。环境评估具有十分重要的意义,与成人不同,95%的儿童重症哮喘患者由变应原致敏[83]。相对于成人,儿童在室内留置的时间更长,因此更需重视对患儿家庭环境的评估。此外,学龄期儿童每天在学校的时间可高达8 h之久,学校环境变应原的评估同样十分重要[86]。
目前我国儿童哮喘的诊治在诊断准确性、治疗规范性、严重程度的判断等方面仍存在诸多不足。因此,如何进一步提高儿童(特别是<6岁儿童)哮喘的诊断、治疗管理水平,应成为广大医师及卫生管理人员关注的重点,也需加强多层次继续教育及卫生宣教,以提高整个社会对儿童哮喘的正确认识。
随着GINA方案在我国的推广以及我国儿童哮喘诊断和防治指南的实施,儿科临床医师对儿童哮喘的诊治和管理水平有了较大提高,但儿童哮喘控制的整体情况仍不容乐观。第3次中国城市儿童哮喘流行病学调查显示,过去1年内61.4%的患儿仍有喘息发作,因喘息导致急诊就诊或住院治疗的患儿比例分别为32.1%和16.3%,22.8%的患儿曾有过重度哮喘发作[65]。国内29个城市哮喘儿童家长知信行调查结果显示,66%的哮喘患儿在近12个月有过哮喘发作,26.8%的患儿有过因哮喘发作的急诊治疗,16.2%的患儿有过因哮喘发作导致的住院治疗[69]。20%的哮喘儿童未得到控制,依从性不佳(44%)是哮喘未控制的最主要原因[87]。北京5岁以上哮喘患儿的控制率仅为65.7%[88]。2020年西安的一项研究显示,良好控制的患儿比例仅为26.07%[89]。
儿童哮喘的治疗要坚持长期、持续、规范、个体化的治疗原则。目前在我国儿童哮喘的管理中,存在着治疗不足和治疗过度并存的现象[76]。全国儿科哮喘门诊调研显示,有近20%的城市儿童哮喘尚未达到良好控制,然而却有近1/4的患儿同时接受了3种以上的联合控制治疗药物,远高于实际临床中儿童重症哮喘患者的占比,究其原因,主要与控制药物的治疗不足和/或不规范有关[87,90]。儿童哮喘治疗不足与治疗过度都应该引起临床医师的足够重视。为此,2016版中国儿童哮喘指南中推出了儿童哮喘治疗的流程图,该流程图强调了哮喘管理中持续进行病情评估,规范化治疗方案制定、调整和治疗效应评估的重要性,早于GINA及其他国际哮喘诊治指南提出的强化干预和预干预或间歇治疗等概念。
比较第2次和第3次城市儿童哮喘流行病学调查结果,10年间我国儿童哮喘规范化治疗的程度已有明显提高,ICS的使用率上升了0.7倍(达到61.7%),尽管还有约1/3的儿童哮喘患者并未使用ICS,仍表明临床医师对于儿童哮喘的管理水平有了明显提高[6]。ICS作为哮喘长期控制治疗的首选药物,不良反应总体发生率低,安全性好,需要长期、规范使用以达到儿童哮喘的良好控制。
临床对于ICS与LABA联合治疗具有协同抗炎和平喘的作用,改善哮喘症状和肺功能、降低急性发作风险,应用布地奈德/福莫特罗作为6岁及以上儿童的哮喘维持和缓解用药的认识有所提高[91]。对于如不具备吸入条件或吸入不配合的轻中度喘息患儿,特别是夜间喘息患儿,可考虑临时应用口服β受体激动剂,如班布特罗等[92]。
白三烯受体拮抗剂(leukotriene receptor antagonist,LTRA)作为儿童哮喘控制治疗的备选药物,单药治疗方案适用于轻度儿童哮喘的控制治疗。第3次城市儿童哮喘流行病学调查结果显示,34.8%的患儿使用了LTRA,说明LTRA在儿童哮喘控制治疗中具有一定的地位[6]。
以抗IgE单克隆抗体(奥马珠单抗)为代表的生物制剂、长效抗胆碱能药物,如噻托溴铵等已逐渐作为儿童重症哮喘附加药物用于临床。国内目前奥马珠单抗用于6岁及以上哮喘儿童有其适应证[25]。
规范的哮喘控制治疗是预防哮喘发作的重要环节。对哮喘患儿病情进行全面评估,给予适当的控制治疗,并定期进行随访评估非常重要。而药物治疗同时需强调环境的控制,避免接触变应原,积极治疗共患疾病[1,48]。
AAP是指导哮喘患儿自我管理的重要工具,对于哮喘的控制治疗、急性发作的及时治疗、及预防哮喘所致的死亡非常重要。对患儿及家长进行哮喘自我管理的教育,促进医师为患儿提供AAP,并指导患儿使用AAP,是哮喘专科医务人员必不可少的工作。
对于难治性哮喘或重度持续性哮喘应及时转诊至专科医院或专科门诊,进一步评估并及时调整治疗。定期随诊,对病情进行评估,调整治疗方案,必要时转诊,也是对哮喘患者和基层医师进行教育的内容之一。
哮喘的教育包括对疾病的认识、哮喘药物和吸入技术的了解、预防哮喘症状、处理哮喘急性发作、哮喘的自我监测和控制、定期复诊、使用AAP帮助患儿和/或看护者识别并处理哮喘急性发作。
近10年来我国发表了多篇与儿童哮喘诊治相关的指南或专家共识,提高了儿科医师哮喘诊断和规范化管理水平,增强了疾病早期管理意识。我国儿童哮喘总体规范化诊治和管理水平已有显著提高。近10年来发表的主要全国性的儿童哮喘诊治相关指南或专家共识见表6。
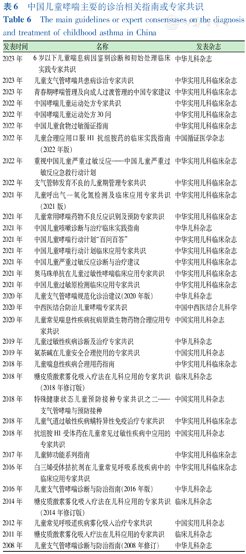
中国儿童哮喘主要的诊治相关指南或专家共识
The main guidelines or expert consensuses on the diagnosis and treatment of childhood asthma in China
中国儿童哮喘主要的诊治相关指南或专家共识
The main guidelines or expert consensuses on the diagnosis and treatment of childhood asthma in China
| 发表时间 | 名称 | 发表杂志 |
|---|---|---|
| 2023年 | 6岁以下儿童喘息病因鉴别诊断和初始处理临床实践专家共识 | 中华儿科杂志 |
| 2023年 | 儿童支气管哮喘共患病诊治专家共识 | 中华实用儿科临床杂志 |
| 2023年 | 青春期哮喘管理及向成人过渡管理的中国专家建议 | 中华实用儿科临床杂志 |
| 2022年 | 中国哮喘儿童运动处方专家共识 | 中华实用儿科临床杂志 |
| 2022年 | 中国哮喘儿童运动处方30问 | 中华实用儿科临床杂志 |
| 2022年 | 中国儿童食物过敏循证指南 | 中华实用儿科临床杂志 |
| 2022年 | 儿童合理应用口服H1抗组胺药的临床实践指南(2022年版) | 中国循证医学杂志 |
| 2022年 | 重视中国儿童严重过敏反应——中国儿童严重过敏反应急救行动计划 | 中华实用儿科临床杂志 |
| 2022年 | 支气管肺发育不良的儿童期管理专家共识 | 中华实用儿科临床杂志 |
| 2021年 | 儿童呼出气一氧化氮检测及临床应用专家共识(2021版) | 中华实用儿科临床杂志 |
| 2021年 | 儿童常用哮喘药物不良反应识别及预防专家共识 | 中华实用儿科临床杂志 |
| 2021年 | 中国儿童咳嗽诊断与治疗临床实践指南 | 中华儿科杂志 |
| 2021年 | 中国儿童哮喘行动计划"百问百答" | 中华实用儿科临床杂志 |
| 2021年 | 中国儿童哮喘行动计划临床应用专家共识 | 中华实用儿科临床杂志 |
| 2021年 | 中国儿童严重过敏反应诊断与治疗建议 | 中华实用儿科临床杂志 |
| 2021年 | 奥马珠单抗在儿童过敏性哮喘临床应用专家共识 | 中华实用儿科临床杂志 |
| 2021年 | 中国儿童过敏原检测临床应用专家共识 | 中华实用儿科临床杂志 |
| 2020年 | 儿童支气管哮喘规范化诊治建议(2020年版) | 中华儿科杂志 |
| 2020年 | 中西医结合防治儿童哮喘专家共识 | 中国中西医结合儿科学 |
| 2020年 | 儿童常见喘息性疾病抗病原微生物药物合理应用专家共识 | 中国实用儿科杂志 |
| 2019年 | 儿童过敏性疾病诊断及治疗专家共识 | 中华儿科杂志 |
| 2019年 | 氨茶碱在儿童安全合理使用的专家共识 | 中国实用儿科杂志 |
| 2018年 | 儿童喘息性疾病合理用药指南 | 中华实用儿科临床杂志 |
| 2018年 | 糖皮质激素雾化吸入疗法在儿科应用的专家共识(2018年修订版) | 临床儿科杂志 |
| 2018年 | 特殊健康状态儿童预防接种专家共识之二——支气管哮喘与预防接种 | 中国实用儿科杂志 |
| 2018年 | 儿童气道过敏性疾病螨特异性免疫治疗专家共识 | 中华实用儿科临床杂志 |
| 2018年 | 抗组胺H1受体药在儿童常见过敏性疾病中应用的专家共识 | 中国实用儿科杂志 |
| 2017年 | 儿童肺功能系列指南 | 中华实用儿科临床杂志 |
| 2016年 | 白三烯受体拮抗剂在儿童常见呼吸系统疾病中的临床应用专家共识 | 中华实用儿科临床杂志 |
| 2016年 | 儿童支气管哮喘诊断与防治指南(2016年版) | 中华儿科杂志 |
| 2014年 | 糖皮质激素雾化吸入疗法在儿科应用的专家共识(2014年修订版) | 临床儿科杂志 |
| 2012年 | 儿童常见呼吸道疾病雾化吸入治疗专家共识 | 中国实用儿科杂志 |
| 2011年 | 糖皮质激素雾化吸入疗法在儿科应用的专家共识 | 临床儿科杂志 |
| 2008年 | 儿童支气管哮喘诊断与防治指南(2008年修订) | 中华儿科杂志 |
儿童哮喘的诊断主要依据呼吸道症状、体征及肺功能检查,证实存在可变的呼气气流受限,并排除可引起喘息相关症状的其他疾病。临床实践中,可根据年龄、性别、既往喘息发作的严重程度和频率、是否存在特应性疾病、特应性疾病家族史、肺功能异常等几个因素进行综合诊断。
反复喘息、咳嗽、气促、胸闷是哮喘的典型症状[93,94,95,96],这些症状多与接触变应原、冷空气、物理、化学性刺激、呼吸道感染、运动以及过度通气(如大笑和哭闹)等有关,常在夜间和/或凌晨发作或加剧。发作时呼气相延长伴双肺可闻及散在性或弥漫性,以呼气相为主的哮鸣音。上述症状和体征经抗哮喘治疗有效,或自行缓解。
肺通气功能检测是诊断哮喘的重要手段,也是评估哮喘病情严重程度和控制水平的重要依据[97]。呼出气一氧化氮等气道炎症指标有助于哮喘诊断。哮喘一旦得到控制时,肺功能可能恢复正常,因此即使肺功能正常也不能排除哮喘[13,98,99,100,101,102,103]。
包括肺部疾病或心血管疾病(如胸部血管畸形、先天性心脏病、气道异常、喉麻痹、支气管软化症、气管软化、不动纤毛综合征等)、感染性疾病(如鼻咽炎、鼻窦炎、支气管炎、肺炎、支气管扩张、肺结核等),和其他肺内外疾病(如过敏性肺炎、支气管异物、心因性咳嗽、声带功能障碍、气道压迫、肺水肿、变应性支气管肺曲霉病、囊性纤维化、结节病、肺栓塞、闭塞性细支气管炎等)。
儿童哮喘的诊断首先判断其是否有反复发作的喘息、咳嗽、呼吸困难,呼气时间延长等哮喘症状。其次询问病史,包括既往喘息发作病史、药物使用、相关检查、个人与家族过敏性疾病史等。最后进行相应的检查,包括肺通气功能测定、支气管激发试验、支气管舒张试验和呼出气一氧化氮等检测。对于肺通气功能测定、支气管舒张试验、呼出气一氧化氮等可能无明显异常的患儿,需进行观察,等儿童出现哮喘症状时,再进行重复测试[97,104,105,106]。儿童哮喘诊断步骤与流程,见图4。
儿童重症哮喘占哮喘患者总数的比例不足5%,但我国重症哮喘儿童的占比仍是一个未知数。有高达55%需要转诊的重症哮喘患儿最后被确定为难治性哮喘,对这部分患儿的评估主要是识别可能导致其哮喘控制不佳的因素,通过调整再评估临床治疗反应。对二者进行鉴别诊断的思路是:首先评估诊断是否有误,与其他具有咳嗽、呼吸困难和喘息等症状的疾病进行鉴别诊断;判断药物治疗是否有效吸入,包括用药的依从性和吸入技术的掌握情况;判断是否存在诱发哮喘加重的危险因素;进行相关检查判断是否存在未控制的并存疾病,如胃食管反流、肥胖、阻塞性睡眠呼吸障碍、变应性鼻咽炎或鼻窦炎、心理焦虑等;除外上述因素后再评估患儿的控制水平和对治疗的反应,确定是否为重症哮喘[83],见图5。值得注意的是,目前对于难治性哮喘和重症哮喘的诊断都是回顾性诊断,首诊不能定义难治性哮喘和重症哮喘。

儿童哮喘治疗目标包括以下方面:达到并维持症状的控制;维持正常活动水平,包括运动能力;维持肺功能水平尽量接近正常;预防哮喘急性发作;避免因哮喘药物治疗导致的不良反应;预防哮喘导致的死亡[97]。
儿童哮喘控制治疗管理方法与流程[1,76]:儿童哮喘长期控制治疗方法仍然以阶梯式降级治疗为基本原则,倡导多向的开放式哮喘管理流程。控制治疗主要策略包括:(1)强调评估的重要性,包括疾病治疗前、治疗中,直至停药以后的再评估,应涵盖疾病的发展全过程;(2)强调儿童哮喘初始强化治疗的理念,使用高强度的药物尽快降低气道炎症程度;(3)强调基于症状控制的哮喘管理模式,避免治疗不足和治疗过度;(4)治疗过程中遵循"评估-治疗-监测-调整"的管理循环;(5)重视药物治疗与非药物治疗相结合,注重非药物治疗在哮喘长期管理中的作用。儿童哮喘治疗管理流程见图6。
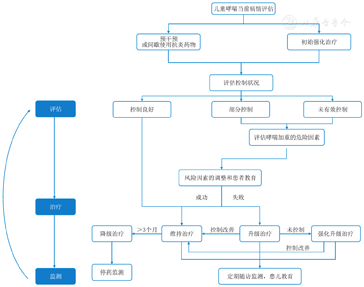

我国儿童哮喘指南根据患儿的临床表现和肺功能,将哮喘分为急性发作期、慢性持续期和临床缓解期,对≥6岁儿童和<6岁儿童分别做了哮喘急性发作的严重度分级;根据喘息的频次、对生活质量的影响及肺功能的严重程度对慢性持续期进行分级,或依据达到哮喘控制所需治疗级别进行回顾性哮喘病情严重程度分级评估[1];对规范化治疗后的儿童哮喘进一步评估哮喘控制情况,确定治疗方案的调整。儿童哮喘一旦确诊,需要根据临床症状判断目前的严重程度,以确定长期治疗方案。通过评估近4周的哮喘症状,确定目前的控制水平。哮喘预后不良的未来危险因素评估包括未来发生急性发作造成的不可逆肺功能损害和药物相关不良反应的风险评估[26,97]。
常用药物有SABA、短效抗胆碱能药物等。SABA是目前最有效、临床应用最广泛的支气管舒张剂,可在出现哮喘症状时按需使用[76]。但过多使用SABA可能掩盖症状的严重度、造成耐药和快速减敏现象,从而增加哮喘严重发作和哮喘死亡的风险。2019年以来GINA不赞成仅使用SABA作为哮喘缓解治疗,建议按需使用SABA的同时应联合低剂量ICS[54]。对于间歇症状6岁以上的哮喘儿童,缓解症状推荐可选用ICS/福莫特罗,这比单独使用SABA能更有效地降低急性发作的风险。GINA推荐ICS/福莫特罗可用于6岁以上儿童中重度哮喘的维持和缓解治疗[51]。
短效抗胆碱能药物与SABA联合使用可更有效控制哮喘症状。大剂量ICS吸入也有助于哮喘症状的缓解,必要时可全身性使用糖皮质激素。氨茶碱不推荐作为儿童哮喘控制的一线用药。长效口服β2受体激动剂,如班布特罗,特别是对于夜间喘息患儿,可以考虑临时口服用药[107]。
(1)ICS:ICS是儿童哮喘长期控制治疗的首选药物。ICS能有效控制哮喘症状、改善肺功能、减轻气道炎症和气道高反应性、减少哮喘发作,在哮喘的长期控制中发挥重要作用[108]。长期、规范的ICS使用不仅降低了哮喘急性加重和哮喘死亡率,也减少了患儿住院治疗的次数。相比于哮喘诊断2~4年后才开始ICS治疗,早期使用低剂量ICS治疗能更有效地改善肺功能[109]。ICS不良反应总体发生率低,安全性好。但ICS的使用对于儿童身高的影响仍然要关注。对于青春前期、学龄期轻中度持续哮喘儿童,虽然ICS治疗的前1~2年可能造成患儿生长速度减慢,但不呈进展性,且无累积效应。有研究表明,持续中剂量数年使用ICS后,哮喘儿童的身高较使用安慰剂者下降了0.7%,但也有研究表明ICS长期维持治疗所致全身不良反应的风险未见升高,即使应用ICS治疗7~11年后,哮喘儿童仍可达到预期的成人身高[108,110,111,112,113]。与严重哮喘带来的风险相比,ICS对身高的影响较小。另外,哮喘控制不良对儿童身高也有不良影响。临床实践过程中需注意尽可能使用低剂量ICS达到哮喘良好控制,并定期监测患儿的生长发育状况。
(2)LABA:LABA药物共同特点是作用维持时间长,具有舒张支气管和协同ICS的抗炎作用,主要包括福莫特罗和沙美特罗,目前主要用于6岁以上儿童中重度哮喘的联合控制治疗,不能单独使用。与沙美特罗相比,福莫特罗属于速效和长效β2受体激动剂,主要特点是起效迅速,作用持续时间长,支气管舒张效应在一定范围内呈剂量依赖性[92]。长效口服β2受体激动剂,如丙卡特罗和班布特罗,能迅速缓解夜间咳嗽、喘息症状[107]。对于不具备吸入条件或吸入不配合的轻中度喘息患儿,特别是夜间喘息患儿,可以考虑β2受体激动剂的临时口服药物[92]。
(3)ICS-LABA复合制剂:联用ICS与LABA具有协同抗炎和平喘作用,可获得相当于(或优于)加倍剂量ICS时的疗效,并可增加患儿的依从性、减少较大剂量ICS的不良反应,尤其适用于中重度哮喘患儿的长期治疗[97]。布地奈德/福莫特罗、丙酸氟替卡松/沙美特罗是代表性药物。研究发现,布地奈德/福莫特罗(80.0/4.5 μg)2吸,2次/d,能显著改善哮喘患儿晨间和晚间呼气峰流量(peak expiratory flow,PEF)[92,114]。吸入ICS/福莫特罗能快速改善肺功能,既可用于哮喘的维持期治疗,也可快速缓解哮喘症状[115]。布地奈德/福莫特罗作为维持和缓解治疗(MART)已引入到6岁以上儿童哮喘的治疗中[116]。青少年哮喘在第1~2级可按需使用布地奈德/福莫特罗,在第3~5级治疗可作为维持和缓解治疗,能更有效地减少哮喘急性发作的风险[51]。
(4)LTRA:LTRA可有效抑制白三烯活性,抑制支气管收缩、减轻气道炎症,是儿童哮喘重要的长期控制药物。LTRA代表药物为孟鲁司特,可用于治疗过敏性喘息、哮喘、变应性鼻炎等变应性疾病。LTRA单药治疗方案适用于轻度儿童哮喘的控制治疗,总体疗效略逊于ICS。LTRA可与ICS联合用于中重度年幼儿童哮喘的治疗[97],可以减少糖皮质激素的剂量,并提高ICS的疗效。孟鲁司特药耐受性好,不良反应少,服用方便,但最近美国食品与药品监督管理局(FDA)已经发出使用孟鲁司特可能出现精神神经事件的警告,临床医师应关注不良事件的风险。
(5)生物制剂:GINA 2022推荐生物制剂可用于儿童重症哮喘[51,76],作为第5级中的优选治疗,但不建议单独使用。生物制剂包括抗IgE单克隆抗体、抗白细胞介素(interleukin,IL)-5/抗IL-5受体单克隆抗体、抗IL-4Rα单克隆抗体和抗胸腺基质淋巴细胞生成素(thymic stromal lymphopoietin,TSLP)单克隆抗体等。①抗IgE单克隆抗体:奥马珠单抗已被批准用于国内6岁及以上儿童重症哮喘的治疗[25]。奥马珠单抗可以在IgE介导的过敏性哮喘合并其他过敏性疾病时使用[25,117]。②抗IL-5/抗IL-5受体单克隆抗体:贝纳利珠单抗可用于过去1年内有哮喘急性发作史且外周血嗜酸性粒细胞> 300/μL的儿童重度嗜酸性粒细胞哮喘的附加治疗。贝纳利珠单抗可以显著缓解12~75岁重度患者(SIROCCO和CALIMA研究)哮喘症状、减少每年急性发作次数、改善支气管舒张剂使用前的第1秒用力呼气容积(FEV1)水平[118,119]。我国正在进行12~75岁重度哮喘患者贝纳利珠单抗的Ⅲ期临床试验。③其他生物制剂:抗IL-4R单克隆抗体和抗TSLP单克隆抗体已有药物面世。对于中重度哮喘患者,如果不能通过基础的治疗达到控制目标,应考虑将生物制剂作为附加治疗选择[120]。长效抗胆碱能药物的抗炎作用使得其也可以作为附加药物使用,研究发现长效抗胆碱能药物作为ICS的附加药物可以改善重症哮喘患儿的肺功能、控制加重风险和症状[121]。
儿童哮喘急性发作需在第一时间内根据患儿年龄、发作严重程度、诊疗条件等予以及时恰当的治疗,以迅速缓解气道阻塞症状。哮喘患儿和/或家长,在出现哮喘发作时,应及时吸入SABA,建议使用压力型定量气雾剂(pMDI)经储雾罐(单剂给药,连用3~6剂,危重者在监护条件下可以增加至10剂)或雾化吸入方法给药。6岁以上儿童可以按需吸入布地奈德/福莫特罗(每天不超过8吸),在给药后5~15 min进行吸入药物效应评估,可在第1小时反复3次。使用SABA时应联合使用ICS,发作严重或SABA治疗效应不佳时可加用短效抗胆碱能药物雾化吸入,大年龄儿童也可直接应用ICS-LABA(布地奈德/福莫特罗)吸入。当初始治疗效果不佳或病情有进行性恶化征象时必须及时就医。如果没有吸入性缓解药物,可以应用任何有利于症状缓解的口服药物,如SABA、氨茶碱、糖皮质激素等,并及时就医。如果无任何缓解药物可用,则建议患儿予以安静端坐,进行心理安抚,并及时就医。
通常应提前给患儿开具缓解哮喘急性加重的药物备用,详细说明药物的疗效、持续时间和使用间隔;对于不经常使用吸入药物的儿童和家庭,还要进行吸入技术的指导。由于儿童每天大部分时间都在学校度过,学校的哮喘管理就变得尤为重要。然而,患儿在学校能紧急获得支气管舒张剂的机会仍然很低,国外一项研究表明,只有14%的儿童在学校能获得快速缓解药物[122,123]。因此需关注现有的学校医务室是否有缓解哮喘急性发作的备药,哮喘儿童是否在书包里备有缓解哮喘急性发作的备药,并建立有效的机制,以确保患有哮喘的学生在学校可以获得能挽救生命的快速缓解药物。
当初始治疗效果不佳或病情有严重恶化的迹象时(表7),患儿应立即就近前往医疗机构就诊。如果出现明显的呼吸困难或意识水平变化(如意识淡漠或躁动),则应马上呼叫救护车[124](图7)。
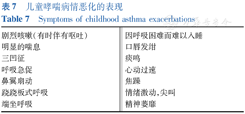
儿童哮喘病情恶化的表现
Symptoms of childhood asthma exacerbations
儿童哮喘病情恶化的表现
Symptoms of childhood asthma exacerbations
| 剧烈咳嗽(有时伴有呕吐) | 因呼吸困难而难以入睡 |
| 明显的喘息 | 口唇发绀 |
| 三凹征 | 痰鸣 |
| 呼吸急促 | 心动过速 |
| 鼻翼扇动 | 焦躁 |
| 跷跷板式呼吸 | 情绪激动,尖叫 |
| 端坐呼吸 | 精神萎靡 |
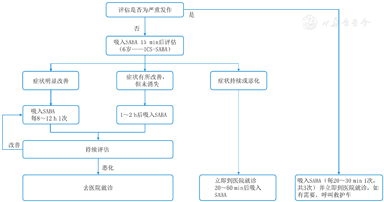

注:SABA:短效β2受体激动剂;ICS:吸入性糖皮质激素;使用SABA时建议联合使用ICS SABA:short-acting β2 agonist;ICS:inhaled corticosteroids;It is recommended to use ICS in conjunction with SABA
(1)临床评估:快速、准确评估哮喘急性发作的严重程度,记录以下症状:①心率:心动过速通常表示哮喘恶化,当哮喘危及生命时也会出现心率下降;②呼吸频率和呼吸困难程度:呼吸困难,讲话无法成句或无法进食提示哮喘恶化;③辅助呼吸肌活动情况及三凹征:通过触诊颈部肌肉来观察;④喘息:随着气道阻塞的增加,喘息可能会变成双相或不太明显;⑤焦虑程度和意识水平。需要注意临床症状与气道阻塞的严重程度并不完全相符,部分急性重症哮喘发作的儿童看起来并不痛苦[125,126]。
(2)辅助检查:①血氧饱和度:支气管舒张剂治疗后非吸氧条件下脉搏血氧饱和度(SpO2)<92%的患儿需要住院治疗;②PEF:支气管舒张剂治疗后可以进行PEF检测,取3次PEF测量值中的最大值可用于评估治疗反应,PEF仍<50%预测值(或个人最佳值)且症状改善不佳的患儿,提示其哮喘发作时间可能会更长;③胸部影像学:不是哮喘的常规检查选项,但如果怀疑气胸、肺炎以及对治疗无反应的危及生命的哮喘,应进行胸部X线检查,情况允许可以胸部CT检查;④血气分析:对中重度哮喘急性发作的患儿尽可能及时进行血气分析,以了解病情的严重程度,并判断预后。在急症患者中,由低碳酸血症向正常碳酸血症的转变往往意味着伴有严重气道梗阻,提示可能需要进行机械通气[127]。
(3)治疗:①氧疗:有低氧血症者,采用鼻导管或面罩吸氧,以维持SpO2>94%。②吸入SABA:可使用pMDI经储雾罐吸药,如没有储雾罐但具备雾化给药条件,可使用雾化吸入。快速起效的ICS-LABA(布地奈德/福莫特罗)也可在≥6岁哮喘儿童作为缓解药物使用。③糖皮质激素:包括静脉、ICS、口服糖皮质激素均是治疗儿童哮喘重度发作的一线药物,早期使用可以减轻疾病的严重度,给药后3~4 h即可显示明显的疗效,所有用SABA患者都建议联合使用ICS,高剂量ICS可能减少或避免全身糖皮质激素的使用。④抗胆碱能药物:短效吸入性抗胆碱能药物是儿童哮喘急性发作联合治疗的组成部分,可以增加支气管舒张效应,其临床安全性和有效性已得到证实,尤其是对于SABA治疗反应不佳的中重度患儿应尽早联合使用。⑤茶碱:由于氨茶碱平喘效应弱于SABA,而且治疗窗窄,应谨慎使用茶碱。⑥机械通气:经合理联合治疗,症状仍持续加重,出现呼吸衰竭征象时,应及时给予辅助机械通气治疗。在应用辅助机械通气治疗前禁用镇静剂。还应注意,哮喘急性发作住院高峰季节为夏末至秋冬季,可能与呼吸道病原体季节分布有关,下呼吸道感染可加重哮喘急性发作期气流受限程度,需要积极联合治疗[128]。
(4)尽快继续或开始维持控制治疗:哮喘急性发作症状缓解即应继续或开始维持控制治疗。
儿童哮喘急性发作期的医院治疗流程见图8。
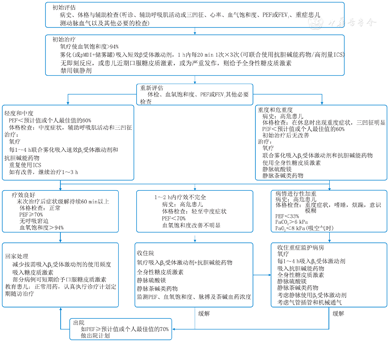

注:PEF:呼气峰流量;FEV1:第1秒用力呼气容积;pMDI:压力型定量气雾剂;ICS:吸入性糖皮质激素;PaCO2:动脉血二氧化碳分压;PaO2:动脉血氧分压 PEF:peak expiratory flow;FEV1:forced expiratory volume in one second;pMDI:pressurized metered-dose inhaler;ICS:inhaled corticosteroids;PaCO2:arterial partial pressure of carbon dioxide;PaO2:arterial partial pressure of carbon dioxide
儿童哮喘急性发作症状得到有效控制后,应充分认识到即使当症状消失或肺功能正常,其气道炎症等特征仍持续存在,应尽量避免急性发作[1,129,130]。在维持控制治疗开始同时制定个体化的控制管理计划,包括:(1)避免诱发急性发作的诱因,并制定回避计划;(2)制定或调整之前的控制治疗方案;(3)实施中国儿童哮喘行动计划(Chinese Children′s Asthma Action Plan,CCAAP);(4)核查吸入技术是否正确;(5)选择维持期药物。
临床根据急性发作症状控制情况、以往病史、治疗等进行"适级"或"强化"控制治疗。6岁以下儿童控制治疗首选ICS,6岁以上推荐使用ICS-LABA。患儿如果之前从未使用ICS,则应开始ICS治疗,对于以前使用ICS的患儿,通常应升级治疗2~4周。根据症状可按需使用缓解药物。
儿童哮喘长期规范化控制治疗每1~3个月需对治疗方案进行审核,根据病情控制情况进行适当调整。如哮喘控制良好、并维持至少3个月,肺功能正常可考虑治疗方案降级,直至确定维持哮喘控制的最低剂量。如果部分控制或未控制,应评估影响控制的危险因素,包括吸入药物依从性与吸入技术的正确性,是否有二手烟和变应原暴露、气候变化等因素存在,是否有变应性鼻炎、鼻窦炎、胃食管反流等合并症存在,哮喘诊断是否正确等。然后进行危险因素的处理,再考虑升级治疗或强化升级治疗,以达到良好控制。控制治疗的剂量调整和疗程如下。
尝试在达到并维持哮喘良好控制3个月,肺功能正常后将剂量减少25%~50%,至最低剂量ICS每日1次给药,一旦出现不可避免的高危因素进行短期升级治疗。哮喘气道炎症是长期的过程,治疗必须是长期的,6岁及以上患儿维持良好控制0.5年以上,可以尝试停用长期控制治疗药物,密切随访观察。
先减少25%~50%的ICS,至达到最低ICS剂量后考虑停用LABA,可延续最低ICS剂量使用方法。临床实际工作中联合使用ICS-LABA者因药物来源及家长的可操作性,以ICS-LABA的最低有效剂量进行儿童哮喘最后阶段的长期控制治疗,并根据病情变化,按需调整剂量,进行维持-缓解治疗。
停药后哮喘可能会复发,应该继续随访与观察。一旦出现不可避免的高危因素,特别是上呼吸道感染时,及时进行短期升级治疗,避免哮喘症状复发。一旦出现哮喘发作,应根据症状发作的强度和频度进行评估确定进一步治疗方案。如仅为偶尔出现轻微喘息症状,对症治疗后可以继续停药观察;非频发的一般性喘息发作,可恢复至停药前的治疗方案;若出现严重和/或频繁发作的喘息,应在停药之前方案的基础上升级或越级治疗[97]。
哮喘儿童部分控制或未控制,可考虑升级或强化(越级)治疗,直至达到控制。对于≥6岁哮喘儿童,ICS-LABA是该年龄段优选升级/强化治疗选择,可根据临床具体情况采用阶段升级治疗(2~3个月)、短期升级/强化治疗(1~2周)或逐日调整(按需)治疗。对于<6岁哮喘儿童,加倍ICS是升级/强化治疗的优选考虑[76]。
AIT是通过逐渐增加变应原提取物剂量,使过敏患儿进行反复接触变应原,提高患儿对此类变应原的耐受性,从而控制或减轻过敏症状的一种治疗方法[131]。多个过敏性鼻炎的指南将AIT作为一线治疗方法,我国2019年过敏性哮喘诊疗指南建议将AIT治疗纳入哮喘治疗和管理的总体框架[132]。AIT可以作为5岁以上轻中度过敏性哮喘患儿的一种对因治疗手段,适用于症状持续、采取变应原避免措施和控制药物不能完全控制症状的轻中度哮喘或哮喘合并变应性鼻炎的患儿。AIT是目前唯一可能改变过敏性疾病自然进程的治疗方法[131],但不能作为儿童哮喘的初始治疗,也不能作为主要治疗,也不应将AIT应用于症状未得到控制的重症哮喘患者[26]。临床上最常使用的AIT方法为皮下注射特异性免疫治疗(subcutaneous immunotherapy,SCIT)和舌下含服特异性免疫治疗(sublingual immunotherapy,SLIT)(舌下脱敏治疗)。AIT治疗过程分为剂量递增和剂量维持2个阶段,总疗程推荐3~5年[131]。AIT治疗过程中需常规配备急救设施,患儿在每次注射治疗后留院30 min,观察是否发生局部或全身速发不良反应,及时处理各级速发局部或全身不良反应,并对后续注射剂量进行调整。
SCIT为AIT的传统给药方式,临床疗效和安全性已经得到充分论证,但仍然有发生全身性不良反应的风险。因此,SCIT必须在医师的监督下进行,须由受过相关专业培训的医务人员在医疗机构进行操作,选择合适的患儿,并提前做好应急预案[131]。此外,目前研究也发现,抗IgE治疗与SCIT联合应用可有效改善哮喘患儿症状、提高生活质量、减少急性发作次数及减少ICS用量,对于合并症的改善也有一定疗效[133]。
与SCIT相比,SLIT的不良反应更少。对已完成4年特异性免疫治疗的160例哮喘儿童伴变应性鼻炎患儿进行的回顾性研究表明,标准化粉尘螨变应原疫苗SLIT可有效控制鼻炎和哮喘症状、改善肺功能,尤以3年疗程效果最好[134]。
儿童哮喘管理由接受过哮喘管理培训的医疗专业人员承担,定期对哮喘患儿进行临床检查、监测、评估。目的是评估当前症状控制情况以及哮喘对日常活动和生活质量的影响,评估哮喘发作的未来风险,并制定相关的管理策略。
儿童哮喘的规范化管理中,CAAP是哮喘综合管理的重要组成部分。作为医师为哮喘患儿制定的个性化自我管理文件内容包括:提醒患儿按计划接受治疗,早期识别哮喘急性加重的征兆并判断严重程度,及时采取相应的措施(调整药物剂量和疗程)以预防或减少哮喘恶化的严重程度,以及何时需要急诊就医等。
CAAP主要目的是帮助患儿及其监护人早期识别哮喘急性加重并启动相应的缓解措施,预防或减轻哮喘急性加重,维持哮喘长期的稳定控制。泰国一项研究纳入49例5~18岁患儿,对所有患儿均用CAAP进行哮喘管理,6个月后发现CAAP管理后患儿急诊就医次数、非计划门诊就诊次数、入院天数和缺课天数均显著降低[65]。另一项研究报道,CAAP管理的儿童哮喘控制率为62%,而无CAAP管理的哮喘控制率仅为21%[135]。CAAP管理对于哮喘儿童在减少急诊就医次数、非计划门诊就诊次数、入院次数、缺课及家长误工天数,改善患儿用药依从性,增强治疗信心,有效提高控制水平等方面具有重要意义[136]。
尽管CAAP已提出近30年,国内外指南均推荐每个哮喘儿童都应该拥有CAAP并定期更新,但CAAP的知晓率和应用率却很低。2013年美国疾病控制与预防中心(CDC)哮喘控制计划委员会报道哮喘儿童CAAP的应用率仅为48.6%[137],我国拥有CAAP的患儿不足30%。如何有效加强和推动CAAP实施与执行,是我国哮喘儿童自我管理教育面临的一项重要挑战。
为患儿制定书面哮喘行动计划(Written Asthma Action Plan,WAAP)有助于早期发现和控制病情的加重。GINA委员会在指南修订中逐渐明确了WAAP的概念,并建议医师为每个哮喘患儿制定与其年龄和文化水平相适应的个性化WAAP。WAAP为患儿定制了适合自己的指导方法,其告知患儿何时、如何调整药物以及何时进入医疗系统以应对日益恶化的哮喘,何时增加治疗强度、如何增加治疗强度、持续多久以及何时寻求医疗帮助[138]。
我国于2016年12月完成了CCAAP的方案和设计,同时开发了电子版哮喘行动计划——"悠然呼吸儿童哮喘管理手机APP"。2017年启动了CCAAP微信公众号[139]。该计划适用于所有年龄阶段的哮喘儿童,依据哮喘症状及PEF检测进行自我管理[140]。
CCAAP在形式上通常采用交通信号灯的绿、黄、红3种颜色,分别代表哮喘患儿目前的疾病状况、已应用的药物和需要采取的干预措施。"绿区"是指哮喘获得并维持良好控制,病情稳定,每日使用所需控制用药。"黄区"是指患儿出现哮喘发作先兆,需及时识别并采取措施,控制症状。"红区"是指患儿哮喘发作,应立即进行自我救治和就医。CCAAP同时标注了患儿个人变应原的致敏情况及常见触发因素,强调回避触发因素是非药物干预的重要手段。这些个体化的哮喘管理方式有助于最大程度地发挥CCAAP的作用[139,141]。正在进行的研究发现执行CCAAP可提升患儿的"知信行",使哮喘患儿及家长能更好地了解正确的哮喘知识。使用CCAAP还可以帮助了解不同的哮喘触发因素,年龄、性别和地理分布是特定的哮喘触发因素,可以根据患儿特定的哮喘诱因来实施预防措施[142,143]。
2018年我国成立了CCAAP专委会,启动全国范围内的巡讲。2019年完成了全国范围内80多场的临床宣讲,完成了全国30个省的临床应用启动,并提出了让中国每一个哮喘患儿都有自己的AAP。2019年8月完成"儿童呼吸标准化项目平台"线上申请/评审微信公众号升级。患儿可以通过悠然呼吸向医师发起问诊申请,从2021年9月至2022年2月的5个多月中,实现问诊2 400余次,开具处方769次,为患儿提供健康指导139次,使得哮喘患儿可以足不出户,即完成复诊和治疗方案的调整,真正实现了互联网医疗和远程医疗管理。
2021年推出了CCAAP第2版,完善了行动计划的内容和管理方案,发表了《中国儿童哮喘行动计划临床应用专家共识》和《中国儿童哮喘行动计划"百问百答"》,并启动了悠然呼吸"一键问诊"[2,144]。第2版CCAAP结合第1版使用中的经验,对内容进行了更新,增加了常用的药物,优化了格式。同时,"悠然呼吸APP"哮喘管理平台的功能在使用中也得到不断更新和优化。该平台除了包括电子版的哮喘行动计划、峰流量监测系统之外,还定期推送包括药物吸入技术视频、环境控制、文献速递在内的哮喘诊疗知识和科普教育等内容,为医师和患儿提供了一个全面的管理平台。至2022年2月,"悠然呼吸APP"注册总医师数为7 163名,来自全国32个省、市,319个城市和地区,覆盖全国2 155家儿童医院或综合医院,注册患儿超过16 000人。在我国,首诊医师或护士是最主要的推动者。对于各级医疗单位,尤其是基层医师和护士的哮喘防治技能培训应持续关注并推广,护士学习哮喘规范管理,可以有效解决医师时间精力不足的问题,帮助医师向患者及家属介绍实施AAP。
儿童哮喘标准化门诊是哮喘诊断及治疗的基础平台,将哮喘门诊标准化、对相应工作人员进行培训、对患儿进行哮喘教育,大大提升了哮喘的诊治和控制水平。在哮喘标准化门诊实施CAAP便于患儿在家中识别哮喘急性发作的预兆,有利于积极控制哮喘。我国于2018年4月发布《儿童哮喘门诊的标准化建设和规范化管理》项目书第2版。截至2020年12月已建成1 289家儿童哮喘标准化门诊,区域示范中心135家;已开展56期培训会,累计培训医师2 560名和护士650名,覆盖全国2 560家医院;开展4 518场患者教育会,线上宣传累计覆盖100万人次,年平均服务患者133万人,哮喘控制率达到84.1%[145]。
CCAAP是中国儿童哮喘标准化门诊评审中的重要组成部分,贯穿中国儿童哮喘标准化门诊评审中所有的环节,开启了新的儿童哮喘管理模式。二者结合存在以下优势:(1)建立医护人员与家长、患儿的伙伴关系,便于施行电子版AAP对哮喘患儿进行日常管理。(2)方便指导哮喘患儿及家长坚持做好哮喘治疗,掌握哮喘长期控制药物及急性发作缓解药物的使用,选择正确的吸入装置。(3)可视化哮喘管理,保证患儿坚持长期、持续、规范个体化的哮喘治疗。(4)大数据的采集有利于开展临床相关研究,为临床提供有力数据,进一步提升医师对哮喘患儿管理的能力及哮喘患儿的控制水平。
在新型冠状病毒流行期间,长期居家隔离,互联网+CCAAP管理模式在疫情期间给广大哮喘患儿带来了便利,疫情期间只有13.95%的患儿受到了中等程度以上的影响,所受影响中哮喘发作者仅占2.6%,71.87%的患儿医疗费用下降,充分说明了CCAAP的有效性[146]。
许多过敏性疾病都会引起哮喘的患病率甚至死亡率增加,比如特应性皮炎、过敏性鼻炎、慢性鼻窦炎伴息肉、食物过敏、嗜酸细胞性食管炎、过敏反应、荨麻疹和药物过敏[147]。《中国儿童严重过敏反应诊断与治疗建议》[56]和中国儿童严重过敏反应急救行动计划(纸质版),为哮喘儿童和家长/照护者提供了在发生严重过敏反应时的急救方案[62,148,149,150,151]。此外,中国医学教育学会儿科专业委员会和世界过敏组织于2018年启动了儿童过敏联合培训项目。联合培训项目的主要目标是:(1)解决中国各地儿童过敏人数日益增长的健康问题;(2)在临床培训中应用国际标准;(3)加强中国儿科医师与海外同行之间的医学交流。截至2021年12月,中国医学教育学会/世界过敏组织联合项目在中国共培养了4 187名儿科医师,其中全国培训师培训项目培养了毕业生269人(覆盖26个省,87个市,127家医院),省培训师培训项目培养了毕业生3 918人(覆盖31个省,234个市,1 275家医院)。这是国内第1个系统的儿科过敏临床培训项目,也是中国第1个获得世界过敏组织认证的培训项目。所有毕业生均获得经社理事会和世界农业组织联合颁发的证书。中国医学教育学会和世界过敏组织计划创建一个医学教育平台,到2023年在中国培训5 000名儿科医师。
研究表明,使用pMDI、Diskus及Turbuhaler类吸药装置的哮喘患儿,64%没有完全掌握吸入技术。医护人员定期检查并纠正家长或患儿的错误方法,可提高吸入技术的准确性。
研究表明,在急性发作的患儿中有24%未能坚持ICS治疗;停用ICS的患儿发生哮喘急性发作的风险是坚持治疗者的2.35倍,ICS应用比例低以及治疗依从性差是我国儿童哮喘控制不佳的最主要原因[152,153,154]。当无法控制患儿哮喘症状时,应首先检查患儿使用吸入ICS的依从性。
针对哮喘发作的诱因进行检查,包括:(1)对尘螨吸入性变应原过敏的哮喘患儿,接触室内外灰尘中的尘螨变应原可以触发过敏性哮喘患儿的发作;(2)对食物中牛奶和鸡蛋过敏的儿童,5岁时大部分都已耐受。但对花生、树坚果和小麦的过敏则有可能延续,经食物激发试验一旦确诊,要严格回避这些食物[155],并定期随访评估;(3)家庭烟雾和环境空气污染是诱发哮喘的重要诱因,对家庭成员实行戒烟和根据空气污染水平来调整患儿活动,可以减轻和避免哮喘发作。
哮喘儿童的共患疾病(如变应性鼻炎、鼻窦炎、胃食管反流病等)是哮喘加重的危险因素,我国的研究发现,近70%的哮喘患者存在变应性鼻炎,慢性鼻窦炎患者中约11%共患哮喘,而30%~80%的哮喘患者共患胃食管反流病。哮喘的慢性病程,急性发作特点也使得哮喘易合并焦虑、抑郁,哮喘合并焦虑或抑郁与哮喘疾病不良预后相关。既往研究表明,哮喘共患病的花费要远高于哮喘疾病本身的花费,而精神心理疾病是共病成本的最大组成部分。当患儿哮喘控制不佳时,应注意共患疾病的检查与处理[156]。
一方面,相应的卫生管理部门应加大儿童哮喘自我管理的政策层面支持力度;另一方面相应的学术团体在学术层面予以硬件与软件的支持。儿童哮喘门诊的标准化建设和规范化管理项目、CCAAP纸质版和微信公众号、"悠然呼吸APP"哮喘管理平台等,在对儿童哮喘的治疗评估、管理教育、交流互动、提高治疗依从性和哮喘控制率、减少患儿误学和家长误工、降低社会和家庭经济负担等方面做了非常有益的尝试,值得在临床中推广应用。
哮喘作为具有复杂表型和内型的异质性疾病,发病机制复杂,迄今为止仍未完全阐明。在过去的30多年里,我国学者对过敏性疾病和哮喘进行了大量基础研究,推进了对具有潜在新靶点的分子和免疫机制的理解。
本部分内容以"asthma"及年份为检索词在"PubMed"进行检索,共检索出166 817篇文章,筛选出作者单位为中国的为6 983篇,根据摘要筛选出哮喘相关基础研究共1 667篇,最终通过人工去重及排除发表期刊质量低、研究内容简单的文献后获得文献83篇。
研究发现,变应原刺激气道上皮细胞后,气道上皮细胞中成纤维细胞生长因子2、Intelectin的表达升高促进气道炎症的发生[157,158]。上皮来源的IL-25和IL-33亦可诱导2型固有淋巴细胞的肺内积聚从而参与哮喘的发生发展,而IL-33在该过程中发挥直接的趋化作用[159]。此外,我国学者研究发现脂多糖暴露诱导上皮细胞脱敏,降低辅助性T细胞(help T cell,Th)2免疫反应,预防过敏性哮喘的发生[160]。
我国学者研究发现,屋尘螨刺激气道上皮产生的外泌体通过其中的蛋白质成分接触蛋白1(CNTN1)经CNTN1-Notch2信号轴促进单核细胞衍生树突状细胞(dendritic cells,DCs)的募集、增殖、迁移和活化,诱导Th2/Th17免疫应答[161]。另有研究显示,chemerin(一种趋化蛋白)通过抑制炎性CD11c+CD11b+DCs的募集,从而在过敏性哮喘中发挥保护作用[162]。此外,DCs中高表达的膜相关RING-CH1通过促进OX40配体表达诱导Th2分化,促进哮喘发生[163]。
生命早期营养不良诱导雷帕霉素机制性靶标1依赖性糖酵解,导致T细胞活化、增殖和Th2分化增加,使其易患哮喘[164]。卡介苗可诱导强烈的Th1反应,抑制过敏性气道炎症和气道高反应性[165,166]。山白菜素、抗IL-17F可改善中性粒细胞浸润,并降低Th17免疫反应[167,168]。血红蛋白加氧酶-1通过增强IL-10的分泌和促进调节性T细胞(regulatory T cells, Treg)分化,对哮喘有抗炎作用[169]。最新研究表明,Th9细胞亦参与哮喘的发病过程,雷帕霉素机制性靶标2、Forkhead box P2可影响Th9细胞分化[170,171],抑制气道炎症。CD4-CD8-双阴性T细胞(DNT)对于维持免疫系统的稳定至关重要,研究发现过继回输离体产生的变应原特异性DNT细胞可抑制Th2细胞分化,减轻过敏性哮喘小鼠的气道高反应性、气道炎症和黏液分泌,揭示DNT细胞的疗法治疗过敏性哮喘的潜在用途[172]。
Forkhead box O1通过抑制Prdm1负向调节产IL-10的B细胞分化,可减轻过敏性哮喘[173]。IL-4可在体内外诱导B细胞自噬,B细胞自噬缺失导致哮喘病理改变减轻[174]。
研究显示,C/EBP同源蛋白、Gαi1和Gαi3的表达以及敲除脂肪酸结合蛋白5均可增强巨噬细胞M2极化加剧过敏性气道炎症[175,176,177],自分泌运动因子受体通过调节肺泡巨噬细胞功能在促进哮喘炎症反应中发挥重要作用[178],可能成为哮喘治疗的潜在靶点。
我国学者研究发现,支气管肺泡灌洗液中的嗜酸性粒细胞胞外陷阱与患者哮喘的严重程度有关,嗜酸性粒细胞胞外陷阱通过CCDC25-ILK-PKCα-CRTC1通路激活肺神经内分泌细胞并通过神经肽和神经递质放大过敏性免疫反应[179]。
IL-38是IL-1家族中一种新发现的细胞因子,我国学者研究发现,IL-38显著抑制促炎性细胞因子和趋化因子的产生,并拮抗细胞内STAT1、STAT3、p38 MAPK、ERK1/2和核因子(NF)-κB通路的激活,在过敏性哮喘中发挥抗炎作用[180]。
miR-29b可通过抑制B7-H3和STAT3途径抑制Th2细胞分化,减轻哮喘的免疫病理[181]。上皮细胞miR-206上调气道IL-25、TSLP的表达,成为2型哮喘的新的治疗靶点[182]。雌激素受体2在转录上抑制miR-423表达致炎症小体激活,导致哮喘恶化[183]。miR-200b和miR-200c通过调节IL-33的表达在哮喘中发挥作用[184]。
研究发现lncTRPM2-AS通过阻断TRPM2泛素化,抑制自噬诱导的凋亡,促进哮喘中巨噬细胞炎症[185]。lnc-bromodomain adjacent to zinc finger domain protein 2B(BAZ2B)通过增强BAZ2B的表达促进M2巨噬细胞活化并加剧肺部炎症[186]。
研究发现,circS100A11和S100A11可促进哮喘中M2a巨噬细胞活化和肺部炎症[187],可能成为哮喘潜在的治疗靶点。
婴幼儿期病毒感染会增加日后反复喘息或哮喘的风险,RSV感染患儿上皮细胞后引起固有免疫和适应性免疫失调与过敏炎症反应协同作用可引起长期慢性气道炎症和持续的气道神经网络异常,与后期发生哮喘相关[188]。CD8+T淋巴细胞在RSV诱导的气道炎症和气道高反应性的发展中起关键作用[189]。RSV能逆转新生BALB/c小鼠接种卡介苗后抗哮喘的作用[190]。此外,黏附分子ITGB4缺乏参与了早期RSV感染的发展,并通过气道上皮细胞中的EGFR/IRF-1途径下调干扰素(IFN)-γ,增加了后期对屋尘螨的敏感性[191]。
利用人偏肺病毒感染的IL-17 KO小鼠模型,研究者发现,病毒感染肺中的Treg细胞增加,Th1和Th2细胞减少,这表明缺乏IL-17会使肺中的免疫反应向抗炎状态倾斜[192]。
有数据表明,CXC趋化因子配体3(CXCL3)和CXCL5可能通过募集CXC趋化因子受体2(CXCR2)阳性中性粒细胞,促进2型炎症,在RV诱导的哮喘恶化的持续状态中起关键作用。靶向CXCL3/CXCL5/CXCR2轴可能为减轻RV诱导的哮喘恶化提供一种新的治疗方法[193]。
在哮喘学龄前儿童中,针对常见呼吸道病原体的标准儿童疫苗接种对哮喘控制具有有益作用,并可能调节与哮喘发病机制相关的免疫反应[194]。
目前研究认为空气污染是哮喘急性加重的危险因素之一。气道上皮细胞暴露于环境污染物或变应原会诱导氧化应激,活性氧对钙调蛋白依赖性蛋白激酶Ⅱ氧化与哮喘有关,减少活性氧对钙调蛋白依赖性蛋白激酶Ⅱ的氧化的产生可能成为治疗哮喘的一种新方法[195]。体外研究表明,PM2.5可通过激活树突细胞增强Th17相关的过敏性炎症反应[196]。此外,母体暴露于室内环镜NO2会导致后代在没有任何后续肺部刺激的情况下出现过敏性哮喘,这种反应与Th2的免疫反应和IL4基因的DNA甲基化有关[197]。
围生期母亲、婴儿生命早期肠道菌群失调是哮喘患病风险增加的危险因素。城市与农村环境的不同也会导致儿童肠道菌群的变化,从而导致不同的哮喘易感性[198]。体外实验发现断奶后小鼠体内某些共生细菌通过NLRP3/IL-1β信号通路加重卵清蛋白诱导的过敏性哮喘[199]。口服干酪乳杆菌以菌株依赖的方式增加了乙酸盐和丙酸盐的含量,通过影响肠道微生物群和免疫反应对慢性气道炎症性哮喘有预防作用[200]。此外,呼吸道鼻咽部菌群的不同与哮喘急性发作发生率相关。鼻咽部嗜血杆菌属和莫拉菌属为主的患儿更易发生哮喘急性发作;与其他菌群相比,嗜血杆菌属炎症因子CXCL8表达更高,莫拉菌属IL-6和IL-10表达更高[201]。
中药通过减轻气道炎症、降低气道高反应性、舒张气道平滑肌等作用改善气道重塑,在哮喘治疗中起到重要作用。大量研究表明,无论中药方剂或成分之一均在防治哮喘具有坚实的理论基础和确切的治疗作用。国内学者通过随机抽取的100万例患者队列研究,发现学龄哮喘儿童中药使用者明显多于非中药使用者,最常见的中药处方是定川汤或杏仁作为单一草药[202]。定川汤可通过减少哮喘小鼠气道黏液、嗜酸性粒细胞浸润和Th2活性来抑制过敏反应[203]。小青龙汤在哮喘小鼠体内通过上调或激活肺内的CD8+和双阴性T细胞群来调节T细胞亚群,从而抑制气道炎症[204]。麻杏石甘汤在哮喘豚鼠中主要是通过刺激支气管平滑肌上的β2肾上腺素受体和抑制中性粒细胞进入气道来实现抗炎作用[205]。固本防哮饮可能通过激活腺苷酸活化蛋白激酶通路调节脂肪酸代谢,也可通过显著抑制M2型巨噬细胞极化,从而缓解哮喘[206,207]。黄芪防风汤通过调控上皮源性TGF-β1抑制上皮-间充质转化,从而保护哮喘小鼠变应性气道重塑[208]。玉屏风散在哮喘缓解期用药可通过恢复桥粒芯糖蛋白1和降低TSLP的过表达显著减轻了屋尘螨诱导的哮喘复发[209]。显著抑制U937细胞肿瘤坏死因子(TNF)-α、IFN-γ和IL-1β的表达,而对IL-4的抑制作用持续较低。且玉屏风散中的重要成分升麻素通过与墨蝶呤还原酶结合并以非酶促方式调节其蛋白表达,从而抑制2型气道炎症,缓解过敏性哮喘[210]。加味补肾益气方可抑制IL-17信号通路改善哮喘小鼠的气道高反应性及气道炎症[211]。主要成分为黄芪和虫草的黄芪-虫草合剂和中药白花前胡的白花前胡甲素均可通过抑制TGF-/Smad信号通路,改善气道重塑[212,213]。单一中药成分例如黄芪可通过抑制Th2反应亢进,也可通过调控CD4+CD25+Foxp3+Treg细胞发挥抗炎作用[214,215]。黄芪的提取物黄芪多糖可通过调节内质网应激,显著降低气道炎症并抑制黏液的高分泌,在哮喘中发挥重要作用[216]。银杏内酯B可通过抑制ERK/MAPK可以在哮喘发病机制中发挥抗炎作用[217]。川芎嗪通过逆转Th2细胞因子模式,抑制气道炎症[218]。麻素通过调节线粒体自噬和凋亡减轻哮喘气道炎症[219]。五味子中的关键成分五味子醇B可调节NF-κB信号通路,抑制促炎因子表达,对哮喘起到治疗作用[220]。丹参提取物可通过降低气道炎症细胞浸润、Th1/Th2细胞因子数量和杯状细胞增生对哮喘小鼠起保护作用[221]。免疫抑制剂霉酚酸酯和雷公藤甲素可通过抑制骨髓嗜酸性粒细胞生成减轻哮喘模型小鼠气道炎症[222]。芝牛蒡苷元被首次发现可减少PKB/Akt诱导磷酸二酯酶4D磷酸化,改善cAMP积累并导致气道平滑肌松弛[223]。蛇床子素可通过抑制磷酸二酯酶4D活性,改善哮喘肺功能的气道松弛机制及结构[224]。穴位贴敷治疗通过降低p65和IκB的磷酸化发挥抗炎作用,用于哮喘的治疗[225]。
研究表明,血清sCD86、sCTLA-4在吸入变应原后表达上调,糖皮质激素治疗后可使其下调[226,227]。磷酸酯酶与张力蛋白同源物蛋白在哮喘小鼠肺组织中低水平表达,糖皮质激素可使张力蛋白同源物蛋白在哮喘小鼠肺组织中水平升高,是糖皮质激素治疗哮喘的新机制[228]。用抗CCR3或地塞米松治疗可以通过调节哮喘小鼠的嗜酸性粒细胞趋化因子/CCR3轴来抑制CD34+祖细胞的迁移和分化,为过敏性炎症作用机制及新免疫疗法提供了新的见解[229]。孟鲁司特通过抑制Th2相关细胞因子减轻哮喘气道炎症[230]。呋塞米可降低基础气道反应性[231]。罗红霉素可通过调节炎性细胞中的MAP激酶/NF-κB通路抑制哮喘的气道炎症和气道高反应性[232]。雾化氯胺酮可通过减少炎性细胞浸润,降低IL-4及诱导型一氧化氮合酶(iNOS)的表达和一氧化氮(NO)的浓度降低气道高反应性及气道炎症[233]。另有研究表明,IL-23通过促进IL-17分泌和Th2极化参与了哮喘的发病过程,沉默IL-23表达可能是治疗哮喘的有效方法[234]。人重组磷脂酶D2显著降低了豚鼠慢性哮喘发作时p65的活性,这表明人重组磷脂酶D2似乎有望成为传统哮喘治疗的有效替代品[235]。抗B7-1抗体可通过降低嗜酸性粒细胞数量,减少周围嗜酸性粒细胞浸润及降低IL-4表达、诱导IFN-γ表达,缓解哮喘症状[236]。人趋化因子样因子1的C-末端肽C19可以通过抑制哮喘小鼠模型中CCR3和CCR4介导的趋化作用来减轻气道嗜酸性粒细胞增多和肺部炎症,在治疗和控制过敏性哮喘方面具有巨大的治疗潜力[237]。
哮喘的监测至关重要,因此哮喘的标志物对哮喘的治疗有重要指导意义。研究发现,哮喘加重时胸腺活化调节趋化因子显著升高,可能是评估儿童哮喘加重的有用炎症标志物[238]。唾液褪黑素和皮质醇昼夜节律紊乱,可能参与哮喘的发病机制[239]。
目前我国学者正聚焦于哮喘的分子机制、精准医学、生物标志物、生物制剂等多个领域展开系列研究,以期为患者寻找新的治疗靶点,改善患者的生活质量。本次哮喘基础研究文献检索,可能存在遗漏,希望在后来的发展报告中补充。
哮喘作为一种气道慢性炎症和异质性疾病可发生于任何年龄,诱因、症状、病程呈多样性改变。哮喘患儿在不同年龄阶段可能就诊于不同的医疗机构与医师,可因缺乏长期且连续的记录,使得医师无法完整地了解哮喘患儿的病史,严重影响了治疗效果。
儿童哮喘的发生、发展过程中存在各种易感因素与触发因素。胎儿时期,特定基因、母亲患有哮喘、母亲在产前有药物和烟草暴露等均增加了哮喘发生的概率。早产、支气管肺发育不良、低出生体重、特应性皮炎、下呼吸道感染、总IgE和变应原特异性IgE水平升高是婴幼儿时期出现哮喘症状的易感因素。在学龄前和学龄儿童,变应原暴露、呼吸道感染、不良环境因素等则是发展成哮喘的重要触发因素。在青少年阶段,治疗依从性差、新的诱因(如开始主动吸烟)、青春期肥胖、过敏、运动、心理和情感因素等对这个年龄段哮喘症状反复起关键作用。
控制哮喘的进展涉及许多与遗传和环境有关的因素[240,241]。哮喘的异质性、复杂性、个体间的诱发与危险因素等都存在着巨大差异。如果制定统一的仅适用于某个高危人群的防治措施,则难免有失偏颇,应考虑制定针对不同年龄段的个性化防治措施。(1)新生儿与婴儿期,应提倡母乳喂养;(2)幼儿与学龄前儿童,对于喘息患儿应早期规范使用ICS;(3)学龄儿童,AIT可以作为轻中度过敏性哮喘儿童的一种对因治疗手段;(4)补充益生菌、维生素D、多食用鱼类等都有一定的效果,但尚无定论[242]。
哮喘在不同年龄的病理生理变化相似,但在疾病的诊断手段、严重度的评估、对不同药物的治疗反应等方面却有明显的不同[243]。在后期的研究中,以下几个领域需要更多研究来推动儿童哮喘到成年的规范化管理:(1)设计大型队列研究,了解哮喘的早期发病因素,尤其是与哮喘进展相关的因素,明确哮喘的自然病史进程;(2)寻找相关生物标志物,尤其是幼儿症状评估的标志物,并进行临床验证;(3)确定可能改变疾病进展的治疗策略;(4)明确哮喘的多种病因及不同年龄段哮喘的主要特征,提供防治策略的证据;(5)建立和完善包括6岁以下儿童喘息诊断流程和共识;(6)建立全国性儿童哮喘流行病学监测网。
哮喘的严重程度评估、治疗和管理方法在不同年龄阶段及成年期之间均有所不同。青春期(12~18岁)是儿童到成年的过渡期。青春期是一个独特的发展时期,个人发展、社会心理和环境变化异常明显。青春期在独立负责疾病治疗、药物依从性等问题变得格外突出。青春期随着父母开始不再监督、哮喘患儿对哮喘认识不足、缺乏有条理的生活习惯以及对疾病消极的应对态度会使其药物治疗依从性下降[244]。青春期其他心理社会影响,如心理困扰、抑郁、家庭冲突等也会影响药物治疗的依从性[245]。青春期哮喘患者的药物依从性差,仅为40%~50%[246]。青春期哮喘患者对体型的过度关注易产生激素恐惧而影响用药。并且青春期哮喘患者更可能在主观上否认自己患病,拒绝疾病角色、对治疗存在负面看法、难以提高遵循医疗建议的认知以及具有否认和低估哮喘症状的倾向,同样可造成青春期哮喘治疗的不足[247]。青春期生理发育和心理发育的不匹配不仅为哮喘管理带来了各种挑战,也在一定程度上增加了青春期哮喘的疾病负担[248]。2019年全球疾病负担研究发现,哮喘在9岁以下和10~24岁人群中的疾病负担分别排在第19位和第27位,在呼吸系统非感染性疾病中,哮喘的疾病负担最重[249]。就我国而言,青春期哮喘死亡人数占哮喘儿童死亡人数的50%以上[250]。青春期哮喘发病率高、死亡率高以及治疗依从性差,与年幼儿童相比,其疾病负担更为明显。
我国《未成年人保护法》规定18岁及以下人群为未成年人,解决青春期哮喘临床就诊和过渡期管理尤为重要。增强哮喘的信息化管理能够显著提高青春期哮喘患者的吸入器使用技术、用药依从性,有助于避免触发因素以及改善哮喘控制。"悠然呼吸"是国内先进的儿童哮喘管理平台,基于CCAAP全面实现了对哮喘患儿的远程管理和数据监测,自2017年2月19日正式发布以来,"悠然呼吸"哮喘移动管理平台为患儿和家长提供了药物说明、诊疗资讯、科普文章和用药技术指导等教育培训资源,提高了哮喘诊疗知识和管理能力。CCAAP使我国青春期哮喘患者的自我管理有据可依,提高了青春期哮喘患者的自我管理水平[144]。
过渡期管理是一个复杂的动态过程,涉及患者、监护人、儿科医师和成人内科医师等的知识教育与技能培训。为了成功向成人治疗过渡,需要组建由儿科和成人医师组成的一个多学科团队。青春期哮喘向成人过渡管理的目标是持续改善哮喘患者生活质量,使其具有最大的独立性,最小程度地中断治疗和照护,避免患者失访、中断治疗和管理。通过医患沟通及针对患者的技能培训等手段,逐步培养青春期患者对疾病的自我管理能力和承担健康责任意识,最终使其具备以下3种能力,实现向成人的成功过渡:(1)自我管理能力(self-management),即利用所获得的疾病相关知识、技能和社会资源对自身疾病进行的一系列干预措施;(2)自我介绍或与医务人员沟通的能力(self-advocacy),即能够自己描述不适,与医务人员进行畅通的交流;(3)自我决策能力(self-decision making),即能够管理自己的健康问题,承担相应的医疗保健责任。
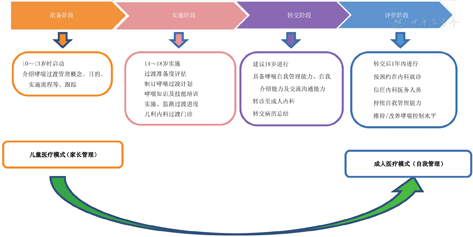
此外,为指导医务工作者更有效地管理青春期慢性疾病,并从"以父母管理为中心"的儿科医疗保健系统转变为"以自我管理为中心"的成人医疗保健系统,部分国家提出了具有其特点的青春期慢性疾病的过渡方案。2020年,欧洲过敏和临床免疫学会(European Academy of Allergy and Clinical Immunology,EAACI)制定了青春期哮喘过渡的临床实践指南,为青春期哮喘成功过渡到成人阶段以及为有效过渡流程的开发提供了通用建议和具体建议[251]。英国国家卫生保健与临床优化研究所(National Institute for Health and Care Excellence,NICE)发布了从儿童服务向成人服务过渡的指导方针,将青春期哮喘者视为平等的伙伴,并让他们的家人、管理人员、初级护理从业者和过渡协调员参与制定这份过渡计划[252]。英国儿科团队总结出"向成人科室移交时患儿需要掌握的知识"(表8)和"医疗团队需要检查的内容清单"(表9),并且总结了"青少年向成人科室移交的清单",用于支持这一过渡过程(表10)。《青春期哮喘管理及向成人过渡管理的中国专家建议》[253]建议组建过渡管理团队以及设立过渡门诊,对无法设立过渡门诊的医疗单位,可以采用网络视频会诊的方式进行。我国提出青春期哮喘向成人过渡通常分为准备、实施、转交(诊)及评价阶段(图9)。由于青春期个体发育水平、认知能力及家庭支持等存在差异,过渡管理的各阶段开始时间并不完全取决于年龄,而应该根据青春期哮喘患者的认知水平、各个医疗单位儿科与成人内科就诊年龄的划分等实际情况,灵活掌握。

向成人科室移交时患儿需要掌握的知识
Information that a child with asthma needs to know when transferring to an adult department
向成人科室移交时患儿需要掌握的知识
Information that a child with asthma needs to know when transferring to an adult department
| 协调员(最好是哮喘专科护士)需要时间和足够的资源,以确保以患儿为中心,儿科和成人团队的成员都有各自明确的目标 |
| 在过渡期结束时,年轻人应该能够了解以下知识: |
| 描述哮喘是什么; |
| 了解自己的诱发因素,以及如何尽可能避免这些因素; |
| 了解他们使用的药物如何起作用,以及定期使用药物的原因,演示正确的吸入技能; |
| 了解生活方式可能会影响哮喘,比如吸烟、节食、锻炼; |
| 了解他们的个人哮喘的行动计划,并能在有需要时寻求帮助 |

医疗团队需要检查的内容清单
List of items for the medical team to examine
医疗团队需要检查的内容清单
List of items for the medical team to examine
| 项目 | 项目 |
|---|---|
| 与父母/监护人讨论过渡计划 | 了解自我护理的重要性 |
| 能够描述哮喘是什么 | 知道如何开重复的处方 |
| 了解药物的目的和作用 | 了解坚持服药的重要性 |
| 避免触发因素 | 演示正确的吸入技能 |
| 了解如何遵循个人哮喘行动计划 | 接受对吸烟/电子烟/非法药物的建议 |
| 单独提供部分/全部门诊时间 | 接受饮食建议 |
| 知道如何预约/更改预约 | 讨论运动 |

青少年向成人科室移交的清单
List provided when transferring from adolescent to adult department
青少年向成人科室移交的清单
List provided when transferring from adolescent to adult department
| 项目 | 内容 |
|---|---|
| 生活背景 | 生活条件 |
| 家庭结构和重大生活事件 | |
| 到诊所距离 | |
| 吸烟 | |
| 非法药物 | |
| 怀孕 | |
| 教育/职业选择 | |
| 检测结果 | 肺功能检测 |
| 呼出气一氧化氮 | |
| 皮肤点刺试验/总IgE /特异性IgE | |
| 血清/痰嗜酸性粒细胞计数 | |
| 成像 | |
| 运动测试 | |
| 支气管镜检查 | |
| 骨密度(DEXA)扫描 | |
| 肾上腺功能检查 | |
| 哮喘控制 | 年恶化率 |
| 急诊次数 | |
| 住院次数 | |
| 最近的ACQ-7/ACT/PAQLQ | |
| 哮喘合并症 | 过敏性鼻炎 |
| 胃食管反流病 | |
| 过敏和过敏性反应 | |
| 支气管扩张 | |
| 湿疹 | |
| 其他诊断/状况 | |
| 依从性 | 控制药物的平均使用量/12个月 |
| 缓解药物的平均使用量/12个月 | |
| 电子设备数据 | |
| 治疗 | 剂量、频率 |
| 设备 |
注:ACQ-7:哮喘控制问卷-7;ACT:哮喘控制测试;PAQLQ:儿童哮喘生活质量问卷 ACQ-7:Asthma Control Questionnaire-7;ACT:Asthma Control Test;PAQLQ:Pediatric Asthma Quality of Life Questionnaire

AAP是哮喘患儿自我管理和各级医师管理哮喘患儿的有效工具,但在实际应用中亦存在一些问题和局限性:(1)医师日常临床工作负荷较重,难以有足够的时间与患儿及家长进行充分沟通;(2)儿科医师需要掌握哮喘规范化诊治的技能,熟悉哮喘各种治疗用药、正确掌握各种吸入装置及PEF仪等的使用、熟知哮喘管理的每一个环节,才能正确指导患儿及监护人,然而一些儿科医师对AAP重视不够或不能获得书面AAP;(3)儿童尤其是年幼儿童需要通过家庭成员或监护人来执行AAP,则难以保证AAP的执行效率;(4)年幼儿童不能使用PEF仪,只能依据临床表现来诊断和监测;(5)由于医疗体系不同,目前尚不能在AAP上明确标注医师联系电话或医院急救电话,导致发生紧急状况时,无法保证医疗服务的可及性及时效性。
随着诊疗技术的提高,我国儿童哮喘的诊断、治疗水平已有显著提高,患儿父母受教育程度较前普遍提高,互联网和物流的高度发达,已具备推广AAP提高哮喘管理水平的客观条件。CCAAP施行3年来,已经推广到31个省、自治区和直辖市,共352个城市,1.6万患儿使用了我国自己的AAP。因此,今后需针对临床实践中存在的问题,采取有效措施,进一步加大推广AAP的应用力度,力争使每位患儿都有自己的AAP,尤其是对那些初诊即重症哮喘发作或复诊哮喘未控制、部分控制以及难治性哮喘的患儿,就诊结束后立即由医师本人或专业护士教会患儿及家长或监护人掌握使用AAP,并定期随诊,核查其使用情况,全方位提高患儿的自我管理水平,不断探讨CCAAP实际应用效果,不断加以完善[144]。
哮喘的发病机制极为复杂,因此哮喘的防治仅用西医或中医都有其局限性,中西医结合可能更有利于儿童哮喘的防治。我国的中医药在防治儿童哮喘方面有其悠久历史、特色和优势。中医治疗采取分期辨证施治,急性发作期当攻邪以治其标,分辨寒热虚实而随证施治;慢性持续期当标本兼治,以祛邪扶正、化痰平喘、补肺健脾益肾为治则;临床缓解期当扶正以治其本,以补肺健脾益肾为主,调其肺脾肾等脏腑功能,消除伏痰夙根。哮喘属于顽疾,宜采用多种疗法综合治疗。《中西医结合防治儿童哮喘专家共识》将中医、西医在儿童哮喘诊断、治疗及预防方面有机结合,规范了儿童哮喘的中西医防治,以确保防治的有效性和安全性[254]。
2016年2月,国务院第123次常务会议审议通过《中医药发展战略规划纲要(2016—2030年)》,自此,中医药的发展上升为国家战略。特别是新型冠状病毒肺炎疫情发生以来,中医药在疫情防控救治中发挥了重要作用。目前,不少中医院设置了儿童哮喘专病门诊,中医药在儿童哮喘的防治中的确有多种方式与途径。但目前尚缺乏系统的、多中心、大样本的临床试验研究依据,妨碍了其在哮喘治疗中的推广应用,使得儿童哮喘中医专科门诊的规范化进程较慢[255]。亟须出台中医儿童哮喘门诊建设的专家共识,并专项推进中医儿童哮喘门诊的建设和规范化进程。
运动是支气管痉挛和哮喘急性发作的诱因早已得到公认[256]。大量研究已经证实,运动可导致哮喘患儿出现支气管痉挛,即使是未被诊断为哮喘的部分人群,在进行中等强度运动后也可能会出现轻微的支气管痉挛[257],而在剧烈运动后则可能出现肺功能明显下降,并表现出类似哮喘急性发作的征象[258]。运动诱发哮喘症状的严重与否本质上取决于气道潜在炎症水平的高低。不同运动持续时间、运动强度和运动方式均能引起哮喘患儿不同程度的呼吸功能下降和呼吸道阻力上升[259]。我国一项横断面研究显示,49.0%的学龄期患儿在最近1个月中存在运动后哮喘相关不适症状和/或因此出现的运动受限[260]。但哮喘作为异质性疾病,个体差别很大,哮喘患儿之间气道炎症程度和类型、个体状态等均不一致,运动对于哮喘儿童并非像传统观点所认为的那样不宜运动,适度的运动可以改善哮喘,并且提高生活质量已逐渐被接受[261]。
由于自身对症状的顾虑、家庭成员和社会因素等影响,哮喘患儿的运动参与程度显著不足。我国对使用CCAAP的哮喘患儿进行线上问卷调查,评估其身体活动水平[262]。发现学龄期哮喘患儿身体活动多数处于中低水平,仅19.6%达到高运动水平,且久坐时间长,在学习日和周末,分别有77.0%和87.9%的儿童久坐时间超过2 h,周末尤甚,这说明我国哮喘患儿普遍存在运动不足的现象[263]。如何在目前的形势背景下,制订规范化、个体化、可行性强的哮喘儿童运动处方,改善哮喘儿童运动现况,成为了亟待解决的问题。
运动可以显著提高人体最大摄氧量,哮喘患儿对运动具有良好的耐受性[264]。哮喘儿童在接受规范药物治疗、良好控制状态经适当的预防措施后,可以进行正常运动[265,266,267]。但应注意运动环境的选择,如干冷环境、空气污染、花粉和其他变应原浓度增加、运动场所空气质量下降(泳池含氯量、杀虫剂、除草剂、油漆及其他挥发性装饰材料等)等情况,易加重运动诱发性支气管痉挛(exercise induced bronchoconstriction,EIB)的发生。呼吸道感染也会加重运动诱发支气管收缩。但在水环境相关的运动对哮喘患儿的影响方面还需要进行更多的研究[268,269]。动物模型表明,运动可改善气道反应性和炎症[270]。临床研究也表明,定期运动可以减少哮喘症状,降低气道反应性,降低哮喘发作的风险,提高运动能力和生活质量,改善肺功能[264,271]。具体可体现在以下方面。
学龄前儿童(0~5岁)应以多样化的形式进行运动,使多个肌群均能得到锻炼,根据不同年龄生长发育情况设置相应的运动,在运动中促进健康发育[278]。
学龄期儿童和青少年(6~17岁),鼓励参加适合年龄特点的、有趣的、多样化运动,促进健康的生长发育,增进心肺耐力、肌肉功能和骨骼健康。儿童青少年对耐力训练、抗阻训练和骨骼负重均有生理适应性,但青春期前的儿童骨骼尚未发育成熟,不适宜参加过多的高强度运动和器械负重抗阻训练,可进行适宜的抗阻训练,建议如下:(1)频率:每周3~5 d,最好每日运动;(2)强度:中等强度(显著增加呼吸、排汗和心率的活动)到高强度(急剧增加呼吸、排汗和心率的活动);(3)时间:每天20~60 min的持续或间歇运动;(4)项目:步行、慢跑、游泳、自行车、瑜伽等。
SABA是常用的EIB防治药物,另外,吸入肥大细胞稳定剂,如奈多罗米钠,也可减弱EIB,但药物作用时间很短[279]。LTRA(孟鲁司特)对部分哮喘患者也可有效预防运动诱发性哮喘。未诊断哮喘但出现EIB的患儿也建议预防性使用ICS,特别是对进行规律运动的患儿[280]。规律使用ICS、LTRA等控制药物可减少运动诱发的哮喘发作,并可减轻其严重程度。
鼓励哮喘儿童进行规律的体育运动,但目前尚无证据表明哪种类型的身体活动具有最佳效果,故无法推荐最合适的锻炼方式[51]。《健康中国2030规划纲要》中强调要加强体医融合,发布体育健身活动指南,指导不同人群进行科学和规律的运动[281]。医务工作者应积极加强哮喘儿童运动相关知识的科普宣传,消除认识误区。同时,临床医师应积极学习指导哮喘儿童运动的科学方法,并与运动专家协作,将哮喘儿童运动处方不断科学化、标准化,并充实运动处方内容。应重视儿童营养学和心理学在哮喘管理和科学运动中的重要作用,通过多学科合作,全面提高我国儿童哮喘管理水平[278]。
儿童哮喘是我国的主要公共卫生问题之一,在医疗、护理、经济等方面给家庭和社会带来巨大的负担。2021年《中国哮喘患儿家长的信息需求、资源和自我管理挑战》的评估揭示:(1)了解并理解与哮喘相关的信息;(2)将哮喘视为一种可能影响终生的慢性疾病;(3)需要经历痛苦;(4)建立支持网络,包括家庭成员、学校工作人员和儿童哮喘专家的需求;(5)满足患儿的心理和情感需求等方面面临严峻的挑战[282]。儿童哮喘需要长期和持续的治疗,在规范化的同时,应该针对每个儿童的独特需求进行个性化治疗[78]。医院-社会-家庭医师-互联网-患儿家长的管理模式有助于哮喘儿童得到全程管理[283]。
哮喘控制不佳原因之一是未充分认识到家长与患儿在哮喘管理中的重要地位[8]。要重视医院之外的哮喘管理。儿童哮喘管理的核心是哮喘儿童的自我管理(幼儿是家长),患儿必须处于控制哮喘所有努力的中心。哮喘自我管理的主要内容包括哮喘自我管理相关的健康教育(哮喘疾病知识、哮喘的预防和治疗、吸人装置的使用指导和培训、用药和随诊的依从性教育等)、哮喘自我管理的工具(哮喘控制测试评分表、PEF、哮喘日记及WAAP)、哮喘急性发作先兆的识别和处理3个方面[284]。临床医师作为儿童哮喘控制的主要参与者,大部分时间都在卫生保健领域之外,需要建立以社区为基础的卫生保健体系,由临床医师、社区卫生保健、家庭、老师等共同协助儿童哮喘的管理。社区在活动场所、策略方案实施等各个环节提供必要的支持,旨在全面改善和提高儿童和家庭的生活质量。基于社区的干预措施有效改善儿童哮喘控制流程见图10。


中国哮喘儿童家长知信行调查项目组对我国29个城市2 960例哮喘患儿家长进行的调查表明,家长对哮喘的认知、态度和行为均较差,仅有18.31%的家长答对60%以上的认知相关问题,由于父母对哮喘认知不够以及重视度不够,直接导致实际管理与预期控制程度间存在差距[285,286]。比较集中的问题表现在:(1)对哮喘本质缺乏正确的认识,不认为哮喘是一种慢性气道炎症疾病,即使临床没有症状,但气道炎症仍然存在,其治疗需要遵守早期、长期、规范、个体化的原则。(2)慢性气道炎症其最有效的抗炎药物是糖皮质激素,缓解期也需长期ICS用药,对激素的恐惧心理也使得他们对缓解期用药的依从性差,不能遵守医嘱或不正确使用药物。67%的父母担心ICS对孩子的成长产生负面影响,41%担心药物依赖,24%担心对孩子的智力造成潜在伤害[287]。(3)缺乏对儿童哮喘治疗必要性的认识。认为儿童哮喘症状可以自行缓解,缓解期可无任何症状,不能接受规范化的治疗。11%的哮喘患儿没有服用任何药物[87]。(4)对运动有误解,既有认为一点不能运动,又有认为可以随意运动。(5)对自我缺乏管理意识,不能充分认识可能诱发自身哮喘急性发作的环境因素。(6)一旦急性发作,不能应急处理,导致症状加重,甚至威胁生命。
基层社区医院开展哮喘防控工作,为患儿及家属带来积极的影响。有调查显示,工作5年以上以及主治医师对哮喘的本质和用药比较了解,而住院医师对哮喘本质和用药的了解程度较低,相关知识较为贫乏。因此,提高社区基层医师对哮喘的认知程度,加强基层医师、民营及个体诊所医师对于儿童哮喘的诊断和用药知识的培训是控制我国儿童哮喘的一个重要环节[288]。
哮喘知识教育意义在于教育家长与患儿以及相关医护人员对哮喘基本知识有一个全面认识:(1)哮喘作为慢性疾病需要坚持长期及规范化吸入激素治疗的重要性;(2)哮喘的急性发作可能导致患儿的死亡,保证家长与患儿掌握急性发作的处理;(3)避免接触诱发哮喘急性发作的环境因素,针对出现的状况,如何应对;(4)适度运动对于哮喘儿童的生长发育和疾病控制的重要性;(5)增强自我管理能力,并持之以恒;(6)遵从医嘱、定期复诊、坚持长期规范化的治疗。从而有效地降低哮喘儿童的急诊率、住院率和死亡率[289]。
哮喘知识教育的内容应包括:(1)哮喘的本质、发病机制;(2)避免接触诱发哮喘发作的因素,并知晓家庭自我处理方法[290];(3)自我管理与监测,掌握PEF的测定方法、记哮喘日记,应用"儿童哮喘控制测试"等控制问卷,判断自身哮喘控制水平,并及时调整方案;(4)要了解各种长期控制及快速缓解药物的作用特点、药物吸入装置使用方法(特别是吸入技术)及不良反应的预防和处理对策;(5)哮喘发作的征象、应急措施和急诊指征;(6)心理因素在儿童哮喘发病中的作用。
护士或社区卫生工作者的家访越来越多地成为基于社区管理的一个重要部分。家访重点在于有关哮喘的教育以及如何改变室内环境以减少尘螨、蟑螂、动物皮屑和其他被认为是潜在诱发哮喘的物质。指导家庭高温下清洗床上用品以阻止螨虫以及如何使用加湿器或除湿器、吸尘器和清扫房屋。
"供需存在差异,缺少权威声音"是当下儿童哮喘健康教育的困境之一,需要积极推广健康教育,尤其是传播科普。目前,我国很多医院都开始了儿童哮喘的科普工作,注重由传统的门诊教育转变为门诊教育与科普教育相结合的方式,从政策上鼓励和支持儿童哮喘的系列科普创作,使得家长有更多的途径获取通俗易懂的防治知识,对于帮助家属理解病情,配合治疗有非常重要的社会意义[291,292]。
但目前科普工作仍面临不少困难,如医务人员重视科普的工作参与度与热情不够,科普内容专业术语较多,大众接受比较困难。强调儿童哮喘的科普教育应围绕哮喘患儿及家长最关心的问题开展科普创作,把晦涩难懂的科学道理以生活化方式形成通俗易懂的语言,科学性与趣味性相结合,结合新传播方式,便于大众理解和接受。由于儿童哮喘健康教育社会需求量大,不同医院共识性强,易于开展协作,尤其在儿童哮喘科普创作、专家知识库建设等方面发挥资源特长,形成合力,将健康教育"小、散、弱"局面转变为"大、聚、强"[286]。
国外统计,每年小学生患儿在学校经历高达12次的喘息[293]。哮喘患儿每天待在学校超过6 h,学校校医、护士比父母有更多时间评定哮喘患儿自我管理水平,并及时满足他们的需要。患儿父母也需要依赖学校校医、护士去获得有关哮喘患儿的动态信息。学校校医、护士对慢性疾病管理具有积极的影响,针对家长、学生和学校主管卫生领导和校医(保健医)的哮喘知识宣教非常重要和必要,学校积极的管理可以提高免疫接种率、减轻哮喘加重,减少因哮喘而缺课的情况[294],因此,学校可以成为影响哮喘儿童行为改变的重要机构[295]。以学校校医、护士作为纽带,学校、医师、家庭三方建立紧密的合作关系,便于轮流为哮喘患儿服务,以学校为中心的哮喘儿童管理攻略可以更有效地来改善哮喘药物和AAP在学校的使用,可以减少哮喘的急性发作和提高出勤率[296,297,298,299,300]。
我国学校在哮喘防治干预上的空白,极大程度上增加了儿童哮喘发作的风险。绝大多数学校虽已建立校园医疗的标准化管理体制,但学校医疗水平有限,医疗设施相对简陋。整体校园医疗服务体系仍然处于一个探索阶段。根据"学校卫生工作条例"规定:城市普通中小学、农村中心小学和普通中学设置卫生室,按学生人数600∶1的比例配备专职卫生技术人员[301]。而这些直接服务学生的卫生技术人员中,12.16%无临床实践经验,43.46%未接受过规范化培训,情况堪忧。我国学校医疗服务却仍停留在被动地处理突发事件,而非深入地对在校哮喘患儿进行主动干预。学校护士在应对新型护理模式的转变上反应滞后,在细化学校护理工作的进程上,我国仍需深入的研究和政策的支持[302]。
2016年美国过敏、哮喘和免疫学学会(AAAAI)与美国学校护士协会合作,开发了基于学校的哮喘管理计划(school-based asthma management program,SAMPRO),并与国家合作伙伴进行了广泛的认可和传播,值得我们借鉴[303]。SAMPRO包含以下4个方面的内容:(1)支持圈:患儿、家属、临床医师和学校护士之间沟通的协调模式(图11)。①在家庭、临床医师和学校护士之间建立围绕儿童的伙伴关系和沟通渠道;②确保临床医师在学年开始时开发个性化的AAP、药物和完整的授权表格,以优化系统监控和学校哮喘药物的提供;③通过哮喘教育项目对学校护士和家庭进行教育;④减少支持圈所有成员之间的沟通障碍。


注:SAMPRO:基于学校的哮喘管理计划 SAMPRO:School-based asthma management program
(2)在学校提供紧急和个性化哮喘护理。哮喘管理计划包括哮喘紧急治疗计划和供家庭和学校的哮喘儿童AAP。哮喘紧急治疗计划为学校中出现急性哮喘症状的儿童提供了一个应急管理计划。学校哮喘紧急治疗计划可以为急需医疗的儿童提供抢救药物,并支持在所有学校储存SABA。除了哮喘紧急治疗计划外,该计划还提倡使用为在家庭和学校使用而制定的个性化AAP。
(3)对患儿、家庭和学校进行全面的哮喘教育。为家庭和学校制定综合教育计划,识别哮喘儿童,识别哮喘症状,评估哮喘控制,并在家庭和学校内使用护理协调、沟通和哮喘管理方面的最佳实践。学校卫生官员和学校护士可以推广正规教育项目的使用,这在SAMPRO的工具包里面都有链接。
(4)减少学校环境触发因素的策略。倡导减少学校环境中哮喘诱因的暴露,环境暴露会影响哮喘症状的发展,而学校具有影响儿童哮喘的触发因素[304,305]。具体触发因素可能因学校的环境和资源而异。例如,在内城区的学校环境中,老鼠变应原的含量非常高,可能与哮喘发病率增高有关[86,306];由于靠近高密度交通、通风不良以及建筑通风和维护不理想,儿童可能接触到更高水平的空气污染物[307]。现有证据和专家共识都支持通过多方面干预措施去除变应原、害虫,管理和缓解学校环境中的空气污染物[308]。美国环境保护局已经制定了室内质量工具计划(http://www.epa.gov/iaq/schools/managingasthma.html)授权学校和家庭在各自的学校环境中减少相关的变应原和污染物暴露。
(1)成立专项工作组。工作组应该有多个相关方组成,包含公共卫生部门、医院、学校、政府、基金会等组织,从专业和法律法规以及资金等各个层面集中资源,进行专项推进。
(2)推出经过论证和广泛认可的资源包、工具箱,并建立官方网站。方便获取:①行动计划;②管理计划;③哮喘严重程度评估表;④访视清单;⑤护理清单;⑥环境检查表;⑦针对各种角色的教程:学生、家长、护士、学校教职工。
(3)制定官方中国儿童哮喘学校健康项目白皮书。建立学校诊疗和护理的标准;推动相关法律法规的完善,以支持政府资助和财政激励。
(4)进行多项有代表性的研究。通过农村和城市儿童哮喘学校健康项目的相关研究,评估学校健康项目的效果和收益。
(5)实施、宣传和持续推行。儿童哮喘学校健康管理的可持续性,取决于学校是否有足够的财政资源来维持学校卫生的资金,以协调临床医师的护理、哮喘救援和控制药物的储备,以及培训学校人员哮喘管理的基础设施。
传统的"到医院看病、门诊随访"的医疗模式越来越难以满足人们的需求,而且无法有效地做到对哮喘发作的即刻预警、及时治疗和避免突然死亡[309]。目前,医疗保健相关应用程序和设备的开发是信息和通信技术领域中增长最快的领域。这些应用试图通过移动健康策略,提高患儿护理的准确性、效率和成本效益,同时通过提高可达性(尤其是偏远地区)来改善患儿护理。
移动健康技术的命名尚未统一,如Telehealthcare,eHealth,mHealth等,本文暂称为mHealth(mobile Health)。"Be He@lthy, Be Mobile"(BHBM)倡议是由WHO和国际电信联盟(International Telecommunication Union,ITU)领导的全球合作[310]。其支持在国家卫生系统内扩大mHealth,以帮助对抗糖尿病、癌症、心血管疾病和慢性呼吸道疾病。mHealth应包含一系列针对自我管理行为不同方面的功能,包括自动药物使用提醒以提高依从性、定制的哮喘患儿教育以提高知识或影响行为改变,使用救援治疗,以及在病情恶化时提供行为指导。这些功能可能会使用不同的IT模式(短信、手机、应用程序、电脑游戏、基于云的电子健康记录),并且可能会在不同的环境(初级/社区护理、医院门诊、学校)中使用。
自动提醒(通过短信、闹钟或自动电话发送)可以提高药物的依从性,但对临床结果没有影响。作为更复杂的远程医疗干预的一部分,提醒可能有助于坚持监测或使用药物。
基于行为改变理论的游戏在一定程度上提高了自我管理技能,尽管对症状和医疗资源使用的影响是可变的。一款通用的健康行为游戏,针对具有特定行为特征(如叛逆、自我控制情绪能力差或自尊心强)的青少年,可改善哮喘控制、减少缺勤、降低入院率,但不会降低急诊就诊率[311]。
远程监护是将监测数据从患儿传输到电子健康记录,可与医疗专业人员共享(或由医疗专业人员监测),被认为具有改善结果的潜力。一些研究表明,远程监护至少能使一项临床结果有所改善,如哮喘控制、肺功能、生活质量、活动受限风险降低、缺课、病情恶化和使用非计划护理[312,313,314]。远程监控的效果可能受到人口背景(贫困状况和文化背景)和提供的专业支持水平(监控频率、反馈个性化)的影响。哮喘控制不佳的人通过远程监控比那些控制已经达到最佳状态的人能获得更多益处。
迄今为止,移动健康应用层出不穷,但尚未建立确保现有和新产品质量的中心机构,由于移动医疗环境是一个非常动态的领域,其中一些可能不符合监管要求,并且很少有应用程序经过临床验证,许多应用程序也不是基于指南或临床证据来建立的。由于大量的哮喘患儿可能从移动健康技术创新中受益,所以迫切需要相关组织和部门介入,评估这一领域的最新技术和未来潜力,并规范相关法律法规。
(1)mHealth服务必须满足众多法律领域的要求:①远程治疗的合法性和医疗责任;②患儿医疗记录的敏感数据的保管问题;③伦理问题进一步完善。
(2)依从性的测量规范:需要规范药物或者治疗依从性的评估标准,目前有几种不同的方式可以衡量依从性:总体依从性,控制吸入器的依从性,药物获取(从药店获得药物的比例)依从性,药物依从性量表[315,316]或日常日记[313,317]。
(3)改善依从性和治疗结果的评估标准。例如基线记录的时机和内容,评估周期,评判标准。
(1)流行病学:通过应用程序收集数据,可以从患儿群体中快速收集数据;这将极大地增加该领域流行病学研究的范围。
(2)监测:使用电子临床日记可以对大量患儿的症状进行日常监测,从而对药物治疗和疗效进行简单且成本效益高的现实生活研究。
(3)临床诊断:在这个精准医疗的新时代,使用电子临床日记可以将单个患儿的数据与公共机构登记的环境触发因素轨迹相匹配,确定与患儿相关的触发因素模式,并实施适当的个性化预防策略。
(4)与诊断设备相关的应用程序:智能手机正在成为各种诊断设备和生物传感器获取的客观数据的传输工具;应用程序将这些数据与患儿获取或输入的其他信息集成在一起,并允许对患儿症状和参数进行稳定监控。
数十年来,经过几代儿科医师的不断努力,我国儿童哮喘的规范化诊治水平已有了显著的提高,从1988年首次发表我国儿童哮喘的诊断及分型标准,到2016年完成《儿童支气管哮喘诊断与防治指南(2016年版)》,到2017年提出"中国儿童哮喘行动计划",再到2020年完成《儿童支气管哮喘规范化诊治建议(2020版)》,走过了32年的时间。通过规范儿童哮喘的诊治,有效地实现了哮喘的长期控制,减少了急性发作、计划外就医和住院,通过CCAAP的实施提高了儿童哮喘的管理水平,并改善了患儿及家庭的自我管理。但由于儿童哮喘的疾病进展差异大,临床表现不一,使得我国儿童哮喘的诊断率和控制率尚不尽如人意,未来还有很多有待研究和改善的方向。
项目负责人:申昆玲(首都医科大学附属北京儿童医院;深圳市儿童医院)
参与作者:陈爱欢(广州医科大学附属第一医院);陈育智(首都儿科研究所附属儿童医院);符州(重庆医科大学附属儿童医院);郝创利(苏州大学附属儿童医院);洪建国(上海交通大学医学院附属第一人民医院);刘传合(首都儿科研究所附属儿童医院);刘恩梅(重庆医科大学附属儿童医院);刘瀚旻(四川大学华西第二医院);刘长山(天津医科大学第二医院);潘家华(安徽省立医院);沙莉(首都儿科研究所附属儿童医院);尚云晓(中国医科大学附属盛京医院);孙新(空军军医大学西京医院);徐保平(首都医科大学附属北京儿童医院);殷菊(首都医科大学附属北京儿童医院);张建华(上海交通大学医学院附属新华医院);郑跃杰(深圳市儿童医院)
所有作者均声明不存在利益冲突
本文的编写工作得到了国内多位专家的大力支持和悉心指导,由北京秩韵数据技术有限公司提供写作支持,在此表示诚挚谢意,同时也对所有患儿及家属表示衷心的感谢