
探讨左氧氟沙星在儿科临床中的应用现状和安全性。
回顾性研究2017年1月1日至2022年12月31日首都医科大学附属北京儿童医院和北京儿童医院保定医院使用左氧氟沙星的住院患儿,收集患儿性别、年龄、体重、出院诊断、药品名称、给药剂量、给药途径、给药疗程、病原微生物、不良反应等资料。
共纳入220例患儿,年龄1个月14 d至16岁7个月27 d,主要分布在学龄期(70例)、学龄前期(65例)、幼儿期(44例),占所有患儿数的81.37%。共计13个科室使用,主要集中在呼吸科(77例)、血液科(49例)、感染内科(47例)、儿童重症监护室(14例)、干细胞移植科(9例),占总病例数的89.08%。主要用于肺炎(150例)、全身播散性结核病(25例)、脓毒症(20例)及血液病合并感染(16例)的患儿。常见的病原为肺炎支原体(102例)、肺炎克雷伯菌(14例)、嗜麦芽窄食单胞菌(14例)、鲍曼不动杆菌复合群(10例)、金黄色葡萄球菌(9例)、铜绿假单胞菌(9例)。左氧氟沙星的用法用量中,单次给药剂量不足25例,超剂量使用9例,给药频次错误9例。与左氧氟沙星相关的药物不良反应共3例,其中2例胃肠道反应(1例腹泻,单次剂量15 mg/kg,临床治愈;1例恶心,临床好转),1例皮疹(临床好转),未见严重不良反应。
左氧氟沙星在儿童中短期使用相对安全,应按照正确的用法用量给药,期间需要密切关注胃肠道系统、皮疹、肝肾功能、血液系统、血糖、心脏系统、神经系统等指标。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
细菌感染是医院和社区环境中的常见事件,也是21世纪最突出的公共卫生挑战[1]。喹诺酮类抗菌药物是治疗细菌感染的最有力武器之一[2],是以4-喹诺酮母核为核心发展而来的一系列相关化合物。因其抗菌谱广、抗菌作用强、药物动力学性能好和耐受性好,用于各种感染的治疗[3]。喹诺酮类抗菌药物至今已经有超过50年的使用历史,在全球抗菌药物市场中仅次于头孢菌素类和青霉素类药物[4,5]。1962年萘啶酸上市后不久,1例儿童患者在采用萘啶酸治疗尿路感染时出现单腕酸痛。1972年Bailey等[6]报道了1例22岁女患者由萘啶酸引起的关节肿胀、疼痛、行走困难的病例。喹诺酮类药物被发现在幼年动物发育早期会影响软骨,导致关节病。因此,喹诺酮类药物说明书中限制了其在儿科人群的使用。
随着耐药菌的增加,儿科医师面临着在这一患者群体中频繁使用未经批准的喹诺酮类药物的困境。例如,肺炎支原体对其一线治疗药物大环内酯类的耐药率为80%~90%[7]。在全球病例中有近50万人为利福平耐药结核病,其中耐多药结核病占78%[8] 。左氧氟沙星为第二代喹诺酮类药物,我国批准左氧氟沙星用于6个月至18岁儿童吸入性炭疽暴露后。一项前瞻性安全性研究显示,左氧氟沙星导致儿科患者软骨损伤的风险不常见,在5年内临床上未监测到,或是可逆的[9]。本研究通过分析儿童左氧氟沙星应用案例,了解该药在儿童人群中的应用现状和安全性,为临床使用提供依据。
回顾性研究。选择2017年1月1日至2022年12月31日首都医科大学附属北京儿童医院和北京儿童医院保定医院住院患儿使用左氧氟沙星的病例。本研究通过首都医科大学附属北京儿童医院医学伦理委员会批准[批准文号:(2023)-E-104-R],并豁免知情同意。
收集患儿性别、年龄、体重、出院诊断、出院科室,左氧氟沙星的给药剂量、给药途径、给药疗程、不良反应(胃肠道不良反应、骨骼肌肉系统不良反应、QT间期延长、神经系统不良反应、低血糖、皮肤过敏/药物超敏反应、肝功能异常、肾功能异常、血液系统不良反应)情况,细菌培养及药敏试验结果、标本来源,对资料进行统计分析。
采用描述性分析方法。采用SAS v.9.4软件完成数据整理与统计分析,计量资料以M(IQR)表示;分类资料以频数、率或构成比表示。
共纳入全身使用左氧氟沙星患儿220例,其中首都医科大学附属北京儿童医院137例,占总出院人数0.034%;北京儿童医院保定医院83例,占总出院人数0.629%。其中,男123例(55.91%),女97例(44.09%)。年龄1个月14 d至16岁7个月27 d。学龄期、学龄前期、幼儿期占比较大,分别为70例(31.82%)、65例(29.55%)、44例(20.00%),占所有患儿数的81.37%。6个月以下患儿共9例,未见新生儿期使用者。结果见表1。

使用左氧氟沙星患儿年龄分布
Age distribution of children with Levofloxacin use
使用左氧氟沙星患儿年龄分布
Age distribution of children with Levofloxacin use
| 年龄分期 | 例数 | 百分比(%) |
|---|---|---|
| 青春期(>12 ~<18岁) | 19 | 8.64 |
| 学龄期(6~12岁) | 70 | 31.82 |
| 学龄前期(>3~<6岁) | 65 | 29.54 |
| 幼儿期(>1 ~3岁) | 44 | 20.00 |
| 婴儿期(>28 d~1岁) | 22 | 10.00 |
| 新生儿期(出生~28 d) | 0 | 0 |
| 合计 | 220 | 100.00 |
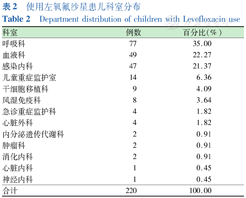
患儿分布在13个科室,其中前5名的科室分别为呼吸科77例,血液科49例,感染内科47例,儿童重症监护室(PICU)14例,干细胞移植科9例,共196例,占总病例数的89.08%。结果见表2。
使用左氧氟沙星患儿科室分布
Department distribution of children with Levofloxacin use
使用左氧氟沙星患儿科室分布
Department distribution of children with Levofloxacin use
| 科室 | 例数 | 百分比(%) |
|---|---|---|
| 呼吸科 | 77 | 35.00 |
| 血液科 | 49 | 22.27 |
| 感染内科 | 47 | 21.37 |
| 儿童重症监护室 | 14 | 6.36 |
| 干细胞移植科 | 9 | 4.09 |
| 风湿免疫科 | 8 | 3.64 |
| 急诊重症监护科 | 4 | 1.82 |
| 心脏外科 | 4 | 1.82 |
| 内分泌遗传代谢科 | 2 | 0.91 |
| 肿瘤科 | 2 | 0.91 |
| 消化内科 | 2 | 0.91 |
| 心脏内科 | 1 | 0.45 |
| 神经内科 | 1 | 0.45 |
| 合计 | 220 | 100.00 |
220例患儿共涉及10类疾病,前3位分别为肺炎150例,全身播散性结核病25例,脓毒症20例,共195例,占比86.63%。结果见表3。

使用左氧氟沙星患儿诊断分布
Diagnostic distribution of children with Levofloxacin use
使用左氧氟沙星患儿诊断分布
Diagnostic distribution of children with Levofloxacin use
| 诊断分布 | 例数 | 百分比(%) |
|---|---|---|
| 肺炎 | 150 | 68.18 |
| 全身播散性结核病 | 25 | 11.37 |
| 脓毒症 | 20 | 9.10 |
| 血液病合并感染(皮肤软组织、泌尿系统) | 16 | 7.27 |
| 导管相关感染 | 2 | 0.91 |
| 中枢神经系统感染 | 2 | 0.91 |
| 腹腔感染 | 2 | 0.91 |
| 感染性休克 | 1 | 0.45 |
| 化脓性关节炎 | 1 | 0.45 |
| X-连锁免疫缺陷病、肝脾脓肿、肺炎 | 1 | 0.45 |
| 合计 | 220 | 100.00 |
肺炎支原体感染102例,细菌感染121例,单一病原菌65例,2种以上病原体11例。肺炎克雷伯菌14例(16.09%),嗜麦芽窄食单胞菌14例(16.09%),鲍曼不动杆菌复合群10例(11.49%),金黄色葡萄球菌9例(10.34%),铜绿假单胞菌9例(10.34%),共计占比48.26%。其他包括结核分枝杆菌5例(5.75%),阴沟肠杆菌4例(4.60%),肺炎链球菌、大肠埃希菌各3例(各占3.45%),表皮葡萄球菌、溶血性葡萄球菌、产吲哚金黄杆菌各2例(各占2.3%),抗酸杆菌、恶臭假单胞菌、嗜水气单胞菌、洋葱伯克霍尔德菌、多食伯克霍尔德菌、脓肿分枝杆菌、洛菲不动杆菌、屎肠球菌、鲍曼醋酸钙不动复合杆菌、肠球菌属各1例(各占1.15%),均为多重耐药菌且前期治疗方案效果不佳。
支气管肺泡灌洗液28例(32.18%),血液标本24例(27.59%),痰标本20例(22.99%),占比82.76%。其他包括尿标本、术后切口处渗出物各4例,胸腔穿刺液3例,咽拭子、脑脊液各2例,腹腔积液1例。
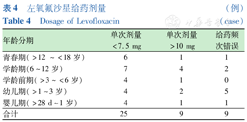
静脉用药176例(80.00%),口服用药39例(17.73%),静脉联合口服序贯5例(2.27%)。静脉途径给药剂量为4~15 mg/(kg·次),单次给药剂量为0.06~0.75 g/次。口服途径给药剂量为4~15 mg/(kg·次),单次给药剂量范围为0.075~0.300 g/次,每日1~2次用药。单次给药剂量<7.5 mg/kg者25例,其中静脉22例,口服3例;单次给药剂量>10 mg/kg者9例(诊断分别为:X-连锁重症联合免疫缺陷病合并全身血行播散性结核、急性非淋巴细胞性白血病合并脓毒血症、非霍奇金淋巴瘤合并脓毒血症、非霍奇金淋巴瘤合并肠道感染、全身播散性结核病合并多发软组织炎、非霍奇金淋巴瘤加强化合并皮肤感染、非霍奇金淋巴瘤合并脓毒血症、原发性免疫缺陷病合并肺炎),均为静脉给药;给药频次错误9例;不合理率占18.18%,见表4。患儿给药时长1~61 d,中位数8(6) d。除结核外,患儿给药时长1~56 d,中位数8(5) d。
左氧氟沙星给药剂量 (例)
Dosage of Levofloxacin (case)
左氧氟沙星给药剂量 (例)
Dosage of Levofloxacin (case)
| 年龄分期 | 单次剂量<7.5 mg | 单次剂量>10 mg | 给药频次错误 |
|---|---|---|---|
| 青春期(>12 ~<18岁) | 6 | 1 | 1 |
| 学龄期(6~12岁) | 7 | 4 | 2 |
| 学龄前期(>3~<6岁) | 4 | 1 | 0 |
| 幼儿期(>1~3岁) | 4 | 2 | 5 |
| 婴儿期(>28 d~1岁) | 4 | 1 | 1 |
| 合计 | 25 | 9 | 9 |
共发生122例不良事件。包括胃肠道反应(8例),低血糖反应(14例),肝功能异常(38例),肾功能异常(11例),血液系统异常(50例),皮疹(1例),未见骨骼肌肉系统、心脏系统、神经系统等其他不良事件。其中3例可能与左氧氟沙星相关,包括2例胃肠道不良反应[1例7月龄26 d患儿单次应用左氧氟沙星注射液15 mg/kg,静脉滴注第1天出现腹泻,持续14 d,临床治愈;1例10岁5个月患儿加用左氧氟沙星注射液10 mg/(kg·次),1次/d,后患儿出现恶心,无呕吐,食欲下降,未给予特殊处理,患儿自行好转]和1例皮疹(11岁11个月患儿给予左氧氟沙星注射液10 mg/kg静脉滴注后出现粟粒样皮疹,给予甲泼尼龙治疗5 d后皮疹消失)。其他不良事件与疾病相关,与左氧氟沙星可能无关,未发生左氧氟沙星相关的严重不良事件。
2019年估计有495万人死于耐药细菌,其中127万人直接归因于耐药病原体[10,11]。随着耐药菌的增加,喹诺酮类药物在儿科人群中的使用逐年增多,美国2000年至2018年门诊使用氟喹诺酮类药物的儿童共3 460万名,共有441 062例门诊氟喹诺酮类药物处方(每1 000人年5.5例),左氧氟沙星占25%[12]。我国2023年《国家抗微生物治疗指南》指出,在无其他低毒高效的抗菌药物可供选用时,尤其是重症患儿,可权衡利弊限制性选用喹诺酮类[13]。本研究显示,左氧氟沙星主要用于幼儿期、学龄前期和学龄期儿童,儿童安全性的评估显得更为重要。左氧氟沙星的使用科室基本分布在感染性疾病高发科室,主要用于肺炎、结核、脓毒症及血液病合并感染的患儿。对于非感染性疾病科室的使用,建议请感染科专家协助评估。
关于喹诺酮类药物在儿童中的使用,不同国家在不同疾病的指南中分别有推荐。国家结核病规划指南——儿童结核病管理(第2版):耐多药结核二线治疗方案推荐左氧氟沙星7.5~10.0 mg/(kg·次),2次/d,最大不超过750 mg[14]。2011年美国美国传染病学会3个月以上婴儿和儿童社区获得性肺炎的管理指南:流感嗜血杆菌、沙眼衣原体感染二线静脉用法选择左氧氟沙星,16~20 mg/(kg·d),12 h给药1次,>5~16岁8~10 mg/(kg·d),1次/d,最大日剂量750 mg;肺炎支原体感染左氧氟沙星用法,16~20 mg/(kg·d),12 h给药1次,最大日剂量750 mg[15]。本研究结果发现,左氧氟沙星的使用剂量为4~15 mg/次,最大剂量不超过750 mg。存在单次剂量不足,单次给药超量以及给药频次错误的问题。其中9例患儿单次剂量超过10 mg/kg,1例7个月26 d患儿使用左氧氟沙星15 mg/(kg·次)后出现腹泻,考虑可能与剂量偏大有关;1例11岁11个月儿童出现皮疹,考虑为左氧氟沙星给药频次超量,应为1次/d,实际为2次/d。因此,临床在使用过程中需要注意在保证疗效的前提下使用最小剂量,以减少对儿童的不良反应。本研究发现3例与左氧氟沙星相关的不良反应,1例腹泻(治愈),1例恶心(好转),1例皮疹(治愈),属于轻度不良反应,未发现严重不良反应。
研究显示,喹诺酮类抗菌药物在儿童中使用最常见的不良反应为胃肠道症状,其次为严重的过敏和皮肤反应及中枢神经系统影响,关节痛和关节病在儿童中相对少见,在停用喹诺酮类药物后症状消失,未发现长期后遗症[16]。日本新型喹诺酮类药物托氟沙星可用于全年龄段儿童,使用大环内酯类药物48 h不退热为启动时机。通过上市后自发报告持续收集药物不良反应信息[17],截至2019年10月,约有1 079万应用托氟沙星儿科患者,其中36例出现关节症状,基本均为轻度。但美国食品与药品监督管理局在喹诺酮类抗菌药物很多安全性方面有持续性警示。1987年第1个氟喹诺酮类药物环丙沙星上市,当时药品不良反应包括癫痫、颤抖、精神状态变化;1990年基于市场病例报告提出中枢神经系统的不良反应,包括颅内压升高和精神错乱;2004年不良反应项增加周围神经病变;2008年增加黑框警告:肌腱炎和肌腱断裂的不良反应,尤其是对于有一定风险的人群;2013年警示周围神经病变的严重不良反应,潜在发生迅速且有永久性风险,对于发生周围神经病变症状的患者应立即停止使用氟喹诺酮类药物;2016年警惕出现致残和可能的不可逆的严重不良反应,警告既往发生过任何严重不良反应者,应立即停止使用氟喹诺酮和避免使用氟喹诺酮类药物,建议氟喹诺酮类药物在没有其他治疗选择的时候保留使用;2018年增加严重低血糖警示和更新6种精神方面的不良反应(注意力、定向障碍、激惹、神经质、记忆缺失、谵妄)。本研究虽然显示了左氧氟沙星在儿童中使用的短期安全性较好,但因回顾性研究有一定的局限性,还需要进一步前瞻性的研究证实。
综上,左氧氟沙星仍为儿童感染性疾病二线用药,仅在早期治疗失败以及在批准用于儿童的其他抗菌药物不能使用时使用。必要时实施抗菌管理策略来限制氟喹诺酮的使用[18]。使用过程中需关注胃肠道、皮疹、肝肾功能、血液系统、血糖、心脏系统、神经系统等方面的指标,另外由于皮质类固醇和氟喹诺酮类药物联用会增加肌腱损伤风险,这些药物应避免联合使用。对于骨骼肌肉系统的远期不良反应需要更多的研究进一步证实。
所有作者均声明不存在利益冲突



























