
要提高下肢动脉硬化闭塞症腔内治疗的疗效,首先要正确评估和区分下肢动脉闭塞的病变性质,选择恰当的血管准备方式并对其结果做出正确评估,在此基础上才能决定到底是选择药物涂层球囊还是植入支架,而要植入支架应先了解每一款支架的性能特性,根据病变性质选择最合适的支架。这就是“ leave the right thing behind”理念。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
近20年来,下肢动脉硬化闭塞症(arteriosclerosis obliterans,ASO)的腔内治疗主要是以单纯球囊扩张(plain old balloon angioplasty,POBA)加镍钛金属裸支架(bare metal stent,BMS)植入为主要方式。随着所治疗的股腘动脉病变越来越复杂,这种简单粗放的治疗模式因其再狭窄、再闭塞(in-stent restenosis/reocclusion,ISR)率较高而越来越不令人满意。由此,以少放支架或少放长段支架为要义的“leave nothing behind(LNB)”理念应运而生,即以减容技术和药物涂层球囊(drug-coated balloon,DCB)的应用为技术基础,尽可能减少支架的应用。一段时间以来,这个理念广受业界同道的推崇。然而,并不是所有病例都能做到LNB的理想状况,由于病变性质的差异,诸如长段、慢性完全性闭塞(chronic total occlution,CTO)、钙化等复杂病变很难绝对做到LNB,支架的使用仍是一个重要的技术选项。然而,面对种类繁多、性能各异的支架,如何才能做出正确选择,将各种支架的特性真正发挥好,这就是所谓“leave the right thing behind”理念的由来。要正确理解其中“right”的含义,笔者认为可以从以下几个方面去思考。
ASO的病变性质,包括病变的长度,狭窄性病变还是CTO,血栓性病变为主还是硬化斑块为主以及病变的钙化程度等都是影响腔内治疗效果最为重要的因素,也是选择开通、血管准备和管腔维持方式的主要依据[1]。按照2015年的外周学术研究联盟(peripheral academic research consortium,PARC)的分级[2],狭窄性病变<50%者为轻度狭窄,50%~69%为中度狭窄,70%~99%为重度狭窄,100%则为闭塞性病变。病变长度≤1 cm者为局灶性病变,1 cm<病变长度<5 cm者为短病变,5 cm≤病变长度<15 cm者为中长病变,≥15 cm者为长病变。2007年的跨大西洋协会间共识(Trans-Atlantic Inter-Society Consensus,TASC)Ⅱ[3]和2019年的全球肢体解剖分级系统(global limb anatomic staging system,GLASS)[4]则均将股腘动脉病变长度>20 cm列为最高分级的4级病变。2017年的欧洲心脏病学会(European Society of Cardiology,ESC)指南则是将长度25 cm作为首选腔内治疗还是旁路手术的分界[5]。
动脉硬化狭窄继发血栓形成是CTO的一种常见形态,临床上可根据慢性病程短期加重的病史,超声或CT的影像提示以及腔内治疗术中导丝通过病变的手感等进行综合判断。
钙化是影响下肢动脉腔内治疗技术成功率和中远期通畅率的重要因素。钙化越严重,导丝通过病变越困难,即使现在有了众多头端克数不一的CTO导丝,但严重钙化病变的开通仍是一大难题,常需应用内膜下通过、逆行开通等技术手段加以辅助。钙化病变POBA效果常不理想,病变不易扩开,易产生夹层和弹性回缩。钙化也会影响DCB药物的转运和吸收。即使植入支架,扩张不良和形态不佳的支架通畅率也大受影响。因此,下肢动脉病变钙化的评估是非常重要的。常用的钙化评估方法有以下几种:(1)周围动脉钙化评分系统(peripheral arterial calcium scoring system,PACSS)[6],即在血管纵向的透视影像上无明显钙化者为0级,单侧且长度<5 cm者为1级,单侧且>5 cm者为2级,双侧且<5 cm者为3级,双侧且>5 cm者为4级。(2)Fanelli的圆周法[7],即在CT横断面上无钙化为0级;钙化占圆周0°~90°,长度<3 cm者为1a级,>3 cm者为1b级;钙化占圆周90°~180°,长度<3 cm者为2a级,>3 cm者为2b级;钙化占圆周180°~270°,长度<3 cm者为3a级,>3 cm者为3b级;钙化占圆周270°~360°,长度<3 cm者为4a级,>3 cm者为4b级。(3)PARC分级法[2]:局灶钙化,<180°(单侧)且长度<病变总长度的1/2;轻度钙化,<180°(单侧)且长度>病变总长度的1/2;中度钙化,180°(双侧)且长度<病变总长度的1/2;重度钙化,180°(双侧)且长度>病变总长度的1/2。血管腔内超声(intravascular ultrasound,IVUS)能更清晰地观察钙化在动脉壁中所处的位置和范围,对于浅层钙化的检测结果与主要依赖透视和造影进行评估的PACSS法和PARC法相符度高,同时也能更好地检测深层和突入管腔的钙化[8]。
尽管目前对于下肢动脉病变性质的评估手段已较为丰富,包括多普勒超声、CT血管造影、MR血管造影、数字减影血管造影、IVUS及光学相干断层扫描术等,但对病变性质的评估仍存在很大的不足,因为所有这些检测手段的结果都需进行人工研判,这就必然存在着一定的主观性和误差率。同时,现有的评估方法对CTO病变中的不同形态(纤维帽的形状、血栓、斑块、休眠血管及微通道等)仍然无法做出更精准的判断。ISR的性质判断也是如此,支架内闭塞物是以血栓形成为主还是内膜增生为主?增生性物质是富含水分还是慢性纤维化为主,判断同样也不够精准,更多是依靠导丝通过时的手感作为判断。所以,对病变性质的正确评估,未来需借助人工智能判读影像的方法来解决这个问题。
所谓血管准备是指应用球囊扩张或减容方式压缩或移除血管腔内导致狭窄或闭塞的内容物以获得管腔,并改善血管壁的顺应性,为后续管腔维持治疗创造条件。血管准备方式选择的依据就是对下肢动脉病变性质的正确评估。
球囊扩张是下肢动脉最为常用的血管准备方式,具有操作简单和费用较低等优势。理想的球囊扩张效果,即获得管腔最大的开放,<30%的残余狭窄和没有血流限制性夹层。球囊根据结构和作用原理的不同,大致可分为以下几种。
1.POBA:按球囊适配的输送导丝直径可分为0.035英寸(1英寸=0.025 4 m)、0.018英寸和0.014英寸三种。按球囊的顺应性可分为顺应性(顺应性>18%)、半顺应性(顺应性为10%~18%)和非顺应性球囊(顺应性为5%~10%)。半顺应性球囊因其有较好的通过性和循迹性,在下肢动脉应用最为普遍。非顺应性球囊因其球囊材质相对较硬,扩张时压力分布更为均匀,能较容易地扩开病变而对相邻区域血管的影响较小。同时,非顺应性球囊具有更高的爆破压,又称高压球囊,能以更高的压力扩张严重钙化等较难扩开的病变[9]。按球囊结构又可分为整体交换型和快速交换型两类。其中,整体交换型球囊因其推送性更好且便于经球囊推注造影剂等优点在下肢动脉应用更为广泛。
POBA的扩张方式可以按照目标血管的直径选择等比例球囊进行一次性扩张,也可以采用“递增式扩张”的方式,即选择多个不同直径的球囊由小至大渐次扩张,如靶血管的直径为D(mm),则依序选择D-2(mm)、D-1(mm)和D直径的球囊,有些钙化较重者还需用D+1(mm)进行扩张。“递增性扩张”方式可有序、渐次地扩张病变,对于减少夹层形成有一定意义,但尚缺乏前瞻性、随机对照的临床研究证据支持[9]。
2.特殊球囊扩张:所谓特殊球囊是指具有特殊结构和功能的球囊,包括以压力聚焦为作用原理的切割球囊和刻痕球囊,以压力控制为作用原理的“巧克力球囊”和以声压波裂斑为作用原理的冲击波球囊等。
广义的压力聚焦球囊包括切割球囊(美国波士顿科学公司)、双导丝球囊(Vascutrak、Ultrascore,美国碧迪公司)和刻痕球囊(Angiosculpt,荷兰飞利浦公司)等,国内也有数个品牌的产品,如Dekutting刻痕球囊(苏州鼎科公司)应用了独特的镍钛三角绕簧刻痕件技术,在保持了切割球囊的扩张性能的同时解决了因刻痕件质地过硬而不能把球囊做长的不足。压力控制型球囊的代表是“巧克力球囊”(美国美敦力公司),其表面由横向和纵向的镍钛约束丝形成类似于巧克力样的凹凸结构,在球囊充盈扩张时有导丝束缚的区域就会形成一个相对低压区,这种枕部和减压槽结合的结构在扩张时能产生一定的缓冲作用来减少球囊扩张对血管内膜的损伤,减少夹层的形成。
压力聚焦球囊和压力控制型球囊是通过对扩张压力的聚焦和限制来实现减少夹层形成的目的,在临床上应用日趋广泛,但对于严重钙化病变扩张效果往往并不理想。
冲击波球囊是将体外震波碎石的技术原理应用于动脉钙化病变的一种新型扩张技术,也叫血管内碎石术(intravascular lithotripsy,IVL)。其将声压波发射电极整合于半顺应性球囊之中,可脉冲式产生高达50 atm(1 atm=101.325 kPa)的冲击压力来震裂钙化斑块,继而以6 atm的低压力扩张来获得管腔。IVL作用时瞬间产生的50 atm正向波可有效裂碎钙化斑块,接近于0的负波压力则避免了对血管壁软组织的损伤,6 atm的球囊扩张压力也减少了以往使用高压球囊扩张所带来的动脉内膜损伤,为处理下肢动脉严重钙化病变提供了新的有效手段[10]。
减容是指利用专用器械进行血栓或斑块清除,从而获得管腔并改善管壁的顺应性,以利于载药器械的药物吸收和转运。现有证据表明减容可有效减少支架的应用。不同的减容器械有着各自不同的适用范围,需要根据病变性质和部位进行正确选择。
血栓性病变的处理可使用导管溶栓术(catheter-directed thrombolysis,CDT)、经皮机械祛栓装置(percutaneous mechanical thrombectomy,PMT)和机械血栓抽吸系统(aspiration mechanical thrombectomy,AMT)等方式进行处理。利用多裂孔的灌注导管行CDT治疗是安全、有效、经济的祛栓方式,操作简单且无需特殊设备,仍是目前临床上应用较为广泛的腔内祛栓方法。但其一般用时较长,不太适合病情急重、需要迅速复通血管的病例,理论上也存在着引起出血并发症的风险。国内可使用的PMT主要有Rotarex(美国碧迪公司)和AngioJet(美国波士顿科学公司),可起到祛除血栓和快速复通血管的目的。前者可治疗急性和亚急性血栓性病变,后者主要用于急性病变。AMT有Acostream(北京先瑞达公司)和Indigo(上海健适公司)两种,尤其是前者,有着4F~12F的不同直径和135 cm的工作长度,可有效弥补PMT不能用于膝下<3 mm的小直径动脉的不足。临床上可根据不同病程、不同部位的血栓性病变将上述多种血栓减容技术联合应用,以达到更好的祛栓效果。
斑块切除系统主要有定向斑块切除系统(directional atherectomy,DA)的SilverHawk/TurboHawk(美国美敦力公司)、准分子激光斑块切除系统(excimer laser atherectomy,ELA,荷兰飞利浦公司)、旋转式斑块切除系统(rotational atherectomy,RA)的Jetstream(美国波士顿科学公司)和轨道式斑块切除系统(orbital atherectomy,OA)等。DA的使用适应证主要是短段、多处、分散病变以及跨关节病变和钙化病变,Turbohawk目前有LXM和SXC等型号,分别适用于3.5~7.0 mm和2.0~4.0 mm直径的血管。目前国内使用的ELA主要是Turbo-elite导管,直径为0.9~2.5 mm,适用于直径2 mm以上血管的CTO病变和ISR。即将在国内上市的Jetstream,理论上可用于从血栓至钙化的不同性质的病变,包括XC(刀头可扩展)型和SC(单刀头)型,XC型有2.1 mm/3.0 mm 和2.4 mm/3.4 mm 两种规格,分别适用于3.0 mm和4.0~ 5.0 mm以上直径的血管。SC型有1.6 mm和1.85 mm两种,分别适用于2.0~2.5 mm和2.6~3.0 mm直径的血管[11]。OA系统国内尚未上市。
血管准备结果评估的准确性,关系到是否需要植入支架这一选择的正确与否。理想的血管准备要求是最大限度地获得管腔的开放,最低限度的弹性回缩导致的残余狭窄(<30%)和没有血流限制性夹层形成。对于夹层的评估,目前仍是沿用的冠状动脉NHLBI分类法[12],即A型:血管腔内少许内膜撕裂透亮影,造影剂排空大致正常;B型:平行的内膜撕裂成双腔,无明显造影剂滞留或轻度排空延迟;C型:假腔形成伴造影剂排空延迟;D型:螺旋形夹层伴造影剂滞留;E型:新出现的持续造影剂充盈缺损;F型:管腔完全闭塞。一般认为,A、B两型属于非血流限制性夹层,可不植入支架,而C型以上者为限流性夹层,需植入支架。在临床实际应用中对夹层分型更多地需依赖术者的主观判断,具有一定的漏诊率和误判率,同一个夹层不同的术者、不同的造影角度都可能得出不同的评估结果。动脉压力梯度测定和IVUS等方法可提高对夹层性质判断的准确性。但上述评估方式都仅是对单一夹层的形态进行评估,对夹层长度和多个夹层的累积效应对血流动力学和通畅率的影响未作考虑。
新近发表的Delphi共识小组的DISFORM研究对股腘动脉的夹层做了新的分型,其从管腔直径(D)、螺旋形态(S)、对血流的影响(F)和夹层的形态包括数量及长度(M)共四个维度进行评估,并据此作出是否需要植入支架的推荐意见(表1、图1)[13]。DTSFROM分型看似复杂,但只要理解其四个维度分型的内在逻辑关系,即从D至M进行逐层递减式的分析判断,该分型方法还是比较简单、实用的。

外周动脉夹层DISFORM分型
外周动脉夹层DISFORM分型
| 参数 | 描述 | ||
|---|---|---|---|
| D | 直径减小 | D0 | 直径减小<50% |
| D1 | 直径减小50% | ||
| S | 螺旋形态 | S0 | 无螺旋(线性) |
| S1 | 任何螺旋形态 | ||
| F | 血流影响 | F0 | FLIPI0:正常顺向血流 |
| F1 | FLIPI1:顺向血流减少 | ||
| F2 | FLIPI2:轻微顺向血流外溢 | ||
| F3 | FLIPI3:夹层段血流中断, 仅侧支充盈 | ||
| M | 形态 | M0 | 单一夹层,长度<2 cm |
| M1 | 多个夹层,长度<2 cm或 单一夹层,长度2 cm | ||
| M2 | 多个夹层,长度2 cm | ||
注:FLIPI为外周介入中的血流影响程度
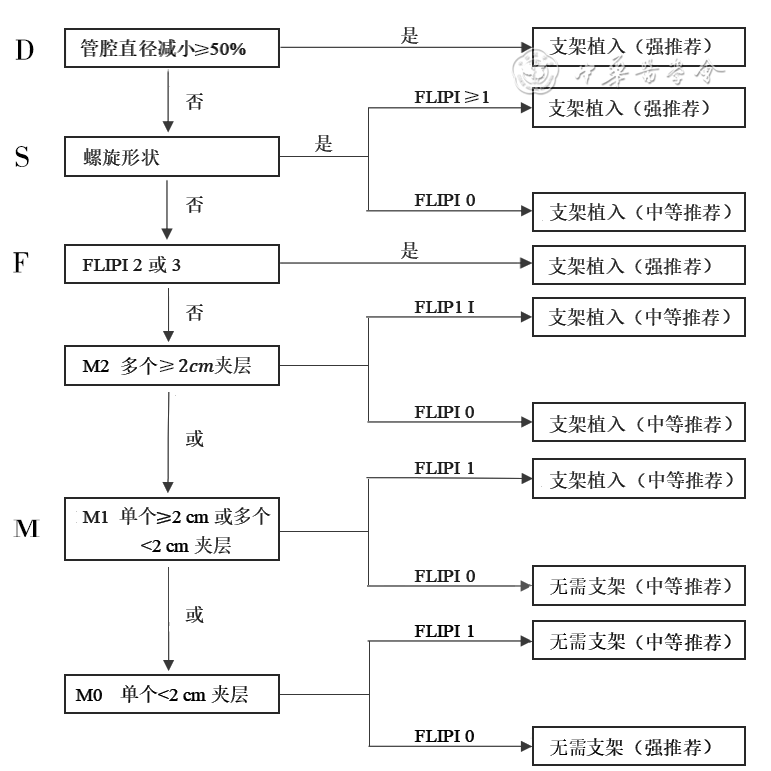

注:FLIPI为外周介入中的血流影响程度
完成血管准备以后,在对其结果作出准确评估的基础上才能选择应用DCB还是植入支架来作为管腔维持的方式。一般认为,出现30%以上的残余狭窄、C级以上的限流性夹层、及动脉压力梯度差>20 mm Hg(1mm Hg=0.133 kPa)就应该植入支架[9]。
目前临床上应用的下肢动脉支架大致可分为标准镍钛雕刻支架(standard nitinol stent,SNS)、镍钛编织支架、覆膜支架和紫杉醇药物洗脱支架(drug-eluting stent,DES)。SNS品牌众多,性能特点各异,第一款进入国内市场的高柔顺性支架EverFlex(美国美敦力公司)、EverFlex升级版Entrust(美国美敦力公司)、多维螺旋结构的Lifestent(美国碧迪公司)、中段开环两端闭环的复合支架(Innova,美国波士顿科学公司)、全联接支架(SmartFlex,美国Cordis公司)、薄壁支架Pulsal18(北京百多力公司)和Absolute(美国雅培公司)等。尽管这些支架在径向支撑力、柔顺性及断裂率等方面较以往的支架都有较大改进,但随着治疗的长病变越来越多,SNS的再狭窄率较高仍是不可回避的问题。因此,SNS目前更多的是用作DCB使用后的补救支架。
具有一定仿生性能的编织支架(Supera,美国雅培公司)以其强支撑力和高柔顺性在高钙化和跨关节病变具有一定的优势[14]。覆膜支架(Viabahn,美国戈尔公司)因有覆膜的机械屏障,具有阻隔动脉硬化进展和内膜增生的优势,Viastar和Reline等临床研究结果都显示其对于长段股腘闭塞性病变和ISR都有着良好的疗效[15, 16]。
紫杉醇药物支架目前有Zilver PTX(美国库克公司)和Eluvia(美国波士顿科学公司)两款。前者是直接涂药、无聚合物的药物支架,也称药物涂层支架;后者则是应用了特殊的聚合物涂层技术,是真正意义上的DES,其药物释放时间可长达1年,相对而言可能具有更好的抗内膜增生效果和更好的通畅率。头对头比较这两款药物支架的RCT研究Imperial随机对照研究结果显示,Eluvia组和Zilver PTX组2年一期通畅率分别为83.0%和73.1%,靶病变再干预率分别为12.7%和20.1%[17]。在该研究的日本人群中,两款支架的2年一期通畅率分别为88.5%和80.4%,靶病变再干预率分别为5.6%和18.5%[18]。单面涂药的Zilver PTX单位面积紫杉醇剂量为3.0 μg/mm2,Eluvia为0.167 μg/mm2,药物总剂量均远低于同等长度的DCB。
DES理论上适用于需要植入支架的任何形态的股腘动脉病变,因其具有紫杉醇药物的抗增生作用,与SNS相比更适合于长段、CTO、钙化等复杂病变,且全程应用比局部、补救性应用者效果更佳[19]。然而,DES毕竟是以SNS为支架平台的,同样存在SNS的径向支撑力相对较弱和有一定的断裂率等不足,因此,对于钙化严重且血管准备不良、管腔获得不佳和跨关节应用者应持谨慎态度,最小直径为6 mm的DES也不宜用于<4.5 mm的血管[20]。在DES使用前的血管准备上,对于长段、CTO、钙化、全程内膜下通过及高龄CLTI患者等应用场景,需要植入支架的概率较大时可以采取相对简单的血管准备方式,但方式可以简化,管腔获得不能马虎,因为DES植入后展开不良和残余狭窄>25%也是其术后发生再狭窄的重要危险因素[21]。
SNS、编织支架、覆膜支架和DES有着各自不同的作用机理和应用场景。SNS更多的是作为DCB使用后的补救性支架。编织支架更适合于严重钙化和跨关节病变,但在股浅动脉近端使用存在定位不准的问题。覆膜支架更适用于长段、CTO、合并血栓及ISR等病变,但也存在边缘狭窄、腘动脉管径过小、覆盖膝关节周围网和股深动脉等不足或限制。由于通畅率的不同,应尽量避免将编织支架、覆膜支架和DES等特殊支架与SNS混合应用,确需混用时也应尽量减少SNS的长度,以减小SNS对通畅率带来的“短板效应”。特殊支架则可以在合理范围内联合应用,以弥补各自的缺点与不足,如覆膜支架与DES联用以避免覆盖股深动脉和解决边缘狭窄,编织支架与DES联用可以解决前者定位不准和后者不适合跨关节等问题,覆膜支架与编织支架联用以解决严重钙化病变扩张不良、扩张破裂和支架支撑力不够等问题(即pave and crack技术)。
与股腘动脉不同,主髂动脉闭塞症(aortoiliac occlusive disease,AIOD)腔内治疗的5年一期通畅率可达70%以上,二期通畅率接近90%[22],其疗效已接近传统旁路手术,且具有明显微创优势,已成为AIOD治疗的首选方式。
AIOD腔内治疗以POBA加支架植入为主,合并血栓者可结合CDT、PMT及AMT等祛栓治疗,不推荐使用特殊球囊、斑块切除、DCB及DES等方法[23]。在支架类型的选择上,相较BMS,覆膜支架在长段、钙化等复杂病变具有一定优势[24],尤其是有助于防止钙化髂动脉破裂。BMS和覆膜支架都有自膨式和球扩式两种。自膨式支架长度选择更多,柔顺性好,更适用于长段、扭曲的血管病变;球扩式支架定位精确且径身支撑力强,更适用于短段、开口、钙化病变。
常用的AIOD腔内重建方式主要有对吻/平行支架植入、一体化大支架植入和覆膜支架腔内重建腹主动脉分叉技术(covered endovascular reconstruction of the aortic bifurcation,CERAB)三种。对吻/平行支架技术最为简单,疗效满意,适用范围广,可用于从单纯髂动脉病变到累及肾动脉水平腹主动脉的各型AIOD。一体化腹主动脉支架重建更符合腹主动脉分叉部血流动力学的生理状态,但对髂动脉和入路血管的直径等血管条件及病变通过方式有更高的要求,临床上并不常用。CERAB是应用球扩式覆膜支架可变径的特点来相对生理地重建腹主动脉分叉,减少分叉处支架交汇部形成的“间隙”,从而减少血液湍流导致的血栓形成,减少剪切应力引起的内膜增生,改善通畅率[25]。但从一项荟萃了66个研究,9 319例AIOD患者治疗结果的研究表明,标准的对吻支架技术与CERAB技术的通畅率差异并无统计学意义[22],而且CERAB技术对于累及长段腹主动脉的病变有覆盖肠系膜下动脉和支架在近肾动脉处球囊扩张释放时更易引起内脏动脉栓塞等缺点,为保留肠系膜下动脉而行烟囱CERAB似更有“画蛇添足”之嫌。笔者认为,还是应根据不同的病变形态和长度来选择重建方式。单纯髂动脉病变可行单侧或对吻支架技术,髂动脉病变合并腹主动脉中下段病变可应用CERAB技术,长段乃至平肾的AIOD还是以对吻/平行支架技术更为安全、可靠。采用CERAB重建方式要注意把握该方法的技术要点和支架直径的选择原则[26]。
综上所述,正确的“leave the right thing behind”理念就是要对病变性质做好正确的评估,在此基础上选择恰当的血管准备方式并对其结果做好正确的评估,同时要正确了解每一种支架的特性和使用适应证,从而根据不同病变、不同部位及不同血管准备结果来选择DCB或各种类型的支架,必要时可联合应用不同类型的器具,以起到取长补短之效。
包俊敏. 如何正确理解“leave the right thing behind”理念?[J]. 中华血管外科杂志, 2023, 8(3): 246-252. DOI: 10.3760/cma.j.cn101411-20230627-00060.
所有作者均声明不存在利益冲突



























