
诺卡菌病是由诺卡菌引起的机会性感染性疾病,可经血流播散累及多个器官。由豚鼠耳炎诺卡菌所致的诺卡菌病少见,通常发生于免疫功能低下者,临床症状及实验室、影像学检查无特异性。本文报道1例罕见的免疫功能正常者感染豚鼠耳炎诺卡菌引起的播散性诺卡菌病,以提高临床对该疾病的认识及诊疗。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者女,78岁,农民,因“发热4 d”于2022年2月20日门诊收入院。患者4 d前无明显诱因出现发热,体温最高39.3 ℃,无畏寒、寒战,伴食欲差、恶心,无呕吐,2022年2月18日当地医院给予抗感染、退热等治疗(具体不详),患者仍反复发热,伴乏力。于我院门诊行胸部CT检查可见右肺上叶后段见空洞性病变、胸腔积液等(图1,2)。既往有“高血压病”10年余,平素使用降压药物(具体不详),血压控制可;“脑梗死”1年,未遗留后遗症;“血糖升高”2 d。个人史等无特殊。入院体检:体温38.0 ℃、脉率79次/min、呼吸频率20次/min、血压160/73 mmHg(1 mmHg=0.133 kPa)。浅表淋巴结未触及肿大,咽部无充血、扁桃体无肿大,双肺呼吸音粗、双肺未闻及啰音。实验室检查:新型冠状病毒核酸测定阴性;血气分析(未吸氧):pH值7.45,二氧化碳分压35 mmHg,氧分压92 mmHg;血钾2.91 mmol/L;空腹血糖4.92 mmol/L,糖化血红蛋白6.5%;血常规:中性粒细胞百分比(N%)80.10%,中性粒细胞计数(NEU)6.74×109/L,淋巴细胞百分比(Lym%)10.20%,淋巴细胞计数(Lym)0.86×109/L,余未见异常;C反应蛋白(CRP)24.19 mg/L,血清淀粉样蛋白A(SAA)93.44 mg/L,降钙素原0.367 μg/L,ESR为39.00 mm/1 h,IL-6为51.6 ng/L,铁蛋白783.97 μg/L;B型钠尿肽314 ng/L,D-二聚体1.50 mg/L;肝功能:总蛋白68 g/L,白蛋白42 g/L,均在正常参考值范围内。入院初步诊断“右肺空洞性质待定:肺脓肿?肺癌?胸腔积液、电解质紊乱(低钾血症)、高血压病、陈旧性脑梗死”,给予哌拉西林(4.5 g,1次/8 h)联合莫西沙星(0.4 g,1次/d)抗感染等治疗。为明确病灶性质于2022年2月21日行胸部增强CT检查,可见右肺上叶空洞性病变并均匀强化,符合感染性病变并脓肿形成(图3),患者及家属拒绝行支气管镜检查进一步明确病变性质,遂调整为亚胺培南(1 g,1次/8 h)加强抗感染;2月24日尿常规示酵母菌101.40/μl,加用氟康唑(0.2 g,1次/d,静脉滴注)抗真菌;行曲霉血清学试验、真菌D-葡聚糖检测、血培养(5 d)鉴定及药敏、风湿及免疫相关抗体、结核杆菌抗体、肿瘤标志物等均未见异常。因患者仍间断发热,考虑肺脓肿革兰阳性球菌感染风险大,为提高肺内药物浓度,加用利奈唑胺(0.6 g,1次/12 h)覆盖金黄色葡萄球菌、链球菌及MRSA等。
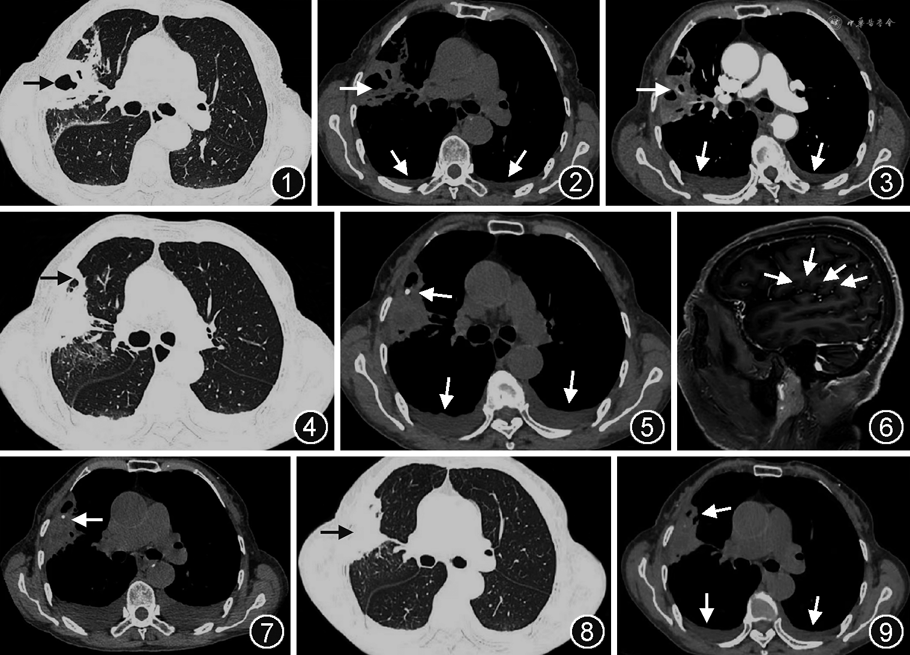

2022年2月27日患者出现神志恍惚、谵妄,急查血气(吸氧浓度33%)示pH值7.56,二氧化碳分压30 mmHg,总二氧化碳分压27.80 mmHg,剩余碱4.7 mmol/L,标准碳酸氢盐29.00 mmol/L,钠111.00 mmol/L、氯78 mmol/L,患者呼吸性碱中毒合并代谢性碱中毒,考虑摄入不足及感染消耗所致低钠低氯血症并出现意识状态改变;治疗后复查血常规:N%为67.60%,NEU为3.48×109/L,Lym%为22.80%,Lym为1.67×109/L,淋巴细胞恢复正常;胸部CT可见右肺上叶空洞性病变较前缩小(图4,5),颅脑MRI及增强可见脑内多发斑点状、小结节状异常强化影(图6),感染性病变与转移瘤待鉴别,因家属拒绝创伤性检查,且亚胺培南难于透过血脑屏障,遂调整为美罗培南(1 g,1次/8 h)继续抗感染,行PET-CT检查见右肺上叶高密度影并FDG代谢增高(图7)、脑内异常FDG代谢增高灶、右侧侧脑室后角局限显示欠清并FDG代谢增高,均考虑感染所致;双肾FDG代谢欠均匀,不除外感染。至此,考虑患者存在肺脓肿、颅脑感染、尿路感染,但致病菌不明确。为明确致病菌行腰椎穿刺术,并留取脑脊液送基因二代测序(next generation sequencing,NGS)。3月11日脑脊液NGS结果回示诺卡菌属(序列数7),豚鼠耳炎诺卡菌(序列数6)。根据PET-CT检查及脑脊液NGS结果,患者豚鼠耳炎诺卡菌病血流感染诊断明确,已播散至肺、脑、肾多部位,加用足量磺胺甲噁唑/甲氧苄啶(SMZ,2.4 g,1次/6 h)治疗。患者治疗后复查血常规、电解质、肝肾功能均未见异常;胸部及输尿管全程CT示右肺上叶空洞性病变较前略减小(图8,9);输尿管全程未见异常。于2022年3月16日好转出院,出院后继续口服利奈唑胺和SMZ治疗。4月28日患者胸部CT示右肺上叶空洞性病变明显减小;自6月4日停用利奈唑胺,口服SMZ(0.96 g,1次/6 h)维持治疗6个月,出院6个月及1年后电话随访,患者一般情况良好,病情未复发。
诺卡菌属是革兰阳性需氧放线菌,常见于土壤、腐烂的植被、水和空气中[1, 2]。通常在免疫功能低下的宿主中引起机会性感染,其中糖尿病、人类免疫缺陷病毒感染和移植后状态是其最常见的危险因素[3]。诺卡菌最常感染人体肺部,其次为中枢神经系统、皮肤等脏器,甚至可通过血液播散导致严重危及生命的感染,如骨髓炎和诺卡菌败血症[4, 5]。与其他诺卡菌相比,豚鼠耳炎诺卡菌病例仅占所有诺卡菌感染的0.3%~2.9%[4,6],在免疫功能正常者中感染更是少见[7]。本患者入院前发现血糖升高,入院后空腹血糖、糖化血红蛋白均正常;淋巴细胞偏低,给予抗感染后升至正常;且结核、肿瘤、风湿及免疫抗体等检查均无异常,不考虑存在免疫抑制情况。患者以发热起病,后出现低氧血症,其临床表现不典型,确诊前给予经验性广谱抗菌药物联合抗真菌药物治疗,效果欠佳。该患者低氧血症给予吸氧、气道管理后纠正,考虑患者胸腔积液使其通气不足有关,亦不排除颅内感染造成意识改变及颅内压增高影响呼吸中枢。
诺卡菌感染以化脓性炎症为主,可形成急性化脓性肺炎、孤立的肺脓肿或散在的粟粒样浸润,慢性病灶表现为进行性纤维化样改变,甚至合并肉芽肿改变[8]。所以,诺卡菌感染影像学以结节影、斑片渗出、实变影多见,其内可有液化或坏死,也可形成空洞,引起周围播散,导致胸膜增厚、脓胸或直接侵犯胸壁[9, 10, 11, 12, 13]。本例患者胸部CT右肺上叶病灶呈片状实变,内见空气支气管相及含气空洞影;增强CT示病灶均匀强化,中心液性密度未见强化,双侧胸膜局限增厚等无特异性影像表现,因此早期诊断困难,需与侵袭性真菌病、肺结核、肺癌、肉芽肿性血管炎等疾病进行鉴别。
诺卡菌病确诊需要明确病原微生物[11]。诺卡菌普通培养3~7 d后才可缓慢生长形成白色菌落,明显繁殖则需要3周[11,14]。因其生长缓慢、阳性检出率低等原因,普通培养方法易造成漏检,从而延长诊断时间,导致错过最佳治疗时机。本例患者血、脑脊液培养均未能提供确诊依据,但脑脊液NGS回报为豚鼠耳炎诺卡菌。由于诺卡菌非正常的定植菌,且造成培养基污染的可能性不大,因此患者身体来源的标本分离出诺卡菌往往提示感染[15]。
诺卡菌感染以抗菌药物治疗为主[2],但药敏试验存在种属差异。诺卡菌的流行病学和耐药性分析表明,所有诺卡菌菌株都对利奈唑胺敏感,其次是阿米卡星(99.3%)和磺胺甲噁唑/甲氧苄啶(99.1%)[16]。国内指南推荐诺卡菌病首选一线方案为口服磺胺甲噁唑/甲氧苄啶药物,疗程为3~4个月[17]。豚鼠耳炎诺卡菌作为诺卡菌属一种亚型,通常对阿莫西林-克拉维酸、氨苄西林等β-内酰胺类药物具有耐药性,对磺胺类药物、利奈唑胺、阿米卡星及万古霉素敏感[16,18];严重肺部感染、中枢神经系统受累和播散性感染等建议将磺胺类药物和阿米卡星与碳青霉烯或第三代头孢菌素联合使用[3,18, 19, 20]。豚鼠耳炎诺卡菌感染需要长期的药物治疗,其中免疫功能正常者建议持续治疗6个月,免疫抑制患者最长持续1年[19, 20],其确切的持续时间则取决于对治疗的反应和疾病的解决。本例诺卡菌感染患者已由严重肺部感染经血流播撒至脑和肾脏,初始给予足量SMZ联合利奈唑胺、美罗培南治疗,患者症状好转后出院继续SMZ和利奈唑胺治疗,2个月后当地复查胸部CT提示病灶明显减少,3个月后改为SMZ维持治疗半年,随访1年病情未复发。
本例免疫功能正常的豚鼠耳炎诺卡菌感染者临床症状不典型,实验室、影像学检查缺乏特异性,确诊需依据病原学,NGS有助于疾病的快速诊断,急性感染早期应联合足量抗生素治疗,待病情稳定后,使用单药或联合维持治疗并定期随访复查。
张龙志, 山长婷, 张守智, 等. 豚鼠耳炎诺卡菌致免疫功能正常者播散性诺卡菌病1例[J]. 中华结核和呼吸杂志, 2023, 46(11): 1127-1130. DOI: 10.3760/cma.j.cn112147-20230516-00243.
所有作者声明无利益冲突



























