
孤立性远端深静脉血栓形成(IDDVT)是指仅累及小腿深静脉的血栓形成过程,占所有下肢深静脉血栓形成(DVT)的30%~50%。研究表明,IDDVT具有向近端深静脉扩散的潜在风险,严重时可引起肺栓塞(PE)。在抗凝治疗方面,近端DVT和PE得到了深入且广泛的研究,目前已有一套基于高质量证据的标准化治疗方案。而IDDVT因现有临床研究结论迥异且缺乏高质量随机对照试验,其抗凝治疗策略尚无共识。本文重点对IDDVT后是否抗凝、抗凝药物选择、抗凝剂量选择以及抗凝疗程选择进行综述。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
下肢远端深静脉,也称为膝下深静脉、小腿深静脉,包括3支轴向静脉(腓静脉、胫前静脉、胫后静脉)及两组肌肉静脉(比目鱼肌静脉、腓肠肌静脉),这些静脉最终均汇入腘静脉[1]。孤立性远端深静脉血栓形成(isolated distal deep vein thrombosis,IDDVT)是指累及一条或多条小腿深静脉,但没有累及腘静脉及以上的血栓形成过程,属于静脉血栓栓塞症(venous thromboembolism,VTE)的一种类型[2]。IDDVT的确切发病率尚不清楚,据统计,IDDVT占所有下肢深静脉血栓形成(deep vein thrombosis,DVT)的30%~50%[3]。多项研究表明[4, 5, 6],IDDVT具有向近端静脉扩散的潜在风险,严重时可引起肺栓塞。不同于近端DVT,IDDVT的抗凝治疗仍有广泛争议,目前存在以下问题:(1)缺乏大规模高质量随机对照试验(randomized controlled trial,RCT);(2)现有临床研究结论之间彼此矛盾;(3)各指南推荐意见尚不统一(表1)。基于此,本文重点对IDDVT后是否抗凝、抗凝药物选择、抗凝剂量选择以及抗凝疗程选择进行综述,另外,本文还对合并特殊临床情况的IDDVT患者的抗凝策略进行了简略回顾,以便于临床医生进行个体化治疗。

国内外各指南在IDDVT抗凝治疗方面的推荐意见
国内外各指南在IDDVT抗凝治疗方面的推荐意见
| 机构(年份) | 抗凝适应证(证据级别) | 抗凝药物类型(证据级别) | 抗凝剂量(证据级别) | 抗凝疗程(证据级别) |
|---|---|---|---|---|
| ACCP(2016)[7] | 存在严重症状或血栓进展危险因素(2C) | - | 治疗剂量(1B) | 有可逆性诱因或诱因不明:3个月(1B) 活动性肿瘤:>3个月(1B) |
| ESC(2018)[8] | - | - | 复发风险低:低剂量;复发风险高:治疗剂量 | 复发风险低:4~6周;复发风险高:3个月 |
| THANZ(2019)[9] | - | - | - | 有可逆性诱因:6周(1B);诱因不明或诱因持续存在:3个月(1B) |
| ESVS(2021)[10] | 有症状、存在血栓进展危险因素、出血风险低(2C) | DOAC(1C) | - | 一般人群:3个月(1A);活动性肿瘤:>3个月(2C) |
| 中国IDDVT诊疗建议(2021)[11] | 出血风险低 | DOAC、低分子肝素、华法林 | 治疗剂量 | 未合并血栓进展因素:3个月;合并血栓进展因素:>3个月 |
注:-为无此项。IDDVT为孤立性远端深静脉血栓形成;ACCP为美国胸科医师协会;ESC为欧洲心脏病协会;THANZ为澳大利亚和新西兰血栓与止血协会;ESVS为欧洲血管外科协会;DOAC为直接口服抗凝药
IDDVT临床转归主要包括血栓溶解、血栓近端扩散[扩散至近端深静脉和(或)肺动脉]、复发性VTE以及血栓后综合征。由于现有临床研究结果异质性很大,是否对IDDVT进行抗凝治疗仍然是VTE领域最具争议的话题之一。2016年美国胸科医师协会(ACCP)[7]建议对存在严重症状或血栓扩散危险因素(D-二聚体升高、血栓范围广泛、血栓靠近腘静脉、无可逆性血栓形成诱因、活动期癌症、VTE既往史、住院状态)的IDDVT进行抗凝治疗而非超声监测。而2021年欧洲血管外科协会(ESVS)[10]并未明确指出适合抗凝的患者群体,认为应根据症状、血栓扩散风险和出血风险综合决定是否行抗凝治疗。需要注意的是,两部指南均强调其证据级别很低(2C),亟需大规模RCT研究证实。另外,2021年中国IDDVT诊疗建议[11]对抗凝持更积极的态度,认为出血风险较低的急性IDDVT患者均应接受抗凝治疗。
1. 支持抗凝:约15%未经治疗的IDDVT可向腘静脉及以上扩散,最终可能导致肺栓塞的发生[7]。ACT研究[12]是一项纳入了70例急诊IDDVT患者的RCT(表2)。该研究表明,随访3个月时主要临床结局(包括血栓近端扩散、肺栓塞、致死性VTE、大出血的复合结局)在非抗凝组中的发生率高于抗凝组,但差异无统计学意义(11.4%比0,P=0.11)。另外,该研究还发现,与接受抗凝治疗的患者相比,未接受抗凝治疗的患者更可能出现疼痛加重(6/35比0/35,P=0.03)。
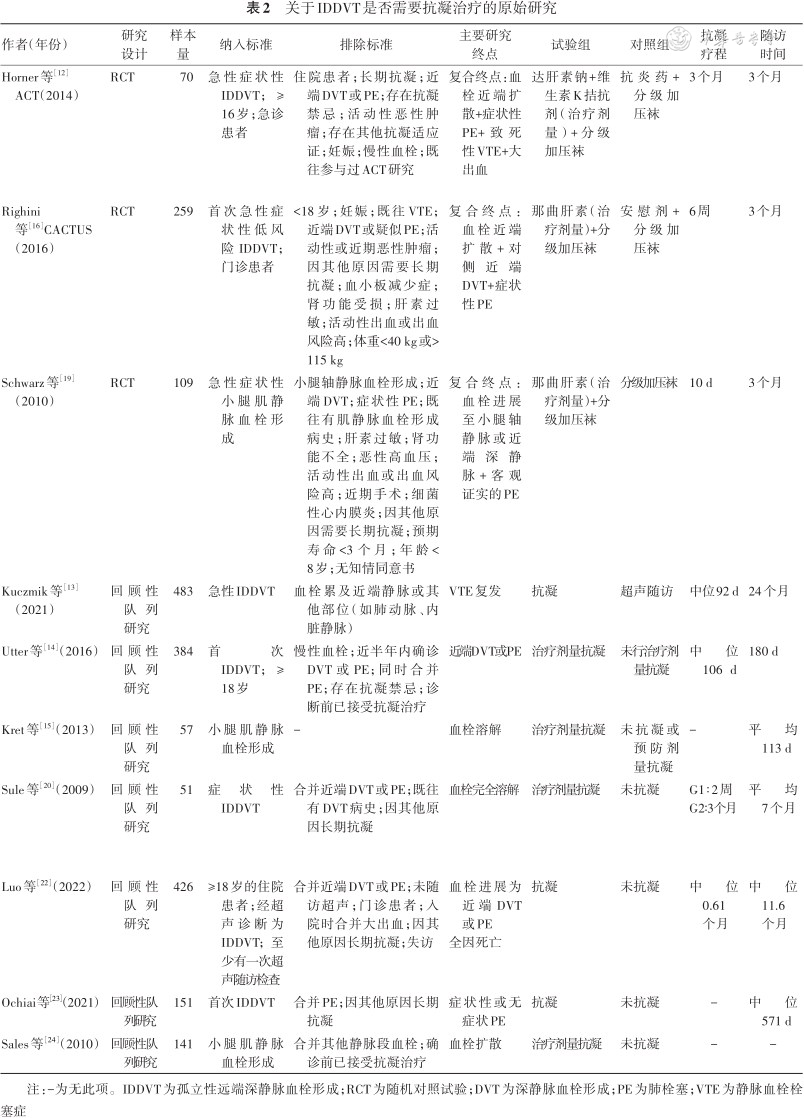
关于IDDVT是否需要抗凝治疗的原始研究
关于IDDVT是否需要抗凝治疗的原始研究
| 作者(年份) | 研究设计 | 样本量 | 纳入标准 | 排除标准 | 主要研究终点 | 试验组 | 对照组 | 抗凝疗程 | 随访时间 |
|---|---|---|---|---|---|---|---|---|---|
| Horner等[12]ACT(2014) | RCT | 70 | 急性症状性IDDVT;≥16岁;急诊患者 | 住院患者;长期抗凝;近端DVT或PE;存在抗凝禁忌;活动性恶性肿瘤;存在其他抗凝适应证;妊娠;慢性血栓;既往参与过ACT研究 | 复合终点:血栓近端扩散+症状性PE+致死性VTE+大出血 | 达肝素钠+维生素K拮抗剂(治疗剂量)+分级加压袜 | 抗炎药+分级加压袜 | 3个月 | 3个月 |
| Righini等[16]CACTUS(2016) | RCT | 259 | 首次急性症状性低风险IDDVT;门诊患者 | <18岁;妊娠;既往VTE;近端DVT或疑似PE;活动性或近期恶性肿瘤;因其他原因需要长期抗凝;血小板减少症;肾功能受损;肝素过敏;活动性出血或出血风险高;体重<40 kg或>115 kg | 复合终点:血栓近端扩散+对侧近端DVT+症状性PE | 那曲肝素(治疗剂量)+分级加压袜 | 安慰剂+分级加压袜 | 6周 | 3个月 |
| Schwarz等[19](2010) | RCT | 109 | 急性症状性小腿肌静脉血栓形成 | 小腿轴静脉血栓形成;近端DVT;症状性PE;既往有肌静脉血栓形成病史;肝素过敏;肾功能不全;恶性高血压;活动性出血或出血风险高;近期手术;细菌性心内膜炎;因其他原因需要长期抗凝;预期寿命<3个月;年龄<8岁;无知情同意书 | 复合终点:血栓进展至小腿轴静脉或近端深静脉+客观证实的PE | 那曲肝素(治疗剂量)+分级加压袜 | 分级加压袜 | 10 d | 3个月 |
| Kuczmik等[13](2021) | 回顾性队列研究 | 483 | 急性IDDVT | 血栓累及近端静脉或其他部位(如肺动脉、内脏静脉) | VTE复发 | 抗凝 | 超声随访 | 中位92 d | 24个月 |
| Utter等[14](2016) | 回顾性队列研究 | 384 | 首次IDDVT;≥18岁 | 慢性血栓;近半年内确诊DVT或PE;同时合并PE;存在抗凝禁忌;诊断前已接受抗凝治疗 | 近端DVT或PE | 治疗剂量抗凝 | 未行治疗剂量抗凝 | 中位106 d | 180 d |
| Kret等[15](2013) | 回顾性队列研究 | 57 | 小腿肌静脉血栓形成 | - | 血栓溶解 | 治疗剂量抗凝 | 未抗凝或预防剂量抗凝 | - | 平均113 d |
| Sule等[20](2009) | 回顾性队列研究 | 51 | 症状性IDDVT | 合并近端DVT或PE;既往有DVT病史;因其他原因长期抗凝 | 血栓完全溶解 | 治疗剂量抗凝 | 未抗凝 | G1∶2周 G2∶3个月 | 平均7个月 |
| Luo等[22](2022) | 回顾性队列研究 | 426 | ≥18岁的住院患者;经超声诊断为IDDVT;至少有一次超声随访检查 | 合并近端DVT或PE;未随访超声;门诊患者;入院时合并大出血;因其他原因长期抗凝;失访 | 血栓进展为近端DVT或PE 全因死亡 | 抗凝 | 未抗凝 | 中位0.61个月 | 中位11.6个月 |
| Ochiai等[23](2021) | 回顾性队列研究 | 151 | 首次IDDVT | 合并PE;因其他原因长期抗凝 | 症状性或无症状PE | 抗凝 | 未抗凝 | - | 中位571 d |
| Sales等[24](2010) | 回顾性队列研究 | 141 | 小腿肌静脉血栓形成 | 合并其他静脉段血栓;确诊前已接受抗凝治疗 | 血栓扩散 | 治疗剂量抗凝 | 未抗凝 | - | - |
注:-为无此项。IDDVT为孤立性远端深静脉血栓形成;RCT为随机对照试验;DVT为深静脉血栓形成;PE为肺栓塞;VTE为静脉血栓栓塞症
聚焦于队列研究(表2),Kuczmik等[13]发现,与超声监测组相比,抗凝组IDDVT患者VTE复发率(7.3%比14.3%;P=0.04)与血栓近端扩散率(2.8%比8.3%;P=0.01)均更低,且两组间出血风险差异无统计学意义,他们认为抗凝相比于保守治疗可能会提高IDDVT患者的临床净获益。Utter等[14]发现,在6个月的随访期间,与非抗凝组相比,治疗性抗凝可显著降低IDDVT患者发生近端DVT或肺栓塞的风险(3.3%比9.2%,OR:0.34,95%CI:0.14~0.83),但同时增加了出血风险(8.6% 比2.2%,OR:4.35,95%CI:1.27~14.9)。另一项研究[15]表明,抗凝治疗较保守治疗能够显著提高IDDVT患者的血栓溶解率。
2.不支持抗凝:CACTUS研究[16]是一项仅纳入门诊低风险(无活动性癌症及VTE既往史)IDDVT患者的RCT(表2)。该研究表明,抗凝组与安慰剂组间主要结局(包括IDDVT近端扩散、对侧近端DVT、症状性肺栓塞的复合结局)发生率差异无统计学意义(3%比5%,P=0.54),但抗凝组出血风险较安慰剂组明显升高(4%比0,P=0.025 5)。另外,该研究在后续随访中发现[17, 18],抗凝治疗并不能减轻IDDVT患者的疼痛症状,也无法预防血栓后综合征的发生。
另一项纳入了109例患者(其中90%为门诊患者)的RCT研究[19](表2)表明,抗凝组与非抗凝组在血栓近端扩散率(3.7%比3.8%,P=0.99)及血栓再通率(66.6% 比60.4%,P=0.23)方面均无明显差异,且两组均无肺栓塞及大出血事件发生。需要注意的是,该研究中抗凝组抗凝疗程仅为10 d,远低于常规疗程(6周或12周),这或许是两组间临床结局差异无统计学意义的主要原因。
除了上述RCT,多项队列研究也表明,抗凝治疗无法降低血栓近端扩散风险(表2)[20, 21, 22, 23, 24]。Ochiai等[23]还发现抗凝治疗不仅不能降低VTE复发风险,还会增加IDDVT患者的出血风险。有研究认为,大多数IDDVT具有自限性,即血栓能够在不抗凝的情况下自行溶解,这可能一定程度上解释了上述现象[25, 26, 27, 28]。
3.汇总分析:一项纳入了8项RCT的荟萃分析[29]表明,与未接受抗凝治疗的受试者相比,抗凝治疗降低了IDDVT患者的VTE复发风险(RR:0.34,95%CI:0.15~0.77)及DVT复发风险(RR:0.25,95%CI:0.10~0.67),但未能显著降低肺栓塞的发生风险(RR:0.81,95%CI:0.18~3.59)。与此同时,抗凝治疗增加了临床相关非大出血风险(RR:3.34,95%CI:1.07~10.46),但未增加大出血风险(RR:0.76,95%CI:0.13~4.62)。
另一项纳入了20项研究(5项RCT+15项队列研究)的荟萃分析[30]发现,与对照组相比,抗凝治疗一方面降低了IDDVT患者的VTE复发率(OR:0.50,95%CI:0.31~0.79)及肺栓塞发生率(OR:0.48,95%CI:0.25~0.91),另一方面增加了出血风险(OR:2.41,95%CI:1.32~4.39),但大出血发生风险在两组间无显著差异(OR:0.64,95%CI:0.15~2.73)。
综合上述荟萃分析研究结果,在权衡血栓进展风险与出血风险后,抗凝治疗相比于保守治疗或许更能够提高IDDVT患者的临床净获益。
目前抗凝药物主要包括肝素类(如普通肝素、低分子肝素、磺达肝葵钠)、维生素K拮抗剂(如华法林)和直接口服抗凝药(direct oral anticoagulant,DOAC),如利伐沙班、阿哌沙班、依度沙班、达比加群。下表总结了不同抗凝药物治疗IDDVT的相关研究(表 3)。
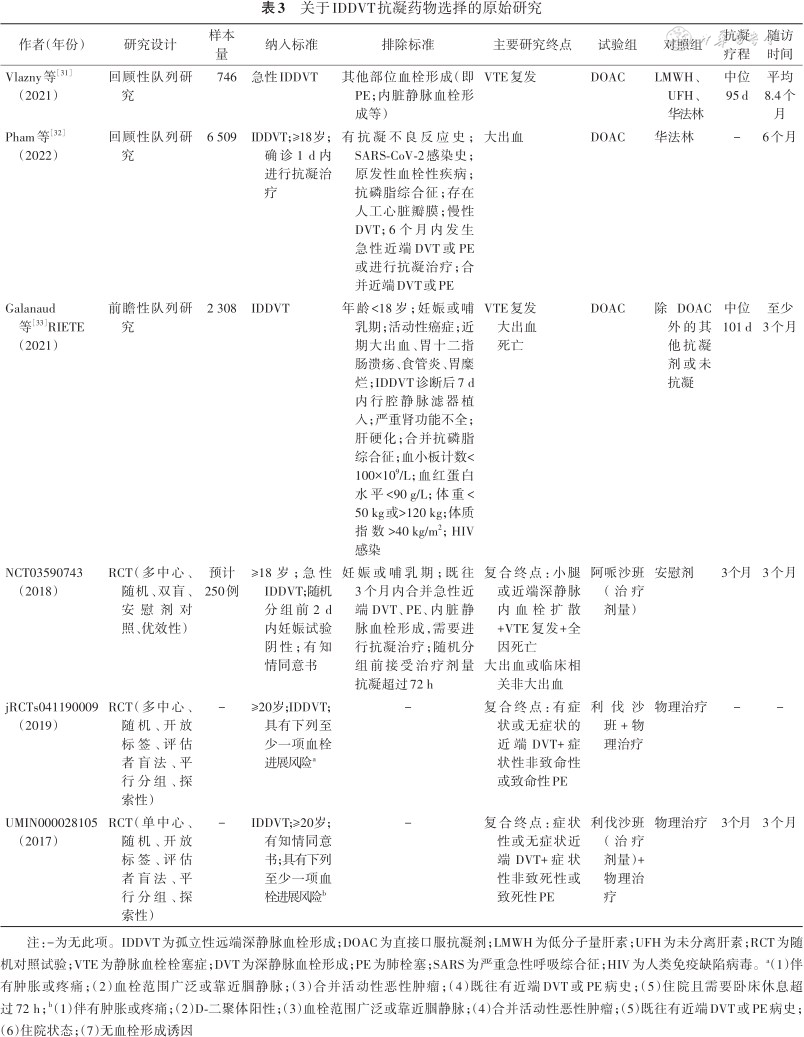
关于IDDVT抗凝药物选择的原始研究
关于IDDVT抗凝药物选择的原始研究
| 作者(年份) | 研究设计 | 样本量 | 纳入标准 | 排除标准 | 主要研究终点 | 试验组 | 对照组 | 抗凝疗程 | 随访时间 |
|---|---|---|---|---|---|---|---|---|---|
| Vlazny等[31](2021) | 回顾性队列研究 | 746 | 急性IDDVT | 其他部位血栓形成(即PE;内脏静脉血栓形成等) | VTE复发 | DOAC | LMWH、UFH、华法林 | 中位95 d | 平均8.4个月 |
| Pham等[32](2022) | 回顾性队列研究 | 6 509 | IDDVT;≥18岁;确诊1 d内进行抗凝治疗 | 有抗凝不良反应史;SARS-CoV-2感染史;原发性血栓性疾病;抗磷脂综合征;存在人工心脏瓣膜;慢性DVT;6个月内发生急性近端DVT或PE或进行抗凝治疗;合并近端DVT或PE | 大出血 | DOAC | 华法林 | - | 6个月 |
| Galanaud等[33]RIETE(2021) | 前瞻性队列研究 | 2 308 | IDDVT | 年龄<18岁;妊娠或哺乳期;活动性癌症;近期大出血、胃十二指肠溃疡、食管炎、胃糜烂;IDDVT诊断后7 d内行腔静脉滤器植入;严重肾功能不全;肝硬化;合并抗磷脂综合征;血小板计数<100×109/L;血红蛋白水平<90 g/L;体重<50 kg或>120 kg;体质指数>40 kg/m2;HIV感染 | VTE复发大出血死亡 | DOAC | 除DOAC外的其他抗凝剂或未抗凝 | 中位101 d | 至少3个月 |
| NCT03590743(2018) | RCT(多中心、随机、双盲、安慰剂对照、优效性) | 预计250例 | ≥18岁;急性IDDVT;随机分组前2 d内妊娠试验阴性;有知情同意书 | 妊娠或哺乳期;既往3个月内合并急性近端DVT、PE、内脏静脉血栓形成,需要进行抗凝治疗;随机分组前接受治疗剂量抗凝超过72 h | 复合终点:小腿或近端深静脉内血栓扩散+VTE复发+全因死亡 大出血或临床相关非大出血 | 阿哌沙班(治疗剂量) | 安慰剂 | 3个月 | 3个月 |
| jRCTs041190009(2019) | RCT(多中心、随机、开放标签、评估者盲法、平行分组、探索性) | - | ≥20岁;IDDVT;具有下列至少一项血栓进展风险a | - | 复合终点:有症状或无症状的近端DVT+症状性非致命性或致命性PE | 利伐沙班+物理治疗 | 物理治疗 | - | - |
| UMIN000028105(2017) | RCT(单中心、随机、开放标签、评估者盲法、平行分组、探索性) | - | IDDVT;≥20岁;有知情同意书;具有下列至少一项血栓进展风险b | - | 复合终点:症状性或无症状近端DVT+症状性非致死性或致死性PE | 利伐沙班(治疗剂量)+物理治疗 | 物理治疗 | 3个月 | 3个月 |
注:-为无此项。IDDVT为孤立性远端深静脉血栓形成;DOAC为直接口服抗凝剂;LMWH为低分子量肝素;UFH为未分离肝素;RCT为随机对照试验;VTE为静脉血栓栓塞症;DVT为深静脉血栓形成;PE为肺栓塞;SARS为严重急性呼吸综合征;HIV为人类免疫缺陷病毒。a(1)伴有肿胀或疼痛;(2)血栓范围广泛或靠近腘静脉;(3)合并活动性恶性肿瘤;(4)既往有近端DVT或PE病史;(5)住院且需要卧床休息超过72 h;b(1)伴有肿胀或疼痛;(2)D-二聚体阳性;(3)血栓范围广泛或靠近腘静脉;(4)合并活动性恶性肿瘤;(5)既往有近端DVT或PE病史;(6)住院状态;(7)无血栓形成诱因
一项回顾性研究[31]表明,接受DOAC进行抗凝治疗的IDDVT患者VTE复发率(0.9% 比5.3%,P<0.001)、大出血率(2.0%比5.4%,P=0.023)和死亡率(13.0%比35.4%,P<0.001)都显著低于使用其他抗凝方案(普通肝素/低分子肝素/华法林)的患者。另一项回顾性研究[32]同样发现,与华法林相比,DOAC能够显著降低IDDVT患者肺栓塞(1.795%比3.590%,P=0.002)和大出血(7.949% 比10.513%,P=0.01)的发生率。RIETE研究[33]是一项国际多中心前瞻性队列研究,该研究发现DOAC在IDDVT的治疗方面与维生素K拮抗剂具有相似的疗效与安全性,考虑到DOAC更稳定的药理学特点,作者认为DOAC可广泛用于IDDVT患者。
遗憾的是,评价DOAC治疗VTE的几项大型随机对照研究[34, 35, 36, 37]都将IDDVT患者排除在外,但考虑到DOAC在近端DVT和肺栓塞中的安全性和有效性,2021年ESVS[10]建议对IDDVT患者使用DOAC进行治疗(1C)。目前已有多项正在进行的RCT(NCT03590743、jRCTs041190009、UMIN000028105)评估DOAC在IDDVT中的有效性与安全性(表3),未来或许能够为IDDVT抗凝药物的选择提供更可靠的证据。
对于近端DVT和肺栓塞,现已明确使用治疗剂量进行抗凝,对于浅静脉血栓形成,预防剂量抗凝即可达到显著疗效,而对于IDDVT,不同剂量抗凝方案的有效性尚不明确。一项纳入了5项研究的荟萃分析[38]表明,与低剂量抗凝相比,治疗剂量抗凝不仅能够显著降低IDDVT患者血栓近端扩散的风险(RR:0.33,95%CI:0.20~0.54),还能提高血栓完全再通率(RR:1.96,95%CI:1.01~3.80)。值得注意的是,该荟萃分析仅包含1项RCT研究,结论证据级别较低。
近期的两项队列研究(表 4)给出的结论不同于上述荟萃分析。其中一项回顾性研究[39]表明,低剂量抗凝组(低分子肝素6 000 U,1次/d)与治疗剂量抗凝组(低分子肝素6 000 U,2次/d)均未发生血栓近端扩散。需要注意的是,该研究样本量极少(低剂量组16例,治疗剂量组17例),且治疗剂量组中位抗凝疗程为99 d,而低剂量组中位抗凝疗程仅5 d,结论缺乏可靠性。另一项前瞻性研究[40]对156例IDDVT患者均使用预防剂量(依诺肝素4 000 U,1次/d或普通肝素5 000 U,2次/d)抗凝,3个月随访期间血栓扩散至近端深静脉及肺动脉的概率分别为7%和6%,由于发生上述不良事件的患者均存在高危因素(骨科手术、脑卒中或恶性肿瘤),作者建议对存在制动状态或活动期癌症的IDDVT患者进行治疗剂量抗凝,而对其他低风险患者采用预防剂量抗凝。
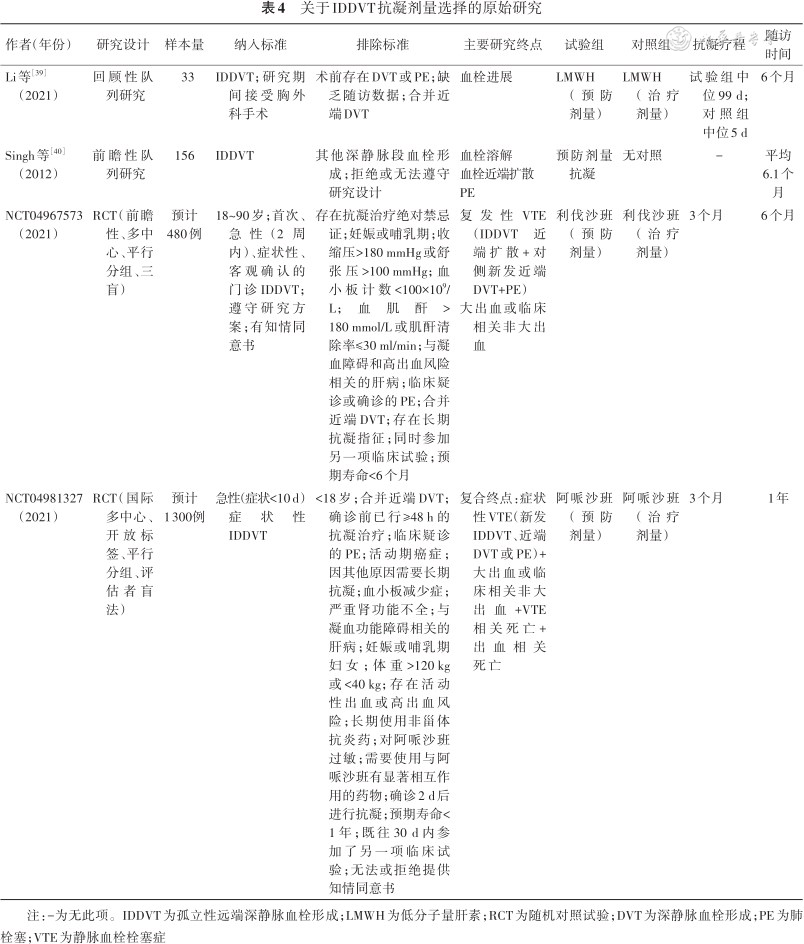
关于IDDVT抗凝剂量选择的原始研究
关于IDDVT抗凝剂量选择的原始研究
| 作者(年份) | 研究设计 | 样本量 | 纳入标准 | 排除标准 | 主要研究终点 | 试验组 | 对照组 | 抗凝疗程 | 随访时间 |
|---|---|---|---|---|---|---|---|---|---|
| Li等[39](2021) | 回顾性队列研究 | 33 | IDDVT;研究期间接受胸外科手术 | 术前存在DVT或PE;缺乏随访数据;合并近端DVT | 血栓进展 | LMWH(预防剂量) | LMWH(治疗剂量) | 试验组中位99 d;对照组中位5 d | 6个月 |
| Singh等[40](2012) | 前瞻性队列研究 | 156 | IDDVT | 其他深静脉段血栓形成;拒绝或无法遵守研究设计 | 血栓溶解血栓近端扩散PE | 预防剂量抗凝 | 无对照 | - | 平均6.1个月 |
| NCT04967573(2021) | RCT(前瞻性、多中心、平行分组、三盲) | 预计480例 | 18~90岁;首次、急性(2周内)、症状性、客观确认的门诊IDDVT;遵守研究方案;有知情同意书 | 存在抗凝治疗绝对禁忌证;妊娠或哺乳期;收缩压>180 mmHg或舒张压>100 mmHg;血小板计数<100×109/L;血肌酐>180 mmol/L或肌酐清除率≤30 ml/min;与凝血障碍和高出血风险相关的肝病;临床疑诊或确诊的PE;合并近端DVT;存在长期抗凝指征;同时参加另一项临床试验;预期寿命<6个月 | 复发性VTE(IDDVT近端扩散+对侧新发近端DVT+PE) 大出血或临床相关非大出血 | 利伐沙班(预防剂量) | 利伐沙班(治疗剂量) | 3个月 | 6个月 |
| NCT04981327(2021) | RCT(国际多中心、开放标签、平行分组、评估者盲法) | 预计1 300例 | 急性(症状<10 d)症状性IDDVT | <18岁;合并近端DVT;确诊前已行≥48 h的抗凝治疗;临床疑诊的PE;活动期癌症;因其他原因需要长期抗凝;血小板减少症;严重肾功能不全;与凝血功能障碍相关的肝病;妊娠或哺乳期妇女;体重>120 kg或<40 kg;存在活动性出血或高出血风险;长期使用非甾体抗炎药;对阿哌沙班过敏;需要使用与阿哌沙班有显著相互作用的药物;确诊2 d后进行抗凝;预期寿命<1年;既往30 d内参加了另一项临床试验;无法或拒绝提供知情同意书 | 复合终点:症状性VTE(新发IDDVT、近端DVT或PE)+大出血或临床相关非大出血+VTE相关死亡+出血相关死亡 | 阿哌沙班(预防剂量) | 阿哌沙班(治疗剂量) | 3个月 | 1年 |
注:-为无此项。IDDVT为孤立性远端深静脉血栓形成;LMWH为低分子量肝素;RCT为随机对照试验;DVT为深静脉血栓形成;PE为肺栓塞;VTE为静脉血栓栓塞症
与2016年ACCP[7]一致,2021年中国IDDVT诊疗建议[11]推荐对IDDVT使用治疗剂量进行抗凝。而2018年欧洲心脏病协会(ESC)[8]认为抗凝剂量应取决于VTE复发风险,推荐对复发风险高者采用治疗剂量抗凝,对复发风险低者采用低剂量抗凝。总之,针对IDDVT抗凝剂量方面的研究很少,但目前已开展多项RCT(NCT04967573、NCT04981327)对比预防剂量与治疗剂量在IDDVT中的有效性及安全性(表4),它们有望为IDDVT抗凝剂量的选择提供更强有力的证据。
抗凝疗程主要取决于VTE的复发风险,一般来说,具有暂时性或可逆性血栓形成诱因(如近期手术、住院、妊娠、长途旅行等)的患者VTE复发风险更低,而具有持续性或不明确的血栓形成诱因(如活动期肿瘤、炎症性肠病、抗磷脂抗体综合征、长期卧床、高龄等)的患者VTE复发风险更高[9]。有研究[41, 42]表明,IDDVT患者VTE复发率仅为近端DVT患者的一半,而另一些研究[43, 44]则认为IDDVT与近端DVT患者的VTE复发风险没有差异。
现有RCT主要比较了6周与12周抗凝在IDDVT中的有效性与安全性(表5)。一项RCT[45]表明,对于IDDVT患者,抗凝治疗6周组和12周组VTE复发率分别为2.0%和3.4%(RR:0.58,95%CI:0.10~3.36),大出血的发生率分别为1.0%和3.4%(RR:0.29,95%CI:0.03~2.72)。由于两组间有效性及安全性无显著差异,作者认为对IDDVT患者进行6周抗凝治疗是足够的。然而,近期发表的另一项RCT[46]得出了不同的结论。该研究发现,在2年的随访中,与6周抗凝相比,3个月抗凝治疗可显著降低IDDVT患者的VTE复发风险(11%比19%,RR:0.59,95%CI:0.36~0.95),且不增加出血风险。需要注意的是,后者纳入的患者中95%存在高复发风险因素,这间接表明长期抗凝对于高复发风险的IDDVT患者是必要的。
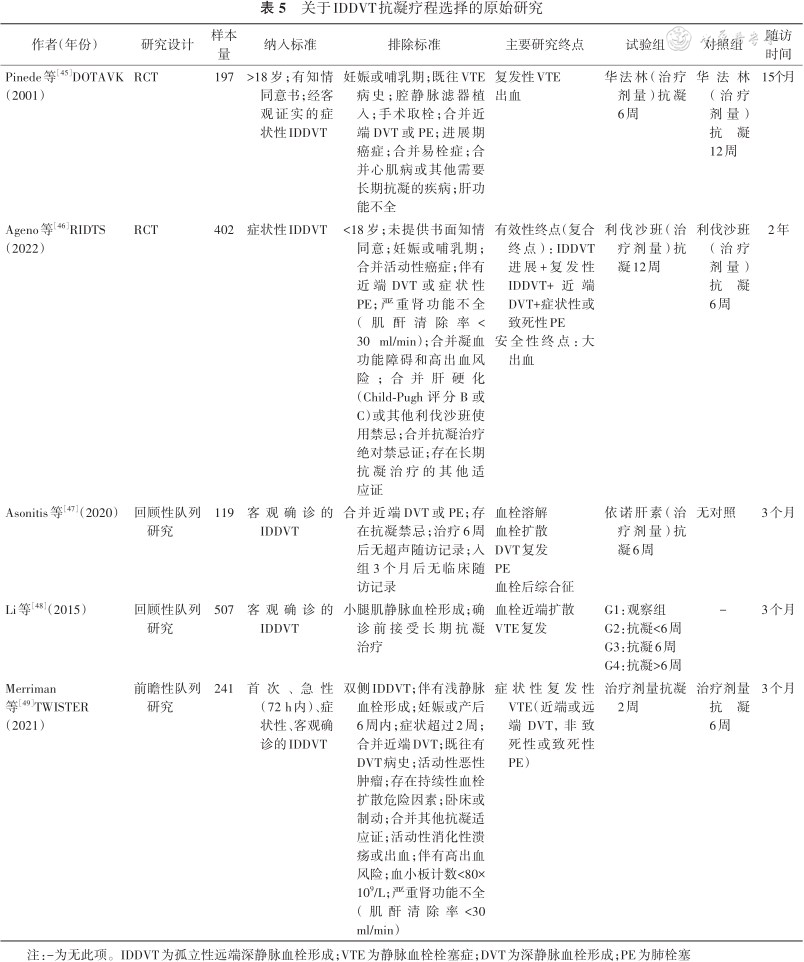
关于IDDVT抗凝疗程选择的原始研究
关于IDDVT抗凝疗程选择的原始研究
| 作者(年份) | 研究设计 | 样本量 | 纳入标准 | 排除标准 | 主要研究终点 | 试验组 | 对照组 | 随访时间 |
|---|---|---|---|---|---|---|---|---|
| Pinede等[45]DOTAVK(2001) | RCT | 197 | >18岁;有知情同意书;经客观证实的症状性IDDVT | 妊娠或哺乳期;既往VTE病史;腔静脉滤器植入;手术取栓;合并近端DVT或PE;进展期癌症;合并易栓症;合并心肌病或其他需要长期抗凝的疾病;肝功能不全 | 复发性VTE出血 | 华法林(治疗剂量)抗凝6周 | 华法林(治疗剂量)抗凝12周 | 15个月 |
| Ageno等[46]RIDTS(2022) | RCT | 402 | 症状性IDDVT | <18岁;未提供书面知情同意;妊娠或哺乳期;合并活动性癌症;伴有近端DVT或症状性PE;严重肾功能不全(肌酐清除率<30 ml/min);合并凝血功能障碍和高出血风险;合并肝硬化(Child-Pugh评分B或C)或其他利伐沙班使用禁忌;合并抗凝治疗绝对禁忌证;存在长期抗凝治疗的其他适应证 | 有效性终点(复合终点):IDDVT进展+复发性IDDVT+近端DVT+症状性或致死性PE 安全性终点:大出血 | 利伐沙班(治疗剂量)抗凝12周 | 利伐沙班(治疗剂量)抗凝6周 | 2年 |
| Asonitis等[47](2020) | 回顾性队列研究 | 119 | 客观确诊的IDDVT | 合并近端DVT或PE;存在抗凝禁忌;治疗6周后无超声随访记录;入组3个月后无临床随访记录 | 血栓溶解血栓扩散DVT复发PE 血栓后综合征 | 依诺肝素(治疗剂量)抗凝6周 | 无对照 | 3个月 |
| Li等[48](2015) | 回顾性队列研究 | 507 | 客观确诊的IDDVT | 小腿肌静脉血栓形成;确诊前接受长期抗凝治疗 | 血栓近端扩散VTE复发 | G1:观察组G2:抗凝<6周G3:抗凝6周G4:抗凝>6周 | - | 3个月 |
| Merriman等[49]TWISTER(2021) | 前瞻性队列研究 | 241 | 首次、急性(72 h内)、症状性、客观确诊的IDDVT | 双侧IDDVT;伴有浅静脉血栓形成;妊娠或产后6周内;症状超过2周;合并近端DVT;既往有DVT病史;活动性恶性肿瘤;存在持续性血栓扩散危险因素;卧床或制动;合并其他抗凝适应证;活动性消化性溃疡或出血;伴有高出血风险;血小板计数<80×109/L;严重肾功能不全(肌酐清除率<30 ml/min) | 症状性复发性VTE(近端或远端DVT,非致死性或致死性PE) | 治疗剂量抗凝2周 | 治疗剂量抗凝6周 | 3个月 |
注:-为无此项。IDDVT为孤立性远端深静脉血栓形成;VTE为静脉血栓栓塞症;DVT为深静脉血栓形成;PE为肺栓塞
现有队列研究则主要评估了短期(≤6周)抗凝对IDDVT临床结局的影响(表5)。两项回顾性研究[47, 48]发现,接受6周抗凝治疗的IDDVT患者血栓近端扩散率及VTE复发率均低于5%。另一项多中心前瞻性研究[49]发现,对低复发风险IDDVT患者(排除了合并妊娠、VTE既往史、活动期肿瘤、长期制动的患者)进行2周抗凝治疗后,若患者腿部症状缓解或无血栓近端扩散,即可安全停药(该群体3个月随访期间VTE复发率仅为1.3%)。总之,多数研究均认为短期抗凝所致的VTE复发风险是可以接受的。遗憾的是,目前尚无RCT证实2周抗凝治疗在IDDVT患者中的有效性。
一项纳入了4项研究(3项RCT+1项队列研究)的荟萃分析[30]表明,与接受6周抗凝治疗的IDDVT患者相比,接受>6周抗凝治疗的患者VTE复发率更低(OR:0.39,95%CI:0.17~0.90)。需要注意的是,此荟萃分析纳入的原始研究数量少,总样本量仅1 243例,结论可靠性有待证实。
国内外指南[7, 8, 9, 10, 11]在IDDVT抗凝疗程方面的推荐意见大同小异(表1)。概括而言,对于高复发风险患者,长期(3个月)抗凝是必要的,而对于低复发风险患者,目前尚无统一意见。
对于IDDVT,由于目前缺乏每种临床情况所特有的RCT研究[10],在此我们对某些特殊类型IDDVT患者的抗凝治疗进行了总结。
1.合并癌症的IDDVT患者:OPTIMEV研究[50]是一项多中心前瞻性队列研究,该研究表明,与未合并癌症的IDDVT患者相比,合并癌症的IDDVT患者具有更高的VTE复发风险(11.5%与5.0%,aCHR:2.0,95%CI:1.0~3.7)、更高的大出血风险(3.6%与1.8%,aCHR:2.0,95%CI:0.6~6.1)以及更高的死亡风险(38.3%与3.5%,aHR:9.3,95%CI:5.5~15.9)。另外有两项研究[51]发现合并癌症的IDDVT患者与合并癌症的近端DVT患者具有相似的VTE复发风险。由此可见,合并癌症的IDDVT可能需要同近端DVT一样,接受更加积极的抗凝治疗,但同时应警惕出血的发生。
对于抗凝药物的选择,2016 ACCP[7]推荐对合并癌症的VTE患者使用低分子肝素抗凝而非华法林或DOAC。然而,Ogino等[52]发现DOAC在合并癌症的IDDVT患者中是安全有效的,Komiyama等[53]也发现DOAC在合并卵巢癌的IDDVT患者中是安全的。值得注意的是,以上两项研究结论均基于低质量回顾性证据,可靠性值得商榷。
大多数指南[7, 8, 9, 10, 11]均认为合并癌症的IDDVT患者需要接受长期(≥3个月)抗凝治疗。而近期一项回顾性研究[52]发现,对于合并癌症的IDDVT而言,短期抗凝组(中位抗凝时间35 d)与长期抗凝组(中位抗凝时间281 d)之间VTE复发风险(P=0.789)与大出血发生风险(P=0.132)均无显著差异。目前一项正在进行的RCT(NCT03895502)致力于探讨癌症相关IDDVT的最佳抗凝治疗疗程,未来或许能够提供更强有力的证据。
2. 住院IDDVT患者:住院IDDVT患者中有6.2%~33.0%合并肺栓塞,远高于门诊IDDVT患者[54, 55]。2016年ACCP指南[7]将住院状态视为IDDVT患者血栓近端扩散的高危因素,建议对该类患者进行抗凝治疗(2C)。一项回顾性研究[56]发现,治疗剂量抗凝不仅降低了住院IDDVT患者血栓扩散风险(OR:0.07,95%CI:0.009~0.610),还降低了其全因死亡率(OR:0.37,95%CI:0.17~0.80),并且没有增加出血风险。由此可见,住院IDDVT患者可能需要更加积极的抗凝策略。
然而,近期的两项研究给出了不同的结论。Luo等[22]发现,与未接受抗凝治疗的住院IDDVT患者相比,抗凝并不能显著降低该类患者血栓向近端扩散的风险(4.9%与5.1%,P=0.925),也无法降低全因死亡率(27.9%与18.9%,P=0.098)。Ochiai等[23]发现,与未接受抗凝治疗的住院IDDVT患者相比,抗凝治疗不仅无法降低VTE复发风险(21.4%与21.6%,P=0.936),还增加了出血风险(23.7%与0,P<0.001)。遗憾的是,上述反对意见均来源于回顾性研究,未来亟需高质量RCT去阐明抗凝治疗在住院IDDVT患者中的地位。
3.手术或创伤后IDDVT患者:不同于普通IDDVT人群,手术或创伤后IDDVT患者不仅存在很高的血栓栓塞风险(制动、使用止血药物等),也存在很高的出血风险。因此,面对此类患者,如何权衡出血与血栓栓塞显得至关重要。
Olson等[57]发现,约13%的创伤后IDDVT患者发生血栓近端扩散,作者建议对该类人群进行抗凝治疗。一项回顾性研究[58]表明,对于创伤后IDDVT患者,抗凝治疗组(IDDVT确诊7 d内进行抗凝)血栓近端扩散率为3%,而保守治疗组(IDDVT确诊7 d后进行抗凝或未抗凝)血栓近端扩散率为12%,两组均无大出血事件发生。基于此,作者认为早期抗凝治疗能够在不增加大出血风险的情况下降低创伤后IDDVT患者的血栓扩散风险。
然而,另一些研究则认为抗凝治疗并不能使手术或创伤后IDDVT患者获益。Kim等[59]发现,对于肾移植术后发生IDDVT的患者,抗凝组(15例)及非抗凝组(34例)在1年的随访中均未出现血栓近端扩散或VTE复发事件。需要注意的是,抗凝组中有6例患者发生出血事件,其中3例为大出血。因此,作者不建议对术后IDDVT患者进行抗凝治疗。Cho和Lee[60]发现,对于急性脊髓损伤后发生IDDVT的患者,抗凝组和非抗凝组在中位17 d的随访中均未出现血栓近端扩散,并且两组间血栓溶解率没有显著差异。Yun等[61]发现,对于膝关节置换术后的IDDVT患者,抗凝组与非抗凝组在6个月的随访中均未出现血栓近端扩散,且两组患者小腿血栓均完全溶解。
遗憾的是,以上均为小样本回顾性研究。由于缺乏针对该类人群的RCT,是否对手术或创伤后IDDVT患者进行抗凝治疗仍然是个悬而未决的话题。
尽管针对IDDVT的抗凝治疗策略尚未达成共识,但有越来越多的证据表明抗凝治疗相比于保守治疗更能够提高IDDVT患者的临床净获益。在抗凝药物方面,目前尚无DOAC用于IDDVT的直接高质量证据,但大多数队列研究表明DOAC在该类人群中是安全有效的。目前关于抗凝剂量方面的研究很少,国外正在进行的多项RCT有望为该领域提供更充分的证据。在抗凝疗程方面,对于存在高复发风险因素的IDDVT患者,3个月抗凝是必要的,而对于低复发风险患者,更短时间(≤6周)的抗凝治疗或许是值得探究的。
对于特殊类型IDDVT患者的抗凝管理,现有证据几乎均基于回顾性研究,未来需重点对该类患者群体进行高质量前瞻性研究,以便为各种临床环境提供个性化抗凝决策。
范盛心, 王晓慧, 刘煜亮, 等. 孤立性远端深静脉血栓形成的抗凝治疗研究进展[J]. 中华医学杂志, 2023, 103(44): 3587-3596. DOI: 10.3760/cma.j.cn112137-20230730-00118.
所有作者声明不存在利益冲突



























