
回顾性分析1例在江西省宜春市人民医院内分泌科就诊的肥胖2型糖尿病患者使用利拉鲁肽联合二甲双胍治疗后血糖达标,最终停药,达到糖尿病缓解的诊治过程。患者为31岁男性,因“口干、多饮半个月”入院,完善相关检查,结果显示其空腹血糖为11.76 mmol/L、餐后2 h血糖14.58 mmol/L;空腹C肽2.73 ng/ml,餐后2 h C肽3.52 ng/ml;糖化血红蛋白(HbA1c)10.20%;尿葡萄糖3+,尿酮体2+;胰岛细胞抗体、胰岛素自身抗体及谷氨酸脱酶抗体均为阴性,结合病史及检查结果,患者2型糖尿病诊断明确,采用“ABCD”评估方法确定该患者达到T2DM缓解基本条件,予二甲双胍0.5 g每日3次+利拉鲁肽1.2 mg每日1次治疗9个月后血糖达标,后停药6个月血糖仍达标,实现糖尿病的缓解。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
2型糖尿病(type 2 diabetes mellitus,T2DM)是一种以血糖升高为主要特征的慢性进展性疾病,其发病机制复杂,一直被认为需要长期使用降糖药物治疗才能达到控制血糖的目标。近年来大量研究结果显示,通过生活方式干预、药物治疗以及代谢手术能够促进合并超重和肥胖的T2DM缓解,使患者在较长时间内免于使用降糖药物。美国糖尿病学会(American Diabetes Association,ADA)发布的《2021共识报告:2型糖尿病缓解的定义和解释》,将停用降糖药物至少3个月后,HbA1c(glycated hemoglobin A1c,HbA1c)<6.5%作为T2DM缓解的诊断标准。T2DM的缓解延缓疾病进展速度,预防并发症发生,大大提升患者生活质量并使其终身受益。我们报道1例新诊断的肥胖T2DM患者使用利拉鲁肽联合口服降糖药二甲双胍治疗,最终血糖达标,代谢综合征得到改善,并在停用降糖药物后,达到糖尿病缓解的诊疗经过,希望为糖尿病的缓解提供参考。
患者 男,31岁,因“口干、多饮半个月”入院。患者主诉半个月前出现口干、多饮,每日饮水量约3 000 ml,尿量增多,与饮水量相当,伴体重下降,近半个月体重下降约5 kg,遂至我院门诊查空腹血糖11.76 mmol/L(参考值3.90~6.10 mmol/L),HbA1c 10.20%(参考值4.0%~6.0%),无明显手套、袜套样感觉,觉视力下降,无恶心、呕吐,无胸痛等,故门诊拟糖尿病收入院。起病以来,患者精神、食欲、睡眠尚可,大便如常,小便如上述。既往史:无特殊,否认胰腺炎病史,否认高血压、心脏病等。否认“肝炎、结核、伤寒”等传染病及传染病接触史。预防接种史不详。否认外伤、输血史。否认青霉素过敏史。否认糖尿病家族史。
入院查体:体温36.5 ℃,呼吸16次/min,脉搏70次/min,血压112/86 mnHg(1 mmHg=0.133 kPa),身高172 cm,体重89.6 kg,体重指数(body mass index,BMI)30.3 kg/m2。神清,体型均匀性肥胖,双肺呼吸音清,未闻及干湿性啰音。心音有力,律齐。腹肌软,腹部可见大量长短不一紫纹,无压痛、反跳痛。肝脾肋下未及肿大。双下肢无水肿。足背动脉搏动可。双下肢痛觉、温度觉、振动觉正常。
入院后实验室检查:口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)示空腹血糖11.76 mmol/L、餐后2 h血糖14.58 mmol/L;空腹C肽2.73 ng/ml(参考值0.8~3.85 ng/ml),餐后2 h C肽3.52 ng/ml;HbA1c 10.20%;尿常规:尿葡萄糖3+,酮体2+;血脂:甘油三酯2.33 mmol/L(参考值0.34~1.7 mmol/L),胆固醇4.21 mmol/L(参考值0.26~5.18 mmol/L),高密脂蛋白胆固醇胆0.73 mmol/L(参考值1.0~1.6 mmol/L),低密脂蛋白胆固醇3.18 mmol/L(参考值0~2.6 mmol/L);血常规、甲状腺功能、肝肾功能、淀粉酶、血酮体、电解质、皮质醇节律未见明显异常;胰岛细胞抗体、胰岛素自身抗体及谷氨酸脱酶抗体均为阴性。颈动脉超声示双侧颈动脉血流通畅,腹部彩超示脂肪肝,胆、胰腺、双肾、双侧输尿管、膀胱、前列腺未见明显异常,心电图未见明显异常。
结合病史及检查结果,患者考虑诊断为2型糖尿病、高脂血症、肥胖症、脂肪肝、代谢综合征。因其合并糖尿病性酮症,先予补液及静脉胰岛素治疗,纠正糖尿病性酮症;患者血糖高,HbA1c>9%,且体型肥胖,合并有高脂血症、脂肪肝,故尿酮正常后开始予二甲双胍0.5 g每日3次,利拉鲁肽0.6 mg每日1次治疗,降糖同时改善代谢指标治疗。经治疗后,患者血糖控制良好,葡萄糖在目标范围内时间(time in range,TIR)达100%,无低血糖发生,伴食欲下降,无明显腹胀、腹泻、恶心、呕吐等胃肠道反应,遵医嘱出院。出院后患者定期门诊随访,继续二甲双胍0.5 g每日3次+利拉鲁肽1.2 mg每日1次治疗,患者血糖达标,无明显消化道不良反应。随访9个月患者HbA1c维持在正常范围内,停用降糖药,继续饮食及运动控制血糖,停药约半年后复查HbA1c正常(表1),实现糖尿病缓解。
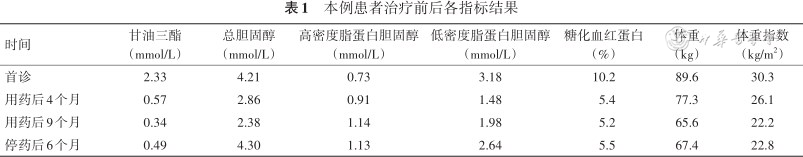
本例患者治疗前后各指标结果
本例患者治疗前后各指标结果
| 时间 | 甘油三酯(mmol/L) | 总胆固醇(mmol/L) | 高密度脂蛋白胆固醇(mmol/L) | 低密度脂蛋白胆固醇(mmol/L) | 糖化血红蛋白(%) | 体重(kg) | 体重指数(kg/m2) |
|---|---|---|---|---|---|---|---|
| 首诊 | 2.33 | 4.21 | 0.73 | 3.18 | 10.2 | 89.6 | 30.3 |
| 用药后4个月 | 0.57 | 2.86 | 0.91 | 1.48 | 5.4 | 77.3 | 26.1 |
| 用药后9个月 | 0.34 | 2.38 | 1.14 | 1.98 | 5.2 | 65.6 | 22.2 |
| 停药后6个月 | 0.49 | 4.30 | 1.13 | 2.64 | 5.5 | 67.4 | 22.8 |
本例患者为青年男性,有口干多饮多尿及体重下降,空腹血糖>7.0 mmol/L,餐后2 h血糖>11.1 mmol/L,糖尿病诊断明确。本例患者为青年起病,入院查尿酮体阳性,需警惕1型糖尿病可能,但本例患者体型肥胖,BMI明显升高,且糖尿病自身抗体为阴性,空腹C肽在正常范围内,故排除1型糖尿病及成人隐匿性自身免疫糖尿病(latent autoimmune diabetes in adults,LADA),糖尿病分型考虑为2型糖尿病。患者体型肥胖,为均匀性肥胖,无四肢纤细,无水牛背满月脸,皮质醇节律正常,考虑为单纯性肥胖,结合血脂结果及肝脏彩超,诊断为2型糖尿病、高脂血症、肥胖症、脂肪肝、代谢综合征。
本例患者经治疗后体重下降26.7%,停药6个月后HbA1c仍维持在正常水平(<6.5%),实现糖尿病的缓解。早在2016年世界卫生组织(WHO)《全球糖尿病报告》就已经明确提出,可以通过减重和限制能量摄入来实现T2DM的缓解。结合国内外研究证据及美国糖尿病学会(American Diabetes Association,ADA)的共识报告,我国于2021年发布《缓解2型糖尿病中国专家共识》[1](以下简称共识)。该共识采用“ABCD”评估方法确定T2DM缓解基本条件:A为糖尿病自身抗体(antibody,抗体),B为BMI,C分为C1(C肽)和C2(complication review,并发症评估),D为病程(duration,病程)。对本例患者进行“ABCD”四个维度评估:A为抗体阴性,B为BMI>25 kg/m2,C1为空腹C肽>1.1 ng/ml,C2为无心血管并发症、严重视网膜病变及肾病并发症,D为病程<5年。经评估,本例患者糖尿病缓解概率较高。同时根据《中国2型糖尿病防治指南(2020年版)》,对于合并动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)或心血管风险高危的T2DM患者,不论其HbA1c是否达标,只要没有禁忌证都应在二甲双胍的基础上加用胰高糖素样肽-1受体激动剂(glucagon-like peptide-1 receptor agonist,GLP-1RA)或钠-葡萄糖共转运蛋白2抑制剂[2]。故针对本例患者,我们选用二甲双胍+利拉鲁肽的治疗方案,从而实现糖尿病的缓解;且Hussein等[3]发现新诊断的2型糖尿病肥胖受试者利用利拉鲁肽治疗后,可稳定血糖,增加胰岛β细胞功能。糖尿病缓解临床试验研究显示,5年内的糖尿病合并肥胖患者减重后,糖尿病缓解率为46%,且减重越多,糖尿病缓解率越高,当体重减轻>15 kg时,T2DM的完全缓解率可达86%[4]。
利拉鲁肽是一种与天然人胰高糖素样肽-1(glucagon-like peptide-1,GLP-1)同源性高达97%的类似物。人体内天然GLP-1的半衰期短,进入循环后极易被二肽基肽酶Ⅳ降解并被肾小球滤过清除[5],使其不能充分发挥作用,基于此,GLP-1RA应运而生。GLP-1受体广泛分布于胰岛细胞、胃肠道、肺、脑、肾脏、下丘脑、心血管系统、肝脏、脂肪细胞和骨骼肌等[6]。GLP-1RA通过与胰岛β细胞中的受体结合,以葡萄糖浓度依赖的方式促进胰岛素的产生、刺激胰岛β细胞的增殖与分化,通过抑制胰岛α细胞分泌胰高糖素,减少肝糖原的产生来降低血糖[7, 8],其低血糖风险极低。本例患者的治疗过程中无低血糖发生,葡萄糖低于目标范围的时间为0%。GLP-1RA除了降糖显著外,还具有减重作用,其减重机制可能与作用于神经系统、胃肠道相应部位的GLP-1受体影响食欲、延缓胃排空、增加饱腹感[7, 8],以及通过白色脂肪棕色化有关[9]。研究发现,GLP-1RA可使非糖尿病组体重减轻约3.2 kg,糖尿病组患者体重减轻约2.8 kg[10],此外,还能降低BMI和腰围[11]。本例患者予利拉鲁肽治疗后体重下降达26.7%,BMI降低至正常范围内。
综上,对于初发的糖尿病患者,可通过“ABCD”四个维度的评估方法来确定是否符合T2DM缓解基本条件。对于符合缓解基本条件的患者,尽早实现糖尿病缓解,对患者后续生活质量的提高、并发症的预防均大有益处,且使患者终身获益。减重治疗和体重管理是糖尿病缓解的核心,利拉鲁肽作为一种GLP-1RA,除了能有效地降糖、不发生低血糖外,还有诸多获益,例如显著减轻体重、改善胰岛功能等。该药的不良反应主要为胃肠道不适,但大多能耐受。与传统降糖药相比,利拉鲁肽在多方面具有优势,临床地位逐步提升,受到国内外诸多指南的一致推荐,为肥胖T2DM患者的治疗提供了一种方法,为糖尿病缓解提供了治疗方案,值得临床应用及推广。
王佳, 李百云, 陈欢, 等. 利拉鲁肽联合二甲双胍治疗肥胖2型糖尿病患者达到临床缓解1例[J]. 中华糖尿病杂志, 2023, 15(Z2): 261-263. DOI: 10.3760/cma.j.cn115791-20230628-00299.
所有作者声明无利益冲突



























