
探讨儿童食管狭窄外科递进式个体化治疗方法的临床疗效。
分析2017年1月至2022年12月在南京医科大学附属儿童医院心胸外科治疗并定期随访的106例食管狭窄患儿的病例资料,其中男59例,女47例;年龄为(3.00±0.75)岁,体重为(9.00±1.25) kg。食管闭锁术后吻合口狭窄58例,腐蚀性食管狭窄47例,先天性食管狭窄1例。应用胃镜直视下球囊扩张、食管黏膜下注射药物、食管支架置入、外科手术的序贯治疗方法治疗儿童食管狭窄。术后通过食管造影、胃镜检查观察食管狭窄程度,结合患儿吞咽困难等级,评估外科序贯治疗的临床疗效。采用t检验或χ2检验法等进行统计学分析。
106例患儿均顺利出院。患儿均进行球囊扩张治疗,其中单纯胃镜直视下球囊扩张55例效果良好;球囊扩张联合食管黏膜下药物注射35例,其中25例效果良好,10例进行食管支架置入治疗;食管支架置入25例,其中21例效果良好,4例进行了外科手术治疗;外科手术5例效果良好。
胃镜直视下球囊扩张、球囊扩张联合食管黏膜下注射药物、食管支架置入、外科手术的递进式个体化方法治疗儿童食管狭窄临床效果确切,方法简单,容易操作与推广。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
儿童食管狭窄是指由于各种因素导致的食管结构异常,通畅性受损,进而引起吞咽困难、进食障碍和呛咳等问题的一类疾病。儿童食管狭窄包括先天性和后天性两类。先天性食管狭窄临床较为罕见,活产新生儿发生率为1/50 000~1/25 000[1]。后天性食管狭窄占儿童食管狭窄的90%以上,主要包括食管手术后吻合口狭窄、化学烧伤等创伤后食管狭窄、胃食管反流所致的食管消化性狭窄等。
儿童食管狭窄根据不同的发病原因及严重程度,需要在不同的时间节点采取不同的处理措施。南京医科大学附属儿童医院心胸外科根据多年临床经验,形成了外科序贯治疗理念,即胃镜直视下球囊扩张、球囊扩张联合食管黏膜下药物注射、食管支架置入、外科手术治疗的序贯治疗。本文回顾性分析了采用该治疗理念对儿童食管狭窄外科治疗的经验,报告如下。
收集2017年1月至2022年12月在南京医科大学附属儿童医院心胸外科治疗并定期随访的106例食管狭窄患儿的临床资料,男59例,女47例;年龄为(3.00±0.75)岁,体重为(9.00±1.25) kg。食管闭锁术后吻合口狭窄58例,腐蚀性食管狭窄47例,先天性食管狭窄1例。由于目前尚无食管狭窄严重程度的准确评估方法,临床上常采用食管造影检查的患儿近、远端食管作为参照,建立食管狭窄指数(stricture index,SI):SI=(D-d)/D[2]。D为狭窄远端食管直径,d为狭窄处食管直径,SI数值越大则狭窄越重。设定当SI<0.3时为轻度,0.3≤SI≤0.44为中度狭窄,SI>0.44时为重度狭窄。
纳入标准:①经食管造影检查或胃镜检查显示为中度及以上食管狭窄;②伴有吞咽困难症状;③无全身麻醉下内镜手术治疗的禁忌证。
排除标准:①年龄>14周岁;②合并恶性肿瘤等严重疾病者;③失访、临床资料不完整者;④凝血功能障碍;⑤拒绝手术治疗者。
本研究经南京医科大学附属儿童医院伦理委员会批准(201801157-1)。所有患儿家属均签署知情同意书。
在扩张术后1周采用Stooler法对患儿吞咽困难程度进行分级[3,4]。依据吞咽症状改善程度进行评定:①显效,管腔直径>0.8 cm,Stooler分级降至1级,且随访3个月后症状不复发;②有效,管腔直径0.5~0.8 cm,Stooler分级降至2级,随访3个月症状无加重;③无效,管腔直径无增加,吞咽症状无改善或加重。
记录患儿扩张后有无出血、胸骨后疼痛、感染、反流及穿孔、支架移位、炎性增生等扩张术后并发症发生。
①扩张前至少7 d停服抗凝药物及非甾体类抗炎药,常规检查凝血功能及传染病五项检查,避免有凝血机制障碍的患儿术中或术后发生大出血。②常规行胸部X线、腹部B型超声、心电图检查、食管钡餐或内镜检查等。③做好患儿思想工作,向患儿家属详细说明扩张治疗的必要性、目的、方法以及可能出现的并发症,取得患儿及家属的同意和配合,并签署知情同意书。④术前禁食6 h并保持食管清洁。如有严重的食管炎,术前应给予质子泵抑制剂抗反流治疗。⑤若儿童年龄过小,不能配合操作,需在麻醉医生协助下于全身麻醉下进行,并备好氧气、吸引器、气管插管等器械,全程行心电监护监测。
超细胃镜、常规胃镜;斑马导丝、亲水涂层导丝、内镜用注射针、镍钛记忆金属自膨式支架(两端膨大呈喇叭状,支架外敷有聚四氟乙烯薄膜,尾端由荷包尼龙线牵引固定,所用支架尺寸依据患儿病变情况个体化制定);丝裂霉素C。
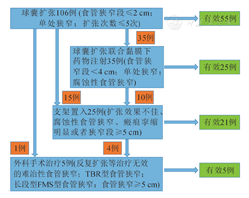

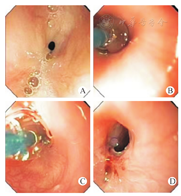
注:TBR,食管壁内气管支气管软骨残留;FMS,纤维肌性狭窄
①球囊扩张 麻醉成功后左侧卧位,行胃镜检查,了解狭窄口大小及上段食管情况,选择比狭窄口大4~6 mm球囊开始扩张,通过胃镜钳通道置入球囊,若狭窄口太小,插入球囊困难时,可在造影下经导丝引导置入球囊。球囊腰部位于狭窄段中央,一般狭窄口上方留出长约0.5 cm球囊,注入生理盐水,使用压力表监测压力达到所需球囊大小,每次持续2~3 min后放水,间隔2~3 min,再充水2~3 min,如此重复3次,见狭窄段扩大、黏膜有撕裂渗血后停止扩张,渗血明显时用肾上腺素盐水局部冲洗。扩张后可用胃镜通过狭窄段进入胃内检查。
②球囊扩张联合食管黏膜下药物注射 麻醉成功后左侧卧位,行胃镜检查,经导丝引导球囊对狭窄部位进行扩张,扩张后观察局部黏膜撕裂情况。胃镜直视下应用黏膜注射针在狭窄段3、6、9、12点方向注射丝裂霉素,每点注射1次,进针深度为1.0~1.5 mm,每点注射0.1~0.2 ml,注射后注意观察出血、穿孔等。丝裂霉素C(10 mg/支)用生理盐水稀释至0.4 mg/ml,注射总量按1 ml/cm2体表面积计算。
③食管支架置入 麻醉成功后左侧卧位,行胃镜检查,结合造影结果并测量需放置支架的病变处与门齿之间的距离。如发现病变段食管明显狭窄者需常规进行适度球囊扩张。扩张时经胃镜活检孔置入软质导引钢丝,在透视下确认导丝通过狭窄段食管进入胃腔,随后沿导丝放置球囊适度扩张。内镜监视下放入定制尺寸的自膨覆膜支架,当到达指定深度时回收支架外套管,支架自行膨开。退出支架输送装置后再次内镜检查支架腔内情况及是否完整覆盖病变区域。必要时通过牵引线或异物钳调整支架高度,确定支架位置正确后将支架尾端荷包牵引线经鼻腔拖出并固定于同侧耳后防止支架向下移位。
④外科手术治疗 目前常用的手术技术包括:狭窄段切除端端吻合术,结肠代食管术、胃代食管术、胃管成形代食管术及小肠代食管术等食管替代术,胃造口食管逆行扩张术,内镜下纵行肌切开术,磁压榨吻合技术等。
扩张后插入8号或10号胃管。术后至少禁食24 h,48 h内进食流质饮食,48 h后可进食流质、半流或固体食物;术后常规静脉用抗生素24 h,中、下段食管扩张后使用奥美拉唑2周。2~4周后可再次扩张。术后1、3、6个月及1年规律行食管造影及胃镜检查。
采用SPSS 26.0软件进行统计学处理,符合正态分布的计量资料采用 ±s表示,多组间比较采用单因素方差分析进行检验;非正态分布的计量资料采用M(Q1,Q3)表示,多组间比较采用Kruskal-Wallis秩和检验进行分析,组间两两比较采用Bonferroni检验方法。定性资料用例(%)表示,采用t检验或χ2检验法进行差异比较。双侧检验,检验水准α=0.05。
±s表示,多组间比较采用单因素方差分析进行检验;非正态分布的计量资料采用M(Q1,Q3)表示,多组间比较采用Kruskal-Wallis秩和检验进行分析,组间两两比较采用Bonferroni检验方法。定性资料用例(%)表示,采用t检验或χ2检验法进行差异比较。双侧检验,检验水准α=0.05。
106例患儿均行球囊扩张治疗,顺利出院,其中单纯胃镜直视下球囊扩张55例,球囊扩张联合黏膜下药物注射35例,食管支架置入25例(10例经过球囊扩张联合黏膜下药物注射治疗),外科手术5例(4例经过食管支架置入治疗)。
55例单纯胃镜直视下球囊扩张患儿取得了良好的治疗效果(图2),平均扩张次数为3~5次/人,其中食管闭锁术后食管狭窄43例,共扩张171次,扩张次数为(3.51±0.92)次/人,术后1例出现食管破裂,经保守治疗后好转;腐蚀性食管狭窄12例,共扩张58次,扩张次数为(4.32±0.84)次/人(表1)。
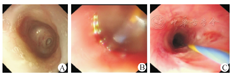


55例单纯胃镜直视下球囊扩张食管狭窄患儿的临床资料
55例单纯胃镜直视下球囊扩张食管狭窄患儿的临床资料
| 狭窄原因 | 性别(例) | 年龄(岁, ±s) ±s) | 狭窄状态 | 狭窄段内径(mm) | 狭窄段长度(mm) | 扩张次数(次/人, ±s) ±s) | 术后并发症 | |
|---|---|---|---|---|---|---|---|---|
| 男 | 女 | |||||||
| 食管闭锁术后狭窄 | 23 | 20 | 2.00±0.45 | 环状狭窄 | 2~4 | ≤10 | 3.51±0.92 | 1例食管破裂 |
| 腐蚀性食管狭窄 | 7 | 5 | 3.00±0.75 | 节段性狭窄 | 1~4 | 10~30 | 4.32±0.84 | 无食管破裂、穿孔、出血 |
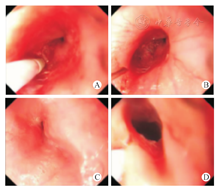
35例腐蚀性食管狭窄患儿进行了球囊扩张联合食管黏膜下注射丝裂霉素C治疗,其中男17例,女18例,年龄为(3.00±0.55)岁,均为节段性狭窄,狭窄段内径为1~4 mm,狭窄段长度为20~40 mm。25例好转,10例术后出现再狭窄,进行了支架置入治疗。患儿共注射52次,注射次数为(1.62±0.83)次/人。药物注射3次10例,注射2次20例,注射1次5例。术后无食管破裂、穿孔、出血、纵隔感染等并发症发生(图3)。

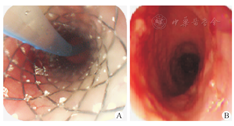
食管支架置入25例,其中10例为球囊扩张联合食管黏膜下药物注射治疗后效果欠佳,另15例患儿狭窄段较长,直接支架置入治疗(图4)。25例患儿中,食管闭锁术后狭窄患儿9例,共置入支架13次,次数为(1.22±0.31)次/人;腐蚀性食管狭窄患儿16例,共置入支架32次,次数为(2.41±0.72)次/人(表2)。15例未经过球囊扩张联合黏膜下药物注射治疗的患儿中,2例为食管闭锁术后吻合口狭窄,13例为腐蚀性食管狭窄。


25例食管狭窄行食管支架置入患儿的临床资料
25例食管狭窄行食管支架置入患儿的临床资料
| 狭窄原因 | 性别(例) | 年龄(岁, ±s) ±s) | 狭窄状态 | 狭窄段内径(mm) | 狭窄段长度(mm) | 支架置入次数(次/人, ±s) ±s) | 术后并发症 | |
|---|---|---|---|---|---|---|---|---|
| 男 | 女 | |||||||
| 食管闭锁术后狭窄 | 5 | 4 | 2.00±0.12 | 环状狭窄 | 2~4 | 10~20 | 1.22±0.31 | 呕吐3例;肉芽增生3例 |
| 腐蚀性食管狭窄 | 9 | 7 | 3.00±0.25 | 节段性狭窄 | 1~4 | 30~50 | 2.41±0.72 | 胸痛4例;再狭窄4例;支架移位3例;呕吐3例;肉芽增生2例 |
共有5例手术治疗患儿,均为节段性狭窄(图5)。腐蚀性食管狭窄4例,均经食管支架置入治疗效果欠佳,其中男2例,女2例;年龄为(4.00±0.55)岁,狭窄段内径1~4 mm,狭窄段长度50~60 mm;先天性食管狭窄1例(男患儿2岁),狭窄段内径2 mm,狭窄段长度20~30 mm。

截至2023年4月,根据Stooler吞咽困难分级,106例患儿中无症状、可正常进食(0级)92例,进食软质食物(1级)14例。
食管狭窄扩张是通过机械张力将食管狭窄处黏膜肌层撑裂来达到扩张效果,是食管狭窄首选治疗方式。食管狭窄食管扩张的时机一般在瘢痕形成早期(3周左右),扩张间隔时间推荐1~4周,但需注意早期食管狭窄处黏膜脆弱或组织粘连,扩张后容易引起食管全层破裂[5]。内镜引导下扩张不接触X线,术中可以监视球囊对食管壁的压力变化、有无活动性出血及穿孔,术后可直视下评估食管裂伤和出血程度。先天性食管狭窄(除食管壁内气管支气管软骨残留外)对球囊扩张的反应良好,成功率可达90%~95%[6];对腐蚀性食管狭窄、食管术后吻合口狭窄均有良好效果[7,8,9]。
本研究106例患儿均进行球囊扩张治疗,55例单纯胃镜直视下球囊扩张患儿取得良好效果,其中食管闭锁术后食管狭窄43例,腐蚀性食管狭窄12例。经球囊扩张后均恢复到正常进食状态。食管扩张术后常见并发症包括食管穿孔、出血等。食管扩张可导致食管破裂穿孔,发生率为2%~10%[10]。本研究患儿食管破裂1例,无大出血病例。以保守治疗为首选方案,经食管内外的通畅引流、抗炎、营养支持等治疗后好转。结合以往的治疗经验,本团队认为满足如下条件的患儿进行球囊扩张会获得良好的治疗效果,甚至单纯扩张治疗就可能治愈:①食管狭窄段≤2 cm;②单处狭窄;③扩张次数≤5次,一般超过3次仍复发,可考虑其他治疗方法。食管闭锁术后吻合口狭窄患儿,球囊扩张治疗效果良好,一般扩张1~2次就可恢复正常进食状态。相比之下,腐蚀性食管狭窄患儿扩张次数增加。
应用局部药物注射联合食管扩张治疗食管狭窄可取得良好的效果[11]。常用的药物为类固醇、丝裂霉素C等。类固醇可抑制炎症反应,抑制基质蛋白基因转录,减少胶原合成,减轻纤维化和瘢痕形成。常用的类固醇包括曲安奈德、倍他米松、地塞米松和甲泼尼龙等。丝裂霉素可抑制成纤维细胞生长,减少胶原合成及瘢痕形成。有报道对食管狭窄反复扩张难以改善的患儿局部使用丝裂霉素治疗,使62.5%的患儿脱离了长期扩张的困境[12]。局部注射激素主要分为多点多次法和多点单次法,并发症有食管穿孔、壁内感染、纵隔感染等。本研究中35例患儿应用球囊扩张联合食管黏膜下注射丝裂霉素C,有一定治疗效果,其中有10例另行食管支架置入治疗,术后未发生出血、纵隔感染等并发症。然而,丝裂霉素本身是化疗药物,延缓瘢痕形成中其使用频率、总剂量等尚无统一标准,临床应用需要慎重。本团队的治疗经验认为满足如下条件的患儿进行球囊扩张联合食管黏膜下药物注射治疗会获得良好的治疗效果:①食管狭窄段<4 cm;②单处狭窄;③腐蚀性食管狭窄。本研究35例患儿中注射3次10例,注射2次20例,注射1次5例,其中注射3次的患儿术后均再狭窄。故本团队认为药物注射1~2次即可,若效果欠佳,则考虑下一步治疗方案。
对于扩张效果不佳、腐蚀性食管狭窄、瘢痕挛缩明显或者狭窄段较长(≥5 cm)的患儿,通过放置食管支架可以改善狭窄症状,目前在儿童中的应用逐渐增多[13,14]。本研究25例患儿行食管支架置入治疗,其中有10例为球囊扩张联合黏膜下丝裂霉素注射治疗后效果欠佳。25例中21例效果良好,顺利出院。另4例发生再狭窄进行了外科手术治疗。食管支架手术并发症包括胸痛、呕吐、支架移位、再狭窄、炎性息肉增生等,临床发生率不高[15,16]。本研究25例中出现胸痛4例,呕吐6例。胸痛、呕吐为最常见的并发症。考虑发生原因:①镍钛合金材料置入人体后,伴随支架温度接近体温而逐渐打开,持续约24 h支架直径达到最大,完全扩张后的食管组织受到牵拉而导致疼痛;②腐蚀性食管狭窄患儿狭窄段周围神经丰富,对疼痛刺激较为敏感[17];③患儿对疼痛的感觉阈值低、耐受差。大多数患儿的疼痛一般1周内可自行缓解,无须使用止痛药,但应密切观察病情,排除出血、气胸及穿孔等并发症。本研究中出现呕吐、胸痛的患儿,1周内均自行缓解。本研究中3例发生支架移位。内径越小或者放置越接近食管上端或者下端的支架越容易发生移位[18,19]。考虑发生的原因可能为:①上杯口直径过小,或炎性水肿消退导致支架上杯口较食管直径相对变小;②狭窄段以上食管扩张明显,支架置入后食管回缩乏力;③不恰当的饮食。对于支架移位的患儿,本团队采用内窥镜联合透视下调整支架位置,有4例支架取出后再狭窄,考虑发生原因为难治性食管狭窄患儿多属于瘢痕体质,狭窄段相对较长,既往多次使用球囊扩张,使得食管黏膜反复撕裂、愈合,加重了瘢痕组织形成。置入的支架虽然可在短期对食管起到"塑形"作用,但支架取出后狭窄段食管具有较强的回缩能力。支架放置时间过短不利于狭窄段塑形,支架取出后容易导致再狭窄,但放置时间过长特别是裸支架存在炎性息肉增生风险,甚至导致支架难以取出,反而增加术后再狭窄概率。本研究中有5例发生炎性息肉增生。可能发生原因:①伴随食管蠕动作用,支架反复刺激食管黏膜,尤其是两端杯口膨大部分对柔性的食管产生横向切割力,造成食管的机械损伤;②支架置入时间过长,胃酸反流可腐蚀食管黏膜,导致肉芽组织增生。炎性息肉往往不需特殊处理,异物刺激解除后,可自行消失。一般在支架置入后3~4周进行胃镜检查,直视下调整支架,使得支架上、下移动,旋转移动。本中心的治疗经验认为满足如下条件的患儿进行食管支架置入治疗会获得良好的治疗效果:①食管狭窄段3~5 cm;②狭窄段开口距离食管上括约肌开口>2 cm。本研究置入支架治疗的25例患儿中,有15例未经过球囊扩张联合黏膜下药物注射治疗,其中2例为食管闭锁术后吻合口狭窄,13例为腐蚀性食管狭窄。2例食管闭锁术后吻合口狭窄患儿的狭窄段是长度约15 mm的节段性狭窄,经反复扩张治疗,效果欠佳。考虑患儿年龄小,经过多次手术治疗,黏膜下药物注射治疗效果可能欠佳,故经扩张后行支架置入治疗。13例腐蚀性食管狭窄患儿中,11例狭窄段长度≥5 cm,2例为多节段性狭窄,故经扩张后行支架置入治疗。置入支架治疗的患儿治疗效果良好,只有2例长段型腐蚀性食管狭窄、2例多节段型腐蚀性食管狭窄效果欠佳,行外科手术治疗。
狭窄段切除端端吻合术是反复扩张无效的短段型狭窄(狭窄段<2 cm)和确诊气管支气管软骨残留型食管狭窄者的标准术式[20,21]。本研究中5例患儿进行了狭窄段切除端端吻合术治疗,术后恢复良好。食管替代术适用于长段型纤维肌性狭窄、腐蚀性食管狭窄等经扩张无效者,是难治性食管狭窄的常用方法[12]。Takamizawa等[22]和Holler[23]等利用磁压榨吻合成功治疗了食管闭锁和食管狭窄患儿,刘仕琪等[24]、叶明棠等[25]近年亦相继报道该技术在食管吻合方面的成功应用。食管狭窄手术后常见并发症:①吻合口漏,常于术后食管造影时发现,经禁食及抗生素治疗多可愈合,但部分患儿需要置入覆膜支架[15];②吻合口再狭窄,常于食管造影检查时发现,狭窄较重者或有临床表现者可再行食管扩张术;③反流性食管炎,可用药物如抑酸制剂、H2-拮抗药、质子泵抑制药、食管动力药等治疗,如药物不能控制,则需要行胃底折叠术。外科手术治疗的5例患儿,术后未见明显并发症。本中心的治疗经验认为如下条件的患儿须进行外科手术治疗:①反复扩张等治疗无效的难治性食管狭窄;②气管支气管软骨残留型食管狭窄;③长段型纤维肌性狭窄食管狭窄;④长段型食管狭窄(≥5 cm)。
总之,儿童食管狭窄外科治疗的总目标是使患儿恢复顺畅的进食、达到同龄健康儿童的生长发育水平。各类食管狭窄若采用单一的治疗措施不一定能达到理想效果,可以相互借鉴,互为补充,力争早期诊断、早期治疗。通过综合应用食管扩张、黏膜下注射药物、食管支架置入,必要时行外科手术,并加强围手术期处理以及出院后的随访管理,使其尽早达到理想的食管形态和功能,满足患儿正常生长发育需求。
所有作者均声明不存在利益冲突



























