
探讨高龄对肝硬化患者肝移植生存预后的影响。
随访统计单中心因肝硬化行肝移植的152例成人受者的资料,其中131例为非高龄组(<60岁)受者,21例为高龄组(≥60岁)受者。采用回顾性研究,收集受者与供者基本信息、手术资料及生存状况,并对受者肝移植术后1、3、 5年累积存活率进行对比分析。
与非高龄组相比较,高龄组中女性比例较高(P<0.05);高龄组受者Child-Pugh评分、终末期肝病模型评分均低于非高龄组(P<0.05);且高龄组急性细胞性排斥反应发生率与胆道狭窄发生率低于非高龄组(P<0.05)。高龄组移植后1、3和5年受者存活率分别为81.95%、58.38%及43.50%,累积中位生存时间为1 410 d;而非高龄组移植后1、3和5年受者存活率分别87.98%、70.99%和44.46%,累积中位生存时间为1 465 d,两组存活率的差异无统计学意义(P>0.05)。
高龄并未降低肝硬化肝移植受者的累积存活率,低风险的高龄患者可获得与非高龄患者类似的长期生存结果。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
慢性肝硬化医疗管理的进步使肝硬化患者寿命延长,同时使需要肝移植的高龄肝硬化患者的数量亦增加[1,2,3]。高龄本身不是肝移植的禁忌,如果受者体质适合,可考虑高龄患者进行肝移植[4]。关于高龄肝硬化患者的肝移植临床评价的报道较少,相关临床数据仍不健全。本文对天津市第一中心医院东方器官移植中心2007年1月至2009年1月间152例肝硬化肝移植受者的临床资料进行分析与总结,旨在探讨高龄对肝硬化肝移植生存预后的影响,为高龄肝硬化患者肝移植手术及预后提供依据。
2007年1月至2009年1月间,成人肝硬化肝移植受者共152例,其中非高龄组(<60岁)131例,高龄组(≥60岁)21例。患者术前诊断均为肝硬化,均无肿瘤。供肝来源于尸体供者或亲属活体供者。供者与受者ABO血型均相符,且Rh血型均为阳性。随访统计5年内(1 825 d)患者的生存状况,随访终点为2014年1月31日,以死亡作为终点事件。所有患者均签署由天津市第一中心医院伦理委员会批准的患者知情同意书,研究符合医学伦理学规定,研究方案获得审查委员会批准。
手术方式均为同种异体原位肝移植术。术后受者常规应用他克莫司(Tac)+吗替麦考酚酯(MMF)+泼尼松的三联免疫抑制治疗;根据血药浓度调整Tac用量,其浓度谷值在术后1~6个月为8~10 μg/L,6~12个月为5~8 μg/L,12~24个月为5 μg/L左右,24个月后为5 μg/L;MMF的剂量为1 g/d,服用至术后6个月,当外周血白细胞低于3×109/L时可以减至0.5 g/d或者停用;术后1~3个月内停用泼尼松。术后常规口服恩替卡韦和更昔洛韦预防乙型肝炎、丙型肝炎病毒复发与巨细胞病毒感染。
术前收集患者基本资料(年龄、性别、血型、身高、体重等),并评估患者的心功能、呼吸功能、肝功能、肾功能等,并行肝功能相应的评分,如终末期肝病模型(MELD)评分、Child-Pugh评分等。术中收集供者的基本资料,同时记录术中供肝冷热缺血时间、手术时间、失血量以及术后肝动脉和门静脉血栓形成、巨细胞病毒感染、胆道狭窄等基本信息。术后定期门诊随访,第1年每个月随访1次,以后每3~6个月随访1次,随访项目包括血常规、肝功能、肾功能、血Tac浓度、乙型肝炎病毒表面抗体滴度,有丙型肝炎病史者每2~3个月行1次丙型肝炎病毒核糖核酸检查;同时详细记录受者的生存状况。
应用SPSS(19.0版)统计软件进行统计学分析。数据以均数±标准差( ±s)表示,S-W检验、Q-Q plot检测数据正态性,组间两两比较用t检验,样本率的比较采用卡方检验,累计存活率分析采用Kaplan-Meier法检验,P<0.05为差异有统计学意义。
±s)表示,S-W检验、Q-Q plot检测数据正态性,组间两两比较用t检验,样本率的比较采用卡方检验,累计存活率分析采用Kaplan-Meier法检验,P<0.05为差异有统计学意义。
受者与供者基本资料见表1,通过S-W检验、Q-Q plot检测数据正态性,样本数据均符合正态分布。高龄组受者年龄为(64.2±3.5),非高龄组受者年龄为(45.3±7.9)岁,两组的差异有统计学意义(P<0.01);并且高龄组女性受者的比例高于非高龄组(P<0.05)。两组间受者身高和体重的差异无统计学意义(P>0.05)。高龄组Child-Pugh评分为(9.21±2.41)分,非高龄组为(11.79±2.88)分,高龄组Child-Pugh评分低于非高龄组(P<0.05);而高龄组MELD评分为(18.4±6.8)分,非高龄组为(22.8±9.8)分,高龄组MELD评分也低于非高龄组(P<0.05)。而两组乙型肝炎病毒感染率、丙型肝炎病毒感染率、肝性脑病发生率、胆红素总量相比较,差异无统计学意义(P>0.05)。两组供者来源、供者年龄、供者性别相比较,差异均无统计学意义(P>0.05)。
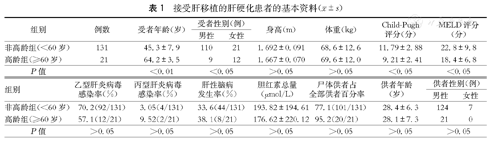
接受肝移植的肝硬化患者的基本资料( ±s)
±s)
接受肝移植的肝硬化患者的基本资料( ±s)
±s)
| 组别 | 例数 | 受者年龄(岁) | 受者性别(例) | 身高(m) | 体重(kg) | Child-Pugh评分(分) | MELD评分(分) | |
|---|---|---|---|---|---|---|---|---|
| 男性 | 女性 | |||||||
| 非高龄组(<60岁) | 131 | 45.3±7.9 | 110 | 21 | 1.692±0.091 | 68.6±12.6 | 11.79±2.88 | 22.8±9.8 |
| 高龄组(≥60岁) | 21 | 64.2±3.5 | 9 | 12 | 1.667±0.070 | 69.6±12.0 | 9.21±2.41 | 18.4±6.8 |
| P值 | <0.01 | <0.05 | >0.05 | >0.05 | <0.05 | <0.05 | ||
| 组别 | 乙型肝炎病毒感染率(%) | 丙型肝炎病毒感染率(%) | 肝性脑病发生率(%) | 胆红素总量(μmol/L) | 尸体供者占全部供者百分率 | 供者年龄(岁) | 供者性别(例) | |
| 男性 | 女性 | |||||||
| 非高龄组(<60岁) | 70.2(92/131) | 3.05(4/131) | 33.6(44/131) | 193.82±194.61 | 77.1(101/131) | 28.4±6.3 | 124 | 7 |
| 高龄组(≥60岁) | 57.1(12/21) | 9.52(2/21) | 38.1(8/21) | 176.62±220.12 | 95.2(20/21) | 28.1±7.3 | 21 | 0 |
| P值 | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 | |
在肝移植术中,两组供肝冷缺血时间、热缺血时间、移植手术时间、失血量、关腹前门静脉压力等方面相比较,差异均无统计学意义(P>0.05,表2)。术后两组肝动脉血栓形成与门静脉血栓形成的差异也无统计学意义(P>0.05)。高龄组受者急性细胞性排斥反应的发生率为0(0/21),而非高龄组受者急性细胞性排斥反应的发生率为17.6%(23/131),高龄组的发生率明显低于非高龄组,差异有统计学意义(P<0.05);同时高龄组胆道狭窄发生率为0(0/21),明显低于非高龄组的16.0%(21/131),差异有统计学意义(P<0.05)。两组巨细胞病毒感染率、住院时间相比较,差异无统计学意义(P>0.05,表3)。
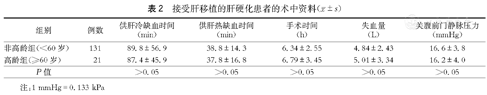
接受肝移植的肝硬化患者的术中资料( ±s)
±s)
接受肝移植的肝硬化患者的术中资料( ±s)
±s)
| 组别 | 例数 | 供肝冷缺血时间(min) | 供肝热缺血时间(min) | 手术时间(h) | 失血量(L) | 关腹前门静脉压力(mmHg) |
|---|---|---|---|---|---|---|
| 非高龄组(<60岁) | 131 | 89.8±56.9 | 38.8±14.3 | 6.34±2.55 | 4.84±2.43 | 16.6±3.8 |
| 高龄组(≥60岁) | 21 | 87.4±45.9 | 37.8±16.8 | 6.79±3.45 | 5.01±3.34 | 16.2±4.0 |
| P值 | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 |
注:1 mmHg=0.133 kPa
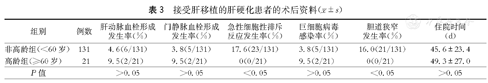
接受肝移植的肝硬化患者的术后资料( ±s)
±s)
接受肝移植的肝硬化患者的术后资料( ±s)
±s)
| 组别 | 例数 | 肝动脉血栓形成发生率(%) | 门静脉血栓形成发生率(%) | 急性细胞性排斥反应发生率(%) | 巨细胞病毒感染率(%) | 胆道狭窄发生率(%) | 住院时间(d) |
|---|---|---|---|---|---|---|---|
| 非高龄组(<60岁) | 131 | 4.6(6/131) | 3.8(5/131) | 17.6(23/131) | 3.8(5/131) | 16.0(21/131) | 45.6±23.4 |
| 高龄组(≥60岁) | 21 | 9.5(2/21) | 9.5(2/21) | 0(0/21) | 9.5(2/21) | 0(0/21) | 49.3±27.0 |
| P值 | >0.05 | >0.05 | <0.05 | >0.05 | <0.05 | >0.05 |
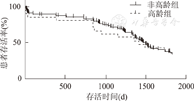
152例患者均随访5年,随访率达100%。高龄组1、3和5年受者存活率分别为81.95%、58.38%及43.50%,累积中位生存时间为1 410 d;而非高龄组1、3和5年受者存活率分别为87.98%、70.99%和44.46%,累积中位生存时间为1 465 d,两组存活率相比较,差异无统计学意义(P>0.05,图1)。非高龄组主要死亡原因为肺部感染(33.71%,30/89)、败血症(15.73%,14/89)、心血管事件(15.73%,14/89,包括冠状动脉粥样硬化性心脏病、心功能衰竭和心律失常等)和原发性移植物功能障碍(14.61%,13/89)等;而高龄组主要死亡原因分别为心血管事件(30.77%,4/13)、脑血管事件(脑出血和脑梗死等,23.08%,3/13)、肺部感染(15.38%,2/13)等(表4)。
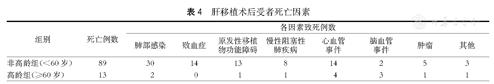
肝移植术后受者死亡因素
肝移植术后受者死亡因素
| 组别 | 死亡例数 | 各因素致死例数 | |||||||
|---|---|---|---|---|---|---|---|---|---|
| 肺部感染 | 败血症 | 原发性移植物功能障碍 | 慢性阻塞性肺疾病 | 心血管事件 | 脑血管事件 | 肿瘤 | 其他 | ||
| 非高龄组(<60岁) | 89 | 30 | 14 | 13 | 8 | 14 | 2 | 5 | 3 |
| 高龄组(≥60岁) | 13 | 2 | 0 | 1 | 1 | 4 | 3 | 1 | 1 |

越来越多的失代偿终末期肝病患者需接受肝移植,这种情况使得肝移植选择标准被重新评估,同时器官分配亦进行了优化[5,6]。在许多中心,老年患者往往被视为风险较高的人群,原因是老年患者肝脏和非肝脏相关并发症发生率以及死亡率较高[7,8]。而高龄患者一个潜在的优势是免疫系统功能的减退,这样的免疫特征可减轻移植排斥反应的严重程度[9],但同时免疫系统功能减退的一个潜在缺点是增加了感染的发生率,以及增加了肿瘤发生的风险。
Zetterman等[10]评估735例尸体肝移植,其中包括年轻受者(<60岁)和老年受者(≥60岁),发现老年受者移植后短期存活有显著恶化。此后,Levy等[11]报道称,住院治疗老年受者短期移植结果显著恶化,而低风险的老年受者可获得类似于年轻受者的结果。Garcia等[12]报道,Child-Pugh评分C级的高龄患者(≥65岁)移植失败的风险较大,而低MELD评分和Child-Pugh评分低于C级的低风险高龄受者与年轻受者(<65岁)相比,其5年受者存活率相类似[13]。因此,许多移植中心开始意识到,只要无严重的肝病和非肝病并发症,不应该拒绝为高龄患者行肝移植术。综合评价肝移植受者,应包括患者状态、MELD评分、门静脉高压的程度等[14]。即使不考虑受者年龄,高MELD评分仍是移植物功能障碍和死亡的显著危险因素,所以MELD评分>20分的高龄患者可能不会考虑行肝移植术。
基于这些背景下,本研究通过对我移植中心肝硬化患者肝移植术后的临床资料进行分析与总结,旨在探讨高龄对肝硬化肝移植生存预后的影响。研究结果表明,相对于非高龄组,高龄组中女性比例较高;高龄组Child-Pugh评分、MELD评分明显低于非高龄组,而在乙型肝炎病毒感染率、丙型肝炎病毒感染率、肝性脑病发生率、胆红素总量方面相比较,以及在供者来源、供者年龄、供者性别方面相比较,两组的差异均无统计学意义。在肝移植术中,两组供肝冷缺血时间、供肝热缺血时间、手术时间、失血量、关腹前门静脉压力以及术后肝动脉血栓形成与门静脉血栓形成发生率的差异均无统计学意义;而肝移植术后高龄组胆道狭窄发生率低于非高龄组,这可能与MELD评分高低相关,因为MELD评分和Child-Pugh评分越高的患者术前凝血功能和肾功能较差,术中出血量多,胆道缺血程度加重,使得胆道狭窄发生概率增加[15]。本研究中,高龄组患者急性细胞性排斥反应的发生率为0,而非高龄组患者急性细胞性排斥反应的发生率为17.6%,急性细胞性排斥反应发生率的差异有统计学意义。Liu等[16]认为,高龄组急性细胞性排斥反应的发生率显著降低与高龄受者体液免疫应答减退有关。免疫功能的减退是一把双刃剑,排斥反应的风险降低,而感染和恶性肿瘤的风险增加。但是,由于严重感染的发展通常与早期移植肝功能和移植前受者状态相关,老年人的免疫特点有减少早期急性细胞性排斥反应发生的可能性。
生存分析提示,高龄组与非高龄组1、3和5年受者存活率的差异无统计学意义,而死亡原因总体而言,非高龄组主要为肺部感染、败血症、心血管事件和原发性移植物功能障碍等,其中肺部感染、败血症所占比例较大,而肺部感染、败血症主要发生在肝移植术后围手术期。而高龄组主要死亡原因分别为心血管事件、脑血管事件、肺部感染等;高龄受者体质储备较差,常伴随慢性疾病,尤其是心脑血管疾病,以致高龄组受者远期死亡原因主要是心脑血管疾病。
统计分析综合评估发现,低风险高龄肝硬化患者进行肝移植,可获得较理想的中、长期结果。本研究的主要局限性是存在选择偏倚,虽然大型多中心研究也许能够克服这些限制,类似的选择偏倚仍可能存在。



























