
探讨自发性低颅压(SIH)的发病机制、临床特点、影像学表现和预后转归。
分析北京协和医院近20年间12例SIH患者的临床和影像学表现,进行长期随访,了解其预后转归。
12例患者均为成年起病,表现为体位性头痛,经保守对症治疗后症状好转。SIH头颅MRI显示脑叶出血、硬膜下血肿、小脑扁桃体下位、蛛网膜下腔出血、脑室变小、垂体充血、脑静脉窦扩张、弥漫性硬脑膜强化。
SIH以体位性头痛为特点,其MRI改变与脑脊液容量减少后发生的代偿改变有关,远期预后较好。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
自发性低颅压(spontaneous intracranial hypotension,SIH),最早报道于1938年,表现为体位性头痛,腰穿脑脊液压力低于或等于60 mmH2O(1 mmH2O=0.009 8 kPa),头磁共振成像(MRI)示弥漫性硬脑膜强化,无硬脑脊膜穿刺或其他引起脑脊液漏的原因[1]。SIH患病率为1/50 000,年发病率为5/100 000[2]。自2004至2012年,世界范围内共报道169例SIH病例(75例男性,84例女性)[3]。鉴于SIH临床报道不多,有随访记录的少见,本研究对12例SIH患者临床及影像特点进行分析,并长期随访了解其预后转归。
1992年1月至2011年5月期间在北京协和医院诊治的低颅压患者,所有患者均行腰穿、头颅CT和核磁共振检查。根据国际头痛疾病分类第3版(ICHD-3)[4]和Schievink等[5]制定的标准,SIH的诊断需满足下述所有条件:(1)头MRI影像上发现脑脊液漏的相关改变(例如,脑膜强化)和(或)脑脊液压力降低(≤60 mmH2O);(2)无近期硬脑脊膜穿刺史;(3)无其他引起脑脊液漏的原因。
采取门诊与电话方式随访,随访间隔每6月一次至1~2年,以后每1~2年一次。
统计描述采用计量资料 ±s,计数资料频数(百分比)表示。
±s,计数资料频数(百分比)表示。
共收集低颅压患者18例,6例为继发性低颅压,其中1例继发于结缔组织病干燥综合征;1例继发于左侧颞前巨大蛛网膜囊肿引流术后,术后出现低颅压、颅内静脉窦扩张、小脑扁桃体下疝并压迫高段颈髓;2例继发于头外伤术后;1例继发于脑室分流术后;1例继发于腰穿之后。其余12例均符合SIH诊断标准。SIH患者平均年龄42.25岁(28~62岁);女性7例。1例患者(病例3)因脑脊液压力测不出未行脑脊液检查,11例患者行脑脊液检查,6例白细胞略偏高,均≤10/mm3,10例蛋白升高(0.30~1.47 g/L),表1。
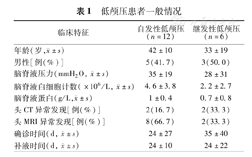
低颅压患者一般情况
低颅压患者一般情况
| 临床特征 | 自发性低颅压(n=12) | 继发性低颅压(n=6) |
|---|---|---|
年龄(岁, ±s) ±s) | 42±10 | 33±19 |
| 男性[例(%)] | 5(41.7) | 3(50.0) |
脑脊液压力(mmH2O,  ±s) ±s) | 35±19 | 28±31 |
脑脊液白细胞计数(×106/L,  ±s) ±s) | 4.6±3.8 | 2.2±2.7 |
脑脊液蛋白(g/L, ±s) ±s) | 1±0.4 | 0.7±0.8 |
| 头CT异常发现[例(%)] | 2(16.7) | 2(33.3) |
| 头MRI异常发现[例(%)] | 8(66.7) | 2(33.3) |
确诊时间(d,  ±s) ±s) | 24±27 | 35±40 |
补液时间(d,  ±s) ±s) | 24±10 | 24±22 |
SIH患者2例头MR平扫结果正常,1例患者既往有高血压病史,头MRI显示侧脑室周围脱髓鞘样改变,余未见异常。SIH头MRI异常表现包括:脑叶出血、硬膜下血肿、脑静脉窦血栓、小脑扁桃体下位、蛛网膜下腔出血、脑室变小、垂体充血、脑静脉窦扩张、弥漫性硬脑膜强化。
所有SIH患者经卧床保守补液治疗后症状好转,无死亡病例。1例患者治疗1个月后失访,其余11例平均随访时间(6.4±1.8)年,预后良好,无复发。
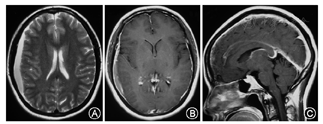
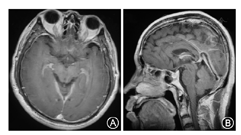
(1)病例1:女,37岁,因"头痛1个月"入院。表现为后颈枕部钝痛,向肩胛部放射伴恶心、耳鸣,躺下后10 min可缓解。病后第2天头CT正常。病后第3天头MRI正常。查体:四肢腱反射活跃-亢进,余神经系统查体(-)。病后第5天腰椎穿刺,压力35 mmH2O,白细胞10×106/L,蛋白0.74 g/L,糖、氯化物正常。病后1个月头CT:右侧颞、顶、额部硬膜下血肿;小脑幕增宽,考虑硬膜下血肿。病后41 d头MRI平扫+增强:右侧额顶颞叶亚急性晚期硬膜下血肿;左侧颞、顶、枕部、双侧小脑幕上硬膜下少量出血;小脑扁桃体下位;弥漫性硬脑膜强化(图1)。颈胸腰椎增强MRI正常。(2)病例2:男,53岁,因"头痛3 d"入院。表现为前额部胀痛,伴后颈背部疼痛,躺下休息可缓解。神经系统查体(-)。病后3 d时腰穿,压力50 mmH2O,脑脊液白细胞6×106/L,蛋白0.65 g/L,糖、氯化物正常。起病当天头CT正常。发病第7天头MRI平扫+增强:硬脑膜、小脑幕异常增厚强化(图2)。头MRV、颈胸腰椎增强MRI正常。(3)病例3:女,39岁,因"头痛20 d,左侧肢体无力5 d"入院。表现为全头搏动性胀痛,平卧位减轻,坐起后加重,伴头晕、头鸣、耳鸣、颈部僵硬感。发病第4天头CT正常。第13天、18天各出现一次癫痫大发作,持续约1 min。第13天时头MRI正常。第15天突发右侧肢体无力,查体:右上肢肌力4级,右下肢0级,右侧Babinski征、Chaddock征(+),颈抵抗(+)。腰穿测不出压力。第19天复查头CT示左额顶叶高密度影,提示硬膜下血肿。第21天头MRI:硬膜下血肿吸收明显,遗留左侧额叶皮质下片状长T2信号。全脑DSA检查正常。(4)病例4:男,44岁,因"头痛半个月"就诊。头顶及颈部持续胀痛,坐起或站立时明显,平卧位可减轻。发病第4天头CT:未见异常。腰穿压力20 mmH2O,白细胞0,蛋白0.8 g/L,糖、氯化物正常。第22天头MRI增强:脑膜强化、脑室缩小。颈胸腰椎增强MRI正常。(5)病例5:女,28岁,因"头痛4 d"就诊。头痛位于头顶及后颈背部,胀痛,平卧时减轻,站立时加重难以忍受,伴头晕、恶心、呕吐。查体:颈抵抗3横指。腰穿压力30 mmH2O,白细胞6×106/L,蛋白1.3 g/L,糖、氯化物正常。发病第2天头CT正常。半个月时头MRI:垂体饱满。头MRA 、MRV和颈椎MRI正常。


脑脊液以0.35 ml/min的速度产生,成人脑脊液容量平均(157±59) ml,人类形成脑脊液的速度通常是恒定的,大部分脑脊液经蛛网膜颗粒从大脑静脉和静脉窦吸收[6]。SIH由自发性脑脊液漏导致,关于自发性脑脊液漏的确切原因尚不得而知,目前普遍怀疑与脊膜结构薄弱有关[7]。SIH的MRI改变与脑脊液容量减少后发生的代偿改变有关,根据Monroe-Kellie假说,脊髓脑脊液的丢失被血管内容物增加所代偿,所以会出现脑膜弥漫性强化、静脉扩张、垂体充血、硬膜下水囊瘤形成,脑位下垂则与脑脊液浮力降低有关[7]。传统脊髓X线造影、CT脊髓造影或者脑池造影术均可发现脑脊液漏,目前认为CT脊髓造影是发现脑脊液漏最敏感和可靠的办法。但SIH患者中,并不总是能发现脑脊液漏,有些学者认定SIH是由于颅内静脉系统压力低使得脑脊液吸收增多所致[8]。
既往对SIH的动态影像学变化及预后转归所知甚少,本研究有助于临床数据补充,典型病例诊断SIH的临床和影像学特点具有代表性。
SIH临床症状多样,常见症状包括体位性头痛、颈痛、恶心、单侧或双侧外展神经麻痹、头晕、听力减退、视物模糊、畏光、视野缺损、肩胛间疼痛、腰背痛、上肢神经根症状。少见或罕见症状有面部麻木或面肌无力、溢乳、神经源性膀胱、昏迷、第三四颅神经麻痹、舞蹈症、帕金森综合征、共济失调、额颞叶痴呆、脑病、颈神经根病和迷路积水[9]。SIH的头痛通常为头部弥漫性疼痛和(或)钝痛,坐起或站立后15 min内加重,易被误诊。
SIH应与其他头痛疾病相鉴别。(1)原发性劳力性头痛是指在做Valsalva型的动作(例如咳嗽、打喷嚏、用力、提重物、做弯曲或推的动作)时诱发的急性一过性头痛,并且颅内无结构性损害[10]。脑脊液漏导致的头痛经常在做Valsalva型的动作时明显加重[10]。(2)偏头痛一般持续4~72 h,单侧多见,日常体力活动会加重头痛,与体位无关,而低颅压性头痛双侧多见并且与体位有关。(3)紧张性头痛一般为压迫或紧缩(非搏动)性头痛,与体位无明显相关性,持续30 min到7 d,无恶心和呕吐。低颅压性头痛常为搏动性头痛、钝痛或胀痛,常伴恶心呕吐、耳鸣、后颈部疼痛或僵硬感等,坐起或站立后15 min内加重。(4)病毒性脑膜炎常有上呼吸道感染、发热、肌痛、乏力等症状,可伴精神症状,血沉增快,脑脊液压力增高,细胞数轻中度增高,蛋白质轻度增高,头MRI等影像学检查可在颞叶、额叶出现病灶。低颅压性头痛通常不伴上呼吸道感染、发热、肌痛、乏力、精神异常等症状。头MRI表现亦与病毒性脑膜炎不同。(5)高颅压头痛脑脊液压力>200 mmH2O,头痛常在用力、咳嗽、弯腰、低头等动作时加重,可合并外展肌麻痹和眼底视乳头水肿。低颅压头痛脑脊液压力≤60 mmH2O。(6)继发性低颅压综合征,包括马方综合征、Ehlers-Danlos综合征、常染色体显性遗传多囊肾、自发性视网膜脱离等,结缔组织病变亦可造成继发性低颅压综合征[7]。
本研究中有2例患者在病初未行腰穿检查情况下,根据头痛误判为高颅压,脱水降颅压治疗使得症状进一步加重。本研究中有1例继发于结缔组织病干燥综合征的低颅压病例,激素加环磷酰胺治疗2周后脑脊液压力即由30 mmH2O恢复至130 mmH2O,蛋白恢复正常(0.54 g/L→0.28 g/L),头晕症状消失。
SIH在MRI上主要表现为硬脑膜弥漫性增强、硬膜下积液或出血、垂体增大、静脉窦扩张、脑室变小以及小脑扁桃体向下移位等[3,7]。20%的患者不出现硬脑膜强化或其他任何MRI异常表现[7]。本文中五例典型患者MRI表现涵盖了SIH大部分MRI特点。SIH的头MRI存在动态演变过程,病程初期MRI结果正常,可以在病程中发生变化,本研究中病例1和3患者的头MRI均存在动态演变过程。
许多文献报道称SIH患者经保守治疗和卧床休息可以改善症状,预后良好[6,11,12]。多数SIH患者症状可以自发缓解,对于寻求医学帮助的患者,治疗方法包括[3]:保守治疗、药物治疗(皮质类固醇、静脉注射咖啡因、静脉茶碱、口服乙酰唑胺)、脊髓硬膜外间隙注射自体血补丁、经皮纤维蛋白封闭、手术治疗和鞘内注射盐水或人工脑脊液。
目前认为头MRI异常并且有局限性脑脊液漏的自发性低颅压患者预后好,而病初头MRI正常并且有弥漫性多水平脑脊液漏的患者预后差[7]。SIH的头MRI影像异常可以随着脑脊液漏的好转而在数天或数周内好转,临床症状的改善通常先于MRI影像,对于脑脊液漏未得到针对性治疗的患者,MRI异常可持续存在,小的硬膜下血肿可在数天或数周内吸收,大的血肿需3个月或更长时间吸收完全[7]。Takahashi等报道26.4%的继发于SIH的硬膜下血肿可以经保守治疗好转[5]。
本研究中12例患者均拒绝了脊髓X线造影或CT脊髓造影的检查,其临床症状经卧床补液保守治疗后好转,长期随访未再复发。1例患者在卧床补液治疗半月后复查腰穿脑脊液压力由45 mmH2O升至65 mmH2O。例3患者硬膜下血肿数天内即吸收完全。
SIH虽然临床不常见,但早期诊断早期治疗很重要,头MRI增强检查阳性发现率较高,颈胸腰椎增强MRI对脑脊液漏的发现阳性率低,大多数患者即使经保守治疗也能预后良好。



























