
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
1912年,Herrick[1]首次阐述冠状动脉血栓与心肌梗死发生的关系。1980年DeWood等[2]证实,在4 h内接受冠状动脉造影的急性心肌梗死(AMI)患者中,88%的梗死相关血管存在血栓。2007年Sianos等[3]也发现,在接受直接经皮冠状动脉介入治疗(PCI)的AMI患者中,91.6%可见冠状动脉血栓。AMI血栓机制确立,推动了再灌注治疗的快速发展。
随着直接PCI的广泛开展,由冠状动脉血栓导致的微循环栓塞等问题日渐突出,血栓抽吸和栓塞防护装置由此应运而生。早在20世纪80年代,就有血栓抽吸装置用于处理冠状动脉血栓的个案报道。2002年,第一项评价机械抽吸导管用于急性冠脉综合征(ACS)的随机对照试验发表[4]。2003年,美国FDA批准第一款带有远段封堵球囊的手动血栓抽吸装置。2005年,第一项在急性ST段抬高型心肌梗死(STEMI)直接PCI时使用手动抽吸导管的随机对照试验发表[5]。2008年发布的TAPAS试验进一步推动了血栓抽吸的临床应用与研究进程[6]。然而,近年发表的TASTE试验[7]和TOTAL试验[8]却使血栓抽吸的疗效与安全性面临质疑。目前,冠状动脉血栓抽吸在临床上存在较多争议与困惑,亟需统一认识,规范技术操作,指导合理应用,进而提高AMI介入治疗的水平。
多数冠状动脉血栓继发于斑块破裂,部分来源于心腔内血栓、细菌性赘生物、人工心脏瓣膜血栓、钙化栓、脂肪栓和癌栓等。无论是血栓形成还是血栓栓塞,其病理成分大致相同,均含血小板、红细胞、中性粒细胞、纤维蛋白和胆固醇结晶等。研究显示,冠状动脉血栓成分与缺血时间密切相关。缺血时间与纤维蛋白含量呈正相关,与血小板含量呈负相关[9]。
根据血栓发生时间的长短,可将血栓分为早期血栓(<1 d)、中期血栓(1~5 d)和晚期血栓(>5 d)。根据病理特征一般将其分为三种类型:(1)白色血栓:主要由血小板和纤维蛋白构成,又称为血小板血栓或析出性血栓。多发生于血流较快的部位(如动脉、心瓣膜、心腔内)或血栓形成于血流较快的时期。(2)红色血栓:一般发生在血流极度缓慢乃至停止之后,其形成过程与血管外凝血过程相同。(3)混合血栓:多发生于血流缓慢的部位,在结构上可分为头、体、尾三个部分。头部由白色血栓形成,常黏附于血管壁形成附壁血栓;体部由红色血栓与白色血栓组成;尾部则由红色血栓组成。实际上,临床上多为混合血栓,单纯的红色血栓或白色血栓均少见。
影像学在冠状动脉血栓的识别、分级、分类、鉴别诊断以及指导介入治疗等方面具有重要意义。除冠状动脉造影(CAG)外,其他影像学方法包括血管内超声(IVUS)和光学相干断层成像(OCT)等。
CAG显示的冠状动脉血栓表现为多个体位投照下冠状动脉内的非钙化充盈缺损,可伴有或不伴有对比剂滞留。当血栓量较少或管腔内存在其他非血栓物质时,CAG识别血栓的价值有限。此外,CAG无法检测微血栓与小血栓,对附壁血栓和中等血栓的检出率也较低,易受投照体位等因素的影响,且无法鉴别血栓的性质。
2001年,Gibson等[10]根据血栓负荷的最大线性尺寸(linear dimension)提出了TIMI血栓分级(TTG):0级,造影下未见血栓影;1级,可疑血栓,表现为造影下管腔显影模糊、云雾影、病变轮廓不规则或完全闭塞部位突出管腔的平滑新月形影像提示但无法确诊血栓;2级,明确存在血栓,线性尺寸≤1/2血管直径;3级,明确存在血栓,线性尺寸为血管直径的1/2~2倍;4级,明确存在血栓,线性尺寸≥2倍的血管直径;5级,血栓形成导致完全闭塞。作者还将TTG 2~5级定义为造影可见血栓。多项研究根据TTG分级将血栓负荷分为高血栓负荷(≥4级)和低血栓负荷(≤3级)两大类。然而,完全血栓闭塞虽被定义为5级,但其实际血栓线性尺寸或血栓负荷未必最大。Sianos等[3]的研究显示,初始血栓分级为5级的患者,在导丝或1.5 mm的小球囊通过(或扩张)以恢复血流后再次进行血栓分级,最后仅有0.4%的患者仍为5级,1/3的患者转变为4级,其余多数患者转变为1~3级。由此可见,冠状动脉急性血栓极不稳定,对于完全性血栓闭塞患者,在导丝或小球囊通过(或扩张)后进行血栓分级可能更为合理。
2002年Yip等[11]提出,满足至少两项以下特征可称为"高血栓负荷":(1)梗死相关动脉目测参考血管直径≥4.0 mm;(2)血栓呈长条状,线性尺寸超过参考血管直径的3倍;(3)"截断"样或齐头闭塞,闭塞近端没有逐渐变细的管腔;(4)闭塞近端血栓堆积(线性尺寸>5.0 mm);(5)闭塞近端存在漂浮的血栓;(6)闭塞远端持续对比剂滞留。
冠状动脉血栓的IVUS特征包括:(1)凸向管腔的分叶状团块;(2)伴有斑点的闪烁样外观;(3)可疑血栓和基础斑块之间有明确的分界;(4)可见明显的血液流经的微通道;(5)可随血流发生局部位移。新鲜血栓以低回声为主,呈现略松散的棉絮状、层片状结构,可在管腔内随血流局部移动。由于血栓回缩和分层机化,陈旧性血栓的回声强度较强,且无新鲜血栓的点状闪烁样回声。
OCT不仅能更好地识别血栓,判断血栓的性质与类型,且在观察血栓形态方面也有独特优势。OCT显示的红、白色血栓均表现为突出于管腔的中等亮度的团块,亮度低于内膜。由于红色血栓富含红细胞,其对近红外光线的遮挡(吸收)作用较白色血栓更强。因此,红色血栓表现为在红细胞形成的高信号表面及其后很强的衰减区域,其密度较低;而白色血栓则表现为与内膜信号相似的突出管腔的不规则团块,其密度较高,且与斑块之间存在联系。突出于管腔的血栓一般较容易识别,而位于溃疡或破裂斑块内部不突出于管腔的血栓易与脂质核混淆,逐帧分析前后图像有助于鉴别。
由于存在加重远端栓塞、增加时间延搁等风险,在STEMI伴有明显血栓负荷的患者,直接PCI术前不推荐常规采用IVUS或OCT等影像学方法评价。然而,当血栓抽吸后需要了解血管病变情况、鉴别夹层与血栓以及指导PCI时,可考虑采用IVUS或OCT评价。
手动抽吸的原理是利用注射器抽吸产生负压吸出血栓。抽吸装置由抽吸导管、压力延长管、抽吸注射器、抽吸物滤网等基本部件组成,抽吸导管一般带有可锁定接头或三通。
目前,临床应用的手动抽吸导管根据头端开孔的设计多为斜面切孔型,也有个别品牌为斜面切孔+侧孔型(如Diver CE)。多数血栓抽吸导管杆部有金属编织结构,且多采用密度相同的固定编织(如ZEEK)。为提高导管远端的柔顺性,部分抽吸导管采用由远及近密度逐渐增高的全程可变编织方式(如Export Advance),极个别品牌杆部无金属编织(如Thrombuster Ⅱ)。多数抽吸导管内配有预置钢丝,可增强其推送性和抗折性。一般采用近远端粗细一致的钢丝,也有部分导管采用由近及远渐细的钢丝(如Export Advance),以增强导管在冠脉内的顺应性和通过性。不同品牌抽吸导管的导丝交换腔长度各异,导丝交换腔越长,抽吸导管的轨道性也越好,且能减少回撤导管时导丝在指引导管头段打折。
抽吸导管的抽吸效率与头端设计、抽吸腔大小、内腔形态以及导管型号等相关。头端抽吸腔有圆形、半圆形、半月形等设计,一般而言,圆形抽吸腔的导管的抽吸效率较高。多数品牌的抽吸导管提供6F和7F两种型号,选择较大型号能提高抽吸效率。常见手动血栓抽吸导管的头端设计与性能参数见图1。
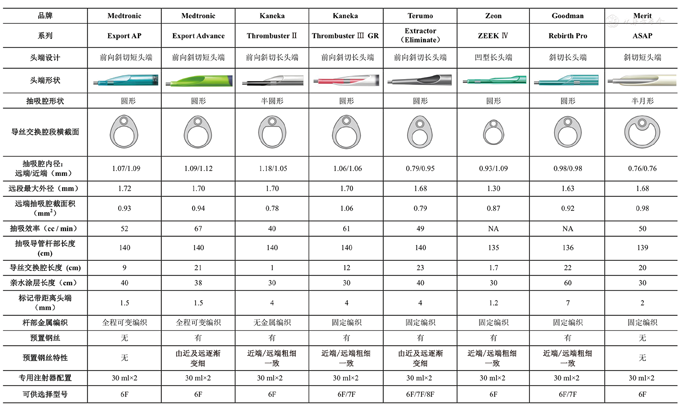

注:远端最大外径,导丝交换腔段最大外径;NA为无数据。相关参数均以6F导管为准
根据工作原理可将机械血栓抽吸装置分为两大类:一类是通过机械性真空泵负压吸引祛除血栓(如Rescue和TVAC),原理与手动血栓抽吸导管类似,只是其负压吸引力由机械性的真空泵产生。在持续形成负压的同时,缓慢推送和回撤导管抽吸血栓。另一类机械血栓抽吸装置则是通过机械的方法将血栓粉碎并排出体外。根据血栓粉碎的机制不同又可分为机械旋切和流体击碎两种。前者以X-Sizer为代表,通过导管头端内置电动切割器的高速旋转将血栓切碎并吸出体外。后者以AngioJet为代表,通过双腔导管的流入腔将高速生理盐水喷向血栓,同时通过流出腔将高速盐水吸出,利用伯努利原理将血栓击碎并排出体外。
冠状动脉血栓抽吸的临床研究在近十年来备受重视。早期多项有关手动血栓抽吸的临床研究显示,直接PCI时常规血栓抽吸存在多重获益。然而,随着TASTE和TOTAL试验等的相继发表,其临床获益和适用范围也出现了较大争议。有关机械抽吸装置的研究起步较晚,目前尚缺乏大样本随机对照研究的结果。
早期研究显示,STEMI患者直接PCI时使用手动血栓抽吸存在多重获益。REMEDIA、EXPIRA试验[5,12]显示,血栓抽吸可明显改善心肌灌注,预防血栓栓塞,缩小梗死面积。TAPAS试验[6]显示,直接PCI前使用Export抽吸导管能减少1年主要复合终点事件(心源性死亡与非致死心肌梗死)。2009年发表的一项荟萃分析[13]共纳入11项研究,结果显示,血栓抽吸能减少全因死亡和主要不良心脏事件(MACE)。2008年欧洲心脏病学会(ESC)STEMI处理指南中血栓抽吸的推荐级别为Ⅱb(证据等级B);预防冠状动脉无复流的推荐级别为Ⅱa(证据等级B)。2009年美国心脏病学会基金会(ACCF)/美国心脏协会(AHA)指南将血栓抽吸的推荐级别调整为Ⅱa(证据等级B)。
2012年发表的INFUSE-AMI试验[14]在6个国家的37家中心入选452例接受PCI的STEMI患者,令人意外的是,血栓抽吸并未缩小梗死面积。随后发布的TASTE试验[7,15](N=7 244)显示,手动血栓抽吸未明显降低全因死亡和再发心肌梗死的风险,但30 d支架血栓和再发心肌梗死的发生率均有降低的趋势。2015年发布的TOTAL试验[8](N=10 063)是迄今有关手动血栓抽吸最大规模的随机对照试验,结果显示,常规手动血栓抽吸非但未能减少主要复合终点事件,还增加了30 d内卒中。近期发表的一项荟萃分析[16]共纳入17项试验20 853例患者,结果也显示,直接PCI时常规血栓抽吸并不能降低死亡、再次心肌梗死或支架内血栓的发生率,反而增加卒中风险。
手动血栓抽吸用于STEMI的研究还存在诸多问题。第一,样本量仍偏小,研究统计效力不够。尽管TASTE研究和TOTAL试验样本量较大,但仍不足以评估主要临床终点事件。第二,高危患者或选择性使用能否获益尚待评价。现有研究主要评价了常规血栓抽吸策略的获益,但该策略本身就存在较大争议。第三,研究终点的选择尚存在争议。多数研究显示,血栓抽吸能改善心肌灌注,减少远端栓塞,但是否应采用硬终点评价其获益有待商榷。第四,血栓抽吸的安全性问题。多数研究显示血栓抽吸安全性良好,TOTAL试验中卒中风险增加的机制尚不明确。第五,对血栓抽吸的规范操作重视不够。临床实践表明,细致、耐心、规范的操作与抽吸效果密切相关。在TOTAL试验中,血栓抽吸与单纯PCI组的操作时间仅相差4 min,操作时间过短或不规范均有可能影响抽吸效果。第六,其他研究缺陷。例如,TOTAL试验中组间交叉与补救性抽吸的比率均较高,也将对研究结果造成影响。
手动血栓抽吸用于NSTE-ACS的研究较少。一项入选70例接受PCI的非ST段抬高型心肌梗死(NSTEMI)患者的研究显示,手动血栓抽吸可以减轻血栓负荷,改善TIMI血流。83%的患者能抽出动脉粥样硬化血栓样物质[17]。新近发表的多中心前瞻性TATORT-NSTEMI试验[18,19]共入选440例NSTEMI患者,结果显示,手动血栓抽吸未能减少微栓塞或改善心肌灌注,亦不能降低死亡和心肌梗死等不良心脏事件风险。
多项研究显示,支架血栓患者使用手动血栓抽吸能改善冠脉和微血管再灌注,提高造影成功率。2014年ESC血运重建指南也建议,支架血栓建议使用血栓抽吸(Ⅱa/C)。静脉桥血管病变使用血栓抽吸缺乏研究。伴有大量新鲜血栓的静脉桥血管病变患者能否从血栓抽吸中获益尚不明确。
综上所述,大多数研究证实,手动血栓抽吸可以改善心肌灌注,减少远端栓塞事件,降低无复流或慢血流的发生率,但能否降低死亡率和减少不良事件尚有待进一步研究证实。
机械血栓抽吸装置相关临床研究较少,不仅样本量均较小,研究设计也存在颇多争议。有关AngioJet的临床研究结果不尽一致,有无临床获益尚不明确。AIMI试验[20]显示,使用AngioJet后梗死面积增大,死亡和MACE事件增多。JETSTENT试验[21]和MUSTELA试验[22]则显示,AngioJet可使大血栓负荷STEMI患者获益。SMART-PCI研究通过OCT评价发现,使用AngioJet的血栓祛除效率高于手动血栓抽吸,并可能改善心肌灌注。Grines等[23]的一项包括11项研究1 018例患者的荟萃分析显示,使用AngioJet后行PCI并不优于单纯PCI。Navarese等[24]的一项荟萃分析共纳入24项研究,结果显示,只有高血栓负荷患者才能从机械血栓抽吸装置(包括AngioJet、TAVC、X-Sizer等)获益。另一项对比单纯手动抽吸和联合应用机械抽吸的研究也发现,联合应用机械抽吸(AngioJet)组术后TIMI3级血流率明显高于手动抽吸组(分别为84.2%和42.1%),联合组6个月的MACE率更低(分别为0%和25.0%)。该研究提示,机械抽吸可作为手动抽吸的辅助治疗手段,初始手动抽吸效果不佳者使用机械抽吸可明显改善PCI术后血流和心肌灌注。
Sianos等[3]研究发现,大血栓负荷可见于40%的STEMI患者,是预测PCI后结果不良的重要因素。不少学者认为,AngioJet现有研究结果不理想,可能与研究设计不合理(如入选患者的血栓负荷程度差别较大)和使用方法不当(如由远及近地开始抽吸)等因素有关。总体而言,机械血栓抽吸装置可能更适于高血栓负荷病变,尤其是手动抽吸无效者。
合理应用血栓抽吸既要参照现有临床研究结果,还需要充分考虑病变血管情况(如血栓负荷程度、TIMI血流分级、罪犯血管的直径与供血范围等)以及器械特点等因素(图2)。
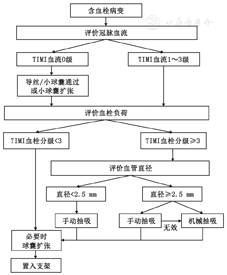

基于现有临床研究证据,血栓抽吸在STEMI患者直接PCI中的应用建议如下:(1)直接PCI时不推荐常规血栓抽吸;(2)血栓负荷较重、TIMI血流0~1级、血管直径或供血范围较大的患者,应用血栓抽吸可能获益;(3)反复手动抽吸无效的患者可以考虑改用机械血栓抽吸。对于心肌梗死后未行直接PCI的患者,择期PCI时使用血栓抽吸能否获益无明确证据。
NSTE-ACS中应用血栓抽吸装置的相关研究证据尚不充分,不推荐常规使用。但当造影发现罪犯血管直径较大、TIMI血流0~1级且存在大量的血栓负荷时,可考虑血栓抽吸。
支架血栓形成患者使用手动血栓抽吸导管是合理的。静脉桥血管应用手动血栓抽吸导管的临床证据尚不充分,但是对于明确含有大量新鲜血栓的静脉桥血管病变,也可考虑使用手动血栓抽吸装置,以减少血栓栓塞和预防无复流。
总之,STEMI患者直接PCI时不推荐常规血栓抽吸,但对于血栓负荷较重、TIMI血流0~1级、血管直径或供血范围较大、支架血栓以及含有大量新鲜血栓的静脉桥血管病变患者,仍可考虑使用。下列患者不推荐血栓抽吸:(1)抽吸装置需要通过无保护左主干病变(狭窄超过管腔直径50%以上);(2)抽吸装置需穿过原有支架网眼才能到达血栓抽吸部位;(3)陈旧性或机化的血栓;(4)严重凝血功能异常(如血液病导致的高凝状态等)。
从包装中取出抽吸导管套件(不要从环鞘中直接抽出抽吸导管),充分冲洗环鞘,以激活抽吸导管头端表面亲水涂层。将延长管连接到抽吸导管尾端。用肝素生理盐水冲洗抽吸导管内腔,排尽导管腔内空气。关闭旋塞阀,连接专用注射器。将注射器抽至最大负压,顺时针旋转锁定。
从环鞘中抽出抽吸导管,沿导引导丝经导丝交换腔插入抽吸导管,充分打开Y阀,固定导引导丝,开始推送抽吸导管。推送速度不宜过快,手握抽吸导管不宜过紧,手握抽吸导管的位置与Y阀入口一般不宜超过5 cm,并尽量使抽吸导管与导引导丝和指引导管保持平行,以免损坏抽吸导管。推送抽吸导管到达血栓病变的近端。
抽吸导管到达血栓病变近端后,关闭Y阀,打开旋塞阀,开始抽吸(部分产品需要先撤出通芯保护钢丝)。在透视下缓缓前送抽吸导管,如出现回血减慢,提示抽吸导管端孔已接触血栓。若遇无回血或回血极度缓慢,不宜快速推送,可在抽吸过程中适当调整导管位置,或将抽吸导管回撤至血栓近端并适度旋转后重新前送并抽吸。抽吸过程中应持续保持充足负压,若抽吸血量已达注射器容量的一半(15~20 ml),应关闭旋塞阀并更换注射器后重新开始抽吸。导管头端到达远端预定部位后,应在负压下缓慢回撤抽吸导管直至血栓病变近端。一般建议,应由近及远地进行抽吸。由远及近地抽吸可能在导管通过病变的过程中引起血栓移位,导致或加重远端栓塞。
一般将导管从病变近端至远端、再由远端至近端移动并抽吸定义为一次抽吸。单次抽吸时间不宜过短,在回血变缓的病变部位应延长抽吸时间。部分患者经单次抽吸即可恢复TIMI3级血流,血栓负荷明显减轻;若抽吸后血栓负荷仍较重或TIMI血流0~2级,应考虑多次抽吸。但抽吸总次数也不宜过多,操作时间不宜过长,一般以回抽总血量不超过200 ml为宜,以免造成患者失血过多。
血栓抽吸后如出现回血速度明显加快、回血过缓或无回血,或已达抽吸终点,应考虑撤出抽吸导管,评价抽吸效果或查找原因。回撤前应首先确认抽吸注射器残余负压是否充足,以免因负压不足造成导管头端血栓脱落。同时确认指引导管已进入冠脉开口内,以免在回撤过程中血栓脱落至主动脉。左冠状动脉血栓抽吸时,若指引导管与靶血管开口不同轴,回撤导管时可能造成血栓脱落至相邻分支。回撤前应将指引导管调整至靶血管开口附近并保持同轴(必要时可超选进入靶血管),可能有利于减少该并发症。建议在负压状态下回撤抽吸导管,先将抽吸导管缓缓回撤至指引导管内,并避免导引导丝在指引导管与冠状动脉开口处打弯乃至扭结。抽吸导管撤入指引导管后应尽快撤出,以免因负压骤减造成导管头端血栓脱落。随后,充分冲洗Y阀并回抽指引导管内血液,以排出可能脱落在指引导管或Y阀内的血栓。
出现下述情况应考虑终止血栓抽吸:(1)抽吸后血栓负荷明显减轻,血流达到TIMI 2~3级;(2)反复抽吸效果仍不理想,残余大量血栓负荷;(3)操作时间过长或回抽血量较多。
抽吸导管不能到达和(或)通过罪犯病变的发生率约为4%~11%,其预测因素为梗死相关动脉的病变近端存在严重迂曲、钙化和分叉病变。对上述病变应首选支撑力强的指引导管,如抽吸导管不能通过罪犯病变,建议先应用小球囊(直径≤2.0 mm)低压扩张后尝试血栓抽吸。若仍不能通过,可采用双导丝支撑、换用支撑力更强的指引导管或更换通过性更好的抽吸导管。
开始血栓抽吸后,若5 s内无回血或回血过缓,应适当调整导管头端位置。在血栓抽吸过程中,若突然出现血流中断,有可能为较大血栓阻塞抽吸导管所致。此时,应在负压状态下撤出抽吸导管,并用肝素盐水反复冲洗,同时充分回抽指引导管内血液。
抽吸导管推送过快或过度弯曲可导致导管打折,并影响抽吸效果。如出现打折,可根据打折程度决定是否更换抽吸导管。
在使用导丝腔较短的抽吸导管时,回撤抽吸导管可导致导引导丝在指引导管外打弯或形成扭结,导致抽吸导管无法撤出。部分患者需要适当前送抽吸导管,在透视下松解导丝打弯或扭结。必要时可将指引导管连同抽吸导管和导引导丝一并撤出。回撤时若遇阻力,应仔细分析查找原因,切忌粗暴操作,以免导致冠状动脉夹层等并发症。
抽吸导管撤出指引导管后,如遇无压力曲线低平或接近直线,应充分放开Y阀,若仍无回血或回血过缓,应考虑血栓阻塞指引导管。此时切忌推注对比剂,并尝试回抽指引导管内血液,必要时可撤出并冲洗导引导管。
抽吸导管到达并通过罪犯病变后,经多次抽吸未见血栓抽吸物的发生率为14.0%~27.3%,其预测因素包括年龄>60岁、梗死相关动脉为回旋支等。主要原因包括:(1)血栓被内源性、抗栓药物或溶栓剂所溶解;(2)介入术前或术中自发的或由于导丝通过病变、抽吸导管的推送使血栓分解并栓塞远端血管;(3)高度狭窄的不稳定动脉粥样硬化斑块导致的冠状动脉闭塞;(4)冠状动脉灌注压下降或部分血栓机化;(5)易碎的抽吸物在通过导管或滤网时碎裂;(6)抽吸导管的抽吸效能不足,应需更换效果更好的导管。
目前国内机械血栓抽吸装置主要以AngioJet为主,因此以下主要介绍AngioJet的操作规范。
术者应掌握抽吸装置的适用血管直径和最小适合指引导管。AngioJet血栓抽吸装置由血栓抽吸导管、喷流泵和驱动单位三部分组成,其最小适用血管直径为2.0 mm。一般自体冠状动脉多选择4F导管,大隐静脉桥血管可以选用5F导管。抽吸前应准备:(1)肝素盐水:一般每1 000 ml生理盐水加5 000 U肝素;(2)系统准备:开启控制台,取出导管,检查无破损后,将喷流泵安装在控制台上,关闭控制台抽屉;然后将针头插入盐水袋,将导管尖端放入肝素盐水,踩下脚踏开关,使肝素盐水充盈导管,直至控制台显示屏时间显示为0 s,系统准备完毕备用。机械抽吸装置的通过性不如手动抽吸导管。因此,一般建议选择支撑力较强的指引导管,必要时可以用小直径球囊扩张后再行抽吸。
在AIMI研究中,有超过50%的病例采用了由远及近的抽吸方法,这可能与其结果不理想有关。由远及近抽吸可能导致血栓在抽吸前即被推送至血管远端,导致远端栓塞,并影响抽吸效果。因此,使用AngioJet时应从血栓近端10 mm左右开始,并由近及远地一边推送导管一边进行抽吸。
无特殊要求,一次抽吸(先由近及远,再由远及近)即可达到祛除血栓的效果。如造影评价血栓负荷仍较重,可再次抽吸,但一般不超过3次。推送抽吸导管不宜过快,推荐推进速度为2 mm/s左右。每次抽吸时间以5 s左右为宜,每工作5 s应该暂停2~3 s,以免导致严重心动过缓。
手动抽吸过程中出现血压、心率下降可见于:(1)血管闭塞或痉挛;(2)血管再通导致再灌注损伤。无论哪种情况,应及时撤出抽吸导管并进行相应的处理。
血栓抽吸回撤过程中栓子脱落可导致非梗死相关动脉栓塞和脑栓塞等。预防措施包括:(1)抽吸导管撤出体外前保持负压;(2)保持抽吸导管和指引导管的同轴性;(3)抽吸导管撤出后,回吸指引导管内的血液避免可能出现的气体或血栓栓塞;(4)使用更大内腔的抽吸导管。
机械抽吸过程中最常见的并发症为缓慢心律失常,可伴血压下降。其可能机制包括:(1)血栓抽吸时喷射高速水流导致一过性缺血;(2)迷走反射;(3)机械溶血时腺苷释放、心肌局部血钾浓度升高。预防处理措施包括:(1)缩短抽吸时间和次数;(2)发生心动过缓时立即停止抽吸并嘱患者咳嗽,多可迅速恢复;(3)必要时可使用阿托品、多巴胺或行临时起搏等。此外,AngioJet血栓抽吸可造成短暂性溶血,严重者可导致血红蛋白尿,应尽量缩短抽吸时间和减少抽吸次数。
冠状动脉内血栓导致远端血管栓塞,影响冠状动脉血流和心肌灌注,增加无复流等并发症。研究表明,STEMI患者直接PCI时应用手动血栓抽吸可以改善TIMI血流和心肌灌注,减少远端血栓栓塞,预防无复流或慢血流。然而,基于现有临床证据,直接PCI时常规血栓抽吸并不能降低死亡风险或减少主要不良事件,因而不推荐常规使用。但对于TIMI血流0~1级、血栓负荷重、血管直径或供血范围较大以及支架血栓等患者,血栓抽吸仍有可能获益。需要设计样本量更大、入选标准和观察终点更合理、并强调规范化操作的临床研究,以明确血栓抽吸的获益人群。在临床实践中,选择合适的患者,采用理想的器械,强调规范化操作,三者均至关重要。
共识专家组名单(按姓氏拼音排序):陈步星(首都医科大学附属北京天坛医院心血管内科);陈珏(中国医学科学院阜外医院心血管内科);陈玉国(山东大学齐鲁医院急诊科);高传玉(河南省人民医院心血管内科);郭金成(首都医科大学附属北京潞河医院心内科);韩雅玲(沈阳军区总医院心血管内科);惠永明(北京大学第一医院丰台医院心内科);季福绥(北京医院心血管内科);荆全民(沈阳军区总医院心血管内科);李保(山西医科大学第二医院心内科);刘宏斌(解放军总医院心血管内科);刘健(北京大学人民医院心血管内科);聂绍平(首都医科大学附属北京安贞医院急诊危重症中心);齐晓勇(河北省人民医院心内科);钱菊英(复旦大学附属中山医院心内科);乔岩(首都医科大学附属北京安贞医院心脏内科中心);沈珠军(中国医学科学院北京协和医院心血管内科);王海昌(第四军医大学唐都医院心血管内科);王浩(解放军总医院心血管内科);王乐丰(首都医科大学附属北京朝阳医院心脏中心);王守力(解放军第三○六医院心血管内科);吴炜(中国医学科学院北京协和医院心血管内科);徐立(首都医科大学附属北京朝阳医院心脏中心);杨丽霞(成都军区昆明总医院心血管内科);杨天和(贵州省人民医院心内科);于波(哈尔滨医科大学附属第二医院心血管内科);曾秋棠(华中科技大学同济医学院附属协和医院心血管内科);张闻多(北京医院心血管内科)
执笔专家:郭金成(首都医科大学附属北京潞河医院心内科);韩雅玲(沈阳军区总医院心血管内科);季福绥(北京医院心血管内科);刘宏斌(解放军总医院心血管内科);刘健(北京大学人民医院心血管内科);聂绍平(首都医科大学附属北京安贞医院急诊危重症中心);沈珠军(中国医学科学院北京协和医院心血管内科);王乐丰(首都医科大学附属北京朝阳医院心脏中心)
秘书:乔岩(首都医科大学附属北京安贞医院心脏内科中心)

























