
Graves眼病是Graves病最常见的甲状腺外表现,是一种器官特异性自身免疫病。估计每100 000人群中每年有16名女性、3名男性发病。其中有3%~5%的Graves眼病患者病情严重,可危及视力,需要积极处理。对临床医师而言,正确评估该病的活动性及严重度对判断该病是否需要干预及采取何种干预措施非常有帮助。该病的干预措施主要包括控制甲亢,缓解局部症状,而对处于活动期的中重度眼病患者采取免疫抑制和治疗,处于非活动期的患者考虑予以康复手术。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者男性,50岁,因"反复心悸8个月,双眼突出3个月"收住入院。患者8个月前出现心悸、消瘦,5个月前当地医院确诊为"甲状腺功能亢进",予以服甲巯咪唑后症状逐渐好转,甲巯咪唑逐渐减量,入院时甲巯咪唑5 mg qd、左旋甲状腺素钠25 μg qd。近3个月患者逐渐出现双眼突出、畏光、流泪、眼胀,长时间阅读可诱发眼痛,近1个月晨起时偶有复视。患者有吸烟史20余年,平均每日20支。患者发现"高血压病"5年余,平时服用降压药物,血压控制可。否认肝炎、结核病史。否认其他自身免疫病。否认精神疾病史。入院后体格检查:一般情况可,甲状腺I度肿大,未触及结节,无震颤及血管杂音,两肺呼吸音清,未闻及干湿啰音,心率70次/min,律齐,血压125/80 mmHg(1 mmHg=0.133 kPa)。眼科检查:最佳视力:右眼0.8、左眼0.6,双眼眼睑中度水肿,双眼眼睑红斑,双眼结膜充血,双眼球结膜水肿,双眼眼阜无肿胀,突眼度:右眼21 mm、左眼22 mm,上睑退缩:右侧2 mm、左侧3 mm,左眼睑闭合不全,眼内压:右眼15.8 mmHg、左眼19.3 mmHg,双眼角膜无异常,前房清,眼底检查无异常。实验室检查:血尿粪常规正常,肝肾功能、电解质正常,甲状腺功能:FT3、FT4正常,sTSH 0.253 μIU/L,促甲状腺素受体抗体(TRAb)12 U/L。眼肌MRI:双眼上下直肌增粗,双眼外肌于T2W(脂肪抑制)可见高信号影。
Graves眼病(GO)是以眼球后及眶周组织的浸润性病变为特征的器官特异性自身免疫性疾病。它可与各种自身免疫性甲状腺疾病并发,Bartley等[1]总结120例GO中,90%为甲亢,1.0%为甲减,3.3%为桥本甲状腺炎,5.8%甲状腺功能正常。与GO关系最密切的Graves病患者中有13%~69%的临床眼病患者,但其中多数为亚临床眼病[2]。GO的发生可先于或迟于甲亢,亦可在接受治疗期间或甲亢控制后再出现。GO的典型特征包括眼睑肿胀,上睑退缩,下落迟缓,瞬目减少,凝视,单眼或双眼突出,眼球活动受限,复视等[3]。GO按病程可分为活动期及静止期,活动期病理表现主要以葡萄糖胺聚糖的聚集和炎症细胞浸润为主,而静止期病理表现主要以纤维化为主[4,5]。通过临床评估对患者GO进行分期可指导选择合适的治疗方案。
目前GO的诊断有Bartly、Frueh和Gorman等标准,其中Bartly标准最常用,Bartly诊断标准:(1)存在眼睑退缩:只要合并以下体征或检查证据之一可做出诊断:①甲状腺功能异常;②眼球突出;③视神经功能障碍,包括视力下降,瞳孔反射、色觉、视野异常,而无法用其他病变解释;④眼外肌受累,眼球活动受限[6]。(2)缺乏眼睑退缩:须具备甲状腺功能异常,还应有以下体征之一:①眼球突出;②眼外肌受累或视神经功能障碍。(3)排除其他眼病引起的类似体征。少数甲状腺功能正常,缺少典型眼征的GO以及单侧突眼的患者必须和其他疾病进行鉴别,如:眼眶炎性假瘤、眼肌炎、眶内肿瘤、眶周感染性疾病等[7]。
该例患者发病时有心悸、消瘦等甲状腺毒症的症状,就诊时查甲功FT3、FT4升高,TSH降低,所以甲状腺毒症诊断明确,结合患者有甲状腺肿大、眼征及TRAb升高,故Graves病基本诊断明确。患者眼科检查提示存在眼睑退缩,同时伴有甲状腺功能异常、双眼突出、眼外肌受累,且眼部MRI排除其他原因导致的突眼,根据Bartly标准GO诊断明确。
对确诊GO的患者应对其眼病病情进行临床评估,并根据结果指导临床治疗决策。目前最常用评估方法是欧洲GO专家组(EUGOGO)管理共识[8]中所推荐的,即严重度(表1)及活动性评估。其中严重度评估内容分为眼睑退缩、软组织受累情况、突眼度、复视、角膜受累、视神经,如前5项中任何一项符合中重度标准则判定为中重度眼病,如角膜严重受累或视神经受压导致视力进行性下降则判定为威胁视力的GO,复视参考Gorman评分。处于活动期的患者对激素等免疫抑制治疗相对较敏感,故治疗前对眼病进行活动性评估尤为重要。根据EUGOGO管理共识推荐活动性评分:(1)球内或球后压迫疼痛感;(2)凝视诱发的疼痛;(3)眼睑充血;(4)眼睑水肿结膜充血;(5)球结膜水肿;(6)眼阜水肿,以上每项计1分,共7分,≥3分判定为处于活动期,分值越高提示炎症反应越显著,前2项为患者主观症状,即休息状态下及凝视状态下是否存在眼胀或眼痛,后5项为客观体征,EUGOGO网站均列出标准评判图示。

严重度评估(EUGOGO管理共识)
严重度评估(EUGOGO管理共识)
| 分级 | 眼睑退缩 | 软组织受累 | 突眼度 | 复视 | 角膜受累 | 视神经 |
|---|---|---|---|---|---|---|
| 轻度 | <2 mm | 轻度受累 | <正常上限+3 mm | 一过性或不存在 | 无 | 正常 |
| 中重度 | ≥2 mm | 中度至重度受累 | ≥正常上限+3 mm | 非持续性或持续性 | 轻度 | 正常 |
| 威胁视力 | 重度 | 受压 |
注:EUGOGO:欧洲Graves眼病专家组;华人正常突眼度上限18.6 mm
本例患者眼科检查提示双眼睑中度水肿,突眼度:右眼21 mm、左眼22 mm,上睑退缩:右侧2 mm、左侧3 mm,均符合中重度眼病标准,角膜及眼底检查未见明显异常,且短期内视力无明显下降,故评估为中重度眼病。患者存在静息状态下存在眼胀,长时间阅读出现可诱发眼痛,双眼眼睑中度水肿,双眼眼睑红斑,双眼结膜充血,双眼球结膜水肿,双眼眼阜无肿胀,患者活动性评分(CAS)为6/7分,处于活动期。
对于GO诊断不明确的患者,例如甲功正常,单眼突出等应行相关影像学检查以作鉴别诊断。如患者视力短期内进行性下降,应行CT或MRI了解视神经受累,其中CT对骨性组织具有良好的分别率,可为去眶减压术入路提供依据,而MRI对判断软组织水肿及变性较有优势[9]。
除此以外,还应对患者一般情况、甲状腺功能状态、吸烟史、是否存在使用激素或免疫抑制剂禁忌症做相应评估。初诊时、视力进行性下降及治疗效果不明显时应有具有GO诊治经验的眼科医师参与评估。
目前研究发现吸烟与GO的发生与恶化关系密切,吸烟能刺激眼眶成纤维细胞增殖并产生葡萄糖胺聚糖,使成纤维细胞在干扰素(IFN)-γ的作用下增强人类白细胞抗原(HLA)-Ⅱ型分子的表达。据EUGOGO的研究,40%以上的GO患者都吸烟,吸烟的Graves病患者发展为GO的风险是不吸烟患者的5倍,且呈量效关系。所以,患者均应及早戒烟或避免被动吸烟。
所有GO患者应当尽快恢复正常的甲状腺功能,与口服药物及手术治疗相比,放射性碘治疗可能诱发或加重GO,部分患者(表2)需要在放射性碘治疗后1~3 d,预防性口服泼尼松(0.3~0.5 mg·kg-1·d-1),逐渐减量,维持3个月后停药[10,11]。放射性碘治疗后定期复查甲功,及时加用左旋甲状腺素替代治疗避免发生甲减。
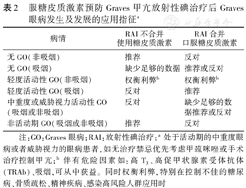
服糖皮质激素预防Graves甲亢放射性碘治疗后Graves眼病发生及发展的应用指征a
服糖皮质激素预防Graves甲亢放射性碘治疗后Graves眼病发生及发展的应用指征a
| 病情 | RAI不合并使用糖皮质激素 | RAI合并口服糖皮质激素 |
|---|---|---|
| 无GO(非吸烟) | 推荐 | 反对 |
| 无GO(吸烟) | 缺少足够的数据推荐或反对 | |
| 轻度活动性GO(非吸烟) | 权衡利弊b | 权衡利弊b |
| 轻度活动性GO(吸烟) | 反对 | 推荐 |
| 中重度或威胁视力活动性GO(吸烟或非吸烟) | 反对 | 缺少足够的数据推荐或反对 |
| 非活动期GO(吸烟或非吸烟) | 推荐 | 反对 |
注:GO:Graves眼病;RAI:放射性碘治疗;a处于活动期的中重度眼病或者威胁视力的眼病患者,如无治疗禁忌优先考虑甲巯咪唑或手术治疗控制甲亢;b伴有危险因素如:高T3、高促甲状腺素受体抗体(TRAb)、吸烟,可从中获益。同时权衡利弊,特别在控制不佳的糖尿病、骨质疏松、精神疾病、感染高风险人群应用时
外出时可佩戴太阳镜减轻强光对眼部刺激;人工泪液防止眼球干燥和局部不适症状;存在眼睑闭合不全的患者夜间可用油膏及湿房镜避免角膜病的发生;部分复视患者可通过配戴三棱镜矫正复视。
GO多具有自限性,病情可在数月至数年内自行缓解,只有少数患者发展为严重的持续性眼病。因此对于轻度的眼病,在一般治疗的基础上可以随访观察(图1)。对部分轻度GO患者,硒治疗可能有效[12],但目前缺乏来自正常硒营养地区的临床证据,同时应注意硒治疗可能增加罹患糖尿病的风险[13]。对于稳定的处于非活动期的患者可行整复手术。
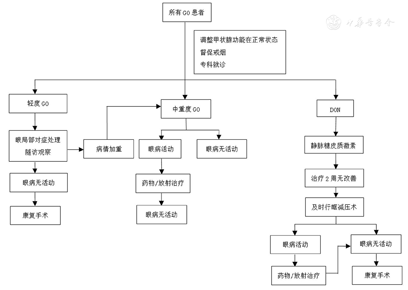

注:DON:甲状腺相关视神经病变Dysthyroid optic neuropathy
处于活动期的中重度眼病,应给予相应的综合治疗,包括前述的基础护理,眼睛的局部治疗。糖皮质激素是最常用及疗效肯定的治疗方法。糖皮质激素在GO中可以全身(口服、静脉)和局部(眶周注射)应用。它对改善局部炎症水肿及解除视神经压迫效果较好,而对突眼度和眼肌功能的改善欠佳。口服糖皮质激素治疗处于活动期中重度眼病反应率为33%~63%[14,15],一项meta分析指出静脉甲泼尼松龙冲击治疗相对于口服激素治疗效果更佳,不良反应更少[16]。一项多中心随机双盲试验对中重度患者分别采用累积剂量为2.25、4.98及7.47 g甲泼尼松龙静脉用药12周,反应率分别为28%、35%、52%,提示中等剂量更适用于大部分患者,复发率最低,不良反应较大剂量组少[17]。瑞金医院一项前瞻性临床研究发现使用相同累积剂量甲泼尼松龙(4.5g)按不同脉冲方案静滴,长程12周组反应率优于短程4周组(76.92%对41.03%),提示长疗程使用激素可更好地控制病情[18]。目前推荐累积剂量4.5g为期12周的甲泼尼松龙周脉冲方案作为处于活动期中重度GO的标准治疗方案。甲泼尼松龙静脉冲击治疗最常见的严重不良反应为肝毒性,当累积剂量达到10~24 g时肝毒性最常见[19],基于安全考虑EUGOGO共识中推荐单疗程累积剂量不超过8 g[20]。另外,也有心脏毒性的相关报道[21]。
眶周注射激素减少了全身应用激素所带来的不良反应,可能对改善眼球的活动度,改善复视,特别是非持续性复视效果较好,但存在损伤周围组织的风险,不作常规推荐[22]。
放疗的治疗反应率报道不一,一项开放性研究提示放疗反应率约60%[23]。临床上常采用每日2 Gy,连续使用2周,累积剂量为20 Gy的治疗方案,也可选择每周1 Gy,连续使用20周,后者患者更易耐受。研究提示大剂量并非更有效。糖皮质激素联合放疗治疗效果优于单用糖皮质激素,可改善眼肌功能,减轻复视[16]。放疗安全性也得到多数专家的肯定,但因缺乏35岁以下年轻患者的安全性评估数据,故不推荐在该人群中应用。球后放疗存在诱发视网膜微血管病变的风险,故也避免在糖尿病及严重高血压患者中应用[24,25]。
利妥昔单抗近年来用于自身免疫病的治疗,亦有不少关于GO治疗的病例报道[26]。2015年初发表了2篇关于处于活动期中重度GO患者利妥昔单抗治疗的随机对照研究(RCT),均将CAS改善≥2分作为主要终点。美国梅奥中心Bahn的研究结果提示利妥昔单抗较安慰剂无明显优势,且中重度不良反应多于安慰剂,其中有2例患者诱发视神经病变,可能与利妥昔单抗导致的细胞因子释放综合征有关[27];而来自意大利Salvi的结果显示无论是高剂量组,还是低剂量组均有效改善GO患者CAS及生活质量评分[28]。关于利妥昔单抗治疗GO的疗效有待更多的RCT评价。
其他的治疗方法还包括免疫抑制剂、生长抑素类似物、秋水仙碱等,疗效缺少大样本临床随机对照试验的验证。而对于处在静止期的Graves眼病则主要选择整复手术治疗,以达到改善复视和外观的目的。
局部护理对严重角膜受累至关重要,必要时可行眼睑缝合术帮助角膜的愈合。对于视神经病变的患者,糖皮质激素和眶减压术是唯一有效的疗法,大剂量静脉糖皮质激素脉冲治疗是一线治疗方法,如果1~2周后改善不明显或无法耐受,需行眶减压术。
另外激素治疗过程中应监测随访血压、肝功能、糖脂代谢、电解质,观察有无消化性溃疡及感染征象。常规予以胃黏膜保护剂、钙剂、维生素D治疗,当口服糖皮质激素超过3个月(泼尼松平均日剂量≥5 mg),或静脉使用糖皮质激素建议使用双膦酸盐。
患者确诊为Graves病,经评估考虑为处于活动期的中重度GO,嘱其戒烟,继续予以甲巯咪唑、左旋甲状腺素控制甲状腺功能,在排除禁忌证后予以甲泼尼松龙静脉周脉冲治疗(500 mg qw,静滴×6周,继予以250 mg qw,静滴×6周),同时予以奥美拉唑、钙剂、骨化三醇治疗。经12周治疗后眼胀较前好转,无明显眼痛,眼科评估提示患者最佳视力:右眼1.2、左眼1.0,双眼眼睑轻度水肿,双眼眼睑无红斑,双眼结膜充血较前好转,双眼球结膜无水肿,双眼眼阜无肿胀,CAS2/7分,突眼度:右眼19 mm、左眼20 mm。
GO是一种由遗传、免疫、环境等多种因素作用导致的疾病,其发病机制至今仍未完全清楚。GO诊治的关键是准确地评估疾病的严重度及活动度,根据结果选择相应的治疗方法。对于处于活动期的中重度眼病患者糖皮质激素仍是首选,而甲泼尼松龙静脉周脉冲治疗疗效确切。除此以外,应做到包括生活方式指导、甲状腺功能控制在内的全面综合管理。



























