
大量临床证据表明在糖尿病合并高血压患者中降低血压能改善心脑血管疾病(CVD)结局,但是最优的降压治疗目标仍难以确定,并于近年成为学术争论的焦点。本文回顾了降压治疗的观察性和随机对照临床研究及近年来对糖尿病患者降压治疗目标的争论,结合我们在中国成年人群中不同糖代谢和血压状态对10年后CVD发病风险的研究,着重分析了在糖尿病和糖尿病前期患者中,在开展降压治疗的随机对照临床试验研究中需要特别关注的方面。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
糖尿病合并高血压显著增加将来发生大血管和微血管并发症的风险[1]。有研究显示在糖尿病合并不同阶段的高血压的患者中(即使是血压处于120~139/80~89 mmHg, 1 mmHg=0.133 kPa),心脑血管疾病(CVD)事件的风险增加近3倍[2]。尽管有大量临床证据表明在糖尿病合并高血压患者中降低血压能改善CVD结局,但是最优的降压治疗目标仍不能确定,并于近年成为学术争论的焦点[3,4,5,6,7,8]。现有的各国指南对糖尿病前期患者何时启动降压治疗也没有什么证据和建议[7]。
糖尿病患者的适宜的降压治疗目标一直以来都是众说纷纭,争论激烈。
在观察性研究英国前瞻性糖尿病研究(United Kingdom Prospective Diabetes Study, UKPDS)36中,收缩压≥120 mmHg就已经和CVD增加相关[3]。最早的严格血压控制的临床试验是UKPDS38研究和高血压最佳治疗(Hypertension Optimal Treatment, HOT)研究[9,10]。UKPDS38共纳入1 148例2型糖尿病合并高血压患者,随机分配到降压目标为<150/85 mmHg和180/105 mmHg组,研究历时8.4年,结果显示与对照组血压降至154/87 mmHg相比,强化降压组的血压降至144/82 mmHg,糖尿病相关死亡及并发症均显著减少。
在HOT研究中,研究对象为来自26个国家的18 790例年龄50~80岁、舒张压101~115 mmHg的高血压患者,平均随访时间3.8年[10]。所有患者均以非洛地平开始,或加用小剂量血管紧张素转化酶抑制剂(ACEI)或β受体阻滞剂或氢氯噻嗪。患者随机分入3个舒张压目标组(≤90 mmHg、≤85 mmHg和≤80 mmHg)。HOT研究的亚组分析发现在合并糖尿病的1 501例患者中,从随访的第6个月起到研究结束,3组的平均血压分别为148/85、146/83和144/81 mmHg。目标舒张压≤80 mmHg组中主要CVD事件(非致死性急性和无症状性心肌梗死、非致死性脑卒中以及各种原因的心血管死亡)的发生率较目标血压≤90 mmHg组降低51%。
糖尿病患者达美康缓释片与百普乐对照评估研究(the Action in Diabetes and Vascular Disease: Preterax and Diamicron Modified Release Controlled Evaluation,ADVANCE研究)是在11 140例55岁以上,既往有CVD病史和多种CVD危险因素的2型糖尿病患者中,采取降压与降糖的2×2析因设计,观察百普乐强化降压与格列齐特强化降糖治疗对减少大血管并发症(脑卒中、心肌梗死和心血管死亡)及微血管并发症(新发或恶化的肾病及视网膜病变)的作用[11]。入组时2组的平均HbA1C为7.5%,强化降糖组的平均HbA1C降低到了6.5%。强化降压组的血压为136/73 mmHg,标准降压组的血压为141.6/75.2 mmHg。ADVANCE研究平均随访5年,主要微血管事件和大血管微血管复合终点的减少均有统计学意义。2型糖尿病患者强化降压治疗使总死亡率降低14%,心血管死亡降低18%,主要心血管事件降低9%。
基于以上研究,在20世纪初之前的糖尿病和高血压的指南中,建议糖尿病患者的降压治疗目标值<130/85 mmHg,并进而降低为<130/80 mmHg[12]。
2010年发布的ACCORD研究,比较了2型糖尿病合并高血压患者收缩压降低至<120 mmHg与降低至<140 mmHg对主要心血管事件风险的影响[4]。ACCORD研究的入选对象为使用3种或3种以下降压药物,收缩压在130~180 mmHg的糖尿病患者。研究发现与<140 mmHg相比较,收缩压降低至<120 mmHg并不能减少2型糖尿病患者致死和非致死的主要心血管事件,而严重不良反应在强化降压组则显著增加。基于ACCORD研究结果,2013年的欧洲高血压协会(ESH)/欧洲心脏病学会(ESC)指南建议糖尿病患者的降压治疗目标为<140/85 mmHg。2014年美国成人高血压治疗指南(JNC)第八版则将糖尿病患者的降压治疗目标调整为<140/90 mmHg。
但是,ACCORD研究的结果因为其终点事件未达到预期目标致使统计学效力降低。而且,ACCORD中2组的平均收缩压值是119.3 mmHg和133.5 mmHg,并不是非常接近140 mmHg。此外,一项对ACCORD研究的事后分析也得出了截然不同的结论[13]。该研究将所有患者按强化血压/强化血糖、强化血压/标准血糖、标准血压/强化血糖和标准血压/标准血糖治疗分为4组。强化血压治疗定义为<120 mmHg,标准血压治疗定义为<140 mmHg。强化血糖定义HbA1C<6.0%,标准血糖定义为HbA1C在7.0%~7.9%。与标准血压/标准血糖治疗组相比,强化血压/强化血糖、强化血压/标准血糖和标准血压/强化血糖治疗组的主要的心血管事件的风险分别为HR 0.71(95%CI 0.52~0.96, P=0.026)、HR 0.74(95%CI 0.55~1.00, P=0.049)和HR 0.67(95%CI 0.50~0.91, P=0.011)。强化降压治疗的2组均有显著的心血管获益。
2015年SPRINT研究结果公布:高血压患者收缩压降低至<120 mmHg比<140 mmHg可以显著降低心血管疾病与全因死亡风险[5]。这对高血压防治领域产生了巨大冲击,很多学者倾向于更为严格的血压管理。SPRINT研究入选的都为收缩压在130~180 mmHg的高危患者,年龄均≥50岁,且伴有至少1项其他心血管危险因素:已知的心血管疾病,慢性肾脏疾病,或者10年动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease, ASCVD)风险≥15%,或者年龄≥75岁。采用的血压测量方法和通常的诊间血压不同,专家委员会普遍接受收缩压130 mmHg的界值。2017年美国心脏病学会/美国心脏协会(ACC/AHA)高血压指南以SPRINT研究结果作为重要依据,建议血压≥130/80 mmHg即诊断为高血压,并推荐糖尿病患者的降压治疗目标为130/80 mmHg。
ACC/AHA指南另一个关注点是对于血压测量方法的推荐和强调总体心血管风险评估的重要性。在SPRINT研究中受试者采用了自动化诊室血压(automated office blood pressure,AOBP)测量,即患者在独处的安静环境中休息后应用自动血压测量工具自测血压。一般认为这种测量方法所得数值比临床普遍应用的诊室汞柱血压计测量结果低5~10 mmHg。因此SPRINT研究中的"120 mmHg"与平时所谈论的130 mmHg更为接近。使用10年ASCVD风险模型评估将来发生ASCVD的风险在近年来的各种指南中备受重视。在2017年ACC/AHA高血压指南中,10年ASCVD风险>10%,同时血压大于130/80 mmHg,就应考虑开始使用降压药物。
ACCORD研究显示严格的血压控制未能使糖尿病患者有更多的获益,而SPRINT研究排除了糖尿病患者。因此,美国糖尿病学会(ADA)不认同ACC/AHA高血压指南,认为进一步下调糖尿病患者的降压目标是缺乏充分证据的。2017年ADA发布了糖尿病和高血压的立场声明,对于糖尿病患者的高血压仍坚持既往诊断标准,即≥140/90 mmHg[6]。ADA认为对于绝大多数糖尿病伴高血压患者的血压目标是<140/90 mmHg,并强调降压目标要个体化。对于心血管疾病高风险的患者,可以设定<130/80 mmHg的血压目标。此外,ADA与ACC/AHA指南都很重视血压的正确测量,并且都鼓励家庭血压监测(HBPM)。推荐的降压药物ACEI、血管紧张素Ⅱ受体拮抗剂(ARB)、噻嗪类利尿剂或二氢吡啶类(CCB),也是一致的。为了达到降压目标,通常会需要多种药物联合治疗。
2017的加拿大高血压教育计划(CHEP)高血压指南建议在已发生大血管靶器官损害或合并存在独立心血管危险因素的患者,平均收缩压≥140 mmHg时应考虑开始降压治疗[8]。糖尿病合并高血压患者的血压应维持于<130/80 mmHg。推荐以下采用标准化的检测技术和经过验证的血压测量设备测量血压:AOBP测量、非AOBP测量、HBPM及动态血压监测(ABPM)。合适的药物选择包括(按英文字母表顺序):ACEI(A级)、ARB(B级)、CCB(A级)及噻嗪类利尿剂(A级)。
在2018年6月的ESH年会上发布了ESC/ESH 2018高血压指南[14]。此次指南依旧沿用了140/90 mmHg的诊断界值。对于高血压合并糖尿病的患者,诊室血压≥140/90 mmHg开始药物治疗,目标是收缩压≤130 mmHg,但不应低于120 mmHg,要密切监测不良事件。≥65岁的老年患者的降压目标是收缩压在130至<140 mmHg,舒张压<80 mmHg,但不应低于70 mmHg。指南特别推荐使用ABPM和HBPM。ABPM测量结果为真实世界血压,具有记录信息多、可以测量夜间血压等优点。HBPM可排除诊室影响、操作方便。对于没有冠心病的患者,推荐使用评分系统进行风险评估。与以往的指南不同,欧洲新指南提倡大多数患者初始治疗应使用药物联合。初始联合用药首选ACEI/ARB与CCB或利尿剂的联合。两种药物联合治疗后血压不能达标者,推荐三药联合方案,即肾素-血管紧张素系统(RAS)抑制剂+CCB+噻嗪类利尿剂。
在2010年的全国糖尿病调查中[15]:糖尿病在中国成年人中的患病率为11.6%,而糖尿病前期在中国成年人中的患病率已经高达50.1%。中国成人高血压患病、知晓、治疗和控制情况调查研究覆盖了我国31个省份,在35~75岁人群中筛查了170万人[16]。发现年龄性别调整后高血压检出率为37%。检出的高血压患者中知晓率、治疗率和控制率分别为36%、23%和6%。糖尿病或糖尿病前期合并高血压使事件风险加倍,对于高血压进行控制的比例如此之低,给居民健康和社会经济的发展带来沉重的负担。
本研究组既往研究发现,单独的糖尿病前期并不导致CVD风险明显升高,但当其合并高血压(≥140/90 mmHg)时,CVD风险较正常人显著增高[17]。既往在糖尿病前期患者中并没有降压治疗的相关研究。一项SPRINT的事后分析按照空腹血糖5.6 mmol/L把所有受试者分为正常血糖和糖尿病前期组,发现强化降压治疗对正常血糖和糖尿病前期的CVD事件和全因死亡率都有相同的获益。但是,该研究仅使用空腹血糖值来定义糖尿病前期[18]。
极少有研究将血糖与血压联合考虑来研究CVD风险。之前进行的一项研究把高血压前期(prehypertension)和糖尿病联合分析得出了类似的结论:单独的空腹血糖受损或糖耐量受损均未显著增加CVD风险,但是,当空腹血糖受损或糖耐量受损在患者收缩压位于120~139 mmHg时,均能使CVD风险显著增高,分别为血糖正常和血压<120/80 mmHg的受试者风险的2.12和2.06倍[19]。但是,该研究主要针对年龄45~74岁的研究对象,也未将高血压患者纳入分析。
自从2017年ADA发布了糖尿病和高血压的立场声明和ACC/AHA发布新的高血压指南以来,高血压诊断和治疗领域争论的焦点围绕在130~139/80~89 mmHg这段血压。本研究组的研究对象来自于一个有代表性的中国成年人群的10年随访队列,该队列人群提供了一个十分难得的观察长期CVD事件的机会,从而能够探索130~139/80~89 mmHg这段血压在不同糖代谢状态时发生CVD的风险[20]。
当把血压分为<130/80 mmHg、130~139/80~89 mmHg和≥140/90 mmHg或者治疗组共3组,发现10年后CVD事件的发病率分别为3.0、6.0和13.9/千人年。在校正性别、年龄等各种因素后,与<130/80 mmHg血压组比较,血压≥140/90 mmHg组CVD风险显著升高(HR=2.68,95%CI 1.36~5.25)。同时发现血压130~139/80~89 mmHg合并糖尿病或10年ASCVD风险≥10%时,其10年后发生CVD的风险增加。而血压130~139/80~89 mmHg在正常血糖和糖尿病前期患者中CVD的风险并不增加(图1)。
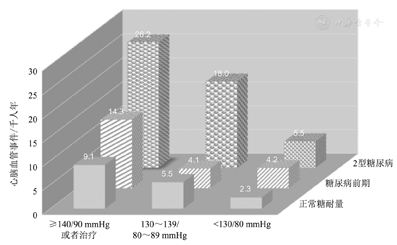

注:1 mmHg=0.133 kPa
以上结果预示:为了预防将来的CVD,在糖尿病患者和10年ASCVD风险≥10%的患者中,需要把血压降低到130/80 mmHg以下。而对于糖尿病前期者,则需把血压控制到140/90 mmHg以下,才能减少10年后发生CVD的风险。
但是以上研究均是观察性研究,我国糖尿病或者糖尿病前期患者的降压治疗目标又该是何去何从,这需要进行降压治疗的随机对照试验(RCT)来提供进一步的证据。
在2013年的《中国2型糖尿病防治指南》中,糖尿病患者的降压目标是<140/80 mmHg;而在2017版中修改为<130/80 mmHg,对老年或伴有严重冠心病的糖尿病患者,可采取相对宽松的降压目标。《中国高血压防治指南2010版》则建议:一般糖尿病患者降压目标为<130/80 mmHg,老年或伴有严重冠心病的糖尿病患者降压目标为<140/90 mmHg。在《中国高血压防治指南2018年版》中,增加130~139/85~89 mmHg范围,也将糖尿病分为新诊断与已治疗但未控制两种情况,分别根据血糖(空腹与餐后)与HbA1C的水平诊断。但是降压治疗的目标尚缺乏中国人群的证据,目前亟需在糖尿病和糖尿病前期患者中开展降压治疗的RCT研究。
由瑞金医院宁光教授和王卫庆教授牵头开展的"中国成人2型糖尿病降压治疗目标(BPROAD)研究",是一项为期5年的全国多中心、开放、平行组设计的RCT研究。通过入选12 702例2型糖尿病合并收缩压升高患者,随机接受强化降压治疗(收缩压降低至<120 mmHg)或常规降压治疗(收缩压降低至<140 mmHg),随访并比较2组主要心血管事件发病风险(包括非致死性心肌梗死、非致死性脑卒中、接受急诊治疗或住院的心力衰竭和心血管原因死亡的复合终点)。希望BPROAD研究能为明确2型糖尿病患者的血压控制目标提供中国人群的证据。
ACCORD研究的主要终点事件包括非致死性心梗、非致死性卒中和心血管原因的死亡。研究发现强化降压治疗并不能减少糖尿病合并高血压患者致死和非致死的主要心血管事件,但ACCORD研究因为其终点事件未达到预期目标致使统计学效力降低而备受质疑。而SPRINT研究的主要复合终点有非致死性心梗、非致死性卒中、接受治疗或住院的心力衰竭和心血管原因死亡,强化降压治疗可以显著降低非糖尿病患者的心血管疾病风险。一项合并分析采用SPRINT的复合终点事件和研究持续时间,将ACCORD研究(全部为糖尿病患者)和SPRINT研究(全部为非糖尿病患者)合并,强化降压治疗(<120 mmHg)和标准降压治疗(<140 mmHg)这2组基线时的10年ASCVD风险没有统计学差别[21]。该合并研究发现:不管是在糖尿病患者还是非糖尿病患者,强化降压治疗都具有相同的心血管事件的获益。
因此,在糖尿病和糖尿病前期患者中开展降压治疗的RCT研究时,在试验设计阶段就要充分考虑到主要终点事件的设置会对整个临床试验结果产生深远的影响。
在RCT研究中,首先需要根据研究对象进入试验时某些重要的临床特征或因素进行分层,如种族、疾病分期等。一般临床试验随机化时的分层因素不超过4个。
欧美国家的ASCVD风险预测模型包括美国Framingham风险评分和ESC的SCORE预测模型等,涉及到的风险参数有性别、年龄、总胆固醇、高密度脂蛋白胆固醇、收缩压、是否接受抗高血压治疗、吸烟、糖尿病[22]。中国人的10年ASCVD发病风险预测研究的终点包括心肌梗死、冠心病死亡以及致死性和非致死性脑卒中,是中国首个以ASCVD为终点事件的风险预测模型。该模型不仅综合考虑了既往预测模型中危险因素,还结合中国实际情况和疾病谱的特点,纳入腰围和ASCVD家族史等,对中国人10年ASCVD发病风险具有良好的预测能力。
ASCVD风险评估本身包含有性别、年龄、血脂、血压、糖尿病和吸烟等重要的临床特征,对将来发生CVD具有良好的预测能力,可以在糖尿病和糖尿病前期的降压治疗的临床试验中作为基线时随机化的分层因素。
在SPRINT和ACCORD研究中,受试者都是采用了AOBP测量,即患者在独处的安静环境中休息后应用自动血压测量工具自测血压。一般认为这种测量方法所得数值比临床普遍应用的诊室汞柱血压计测量结果低5~10 mmHg。
ADA与ACC/AHA指南都很重视血压的正确测量。2017 CHEP的高血压指南推荐以下采用标准化的检测技术和经过验证的血压测量设备测量血压:AOBP测量、非AOBP测量、HBPM及ABPM。ESC/ESH 2018高血压指南特别推荐使用ABPM和HBPM。
因此要充分考虑监测血压的方法对临床试验的影响,选择一种能在多中心统一正确测量血压的方法对降压治疗的临床试验尤为重要。
ADA和中国糖尿病指南都推荐个体化的降糖治疗。HbA1C目标值太高会增加糖尿病引起的血管并发症的风险。糖化血红蛋白控制太低又会增加低血糖风险带来的跌倒等严重不良事件。
低血糖是指血糖水平<2.8 mmol/L或者无其他原因出现的典型低血糖症状。出现短暂的中枢神经系统功能障碍时,必须要他人帮忙才能处理的为严重低血糖,可以自行处理的为轻微低血糖。在ADVANCE人群中,严重低血糖者发生率为2.1%。第一次大血管事件发生距离第一次严重低血糖发作的中位时间是1.56年,在发生严重低血糖的患者中,16.8%随后发生了主要大血管事件。轻微低血糖发作虽然可使微血管事件风险升高,但同时也使大血管和死亡事件风险减少。严重低血糖发作则和各种不利的结果事件如死亡、心血管事件等风险升高都呈强相关,但和发生次数的多少无明显关联。严重低血糖发作是否和上述不利结果事件构成直接的因果关系尚无法确定,但至少是危险的标志[23]。
因为在糖尿病的降压治疗的临床试验中高风险患者居多,降糖治疗时要充分考虑到低血糖对CVD的影响。糖尿病患者的降糖治疗目标应以不出现严重的低血糖为准。
既往的研究表明阻断RAS系统可以在高血压或CVD患者中减少糖尿病的发生。心脏病预防评估试验(Heart Outcomes Prevention Evaluation trial, HOPE)研究显示雷米普利与高危患者新发糖尿病的减少相关[24]。
雷米普利及罗格列酮减少糖尿病的发生(Diabetes REduction Assessment with ramipril and rosiglitazone Medication, DREAM)研究是首个在糖代谢异常患者中进行的ACEI预防糖尿病的研究[25]。经过平均3年的随访发现,糖尿病或死亡的发生率在2组间无显著差异(18.1%对19.5%)。但雷米普利组达到次要终点(血糖回归至正常水平)的患者比例显著高于安慰剂组(HR=1.16,95% CI 1.07~1.27, P=0.001)。
RAS抑制剂在降压治疗时可能会对降糖治疗产生交互作用。在RCT研究选择降压药物时,如果患者均以RAS抑制剂开始治疗,可以有效控制混杂因素。
钠-葡萄糖协同转运蛋白2(sodium-dependent glucose transporters 2, SGLT-2)抑制剂和胰升糖素样肽1(glucagon-likepeptide1, GLP-1)类似物在降糖的同时,都有一定的降压作用[26]。在2型糖尿病患者恩格列净心血管结局(Empagliflozin Cardiovascular Outcome Event Trial in Type 2 Diabetes Mellitus Patients-Removing Excess Glucose, EMPA-REG OUTCOME)研究,每天10和25 mg的恩格列净(empagliflozin)可以使24 h收缩压分别下降3.44和4.16 mmHg,舒张压分别下降1.36和1.72 mmHg[27]。GLP-1类似物也有一定的降压作用,Meta分析发现,与安慰剂、胰岛素和磺脲类相比,GLP-1受体激动剂可使收缩压降低1.84~4.6 mmHg。但是,降糖药物的降压作用对心血管结局的影响尚不明确。所以,在糖尿病患者中进行降压治疗的临床试验时,要充分考虑到降糖药物的选择对血压的影响。
总之,在糖尿病和糖尿病前期患者中开展降压治疗的RCT研究时,因为需要观察到心脑血管终点事件的差异,整个试验入组患者人数较多,需时较长,在试验设计阶段就要充分考虑以上各个方面,排除各种干扰因素的影响,才能保证临床试验顺利的进行。
作者声明不存在利益冲突
1. 2017年美国心脏病学会/美国心脏协会(ACC/AHA)高血压指南建议的降压治疗目标为130/80 mmHg(1 mmHg=0.133 kPa)的主要依据是( )
A. ACCORD研究 B. SPRINT研究 C. ADVANCE研究 D. HOT研究
2.美国糖尿病学会(ADA)认为对于绝大多数糖尿病伴高血压患者的血压目标是<140/90 mmHg并强调降压治疗目标要个体化的主要依据是( )
A. ACCORD研究 B. SPRINT研究 C. ADVANCE研究 D. HOT研究
3.糖尿病患者合并高血压时,合适的药物选择包括( )
A.血管紧张素转化酶抑制剂(ACEI) B.血管紧张素Ⅱ受体拮抗剂(ARB)
C.二氢吡啶类(CCB)和噻嗪类利尿剂 D.以上都是
4.在有代表性的中国成年人群的10年队列研究发现( )
A.血压≥140/90 mmHg者,10年后心脑血管疾病(CVD)风险显著升高
B.血压130~139/80~89 mmHg合并糖尿病时,10年后CVD的风险增加
C.血压130~139/80~89 mmHg且10年的动脉粥样硬化性心血管疾病(ASCVD)≥10%时,10年后CVD风险增加
D.以上都是
5.在糖尿病和糖尿病前期患者中开展降压治疗的随机对照研究需要注意的几个关键问题包括( )
A.研究主要终点事件的设置
B.随机化时引入的分层因素应包括ASCVD风险评估
C.血压监测方法、个体化降糖治疗的目标、肾素-血管紧张素系统(RAS)抑制剂对糖尿病和糖尿病前期的影响和降糖药物对血压的影响
D.以上都是



























