
抗反转录病毒治疗(antiretroviral therapy,ART)的出现与普及大大延长了人类免疫缺陷病毒(human immunodeficiency virus,HIV)感染者的生存期,但同时该人群的心血管疾病患病率也逐步升高。现借鉴国内外指南及学术报道,结合我国艾滋病和心血管病领域专家的临床经验,对中国HIV感染者的心血管疾病预防,特别是血脂异常和高血压这两个危险因素的管理提出建议,为临床医护人员提供参考。HIV感染者的心血管疾病危险因素会随着地域、感染原因的不同而有所差异,本建议基于现有临床证据和国内外文献提出,医护人员在临床实践时需结合当地HIV感染的具体情况确定患者的治疗策略。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
近年来,抗反转录病毒治疗(antiretroviral therapy,ART)显著延长了HIV感染者的生命,越来越多的患者并非直接死于HIV感染,而是由其他因素导致的死亡呈增加趋势[1,2,3]。心血管合并症已成为HIV感染者死亡的主要原因之一[4,5]。对HIV感染者及时进行心血管疾病预防干预,可降低其发生率和病死率。目前,国内对于HIV感染者的心血管疾病风险管理尚无共识意见,现借鉴国内外指南及学术报道,结合我国AIDS和心血管疾病领域专家的临床经验,对中国HIV感染者的心血管疾病预防,特别是血脂异常和高血压这两个危险因素的管理提出建议,为临床医护人员提供参考。
我国居民罹患的心血管疾病主要为脑卒中、冠状动脉粥样硬化性心脏病(以下简称"冠心病")、肺源性心脏病和心力衰竭等[6]。HIV感染者主要的心血管合并症是由动脉粥样硬化引起的冠心病,其发病机制、预防和治疗受到国际学界的关注[7]。
HIV感染人群的心血管疾病风险高于未感染HIV的人群。3项纳入1995年至2006年欧美地区患者的研究数据显示,相较于HIV阴性者,未治HIV感染者合并心血管疾病(心肌梗死、缺血性心脏病)的RR为1.61(95%CI 1.43~1.81,P<0.01)[8]。另一项综合16组1988年至2014年HIV感染者数据的回顾性分析显示,合并心血管疾病的RR为2.16(95%CI 1.68~2.77)[9]。美国纽约市HIV监测登记处2001年至2012年的数据显示,HIV感染者心血管疾病的病死率高出普通人群54%(RR=1.54,95%CI 1.47~1.62) [10]。目前针对亚洲HIV感染者心血管疾病流行病学的研究有限。一项2003年至2017年纳入8 069例亚洲AIDS经治患者的研究发现,心血管疾病发病率为2.2/1 000患者年,与心血管疾病相关的病死率为0.36/1 000患者年[11]。在北美及亚太地区,心血管疾病导致HIV感染者死亡的比例呈上升趋势,主要的致死病因是心肌梗死、心脏骤停和其他冠心病等[12]。
心血管疾病的传统危险因素包括高血压、血脂异常、糖尿病、吸烟和肥胖等。这些危险因素在HIV感染者中往往较在HIV阴性者中更常见。美国一项研究报道,HIV感染者的血脂异常、高血压和糖尿病的发生率均显著高于HIV阴性者,分别为23.3%比17.6%,21.2%比15.9%,11.5%比6.6%(均P<0.01)[13]。我国一项纳入973例HIV感染者的回顾性横断面研究显示,HIV感染者最常见的心血管疾病危险因素为血脂异常(51.7%)、吸烟(23.7%)、高血压(8.4%)、糖尿病(4.6%)和肥胖(1.0%),67.7%的HIV感染者具有至少一项心血管疾病的危险因素[14]。而另一项研究结果显示,泰国HIV感染者中仅37%有一项心血管疾病的危险因素[15]。此外,我国应该接受他汀类药物治疗的HIV感染者(占研究人群的4.8%)中无人接受降脂治疗,高血压的治疗率也仅占5.6%[14]。
我国HIV感染者高血压患病率和血脂异常率较高。云南省传染病医院对2013年收治的99例老年HIV感染者的回顾性分析显示,有11.11%的患者伴有高血压[16]。一项十省市对1 518例患者进行的大型调查和北京佑安医院对106例患者进行的调查均显示,初治HIV感染者的血脂异常率约为75%[17,18]。我国HIV感染人群中总胆固醇和低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)异常率较低,为1.7%~11.0%;而三酰甘油和高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)异常率较高,分别为29%~34%和30.7%~60.0%[14,17,18]。提示在我国HIV感染者长期抗病毒治疗的全程管理过程中,需密切关注心血管疾病风险因素。
抗病毒药物与HIV感染者的传统心血管风险因素之间的关系尚不清楚。一项1984年至2003年对5 578例男性HIV感染者的研究显示,长期进行ART可增加高血压患病率[19];但另一项纳入超过49 000例HIV感染者的研究提示,特定抗反转录病毒药物(antiretrovirals,ARV)与高血压之间的关系尚不明确[20]。另外,无论是否接受ART,HIV感染者的血脂异常率皆较高。在AIDS发病前,HDL-C和LDL-C水平较低,但三酰甘油水平较高[7]。开始接受ART后,总胆固醇和LDL-C水平上升,HDL-C水平变化不大[21]。
有证据显示,即使在校正传统危险因素和接受抗病毒治疗达到抑制病毒水平后,HIV感染者的心血管疾病风险仍高于HIV阴性者,提示存在与HIV及抗病毒药物相关的非传统心血管疾病的危险因素[22,23]。
HIV感染本身是心血管疾病的独立预测因素,其主要致病机制包括病毒感染引起的慢性炎症、促炎细胞因子过量、免疫功能激活,以及血管内皮功能障碍和凝血功能障碍等多种因素互相作用而最终导致的动脉粥样硬化,相较于HIV阴性者,HIV感染者的IL-6、高敏CRP、D-二聚体、可溶性CD14、可溶性CD163等水平升高,与较高心血管疾病风险相关[24,25,26,27]。
一项对5 472例HIV感染者的研究显示,相较于持续进行ART,间歇性进行ART会增加致命性和非致命性心血管疾病的发生率(HR=1.6,95%CI1.0~2.5),由于持续进行ART可维持病毒载量抑制,而间歇性使用ART会导致病毒载量回升,提示病毒载量可能与心血管疾病的发生相关[28]。此外,相比HIV阴性者,CD4+ T淋巴细胞计数<200/μL的HIV感染者心肌梗死的发生率上升76%[29]。
虽然ART能够降低病毒载量,但药物并发症可能会引发其他心血管系统改变,ART是HIV感染者重要的心血管疾病危险因素。对8项2011年以前发表的综述与荟萃分析显示,接受ART的HIV感染者心血管疾病的发病率是未接受ART的1.52倍(RR=1.52,P=0.001)。不同ARV的心血管安全性有差异,见表1。基于蛋白酶抑制剂(protease inhibitors,PI)的治疗方案易导致代谢紊乱,使用含PI方案的心血管疾病发病率比未治感染者增高65%(RR=1.65,95%CI 0.86~3.19,P=0.133),比使用不含PI方案的经治感染者增高41%(RR=1.41,95%CI 1.2~1.65,P<0.01)[8]。所有由利托那韦(ritonavir)或考比司他(cobicistat)增效的PI都会导致三酰甘油和LDL-C水平增高,但较新的PI如阿扎那韦/利托那韦(atazanavir/ritonavir,ATV/r)和达芦那韦/利托那韦(darunavir/ritonavir,DRV/r)对血脂影响相对较小[30]。此外,PI的使用可导致胰岛素抵抗,其机制可能与PI对葡萄糖转运蛋白4 (glucose transporter 4,GLUT4)减量调节的影响相关[31]。
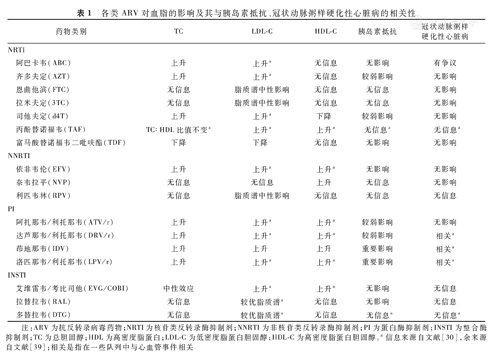
各类ARV对血脂的影响及其与胰岛素抵抗、冠状动脉粥样硬化性心脏病的相关性
各类ARV对血脂的影响及其与胰岛素抵抗、冠状动脉粥样硬化性心脏病的相关性
| 药物类别 | TC | LDL-C | HDL-C | 胰岛素抵抗 | 冠状动脉粥样硬化性心脏病 | |
|---|---|---|---|---|---|---|
| NRTI | ||||||
| 阿巴卡韦(ABC) | 上升 | 上升a | 无信息 | 无影响 | 有争议 | |
| 齐多夫定(AZT) | 上升 | 上升a | 无信息 | 较弱影响 | 无影响 | |
| 恩曲他滨(FTC) | 无信息 | 脂质谱中性影响 | 无信息 | 无信息 | 无影响 | |
| 拉米夫定(3TC) | 无信息 | 脂质谱中性影响 | 无信息 | 无信息 | 无影响 | |
| 司他夫定(d4T) | 上升 | 上升a | 下降 | 较弱影响 | 无影响 | |
| 丙酚替诺福韦(TAF) | TC∶HDL比值不变a | 上升a | 上升a | 无信息a | 无信息a | |
| 富马酸替诺福韦二吡呋酯(TDF) | 下降 | 下降 | 无信息 | 无影响 | 无影响 | |
| NNRTI | ||||||
| 依非韦伦(EFV) | 上升 | 上升a | 上升a | 无影响 | 无影响 | |
| 奈韦拉平(NVP) | 无信息 | 无信息 | 上升 | 无信息 | 无影响 | |
| 利匹韦林(RPV) | 无信息 | 脂质谱中性影响 | 无信息 | 无信息 | 无信息 | |
| PI | ||||||
| 阿扎那韦/利托那韦(ATV/r) | 上升 | 上升a | 上升a | 较弱影响 | 无影响 | |
| 达芦那韦/利托那韦(DRV/r) | 上升 | 上升a | 上升a | 较弱影响 | 相关a | |
| 茚地那韦(IDV) | 上升 | 上升 | 上升 | 重要影响 | 相关a | |
| 洛匹那韦/利托那韦(LPV/r) | 上升 | 上升a | 上升a | 重要影响 | 相关a | |
| INSTI | ||||||
| 艾维雷韦/考比司他(EVG/COBI) | 中性效应 | 上升a | 上升a | 无影响 | 无信息 | |
| 拉替拉韦(RAL) | 无信息 | 较优脂质谱a | 无信息 | 无影响 | 无信息 | |
| 多替拉韦(DTG) | 无信息 | 较优脂质谱a | 无信息 | 无信息a | 无信息a | |
一线核苷类反转录酶抑制剂(nucleoside reverse transcriptase inhibitors,NRTI) ,如富马酸替诺福韦二吡呋酯(tenofovir disoproxil fumarate,TDF)和恩曲他滨(emtricitabine)对脂代谢的不良影响较小[32]。值得注意的是,阿巴卡韦(abacavir)可能与心肌梗死发生率上升相关,但目前对其作用机制尚有争议。阿巴卡韦对血脂影响较小,增加心血管疾病风险的机制可能与血管内皮和血小板功能异常有关。合并心血管疾病或心血管疾病风险较高的HIV感染者应谨慎使用阿巴卡韦[33]。以往研究显示,早期NRTI的使用与胰岛素抵抗及糖尿病的风险上升相关[34,35]。
非核苷类反转录酶抑制剂(non-nucleoside reverse transcriptase inhibitors,NNRTI)中的依非韦伦(efavirenz)可提升LDL-C和总胆固醇水平,临床需引起注意。但有文献报道,依非韦伦可同时提升HDL-C水平,或可减轻其对总胆固醇和HDL-C的不良影响[36]。奈韦拉平(nevirapine)和利匹韦林(rilpivirine)对血脂的影响总体优于依非韦伦[37,38,39]。
国内外指南均建议为所有HIV感染者提供心血管疾病的风险评估和管理[30,33,40,41,42],但目前学界尚未就如何评估该人群的心血管疾病风险达成共识。一般人群的动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)风险评估通常以患者的血压和血脂水平作为风险分层的基本指标,再综合考量其他传统心血管疾病的危险因素。而针对一般人群的风险评估模型往往未将HIV感染特异性危险因素纳入考量,低估了HIV感染者的心血管疾病风险,因此有研究建议开发综合传统心血管疾病危险因素和HIV相关性因素的模型[27]。目前,仅有D∶A∶D5年风险评估模型纳入了HIV特异性危险因素,如CD4+ T淋巴细胞计数和特定ART的应用,但该模型尚未在中国人群中进行验证[43]。欧洲指南建议,HIV感染者应使用弗雷明汉风险评分,或者使用感染者所在地推荐的针对一般人群的评分模型进行心血管疾病的风险评估[40]。在没有针对中国HIV感染人群的评估模型前,可考虑根据患者的血压和血脂情况,选择使用针对中国人群优化过的ASCVD风险评估模型和(或)专门针对血压升高患者的心血管疾病风险水平分层模型[44,45],同时可考虑把HIV感染作为危险因素之一,以便将其增加心血管疾病风险的作用纳入考量[26]。
HIV感染者的心血管疾病风险管理主要有3个方面。第一,选用合适的ART方案以降低药物引发的心血管疾病风险;第二,做好血压和血脂的监测与控制,HIV感染者的血脂异常和高血压治疗与一般人群大体相似;第三,积极进行生活方式干预,如规律运动、控制饮食、戒烟等[41]。
国内外指南均推荐无论CD4+T淋巴细胞计数水平如何,所有HIV感染者都应尽早启动ART[30,33,40,41,42]。对已在接受ART的感染者,如果治疗过程中出现心血管疾病或较高的心血管疾病风险,应考虑调整ART方案,以降低药物相关的心血管疾病风险。国际指南对于初治和经治HIV感染者合并心血管疾病或存在高风险患者的ART方案推荐见表2。

HIV感染者合并心血管疾病或其高风险ART方案的选择、调整推荐
HIV感染者合并心血管疾病或其高风险ART方案的选择、调整推荐
| 指南名称 | ART方案 |
|---|---|
| DHHS指南[30] | 初治患者:①避免基于ABC或LPV/r的方案 |
| ②推荐基于INSTI (RAL、DTG、BICa)、NNRTI (RPV或DORa)的方案 | |
| ③如果使用RTV或COBI增效的PI,建议使用基于ATV而非DRV的方案 | |
| 合并高血脂患者: | |
| ①推荐基于RAL、DTG、BIC、RPV或DOR的方案 | |
| ②避免使用含有PI/r、PI/c 、EFV或EVG/c的方案 | |
| 经治患者: | |
| ①若因心肌梗死、缺血性脑卒中更换药物,可将ABC换为TDF、TAF、FTC、3TC | |
| ②或将RTV或COBI增效的PI、EFV、EVG/c换为对脂代谢影响较小的RAL、DTG、RPV或BIC | |
| ③若因胰岛素抵抗更换药物,可将LPV/r或FPV/r换为INSTI或NNRTI | |
| IAS-USA指南[33] | 初治患者:相较于含ABC的方案,应优先选择含替诺福韦的方案,如TAF/FTC或TDF/FTC |
| EACS指南[40] | 初治患者:①心血管疾病风险>20%的患者谨慎使用ABC |
| ②一项研究显示持续使用DRV会增加心血管疾病风险 | |
| 经治患者: | |
| ①如根据FRS或所在国家推荐的系统评估10年心血管疾病风险≥20%,考虑调整现有ART方案 | |
| ②在现有方案基础上,建议改用NNRTI、INSTI或已知会导致较小代谢紊乱和(或)降低心血管疾病风险的另一种PI/r | |
| ③如现有方案使用AZT或ABC,可用TDF替换;或可使用不包含NRTI的方案 |
注:HIV为人类免疫缺陷病毒;ART为抗反转录病毒治疗;DHHS为美国卫生和公众服务部;IAS-USA为国际抗病毒学会美国分会;EACS为欧洲艾滋病临床学会;ABC为阿巴卡韦;LPV为洛匹那韦;r与RTV为利托那韦;INSTI为整合酶抑制剂;RAL为拉替拉韦;DTG为多替拉韦;BIC为比克替拉韦;NNRTI为非核苷类反转录酶抑制剂;RPV为利匹韦林;DOR为doravirine;COBI与c为考比司他;PI为蛋白酶抑制剂;ATV为阿扎那韦;DRV为达芦那韦;EFV为依非韦伦;EVG为艾维雷韦;TDF为富马酸替诺福韦二吡呋酯;TAF为丙酚替诺福韦;FTC为恩曲他滨;3TC为拉米夫定;FPV为福沙那韦;FRS为弗雷明汉风险评分;AZT为齐多夫定。a2018年取得美国食品药品监督管理局批准上市,目前还未在我国获批上市
如确有必要,可考虑使用两联方案以降低心血管疾病风险。但目前两联方案研究数据有限,仅有少数方案获指南支持,宜谨慎使用并密切监测抗HIV疗效[33,42]。
HIV感染者的血脂异常定义、分级和调脂目标可参考《中国成人血脂异常防治指南(2016年修订版) 》[46]。在确诊HIV感染时和启动ART前需检测血脂水平,如血脂水平正常,启动ART后每年检测1次即可[40]。高水平LDL-C的HIV感染者建议先进行3~6个月的生活方式干预,之后若其10年ASCVD风险仍≥5%,可启动中等强度他汀类药物治疗[47]。正在使用PI的患者或需考虑转换ART方案,但目前各指南并未明确转换时机,有临床试验表明他汀类药物治疗比转换ART方案能更有效地降低LDL-C水平[48,49,50]。
建议患者合并血脂异常时,应据其肝功能等具体情况选择他汀类药物,并依其ART方案调整他汀类药物剂量[30,40],见表3。当他汀类药物不能有效控制胆固醇水平时,可加用依折麦布或依洛尤单克隆抗体[40]。血脂检测与ASCVD风险评估可用于监测降脂治疗效果,亦可为ART开始前和开始4~12周后调整降脂方案提供依据[47]。
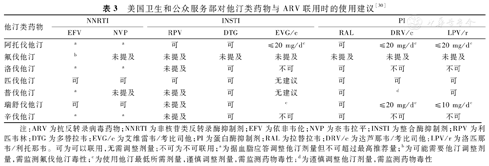
美国卫生和公众服务部对他汀类药物与ARV联用时的使用建议[30]
美国卫生和公众服务部对他汀类药物与ARV联用时的使用建议[30]
| 他汀类药物 | NNRTI | INSTI | PI | |||||
|---|---|---|---|---|---|---|---|---|
| EFV | NVP | RPV | DTG | EVG/c | RAL | DRV/c | LPV/r | |
| 阿托伐他汀 | a | a | 可 | 可 | ≤20 mg/dc | 可 | ≤20 mg/dc | ≤20 mg/dc |
| 氟伐他汀 | b | 未提及 | 未提及 | 未提及 | 未提及 | 未提及 | 未提及 | 未提及 |
| 洛伐他汀 | a | a | 未提及 | 可 | 不可 | 可 | 不可 | 不可 |
| 匹伐他汀 | 可 | 可 | 可 | 可 | 无建议 | 可 | 可 | 可 |
| 普伐他汀 | a | 未提及 | 未提及 | 可 | 无建议 | 可 | d | 可 |
| 瑞舒伐他汀 | 可 | 可 | 未提及 | 可 | c | 可 | ≤20 mg/dc | ≤10 mg/dc |
| 辛伐他汀 | a | a | 未提及 | 可 | 不可 | 可 | 不可 | 不可 |
注:ARV为抗反转录病毒药物;NNRTI为非核苷类反转录酶抑制剂;EFV为依非韦伦;NVP为奈韦拉平;INSTI为整合酶抑制剂;RPV为利匹韦林;DTG为多替拉韦;EVG/c为艾维雷韦/考比司他;PI为蛋白酶抑制剂;RAL为拉替拉韦;DRV/c为达芦那韦/考比司他;LPV/r为洛匹那韦/利托那韦。可为可以联用,无需调整剂量;不可为不可联用;a为据血脂应答调整他汀剂量但不可超过最高推荐量;b为可能需要他汀调整剂量,需监测氟伐他汀毒性;c为使用他汀最低所需剂量,谨慎调整剂量,需监测药物毒性;d为谨慎调整他汀剂量,需监测药物毒性
临床试验表明,阿托伐他汀、瑞舒伐他汀对HIV感染者安全性较好[26,51,52],而2016年欧洲心脏病学会与欧洲动脉粥样硬化学会的联合指南推荐HIV感染者使用普伐他汀[52]。匹伐他汀与ARV共用时不需调整剂量,且能改善HDL-C水平,可能更适用于HIV感染者[26,40,52,53]。辛伐他汀、洛伐他汀不可与PI、艾维雷韦/考比司他共用,与依非韦伦、奈韦拉平共用时因较强的药物间相互作用而需调整剂量[30]。HIV感染者应用氟伐他汀的安全性数据较少,不推荐使用[53]。依折麦布及依洛尤单克隆抗体与ARV均无已知的药物间相互作用[40]。
其他血脂异常的干预措施可参考《中国成人血脂异常防治指南(2016年修订版) 》[46]。除他汀类药物外,非诺贝特、苯扎贝特、鱼油可考虑用于治疗HIV感染者的高三酰甘油血症[52],这3种药物与《中国艾滋病诊疗指南(2018版) 》[42]中列出的NRTI、NNRTI、整合酶抑制剂、PI间均无已知的相互作用。更详细的调脂药物与ARV共用需注意事项可参考美国卫生和公众服务部的指南[30]和利物浦大学开发的网站(https:∥www.hiv-druginteractions.org)。
HIV感染者的高血压定义、分级、诊断及降压目标、治疗指征可参考针对一般人群的《中国高血压防治指南(2018年修订版)》[45]。1级高血压患者如需接受药物治疗,起始可使用单药治疗,亦可采用小剂量联合治疗;2级、3级高血压患者,或血压高于目标值20/10 mmHg(1 mmHg=0.133 kPa)的心血管疾病高危患者,或单药治疗未达目标值的患者,应采用两药联合治疗。见表4。

常用降血压药物与我国现有主要抗反转录病毒药物成分间的相互作用
常用降血压药物与我国现有主要抗反转录病毒药物成分间的相互作用
| 降血压药物 | NNRTI | INSTI | PI | ||||||
|---|---|---|---|---|---|---|---|---|---|
| EFV | NVP | RPV | DTG | EVG/c | RAL | DRV/c | LPV/r | ||
| ACEI | |||||||||
| 依那普利 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | |
| 培哚普利 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | |
| ARB | |||||||||
| 厄贝沙坦 | 弱 | 无 | 无 | 无 | 弱 | 无 | 无 | 弱 | |
| 缬沙坦 | 无 | 无 | 无 | 无 | 无 | 无 | 重要 | 重要 | |
| β受体阻滞剂 | |||||||||
| 比索洛尔 | 弱 | 弱 | 无 | 无 | 弱 | 无 | 弱 | 弱 | |
| CCB | |||||||||
| 氨氯地平 | 重要 | 重要 | 无 | 无 | 重要 | 无 | 重要 | 重要 | |
| 硝苯地平 | 重要 | 重要 | 无 | 无 | 重要 | 无 | 重要 | 重要 | |
| 利尿剂 | |||||||||
| 呋塞米 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | |
| 氢氯噻嗪 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | |
| 吲哚帕胺 | 重要 | 重要 | 无 | 无 | 重要 | 无 | 重要 | 重要 | |
| 螺内酯 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | 无 | |
注:ACEI为血管紧张素转化酶抑制剂;ARB为血管紧张素Ⅱ受体拮抗剂;CCB为钙通道阻滞剂;NNRTI为非核苷类反转录酶抑制剂;EFV为依非韦伦;NVP为奈韦拉平;RPV为利匹韦林;INSTI为整合酶抑制剂;DTG为多替拉韦;EVG/c为艾维雷韦/考比司他;RAL为拉替拉韦;PI为蛋白酶抑制剂;DRV/c为达芦那韦/考比司他;LPV/r为洛匹那韦/利托那韦。无为无药物间相互作用;弱为药物间可能存在弱相互作用,可能不需要额外的监测或者药物剂量调整;重要为药物间可能存在重要的相互作用,可能需要药物剂量、用药时间调整和额外的监测。根据利物浦大学药物间相互作用查询网站中的信息,表中降血压药物仅呋塞米与富马酸替诺福韦二吡呋酯间可能存在弱相互作用,其余降血压药物与《中国艾滋病诊疗指南(2018版) 》列出的所有核苷类反转录酶抑制剂(拉米夫定、阿巴卡韦、齐多夫定、恩曲他滨、丙酚替诺福韦、富马酸替诺福韦二吡呋酯)均无药物间相互作用
单药治疗时,55岁以下患者建议使用血管紧张素转化酶抑制剂(angiotensin converting enzyme inhibitor,ACEI)或血管紧张素Ⅱ受体拮抗剂(angiotensin Ⅱ receptor blocker,ARB),年龄≥55岁患者应使用钙通道阻滞剂(calcium channel blocker,CCB),治疗4~6周仍不达标则应联合用药。联合用药首选ACEI/ARB联合CCB,治疗4~6周后不达标,则加用噻嗪样利尿剂(thiazide-like diuretics,如吲哚帕胺)和螺内酯。再治疗4~6周后仍不能达标,需加用α/β受体阻滞剂,并转诊至专科治疗[40]。患者血压应在开始药物治疗后的1~3个月内(尽可能在1个月内)达标[44,45],其间仍未达标者应转诊至专科医师处继续治疗。
HIV感染者使用降压药物时需考虑其与ARV间的相互作用,ACEI、噻嗪型利尿剂(如氢氯噻嗪)与ARV之间没有相互作用,使用时无需考虑调整剂量;而ARB、CCB、β受体阻滞剂与PI及NNRTI之间存在相互作用,使用时需考虑调整剂量[40]。CCB与PI共用时起始或需使用低剂量,并视患者的血压变化调整用量[54]。更多药物共用时注意事项可查询《欧洲临床艾滋病学会指南》[40]和前述利物浦大学开发的网站。
生活方式干预是心血管疾病一级预防的重要措施,是控制血压、血脂的基本手段,所有HIV感染者均应坚持改善生活方式[40]。高血压患者要减少钠盐摄入(建议每日摄入量<6 g),同时通过食用富钾食物增加钾的摄入量[45];而血脂异常患者需通过调整饮食结构控制脂肪的摄入[46]。
本研究参考国内外多种高血压、血脂异常和艾滋病防治指南,为HIV感染者的心血管疾病预防,特别是ART选择、高血压及血脂异常的疾病管理,提出了针对性建议。建议所有的HIV感染者定期进行心血管疾病风险评估,医师可根据评估结果,参考本建议,为患者选择合适的ART方案,并对高血压、血脂异常的患者采取积极的干预措施,以降低其心血管疾病的发病风险。目前对HIV感染者防治心血管疾病的研究有限,国际上的指南多推荐参照以一般人群为目标的指南来管理HIV感染者的高血压、血脂异常等危险因素。中国在这方面的研究目前较少,未来需开展更多相关研究,为中国HIV感染者的心血管疾病预防推出更有针对性的建议。
感谢吕博、郭金龙和裘祉愉(均为Costello Medical新加坡职员)在稿件准备过程中提供的帮助及支持
所有作者均声明不存在利益冲突



























