
该篇继续教育的文章介绍了与核素11C、13N和18F共价结合的放射性标记PET示踪剂的放射化学。从回旋加速器中放射性核素的生产入手,阐述了PET示踪剂生产的全过程;之后是放射合成的自动化过程,包括相应合成的必要步骤;并最终确定了质量控制要求。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
PET分子显像探针的可获得性建立在3个主要支柱上:放射性核素生产、放射性标记方法和放射性示踪剂生产技术。
深入了解显像探针(放射性示踪剂)的分子行为,潜在的(病理)生理机制以及其与分子靶点之间的相互作用至关重要。PET中可量化的信号与连接显像探针主体的放射性核素直接相关。这些信号直接参与分子过程,因此能够直接反映出体内病理生理变化程度或机体的生物分布[1,2]。
使用一种公认和精确的(放射)化学语言很重要,因此近来在放射性药物学领域出现了一个统一的示踪剂命名法[3]。
本文的目的是巩固包括共价PET放射性标记(例如:18F、11C和13N)在内的最重要的放射性示踪剂的基本原理。
80年后,埃米利奥·塞格雷(Emilio Segré)写给欧内斯特·劳伦斯(Ernest Lawrence)的"回旋加速器显然是一种下金蛋的母鸡"(图1)这一信息(写于在劳伦斯开发的第1台回旋加速器的残余钼带中发现锝之后)[4],仍然有效。事实上,回旋加速器是大多数PET放射性核素(包括11C、13N和18F)的唯一来源。因此,黄金般的放射性核素在回旋加速器中分别由低能量和中能量(10~20 MeV)质子(H+)辐照14N、16O和18O产生,这些质子是在磁场的存在下,通过电场使负氢化离子(H-)以不断增长的螺旋式路径加速后得到的。当达到所需的能量后,加速负离子束经过一层薄薄的石墨薄膜,石墨薄膜会剥离氢化物离子的电子,从而产生所需的质子。然后,产生的质子被引导去轰击一个装有适当材料的目标,在那里发生辐射,从而发生核反应[5]。


1.11C生产[14N(p,α)11C]涉及到使用一个充满氮气(14N2)的气体靶,将其与微量氧气或氢气混合,分别得到被进一步用来标记所需分子的[11C]CO2或[11C]CH4。
2.13N[16O(p,α)13N]一般从液态水([16O]H2O)中得到。
3.18F可通过2种方法生产;第1种以高富集[18O]H2O作为靶材料,通过18O(p,n)18F反应产出[18F]F-;而第2种方法则需要一个充满20Ne的气体靶来获得[18F]F2气体。生产[18F]F2时,用氘核(2H+)替代氢核[20Ne(d,α)18F]来轰击靶标。
然而,11C合成通常包括一个后靶点合成,以将相对稳定的模块[11C]CO2和[11C]CH4转化为活性更高的种类,如[11C]CH3I等。这种转化可以通过湿法或气相法进行。
放射性示踪剂的生产已成为核医学的一个重要课题。合成时间对抵消自然衰变和辐射防护造成的损失有重要影响。因此,优先使用易于操作的全自动合成仪生产放射性示踪剂。最常用的系统是带有可重复使用反应容器的传统加热器或一次性盒式系统。后者可以为每批配备一个新盒,并且可修改活性物质的化学形态(例如浓度或纯度)。一次性盒式系统用于常规生产的示踪剂,如[18F]脱氧葡萄糖(fluorodeoxyglucose, FDG)。不幸的是,这些系统不能用于条件苛刻的标记程序或新开发的化合物;在这些情况下,需要使用传统的容器模块。此外,这种合成器有利于优化或建立新的技术。
在某些情况下,传统的加热系统不足以成功地进行放射性标记。因此,微波加热或微流体系统这种很少使用的技术显示出优越性。与传统加热器不同的是,微波使溶液均匀受热,这加快了反应速度,促进了产物的成功生成。微流体系统被设计用于处理小体积(纳升范围)和微米级的通道尺寸。因为增加压力会促进转化,这2种方法都可以将反应混合物加热到沸点以上。利用这些技术已经成功地生产了几种放射性示踪剂[6,7,8],如[18F]FDG和[18F]氟乙基胆碱。
由于相应的放射性核素的半衰期短(18F,110 min;11C,20 min;13N,10 min),每种被用于诊断的放射性示踪剂必须在使用当日准备。因此,给药前必须仔细检查所用放射性示踪剂的质量。质量控制指南详见放射性药品专著[9]。在准备过程中,关于正确的操作、生产和质量控制,有各种不同的法律、法规和规章。这些在每个国家的医学法律中均有定义。
静脉用放射性示踪剂的强制性质量控制参数如下:物理参数(渗透压、pH值和外观);放射性核素纯度(γ射线谱、半衰期的计算);放射化学纯度(放射性副产物);摩尔活性和化学纯度的测定;溶剂残留;微生物污染(无菌、细菌内毒素)。
葡萄糖类似物[18F]FDG(即2-[18F]氟-2-脱氧-D-葡萄糖;图2)无疑是最成功的PET示踪剂,其能够可视化细胞内的能量代谢。[18F]FDG利用了所谓的Warburg效应,即通常出现在肿瘤或炎性细胞中的新陈代谢向有氧糖酵解的转变,该效应导致对葡萄糖的需求增加[12]。[18F]FDG通过葡萄糖转运蛋白转运,与葡萄糖一样在细胞内磷酸化,但与葡萄糖不同的是,由于有18F原子,[18F]FDG不能进入糖酵解途径,因而被积累。这种所谓的诱捕机制,以及从各种类型的肿瘤到大脑活动的恶性变化的广泛应用,使[18F]FDG成为PET显像的主力军。由于葡萄糖水平的变化和[18F]FDG的摄取不仅仅反映病理过程,也可以反映良性变化,[18F]FDG的通用性同时也是其致命弱点[1]。
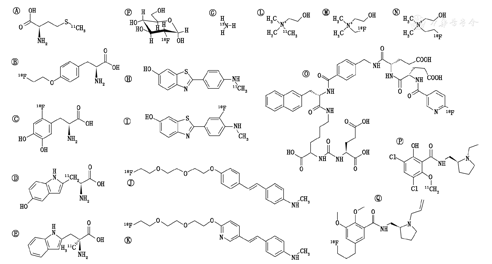

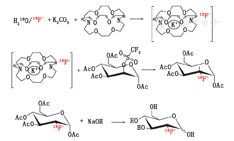
这个成功的故事发生在1976年的布鲁克海文国家实验室,在那里第1次合成了[18F]FDG。原则上,[18F]FDG可以通过亲电加成或亲核取代来生产。以前的原始合成路线使用前体3,4,6-三-O-乙酰基-D-葡萄糖醛作为双键来源来攻击亲电[18F]F2气体。然而,由于化学反应生成放射性和非放射性氟代甘露糖和葡萄糖的混合物,该途径仅有约8%的低产率。不同的亲电试剂如乙酰次萤石,未能提高[18F]FDG的产率,使得用[18F]氟离子实现更高产率的亲核方法得到实施。目前应用较多的合成路线(图3)是在相转移催化剂氨基聚醚[Kryptofix 222(Merck)]的存在下,使用[18F]氟化物对前体1,3,4,6-四-O-乙酰基-2-O-三氟甲磺酰基-β-D-吡喃甘露糖(三氟甘露糖)的取代基进行脂族亲核取代。在整个合成过程中,其他羟基均被乙酰基保护,通常用碱或酸将其除去,以使[18F]FDG的产率高达70%~80%[13,14]。

如今,[18F]FDG合成是完全自动化的,这使高收率和重现性成为可能。此外,18F的半衰期较长,因此可以每天仅生产1次[18F]FDG供所有患者使用,甚至可以将药物配发到其他PET中心。
人脑对葡萄糖的连续利用阻碍了[18F]FDG PET显像策略在脑肿瘤显像中的应用。而由于在健康大脑中的低摄取,放射性标记氨基酸被广泛应用于大脑PET显像中[15,16]。
标记氨基酸的最常见核素是11C和18F,第1种核素可确保氨基酸的结构保持不变,第2种核素可在没有现场生产的PET中心使用。另外,由于D-氨基酸没有生物学功能,因此所需放射性标记氨基酸应包含超过95%的天然L-形式。
目前流行的一种放射性标记氨基酸是用于脑肿瘤显像的L-[甲基-11C]甲硫氨酸,由于11C的半衰期短,该药每次生产量最多只能供2~3例患者使用。[11C]甲硫氨酸的合成主要以L-同型半胱氨酸硫代内酯盐酸盐或L-同型半胱氨酸为前体进行。因此,[11C]CH3I被引入到各前体和碱的混合物中。纯化可通过固相萃取或反相高效液相色谱(high-performance liquid chromatography, HPLC)进行。该反应允许使用多种溶剂,例如乙醇/水、丙酮/水或乙腈[17,18]。文献中描述的其他前体/合成路线由于其复杂性或安全问题不适用于常规生产。
O-(2-[18F]氟乙基)-L-酪氨酸{O-(2-[18F]fluoroethyl)-L-tyrosine, [18F]FET}与L-[甲基-11C]甲硫氨酸具有相似的摄取和图像对比度[19],但由于18F的半衰期长而更具优势。[18F]FET不被代谢,也不被整合到蛋白质的生物合成中,而是通过肿瘤细胞特异的转运来运输。这种转运在恶性细胞中被加速,导致肿瘤组织中[18F]FET的大量积累。[18F]FET最初是通过两步反应合成的,该反应包括乙二醇-1,2-二甲苯磺酸酯的[18F]氟化反应和随后的L-酪氨酸盐的[18F]氟乙基化,并包括2次HPLC纯化[20]。一种高效的常规生产方法(一锅法反应)是从O-(2-甲苯磺酰氧基乙基)-N-三苯甲基-L-酪氨酸叔丁基酯作为前体开始[21],该程序包括随后的酸性脱保护和HPLC纯化。另一种方法是使用2-三氟化溴乙酯作为前体,随后对中间体([18F]溴氟乙烷)进行蒸馏,这需要带有2个反应器的合成模块。该方法有利的是不需要HPLC纯化,可以使用简单的固相萃取来完成纯化[22]。此外,还可用(S)-酪氨酸席夫碱的Ni(Ⅱ)络合物作为[18F]FET的光学纯标记前体[23]。
非蛋白原的氨基酸3,4-二羟基-6-[18F]氟-L-苯丙氨酸{3,4-dihydroxy-6-[18F]fluoro-L-phenylalanine,[18F]FDOPA}反映了突触前多巴胺能合成和芳香族氨基酸脱羧酶的酶活性。[18F]FDOPA在以帕金森病、运动障碍和精神分裂症为首的神经精神疾病中得到广泛应用。此外,其应用范围扩展到脑肿瘤显像和外周肿瘤显像,[18F]FDOPA反映了增殖增加导致的恶性组织氨基酸转运上调。亲核放射氟化方法提供了高化学产率和高摩尔活度的[18F]FDOPA。18F的引入可以用光学纯前体进行,然后进行脱保护和纯化;或者由非手性前体引入,这需要手性转移催化剂来产生对映体选择性产物[24,25]。此外,铜介导的被保护的L-3,4-二羟基苯丙氨酸锡烷的亲核放射氟化反应先前也有报道[26]。
目前用于研究血清素合成的PET示踪剂是色氨酸衍生物α-[11C]甲基色氨酸{α-[11C]methyltryptophan,[11C]AMT}和5-羟基-L-[β-11C]色氨酸。这2种示踪剂的放射性合成都非常复杂,包含多个步骤。[11C]AMT是通过在低温(-55~75 °C)下采用强碱(主要是二异丙基氨基锂)对相应的前体进行质子化制得的。随后,将[11C]CH3I引入溶液中,并在酸性和碱性条件下进行保护后,通过C18固相萃取提纯获得最终产物[27,28]。较少使用的5-羟基-L-[β-11C]色氨酸是通过酶促反应合成的[29]。最近,研究表明色氨酸的18F类似物可实现示踪剂的分布[30,31]。
考虑到前列腺癌在世界范围内的巨大影响,目前已开发几种PET示踪剂用于在体内显像这种恶性肿瘤[32]。胆碱是细胞膜磷脂生物合成的重要分子,因此其被11C和18F标记后(如[18F]氟甲基胆碱和[18F]氟乙基胆碱)可用于靶向前列腺癌和脑瘤。尽管还有其他示踪剂,如[68Ga]前列腺特异膜抗原(prostate-specific membrane antigen, PSMA)-11,[18F]PSMA-1007和[18F]N-[N-[(S)-1,3-二羧基丙基]氨基甲氨酰基]-4-[18F]氟代酶-L-半胱氨酸{N-[N-[(S)-1,3-dicarboxypropyl]carbamoyl]-4-[18F]fluorobenzyl-L-cysteine, [18F]DCFBC}在首次试验中显示了优异的结果,胆碱衍生物仍然是临床上最常用于前列腺癌的PET示踪剂。
放射性标记胆碱衍生物的合成如下:对于[11C]胆碱,用活性物质[11C]CH3I与二甲基氨基乙醇的二甲基甲酰胺溶液反应生成产物,将其纯化并用生理盐水配制。对于[18F]氟甲基胆碱,将[18F]F-干燥,直到完全无水;随后,用二溴甲烷生产标记的模块[18F]溴氟甲烷,将其蒸馏后与二甲基氨基乙醇反应,生成产物[18F]氟甲基胆碱。对于[18F]氟乙基胆碱,放射性合成的过程与[18F]氟甲基胆碱合成相似;但是,加入三氟甲磺酸溴乙酯代替二溴甲烷,以获得标记的化合物[18F]溴氟乙烷。另一种方法使用二甲苯磺酸乙烯酯来提供标记的模块2-[18F]氟乙基甲苯磺酸酯。由于产物的阳离子性质,所有这些示踪剂的纯化都是直接进行的,因此可以用阳离子交换树脂分离产物。
放射性核素13N标记药物[13N]NH3{[13N]氨}被广泛用于评估心肌灌注。[13N]NH3的生产需要现场回旋加速器和快速的合成过程,因为其半衰期短至10 min。通过用质子照射水([16O]H2O)可以生产大量13N[5]。依靠质子能量,在氧存在下的辐射分解产生副产物[13N]亚硝酸盐和[13N]硝酸盐。这些副产物必须在催化剂即Devarda合金的作用下,在碱性溶液中还原,生成50%~90%的[13N]NH3[33,34]。
除了上面提到的具有生物或生理功能的PET示踪剂(例如L-[甲基-11C]甲硫氨酸和[18F]FDG用于代谢,[13N]NH3用于灌注)之外,还有大量直接针对特定受体、转运蛋白、酶和抗原的示踪剂可用于临床常规使用、临床试验或临床前研究。
在肿瘤学中,PSMA具有独特的现实意义。PSMA在前列腺癌和前列腺转移灶中表达上调,并且可以通过放射性标记肽[18F]PSMA-1007靶向。最新数据表明,肿瘤与背景的摄取比值高,药物具有出色的药代动力学特性,因此适用于小肿瘤和转移灶的显像。肿瘤学中的特异性PET示踪剂,如[18F]PSMA-1007,能够用于早期诊断,且是规划理想治疗方案的辅助剂[35]。
受体可通过拮抗剂(受体活性抑制剂)或激动剂(信号转导激活剂)靶向,以显像特定目标(如受体)的密度或表达变化。其基本原理是比较健康对照组和患者之间的显像数据,测量特定治疗前后的表达水平,或者靶向肿瘤中上调的特定受体。另外,借由特定的放射性标记底物可以深入了解转运蛋白的功能。受体的呈现是针对脑功能的临床研究的主要要求。已经开发了大量具有不同靶点(例如多巴胺能系统)的放射性示踪剂,其目的是确定脑部疾病的病理生理变化,确定新的治疗方法并确定治疗效果。其中,[11C]雷氯必利(raclopride)和(S)-(-)-N-(1-烯丙基吡咯烷-2-氨基甲基)-5-氟[18F]丙基-2,3-二甲氧基苯甲酰胺{(S)-(-)-N-(1-allylpyrrolidine-2-N-methyl)-5-(3-18F)-2,3-dimethoxy benzamide; [18F]法鲁必利,[18F]fallypride}在反映D2/D3亚型或锥体外D3受体方面特别有效[36]。
除了细胞内神经纤维缠结外,灰质中的细胞外淀粉样蛋白斑块是阿尔茨海默病的病理特征[37]。目前已经开发了几种PET示踪剂来观察体内的纤维状β-淀粉样蛋白斑块。
[11C]匹兹堡化合物B{[11C]Pittsburgh compound B,[11C]PIB}{2-[4-(甲基氨基)苯基]-1,3-苯并噻唑-6-醇}是首个特异性β-淀粉样蛋白斑块显像的PET示踪剂。其为一种硫代黄素-T类似物,一种用于在体外对淀粉样蛋白斑块进行染色的荧光染料。放射合成由未保护的前体2-(4′-氨基苯基)-6-羟基苯并噻唑的苯胺部分直接11C-甲基化组成[38]。随后通过反相HPLC进行纯化[39]。18F标记的淀粉样蛋白示踪剂已被引入临床广泛使用,药物可从一个生产场所被分配到多个PET中心。
[18F]氟美他莫(flutemetamol,商品名:Vizamyl;生产商:GE Healthcare)是[11C]PIB的氟代衍生物[40]。另外2个18F标记淀粉样蛋白示踪剂[18F]氟比他班(florbetaben,商品名:Neuraceq;生产商:Piramal)和[18F]氟倍他帕(florbetapir,商品名:AMYViD;生产商:Eli Lilly)[41,42,43]均由二苯乙烯衍生而来。上述药物是通过亲核取代各N-Boc保护的甲苯磺酸酯前体,直接[18F]氟化反应合成的。为了除去N-Boc保护基,反应后加入HCl水溶液。所有3个18F标记示踪剂均通过反相HPLC纯化。
共价结合的放射性核素的多功能性和适用性是巨大的,尤其是与金属放射性标记PET示踪剂相比,化学结构没有改变(11C)或只有轻微改变(18F)。局限性主要由时间因素和设备(如便于从生产现场到PET中心的供应的现场回旋加速器)导致。



























