
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
新型冠状病毒(2019-nCoV)肺炎(coronavirus disease 2019, COVID-19)以轻症居多,但仍有部分患者表现或发展为重型及危重型肺炎[1,2,3]。多项研究显示,非甲状腺疾病综合征(nonthyroidal illness syndrome, NTIS)与多种非甲状腺疾病的其他重症疾病预后相关[4,5,6,7],表现为一系列甲状腺激素(thyroid hormone, TH)的改变。超敏C反应蛋白(hypersensitive C-reactive protein, hs-CRP)作为一种急性时相反应蛋白,在机体发生感染时可异常升高,被广泛用于监测炎性疾病。本研究对COVID-19患者的TH、hs-CRP进行分析,探讨两者与疾病严重程度的关系,为判断预后提供依据。
1.患者资料及分组。回顾性选取2020年1月21日至2020年2月7日本院定点收治的81例COVID-19确诊患者为研究对象,其中男44例,女37例,年龄15~80(47.2±14.7)岁。纳入标准:符合《新型冠状病毒肺炎诊疗方案》(试行第七版)的确诊病例诊断标准[8],临床分型分为轻型、普通型、重型及危重型。排除标准:既往有甲状腺疾病史;近1个月内服用过影响甲状腺功能的药物和食物;近期其他部位有急性感染者。本研究符合《赫尔辛基宣言》的原则,并获得重庆三峡中心医院伦理委员会批准[伦理批件号:2020-11(论)]。
根据疾病严重程度,对患者进行分组:(1)轻症组(包括轻型及普通型)59例,男33例,女26例,年龄(43.2±11.5)岁;有基础疾病者19例,其中高血压6例,糖尿病3例。(2)重症组19例,男8例,女11例,年龄(58.6±17.7)岁;有基础疾病者9例,其中糖尿病4例,高血压2例。(3)危重症组3例,均为男性,年龄(60.3±8.5)岁;有基础疾病者1例,为糖尿病酮症。
2.检测方法。所有患者行入院常规检查,并于次日空腹采血4~6 ml送检。采用瑞士罗氏公司Cobas8000电化学发光法检测三碘甲状腺原氨酸总量(total triiodothyronine, TT3)、甲状腺素总量(total thyroxine, TT4)、游离三碘甲状腺原氨酸(free triiodothyronine, FT3)、游离甲状腺素(free thyroxine, FT4)、促甲状腺激素(thyroid stimulating hormone, TSH)、甲状腺球蛋白(thyroglobulin, Tg);采用深圳新产业生物医学工程股份有限公司Maglumi4000化学发光法检测反三碘甲状腺原氨酸(reverse triiodothyronine, rT3);采用瑞士罗氏公司C701免疫透射比浊法检测hs-CRP。上述指标正常参考值范围分别为1.30~3.10 nmol/L、66~181 nmol/L、2.8~7.1 pmol/L、12~22 pmol/L、0.27~4.20 mU/L、3.5~77.0 μg/L、0.31~0.95 μg/L和0~11 mg/L。
3.统计学处理。应用SPSS 17.0软件进行统计学分析,符合正态的定量资料采用 ±s表示,不符合正态分布的定量资料用M(P25,P75)表示。多组间变量分析采用单因素方差分析及最小显著差异t检验、Dunnett′s T3法或Kruskal-Wallis秩和检验。定性资料以例数及百分比表示,采用χ2检验或Fisher确切概率法进行分析。两变量间的相关性采用Spearman秩相关分析,P<0.05为差异或相关性有统计学意义。
±s表示,不符合正态分布的定量资料用M(P25,P75)表示。多组间变量分析采用单因素方差分析及最小显著差异t检验、Dunnett′s T3法或Kruskal-Wallis秩和检验。定性资料以例数及百分比表示,采用χ2检验或Fisher确切概率法进行分析。两变量间的相关性采用Spearman秩相关分析,P<0.05为差异或相关性有统计学意义。
1.一般资料比较。轻症组、重症组和危重症组患者年龄差异有统计学意义(F=11.540,P<0.05),其中轻症组年龄低于另外2组(均P<0.05)。3组间性别构成差异无统计学意义(χ2=3.727,P>0.05)。
2.NTIS构成与转归。81例患者中,32例发生NTIS,占39.51%(32/81)。32例NTIS中,合并基础疾病者14例,无基础疾病者18例;合并基础疾病与无基础疾病的COVID-19患者NTIS构成比差异无统计学意义(χ2=0.938,P>0.05)。轻症组、重症组和危重症组患者中NTIS分别有17、13和2例,构成比差异有统计学意义(χ2=10.396,P<0.05),其中重症和危重症组NTIS发生比例为68.18%(15/22),而轻症组为28.81%(17/59)。轻症组中有5例转为重症或危重症,其中3例伴NTIS,转变比例3/17;2例不伴有NTIS,转变比例4.76%(2/42)。随访1个月,22例重症和危重症患者中,19例存活,其中13例伴有NTIS;3例死亡,其中2例伴有NTIS;两组间NTIS构成比差异无统计学意义(Fish确切概率法,P>0.05)。
3.3组患者临床指标的比较(表1)。TT3、TT4、FT3、FT4、TSH、Tg、rT3及hs-CRP批间CV%分别为:3.950%、2.440%、4.810%、6.540%、2.710%、2.400%、8.580%和2.240%。除TT4、TSH和Tg(F=2.321,H值:4.897和1.058,均P>0.05)外,余指标在3组间差异均有统计学意义(F值:3.643~12.878,H=29.963,均P<0.05)。其中,重症或危重症组TT3、rT3明显低于轻症组(均P<0.05),且危重症组降低更为明显。重症组FT3明显低于轻症组(P<0.05),而FT4明显高于轻症组(P<0.05)。
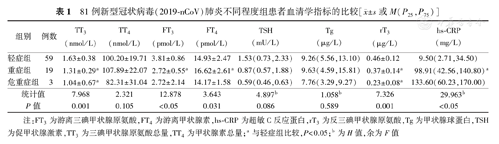
81例新型冠状病毒(2019-nCoV)肺炎不同程度组患者血清学指标的比较[ ±s或M(P25,P75)]
±s或M(P25,P75)]
81例新型冠状病毒(2019-nCoV)肺炎不同程度组患者血清学指标的比较[ ±s或M(P25,P75)]
±s或M(P25,P75)]
| 组别 | 例数 | TT3(nmol/L) | TT4(nmol/L) | FT3(pmol/L) | FT4(pmol/L) | TSH(mU/L) | Tg(μg/L) | rT3(μg/L) | hs-CRP(mg/L) |
|---|---|---|---|---|---|---|---|---|---|
| 轻症组 | 59 | 1.63±0.38 | 100.20±19.71 | 3.81±0.86 | 14.93±2.47 | 1.53(0.73,2.33) | 9.26(5.56,13.10) | 0.46±0.12 | 9.50(2.71,34.50) |
| 重症组 | 19 | 1.31±0.29a | 107.89±22.07 | 2.72±0.55a | 16.62±2.61a | 0.87(0.57,1.88) | 9.63(4.59,15.81) | 0.37±0.14a | 98.91(42.56,140.80)a |
| 危重症组 | 3 | 1.04±0.67a | 82.31±31.04 | 2.72±2.14 | 14.17±1.58 | 0.59(0.46,0.63) | 7.76(3.29,9.27) | 0.23±0.08a | 133.60(60.23,170.00) |
| 统计值 | 7.968 | 2.321 | 12.878 | 3.643 | 4.897b | 1.058b | 7.326 | 29.963b | |
| P值 | 0.001 | 0.105 | <0.05 | 0.031 | 0.086 | 0.589 | 0.001 | <0.05 |
注:FT3为游离三碘甲状腺原氨酸,FT4为游离甲状腺素,hs-CRP为超敏C反应蛋白,rT3为反三碘甲状腺原氨酸,Tg为甲状腺球蛋白,TSH为促甲状腺激素,TT3为三碘甲状腺原氨酸总量,TT4为甲状腺素总量;a与轻症组比较,P<0.05;b为H值,余为F值
4.相关性分析。81例患者确诊时hs-CRP水平[16.55(3.28,59.24) mg/L]与FT3[(3.52±0.98) pmol/L]、TT3[(1.53±0.40) nmol/L]呈负相关(rs值:-0.480、-0.260,均P<0.05),与rT3[(0.43±0.14) μg/L]、TT4[(101.34±20.98) nmol/L]、FT4[(15.30±2.56) pmol/L]、TSH[1.41(0.63,2.24) mU/L]未见相关性(均P>0.05)。
尽管大多数COVID-19患者表现为普通型和轻型,但仍有部分患者会进展为重型及危重型[9]。不同疾病的危重患者易伴发NTIS,其机制包括:(1)下丘脑-垂体-甲状腺轴(hypothalamic-pituitary-thyroid axis, HPT)的改变:重症状态使TSH释放激素(thyrotropin-releasing hormone, TRH)基因表达减少,TSH脉冲分泌亦减少,对三碘甲状腺原氨酸(triiodothyronine, T3)、甲状腺素(thyroxine, T4)负反馈应答,对TRH的反应能力减弱。(2) TH转运和代谢异常:甲状腺素结合球蛋白(thyroxine-binding globulin, TBG)、白蛋白的减少;5′-脱碘酶的活性受抑制;T3受体的上调;血硒浓度的下降等;(3)细胞因子、应激激素的作用:白细胞介素1(interleukin 1, IL-1)和IL-6、肿瘤坏死因子-α、干扰素-β、皮质醇的增多可抑制HPT,下调TBG数量及降低5′-脱碘酶活性[10,11]。
本研究显示,不同程度COVID-19患者均可发生NTIS,重症及危重症NTIS发生率明显高于轻症患者(68.18%与28.81%),而合并基础疾病与否对患者NTIS的发生似乎并无明显影响。COVID-19患者主要表现为TT3、FT3、FT4、rT3异常,其中重症组TT3、FT3、rT3明显低于轻症组,且TT3、rT3在危重症组降低更为明显。与既往研究一致[10],本研究中COVID-19重症及危重症患者TT3及FT3降低,TSH正常或偏低;但rT3并无升高,反而随病情程度加重而降低。既往研究认为,rT3增高是由于脱碘酶异常使TT4向rT3转换增多及rT3降解减少所致[10],本研究重症组TT4较轻症组差异虽无统计学意义,但有升高趋势,是否可能提示重症患者TT4并未向rT3转换而导致rT3降低?但危重症组TT4又较重症组出现明显骤降,rT3继续降低难以解释。据报道,并非所有NTIS都呈现rT3增高,如人类免疫缺陷病毒(human immunodeficiency virus, HIV)感染的群体可表现为FT3、rT3、FT4降低,且降低的rT3会随入院后发生的机会性感染而升至正常水平[11]。众所周知,HIV与新型冠状病毒(2019-nCoV)均属RNA病毒,HIV蛋白酶抑制剂洛匹那韦/利托那韦被纳入COVID-19诊疗方案用于一般的抗病毒治疗[8],尽管近期一项随机对照临床试验证实其不能改善重症患者临床症状及降低死亡率[12],同期述评给予该试验高度评价,但同时认为疗效不显著可能与所选择人群病情偏重及人类目前对病毒复制的组织中药物浓度知之甚少有关[13]。除此之外,艾滋病及COVID-19患者的免疫系统均受到病毒攻击,致使免疫功能紊乱甚至崩溃。由此推测,COVID-19患者rT3可能呈现出与HIV感染类似的下降,但具体机制不详。本研究中,重症组FT4明显高于轻症组,据报道最初饥饿24~48 h时FT4可能轻度升高,这是由于饥饿时升高的游离脂肪酸可抑制TH和蛋白质结合,但随着连续的饥饿及疾病进展,FT4会逐渐降低[14]。COVID-19重症患者食欲差,因此,不排除饥饿导致FT4增高。
早期流行病学调查及近期研究表明,年龄与COVID-19严重程度及死亡相关[9,15]。本研究重症患者较轻症患者年龄亦偏大(平均年龄58.6与43.2岁)。Hs-CRP是炎性反应的敏感指标,与病情变化及严重程度有一致性[16]。本研究显示,重症患者hs-CRP水平较轻症明显增高,hs-CRP与FT3、TT3呈负相关,提示COVID-19患者早期炎性反应越重,NTIS发生率越高,患者病情亦偏重,但伴有NTIS的COVID-19患者死亡风险并未相应增加。
综上,本研究显示,COVID-19重症患者年龄偏大,且较轻症患者更易合并NTIS,主要表现为TT3、FT3及rT3的降低。患者早期炎性反应越重,NTIS发生率越高。本研究也存在不足:病例数少、无同期健康对照、组间例数相差较大、未能动态监测COVID-19患者甲状腺功能变化;另外,COVID-19属于新发传染病,并发NTIS尤其是rT3降低的原因尚待进一步探讨。
所有作者均声明不存在利益冲突


























