
患者男,62岁,运动迟缓17年。患者于2005年无明显诱因逐渐出现全身运动迟缓,表现为双手笨拙,起立困难,行走缓慢,小步前驱,脚底有黏滞感,转动时动作分解,伴面部表情减少。此后患者运动迟缓症状逐渐加重,逐渐出现四肢僵硬,站立姿势不稳,伴嗅觉丧失、言语模糊、嘴角流涎、全身多汗、便秘、勃起功能障碍。患者否认静止型震颤、精神行为异常、抑郁焦虑、淡漠、睡眠障碍等症状。2015年起用多巴丝肼、盐酸普拉克索、盐酸司来吉兰片等药物治疗,症状改善明显。2018年出现药物起效慢,药效维持时间短,伴用药后明显异动,症状逐渐加重,遂于2022年7月入本院治疗。入院体格检查示患者言语模糊,记忆、计算力差,自发张嘴,可见流涎,全身可见明显不自主运动,四肢肌力5级,四肢肌张力明显"铅管"样增高,双手对指、握拳、轮替试验缓慢,双足点地缓慢,幅度小,起立困难,起步困难,行走小步前驱,双手伴随动作少,转身分解,站立有自发跌倒趋势。结合患者病史、症状、体征,临床考虑帕金森病(Parkinson′s disease, PD),患者存在锥体外系、嗅神经、自主神经等多个系统受累。
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者男,62岁,运动迟缓17年。患者于2005年无明显诱因逐渐出现全身运动迟缓,表现为双手笨拙,起立困难,行走缓慢,小步前驱,脚底有黏滞感,转动时动作分解,伴面部表情减少。此后患者运动迟缓症状逐渐加重,逐渐出现四肢僵硬,站立姿势不稳,伴嗅觉丧失、言语模糊、嘴角流涎、全身多汗、便秘、勃起功能障碍。患者否认静止型震颤、精神行为异常、抑郁焦虑、淡漠、睡眠障碍等症状。2015年起用多巴丝肼、盐酸普拉克索、盐酸司来吉兰片等药物治疗,症状改善明显。2018年出现药物起效慢,药效维持时间短,伴用药后明显异动,症状逐渐加重,遂于2022年7月入本院治疗。入院体格检查示患者言语模糊,记忆、计算力差,自发张嘴,可见流涎,全身可见明显不自主运动,四肢肌力5级,四肢肌张力明显"铅管"样增高,双手对指、握拳、轮替试验缓慢,双足点地缓慢,幅度小,起立困难,起步困难,行走小步前驱,双手伴随动作少,转身分解,站立有自发跌倒趋势。结合患者病史、症状、体征,临床考虑帕金森病(Parkinson′s disease, PD),患者存在锥体外系、嗅神经、自主神经等多个系统受累。
PD是成人最常见的神经变性疾病之一,由脑内多巴胺能神经元变性丢失所致,主要表现为静止型震颤、运动迟缓、强直及姿势不稳等症状[1]。临床上需要将PD与其他形式的帕金森综合征进行鉴别,因为上述疾病对多巴胺能药物的治疗反应不同,只有准确进行临床诊断,才能正确地使用PD治疗药物。目前尚无确诊PD的生理学、影像学或血液学检查,其诊断仍主要依靠临床医师识别特征性的体征和相关症状等。PD的核心症状是运动迟缓与静止性震颤或肌强直。除此之外,PD还包括一系列神经精神及非运动表现,如认知功能障碍、心境障碍、胃肠道功能障碍以及自主神经功能障碍等。临床上多用国际PD与运动障碍协会的诊断标准来诊断PD[2],该标准要求患者存在PD的核心症状,同时符合支持性标准,且不符合绝对排除标准。在支持性标准中,间碘苄胍(metaiodobenzylguanidine, MIBG)显像所反映的心脏去交感神经支配就是其中之一,这提示患者存在自主神经功能障碍。
自主神经广泛分布于内脏、腺体及心血管,对其功能活动进行调节,又称为内脏神经。自主神经包括交感神经、副交感神经以及肠神经系统。其中,交感神经主要参与机体在应激状态下的反应,会引起心率加快、血压升高、呼吸深快、糖原分解增加等现象;副交感神经主导机体平和状态下的功能,使机体心率减慢、血压降低、支气管收缩。对于交感神经,从神经中枢到效应器会经过2个神经元:节前神经元胞体位于脑干或脊髓,轴突延伸至外周的神经节,以乙酰胆碱作为神经递质;节后神经元胞体位于神经节内,轴突延伸至所支配的器官,以去甲肾上腺素作为神经递质。交感神经节后神经元通过突触前膜释放去甲肾上腺素至突触间隙,去甲肾上腺素与突触后膜的受体结合进行信号传导,而一部分突触间隙的去甲肾上腺素会被重新转运至节后神经元中。MIBG是去甲肾上腺素的类似物,也可通过去甲肾上腺素的转运蛋白转运至细胞内。心脏中分布着大量的交感神经,因此在健康人中通过MIBG显像可以观察到心脏的显像剂浓聚;而在交感神经支配受损的患者中,MIBG的显影程度会减低。本例患者为评估心脏交感神经支配情况、进一步明确PD的诊断行131I-MIBG显像(图1),可见心脏区域无明显显像剂浓聚,15 min心脏/纵隔计数比为1.44,4 h心脏/纵隔计数比为1.22,考虑为心脏交感神经失支配,支持PD的诊断。
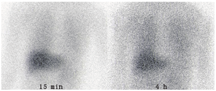

131I-MIBG心脏交感神经显像有一系列的注意事项。首先,在检查前,患者应在医师的指导下停用可能影响MIBG摄取的药物,如胺碘酮、多巴胺、钙通道拮抗剂、α受体阻滞剂、血管活性药物、麻黄碱、抗精神病药物、三环类抗抑郁药物等[3]。其次,在注射131I-MIBG前1 d应开始应用复方碘溶液或碘化钾2~3 d,以封闭甲状腺。注射131I-MIBG时应经患者外周静脉缓慢注射(宜持续5 min以上),以免MIBG引起生理性的不良反应,如心动过速、恶心、呕吐等。注射MIBG后,应嘱患者大量饮水以促进药物排泄。注射药物后15~20 min行早期显像,3~4 h行晚期显像,扫描范围包含胸部,采集时用高能平行孔准直器。
正常的131I-MIBG显像肝本底摄取较高,另外脾、肺、唾液腺、甲状腺及心肌也有一定水平的生理性摄取,这与交感神经的分布相符。由于PD患者存在自主神经功能障碍,其131I-MIBG显像会表现为心脏摄取减低,提示心脏交感神经支配受损,病理学研究也证实PD患者的心肌组织中存在交感神经功能失常[4,5,6,7,8]。有意思的是,虽然交感神经在心脏、肺、甲状腺、唾液腺、肠道等诸多器官中均有分布,但PD患者的MIBG显像仅会出现心脏的摄取减低,而其他脏器的摄取与健康人无异[9,10,11]。
131I-MIBG心脏交感神经显像阅片可以从定性和定量不同角度进行评估。定性评估主要观察心脏区域是否存在显像剂浓聚,心脏显影是否清晰。其中早期显像主要反映交感神经系统的完整性和心交感神经的分布情况,晚期显像主要反映神经元对MIBG的主动摄取能力。定量评估是通过在心脏和纵隔区域勾画ROI,计算心脏和纵隔的放射性计数比值(heart/mediastinum, H/M)。健康人的H/M约为2.24±0.14,PD患者的H/M约为1.31±0.15,较健康人群明显降低[12]。
除PD外,神经退行性帕金森综合征还包括进行性核上性麻痹(progressive supranuclear palsy, PSP)、多系统萎缩(multiple system atrophy, MSA)、皮质基底节变性(corticobasal degeneration, CBD)等疾病。这些疾病临床症状相似,但治疗方式及预后存在明显差异,MIBG显像可以在这些疾病的鉴别诊断中发挥作用。PD患者存在心脏交感神经失支配,心脏MIBG的摄取下降,而PSP、MSA、CBD患者的心脏MIBG摄取基本正常(图2)。
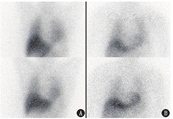

核医学是功能影像的代表,虽然其空间分辨率不够高,有时像在"雾里看花",但其能够反映疾病的某种特有病理生理变化,这使其在疾病的诊治体系中有着独特的魅力。
所有作者声明无利益冲突


























