
总结采用机器人辅助腹腔镜下切除前列腺小囊并同期行精道重建的临床经验。
回顾性分析2019年7月至2019年9月收治的5例反复出现附睾炎和尿路感染的尿道下裂术后患儿的临床资料。本组年龄为(47.2±42.2)个月,均行泌尿系统超声和排尿造影明确前列腺小囊存在,并采用机器人辅助腹腔镜下切除前列腺小囊并同期行精道重建术。术后均行泌尿系统超声及小便常规检查。
5例患儿手术均获得成功,手术时间为(133.0±77.1)min,无中转开放手术及术中并发症发生。随访4~6个月,本组未再出现反复附睾炎和尿路感染等术后并发症。
机器人辅助腹腔镜下切除前列腺小囊并同期行精道重建安全有效,但精道通畅性和成年后的生育率仍需要更长期的随访和数据支持。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
尿道下裂是小儿泌尿系统最常见的疾病之一。尿道下裂常合并前列腺小囊(约11.4%),而在会阴型尿道下裂中这一情况更高达50%[1]。大部分前列腺小囊不会出现任何症状。若前列腺小囊引起尿路感染、附睾炎等并发症,早期可采用抗生素治疗。一旦药物治疗失败或反复复发,则需要进行手术。也有报道指出,尿道下裂合并前列腺小囊的病例中有50%会出现临床症状,需要手术治疗[1]。手术方式可分为开放切除手术和腹腔镜或机器人辅助腹腔镜下切除手术。因为儿童盆腔狭小开放手术和腹腔镜手术操作较困难,且切除前列腺小囊的同时会切断双侧输精管,导致精道连续性中断。因此,尿道下裂合并出现并发症的前列腺小囊的手术治疗具有挑战性。2019年7月至2019年9月我们尝试对5例反复出现附睾炎和尿路感染的尿道下裂术后患儿通过机器人辅助腹腔镜切除导致并发症的前列腺小囊并重建精道,现报道如下。
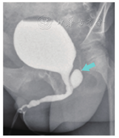
5例患儿年龄为(47.2±42.2)个月,范围在1岁至9岁4个月,中位数为36个月。附睾炎和尿路感染发作3~6次,平均3.8次,中位数4次,附睾炎均为单侧发作。行泌尿系统彩色超声和排尿性膀胱尿道造影检查显示后尿道可见前列腺小囊(图1);患儿尿道下裂术后排尿通畅,最大尿流率(Qmax)为(6.3±1.8)ml/s,中位数为5.6 ml/s。本研究已通过医院伦理委员会审核[伦审(研)2020年第99号],并获得所有参与研究患儿家属的知情同意。

患儿取截石位,在全身麻醉下行膀胱镜检查尿道膀胱,明确前列腺小囊位置及其大小,了解其底部有无子宫颈结构存在。在膀胱镜引导下安置尿管。
患儿换仰卧位呈头低脚高。由脐上缘置入1.2 cm的Trocar作为镜头孔,建立气腹,压力维持在10 mmHg,置入达芬奇机器人系统镜头,在直视下于腹直肌两侧边缘各建立一个8 mm操作通道,分别放入1号和2号机械臂。在镜头孔与右侧操作通道中点上方5 cm处设置5 mm辅助通道。将带针线穿过前腹壁、膀胱再穿回前腹壁,牵拉起膀胱,暴露膀胱后方手术区域。
打开盆底腹膜,沿双侧输精管寻找前列腺小囊。由前列腺小囊的顶端向盆底方向游离前列腺小囊,避免损伤直肠和输尿管(图2)。游离前列腺小囊至尿道。于前列腺小囊前壁远端纵向切开囊壁,明确前列腺小囊汇入尿道的位置,避免尿道损伤。于双侧输精管汇入前列腺小囊顶端的水平切断前列腺小囊。于靠近尿道处切断前列腺小囊颈部。移除中间段的前列腺小囊组织,用6-0 Vicryl将连着双侧输精管的前列腺小囊壁与尿道端的前列小囊残壁进行吻合(图3)。在盆底放置一根引流导管。
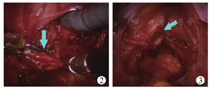

注:箭头所指为将双侧输精管吻合至后尿道上处
本组手术均顺利完成,无中转开放及改变术式者。术中发现5例均于精阜位置存在前列腺小囊开口,囊底无子宫颈结构,双侧输精管开口于前列腺小囊顶部或顶部两侧。手术时间为(133.0±77.1)min,范围在60~250 min,中位数为100 min。术后住院时间7~9 d。术后5~7 d拔除引流管。患儿术后均恢复顺利,引流管内未引流出尿液样液体。
本组随访时间在4~6个月。所有患儿术后症状均未再出现附睾炎和尿路感染,无下尿路症状及排尿困难。术后3个月复查泌尿系统超声未见明显盆腔囊肿和积液。所有患儿均继续行随访观察。
尿道下裂患儿的前列腺小囊是泌尿生殖窦发育过程中双氢睾酮不足而引起的[2]。由于其在解剖学和临床表现上与苗勒管残件/囊肿有许多共同特点,因此在相当多的报告中前列腺小囊被错误地命名[3]。尿道下裂患儿在妊娠早期(9周)阴道正常退化时,由于没有足够的双氢睾酮抑制,从而导致阴道板空腔化形成阴道下三分之一,也就是前列腺小囊[2]。而睾酮局部作用于午非氏管,靠近睾丸的部分弯曲形成附睾,远端与尿生殖窦相连形成精囊腺。本组患儿双侧输精管均开口于前列腺小囊的顶端或顶端两侧。但为何患儿每次术后均出现单侧附睾炎症状,现在暂无文献提出原因和支持证据。作者认为可能附睾炎更易出现在输精管开口直径更大的一侧。另外,苗勒管残件/囊肿是因为在孕7~9周时,睾丸支持细胞所分泌的抗苗勒管激素(Anti-Müllerian hormone,AMH)不足或其受体功能障碍,导致苗勒管退化不全而形成。因此,前列腺小囊是退化不全的阴道下三分之一结构,而苗勒管残件/囊肿是退化不全的阴道上三分之二、子宫和输卵管结构。有无子宫颈结构是临床上区别前列腺小囊和苗勒管残件/囊肿的重要依据。膀胱镜检查可经尿生殖窦进入阴道并明确阴道底部有无子宫颈结构。尿道下裂合并前列腺小囊患儿的睾丸功能和精道发育通常是正常的,双侧输精管汇入前列腺小囊顶端。因此,有研究主张在前列腺小囊的切除术中尽量保留输精管以保护患儿自然生育的可能性[4]。相反,存在苗勒管残件/囊肿的患儿,往往睾丸支持细胞存在严重功能障碍,支持细胞功能与精子生成密切相关。因此,在性发育异常疾病中含有苗勒管残件/囊肿者往往是没有生育潜能的[5]。所以,在苗勒管残件/囊肿切除术中,输精管离断对其自然生育率的影响并不是关键因素。
以往在前列腺小囊的外科切除术中,深部手术和输精管离断问题被认为是此手术最具有挑战性和争议的问题。国内曾采用经尿道电切扩大前列腺小囊开口[6]、经腹或经会阴的前列腺囊肿切除术[7]等手术方式来处理有症状的前列腺小囊,取得了一定的效果。但腹腔镜手术比开放手术提供了更好的手术途径和手术视野,因此越来越多的国内外学者认为腹腔镜手术是治疗前列腺小囊一种更优越的方法[8,9,10]。但由于空间狭小,单纯腹腔镜下仍然无法完成输精管与尿道的吻合这一精准且高难度的步骤。最近,机器人辅助的腹腔镜入路在男性膀胱后囊肿手术中被报道[4,11,12,13,14,15]。机器人辅助通过三维视觉和简单的仪器操作可视化极好,允许在深而窄的空间(如盆底)进行精确的解剖和重建。我们的实践进一步证明了机器人辅助腹腔镜下对有症状的前列腺小囊患儿在进行前列腺小囊切除后可更进一步完成精道重建。
我们认为,对于有以下情况的患儿,应行前列腺小囊切除和精道重建:①反复尿路感染或附睾炎(至少3次),或保守治疗失败者;②在膀胱尿道镜检查中明确为前列腺小囊而非苗勒管残件/囊肿者;③父母要求精道重建,获得充分知情并同意。有人发现青春期前精道阻塞可能会造成成年后生精上皮发育不良和精子成熟障碍[16,17]。这提示我们在儿童期进行前列腺囊切除术后若不能完成精道重建并确保精道通畅,将有可能导致成年后睾丸生精功能障碍。另一方面也表明单侧输精管切除术并不是治疗前列腺小囊导致反复附睾炎的最理想方法。前列腺小囊切除后,实现精道的解剖重建可能优于目前报道的其他技术。
吻合的输精管应监测其反流和闭塞情况。然后限于患儿年龄小,我们暂时无法通过现有的技术,如精道镜、精道造影等,来明确吻合的输精管是否通畅。另一方面,手术中对后尿道和输精管的热损伤是另一个值得注意的问题。目前短期的随访似乎未见明显异常,但还需要进行更长期的随访。生育能力是这项技术的最终目标,我们将对这些患儿进行随访,直到他们成年。
所有作者均声明不存在利益冲突



























