
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
肾输尿管重复畸形是泌尿系统常见的先天畸形,指患侧肾脏存在上、下2套集合系统(少见也有2套以上),如果2条输尿管分别开口于膀胱或其他部位,此为完全型,如果2套集合系统在进入膀胱前融合,只有一个共同的输尿管开口于膀胱,表现为分支型肾盂及"Y"形输尿管,则为不完全型。肾输尿管重复畸形临床表现各异,治疗方案多且有些尚存争论,欧洲泌尿外科协会(European Association of Urology,EAU)从其并发畸形入手制订了相关诊疗指南,目前国内尚无关于此病的指导性建议。中华医学会小儿外科学分会泌尿外科学组及小儿尿动力和盆底学组借鉴国外相关指南,结合国内临床实际及小儿泌尿外科医生诊治经验,针对肾输尿管重复畸形的诊断、治疗、随访等编写本共识。
肾输尿管重复畸形发生率约为0.7%[1],左侧略多于右侧,约20%为双侧发病,女性约是男性的2倍。在出生前诊断为肾积水的患儿中,5%~7%是肾输尿管重复畸形引起[2]。在泌尿系感染(urinary tract infection,UTI)的儿童中肾输尿管重复畸形高达8%[3]。
不完全型重复肾大多无其他泌尿系异常,完全型重复肾常伴发输尿管膨出、输尿管异位开口、膀胱输尿管反流(vesicoureteral reflux,VUR)等畸形,少见合并肾盂输尿管连接部梗阻(ueteropelvic junction obstruction,UPJO)[4]。UPJO和VUR常发生于下肾输尿管,输尿管异位开口及输尿管膨出主要发生于上肾部输尿管。重复肾也可伴发心脏、生殖道、腮耳等其他系统畸形[5]。60%重复肾患儿无特异临床表现,多为体检或偶然就诊发现。UTI是常见临床症状,偶见腰痛,女性少见输尿管膨出脱垂,输尿管异位开口的女性患者可表现为二次正常排尿间歇外阴持续性尿滴沥,而男性患者通常无尿失禁,而表现为受累系统的疼痛或感染(附睾炎)[6]。
肾输尿管重复畸形的诊断主要依靠影像学检查,尤其在手术干预前,需对泌尿系统进行详细的形态及功能性评估。
超声是便捷、无创性检查,可显示泌尿系结构形态、肾实质厚度及回声特点、积水程度、输尿管膨出位置及大小等,基本可明确肾输尿管重复畸形的诊断,为筛查、手术前后对比、随访等提供可靠资料。推荐超声作为首选检查方法。
静脉肾盂造影(intravenous pyelography,IVP)不仅可显示肾盂、输尿管、膀胱形态,还能定性评估肾功能,肾功能差或肾盂输尿管严重扩张时显示不佳。用于解剖结构不明确的肾输尿管重复畸形,或确定无集合系统扩张的尿失禁患儿有无输尿管异位开口。
排尿期膀胱尿道造影(voiding cystourethrogra phy,VCUG)可明确是否合并VUR以及输尿管膨出,并评估膀胱、尿道功能,确定有无膀胱出口梗阻(bladder outlet obstruction,BOO)、膀胱形态及排空情况。常规推荐此项检查,并建议在手术干预前完成[7]。
磁共振尿路造影(magnetic resonance urography,MRU)或CT尿路造影(computed tomography urography,CTU)可提供泌尿系统解剖形态[8],用于其他影像学不能确诊的复杂病例。CTU还可根据肾实质厚度及强化程度了解上肾功能,同时显示输尿管形态。MRU及CTU费用高,需安静状态下进行,不能配合者可镇静或麻醉,根据临床具体情况酌情选择。
肾核素显像是评价肾功能的金标准,通常选用99mTc-二巯基琥珀酸(dimercaptosuccinic acid,DMSA)成像。重复肾的上肾功能是评估的重点,其他肾单位在合并VUR或肾积水时也需要评估。结合超声或其他影像学检查,DMSA可显示重复肾区域的皮质厚度和核素摄取情况,临床意义在于确定是否保留上肾单位[9]。肾动态核素显像常用99mTc-二亚乙基三胺五乙酸(diethylenetriaminepentaacetic acid,DTPA)成像,用于输尿管膨出随访,了解肾滤过功能及梗阻缓解情况。通常上肾功能≤10%定义为无功能[10],但仍无确切客观参数标准来衡量上肾的切除或保留,而且术前评估也无法预测术后远期的功能恢复情况。
膀胱尿道镜检查及逆行泌尿系造影非必须的,主要用于上述影像学检查仍难以确诊,或术前为手术方案制定需要明确输尿管膨出类型、输尿管开口位置、输尿管形态等。由于输尿管膨出导致BOO,或输尿管异位开口及输尿管膨出导致膀胱颈部关闭不全,均可引起膀胱功能障碍,所以膀胱功能评估不可忽视。超声和VCUG可对评估功能进行初步评估,必要时仍需行尿流动力学评价,尤其对行下尿路重建手术后出现的膀胱功能障碍者。
共识1 超声作为筛查、随访的首选检查;VCUG常规推荐,需在手术前完成;肾核素扫描通常用DMSA成像,无客观参数标准来确定上肾的切除或保留;其他检查根据情况酌情选择。
肾输尿管重复畸形较复杂,其病理的复杂性决定治疗方案的多样性,且有些尚存争议,近年来总体趋势越来越保守。其基本治疗原则为:尽量保存肾功能、解除梗阻及VUR、控制UTI、维持尿控、尽可能减少手术干预及降低并发症。治疗方式的选择在遵循方案个体化基础上,需综合患儿的临床表现、年龄、肾输尿管积水(hydroureteronephrosis,HUN)程度及上肾的功能、是否存在VUR、输尿管膨出类型、法定监护人意愿及外科医生的经验等诸多因素。
肾输尿管重复畸形多数是胎儿期超声检查发现的。超声下显示是2个单独的不连通的肾盂,局限在上极的扩张肾盂及扩张的输尿管,或存在输尿管膨出等典型特征性表现时有助于诊断。当肾输尿管无积水时,超声诊断有一定难度[8],未能确诊者建议出生后进一步影像学检查明确诊断。
胎儿期即诊断肾输尿管重复畸形者,建议到小儿泌尿外科进行咨询,制订随访及出生后治疗计划,以尽量减少出生后UTI,并防止肾脏进行性损害[11]。输尿管异位开口无需胎儿期干预。胎儿期输尿管膨出引起的BOO导致上尿路损害过程缓慢,所以无论单侧或双侧重复肾,即使合并肾积水或BOO者,只要不是双侧肾发育不良,均可待出生后再处理且预后良好。输尿管膨出引起严重BOO并双侧肾发育不良导致羊水量明显减少者,生后有发展为终末期肾病的风险,需要胎儿期干预,但此种情况罕见[12]。胎儿期干预措施有超声下膀胱穿刺引流和胎儿膀胱镜下行输尿管膨出经尿道内切开术(transurethral incision,TUI),虽然减压效果良好,但有胎膜早破、早产、感染、出血、甚至胎儿死亡等风险,实施需谨慎[13,14]。
如合并心脏、生殖、腮耳等其他系统畸形,可能与多基因缺陷有关[5]。需和家属沟通,行MRI或羊水穿刺基因学筛查。
共识2 胎儿期检查一旦确诊,建议超声随访观察,出生后评估并制订诊疗计划。胎儿期干预风险大,多无必要,不推荐,若全面评估确定需胎儿期干预的必须非常慎重。
出生后评价应首先做超声检查,存在HUN者需行VCUG检查,肾功能评价通常在>2月龄后进行。上肾无严重HUN、存在Ⅲ级及以下VUR、无BOO及临床症状者,可予观察。3~6个月后再行超声、VCUG检查、肾功能等评估。
严重输尿管扩张是发生UTI的风险因素,原发性非反流性输尿管扩张患儿发热性UTI的发生率要比单纯肾积水患儿高[15]。所以,对于存在严重HUN,无论是否合并输尿管膨出,即使无下肾输尿管反流也可以考虑采取预防措施以减少感染的风险[16],特别是在诊断性检查完成之前。关于此类患儿抗生素预防治疗的适应证及用药疗程目前均无明确标准。建议3~6月龄以内,有输尿管扩张、VUR,2次及以上发热性泌尿系感染(febrile urinary tract infection,fUTI)病史者,可根据需要及家长意愿选择部分病例予持续口服抗生素预防(continuous antibiotic prophylaxis,CAP)治疗[17]。CAP虽然降低了UTI发生率,但增加耐药细菌引起感染的风险[18]。抗生素会影响人体正常的微生物群,对患儿身体功能和生长发育可能产生不良影响,远期风险尚未确定[19]。另外,包茎是婴幼儿期UTI的高风险因素,在无反流的上尿路扩张或输尿管膨出中其意义不确定,在有高级别VUR的男孩中包皮环切术对预防fUTI有一定作用[20,21]。
UTI可发生于任何年龄,发热呈多样性,脓毒症状明显者建议应用足量、敏感抗生素治疗,疗程视感染控制情况而定,一般不少于10~14 d,通常UTI可得到控制;如果UTI控制不佳、脓毒症状重并有明确的输尿管梗阻导致的严重HUN者,需及时减压解除梗阻引流尿液,利于缓解脓毒症状并控制感染。减压手术有以下几种:①肾盂或输尿管穿刺造瘘术,操作简单,效果确切,需留置体外引流管,适用于输尿管梗阻导致严重HUN者;②合并输尿管膨出者可行TUI术,梗阻缓解率高,少数梗阻缓解不明显者可再次穿刺,无需留置体外引流[22];③输尿管异位开口伴有脓毒症或严重HUN者可行姑息性输尿管远端皮肤造口术,可立即减压,术后根据肾功能恢复情况制定进一步治疗方案,并需再次手术处理输尿管[23]。
共识3 出生后进行影像学评价,3~6月龄以下者多保守治疗。根据病情需要及家长意愿选择CAP治疗,但CAP适应证及用药时间等无明确标准,远期风险不确定。fUTI者需行抗感染治疗,对于UTI控制不佳、脓毒症状重并有明确输尿管梗阻者,需行输尿管减压手术利于控制感染。
保守策略基于对重复肾输尿膨出患儿自然病程的了解,但目前的了解仍有限。无严重HUN、同侧下肾或对侧Ⅲ级及以下VUR、无BOO、无肾功能下降、无临床症状者,不论上肾功能如何均可选择保守观察[10,24],存在VUR者可予CAP治疗。随访观察中可能无任何临床症状、无UTI、HUN及VUR也可能自行缓解或消退,但仍可能出现不可预测的fUTI,HUN及VUR加重等。保守观察的长期风险和临床预测指标仍不确定,给予此方案需仔细筛选病例和权衡,并需按期随访。如果观察过程中出现了以CAP治疗前提下的突破性尿路感染(breakthrough UTI,BT-UTI)、BOO或上尿路HUN加重,则需要手术治疗。
共识4 保守观察需仔细选择病例,严格控制适应证,因存在潜在的不确定风险,需定期随访,根据病情变化及时调整治疗方案。
根据肾输尿管重复畸形临床表现、上肾功能、输尿管畸形的病理形态,其治疗方法也不同。手术指征包括:存在进行性HUN加重或肾功能下降、Ⅳ级及以上VUR、BOO、输尿管异位开口导致尿失禁、规范的CAP治疗后仍然出现BT-UTI等。
上肾发育差或无功能、HUN明显、输尿管引流不畅者,无论是合并异位开口还是输尿管膨出,首选上肾切除术(upper pole heminephrectomy,UHN)。手术可以选择开放或腹腔镜方式,腹腔镜下UHN经腹腔或腹膜后途径手术效果差异无统计学意义[25],但比开放手术后输尿管残端炎发生率低,这可能与腔镜下输尿管远端显露切除更彻底有关[26]。UHN疗效确切,去除病变肾及输尿管,降低泌尿系感染发生率,术后残留的输尿管膨出逐渐瘪陷,减轻对上肾输尿管开口及膀胱出口压迫,若无BOO及残端炎,可无需处理。输尿管膨出合并下肾输尿管低度VUR者中,UHN术后下肾VUR也有可能消失[27],从而避免膀胱水平手术对膀胱三角局部结构破坏,减少排尿功能障碍发生[28]。UHN最严重的并发症是下肾血管损伤导致下肾功能丧失。腹腔镜下UHN术后尿性囊肿发生率可达20%,多发生于创面未缝合病例中,是下肾损伤还是上肾实质残留所致尚不清楚,多无临床意义,无症状及无进行性增大的尿性囊肿可随访观察。随着腔镜技术普及提高,UHN术后并发症发生率呈逐渐下降趋势。术前影像学评估重复肾类型对手术方式选择及术中操作有帮助[29],应尽量避免下肾血管及集合系统损伤。
鉴于上肾切除可能损伤下肾血管,也有学者对上肾功能差或无功能的输尿管异位及梗阻型输尿管膨出者行单纯的上肾输尿管结扎术[30,31]。虽然术式简单,但术后有持续性肾盂积水、fUTI甚至脓肾等并发症,远期疗效仍不确定,不推荐临床应用。
重复肾上肾有功能且发育好者,下输尿管无VUR及梗阻者可行上、下肾盂或输尿管的端侧吻合术,包括肾盂-肾盂吻合术、输尿管-肾盂吻合术、输尿管-输尿管端侧吻合术(ureteroureterostomy,UU)等[32]。UU最常用,其吻合口水平选择可根据输尿管扩张情况及医生经验选择,上肾输尿管扩张明显者,可在近端水平行肾盂-输尿管吻合或输尿管-输尿管吻合术,尽量多的切除迂曲扩张之上输尿管,减少术后UTI发生[33],远端在避免损伤下输尿管的原则下尽可能低位切除[23]。UU术后临床效果好,很少发生吻合口狭窄;术后是否存在"YO-YO"反流尚缺乏证据,其临床意义也不明确。此术式损伤小,手术风险低,不仅保留了有功能上肾,也避免下肾血管损伤,降低创面出血、尿外渗等并发症发生。对于上肾功能差或下肾轻度VUR者能否行UU存在争议,保留无功能上肾可能增加高血压风险,下输尿管反流可能消退缓慢或持续存在而需再次手术,不建议UU应用于上述情况。
输尿管膨出合并下肾Ⅲ级及以下的低级别VUR患儿,尽管不会增加VUR等级、感染发生及肾瘢痕形成的风险,长期随访VUR自发缓解率同单集合系统VUR缓解率差异无统计学意义,但消退所需时间长[34]。术前下输尿管存在高级别VUR的输尿管膨出者,行UHN术后几乎不可避免地需要再次手术。因此,重复肾上肾有功能并下肾输尿管VUR者,建议同时行上下输尿管共鞘再植或UU后单根输尿管再植手术[35]。部分患肾单纯上或下部输尿管异常者,双输尿管共鞘再植对正常的下肾输尿管一并手术,增加了医源性损伤的可能,可经膀胱外行单纯上或下部输尿管再植术[36],避免损伤另一无病变的输尿管,也无需考虑UU术时输尿管管径不匹配,降低术后VUR发生率,但输尿管膨出未切除,远期有再次手术可能。
共识5 对上半肾发育不良、或肾功能差甚至无功能者,建议首选UHN;上肾发育良好、有功能者建议保留上肾,若下肾输尿管无VUR及梗阻可行UU。上肾有功能并下肾输尿管VUR者,建议同时行上下输尿管共鞘再植或UU后单根输尿管再植手术。
下尿路重建手术包括输尿管膨出切除、膀胱修补、输尿管抗反流再植术等,适用于异位输尿管膨出较大导致BOO并下肾VUR者,或输尿管膨出行TUI术后减压无效,存在严重的VUR、BOO、反复fUTI者[37]。此手术同时解除梗阻并纠正VUR,完全切除输尿管膨出,无肾脏损伤风险,缺点是手术较复杂,有发生膀胱功能障碍可能。输尿管膨出切除具体手术方式的选择需结合病情、术中情况及术者经验决定。输尿管膨出下方逼尿肌有必要同时修补,远端部分游离时避免损伤膀胱颈及尿道括约肌,不能完整切除时可仔细电切后两层缝合关闭。不论何种手术术后都需确定残余膨出是否影响排尿。两条重复输尿管不可强行分离,避免影响血运。有报道输尿管膨出切除及双输尿管共鞘再植术后再反流发生率高达5%~10%[38],可能是输尿管管径与膀胱黏膜下隧道长度比例失衡导致。婴儿期膀胱小,技术困难,术后发生反流或梗阻等并发症风险高,建议6月龄后实施。
输尿管膨出行下尿路重建术后出现膀胱功能障碍发生率在0~13% [39,40],可能因输尿管膨出存在膀胱颈、尿道解剖或功能缺陷有关,但也不除外手术导致神经肌肉等医源性损伤的可能。对出现膀胱功能障碍患儿建议行VCUG及尿流动力学等检查综合评价,其治疗方案取决于病因,存在膀胱尿道功能障碍者可通过口服抗胆碱类药物、排尿训练、生物反馈等综合治疗,若疗效不佳,可能需行膀胱和三角区重建或膀胱颈修复、间歇性导尿等治疗[38]。
共识6 下尿路重建手术同时解除梗阻并纠正VUR,适用于异位输尿管膨出导致BOO、或合并下肾VUR者,TUI术后减压无效或存在严重的VUR有症状者。缺点是手术较复杂,术后有发生膀胱功能障碍可能。出现膀胱功能障碍者建议行影像学及尿流动力学检查全面评估,根据病因进行综合治疗。
经尿道输尿管膨出切开/穿刺术(transurethral incision/puncture,TUI/TUP)或输尿管膨出开窗术(Ureterocele Fenestration)等均可有效解除输尿管末端梗阻达到减压目的,但此类手术存在争议,主要是术后新发VUR、再手术的风险及预后均存在不确定性。
TUI术后新发VUR发生率在0~65%。TUI术后新发VUR最常见上肾输尿管,也可发生同侧下极及对侧,部分可自然缓解,若不缓解或导致反复fUTI,可手术治疗[41,42]。TUI术后新发反流发生率与输尿管膨出类型、操作技术等有关。原位型输尿管膨出TUI术后约70%~80%的病例达到减压而无VUR达到治愈的目标,而异位输尿管膨出TUI术后新发VUR及再手术率要明显增高[43]。同横切口及常规穿刺技术相比,采用"Watering Can"喷壶式多点穿刺技术可显著降低异位输尿管膨出术后新发VUR发生率及反流级别[44]。
TUI术后再手术率差别很大,与术前病例选取的输尿管膨出类型及是否合并VUR、术中操作技术、术后再手术指征的选择有关[45,46]。术前下肾部输尿管存在反流和输尿管膨出的类型对TUI疗效的有重要影响,下肾输尿管存在反流的再次手术率是无反流的1.74倍,异位输尿管膨出的再手术率则高出2.78倍[43]。随着内镜切开技术的改进,TUI后再手术率明显下降[47]。再手术原因主要有减压不充分持续存在梗阻、持续或新发VUR、反复fUTI等。与其他开放手术相比,TUI操作简便,有部分治愈可能,即使需再次手术,输尿管减压后可不同程度收缩,也有利于后期手术的实施[41]。TUI术后造成的新发VUR即使行UHN或UU,残端输尿管反流可能还需处理,需同时行输尿管膨出切除及下输尿管膀胱再植术[46];尤其异位输尿管膨出,使再次手术概率及难度增加,有膀胱功能障碍发生可能[28],临床应用仍需谨慎。
TUI术存在争议的焦点在于如何权衡梗阻解除与新发反流之间的利弊,若能接受"解除梗阻并接受反流"的理念,TUI术后再手术率可能降低,TUI术后上肾输尿管梗阻解除而无高级别反流、无BOO、无临床症状者,可不必进一步手术干预,可随访观察。反流性的输尿管膀胱侧侧吻合术[48]也基于此理念,使非反流性的HUN严重者达到减压目的,但术后VUR也可能引起肾脏损害,且此手术创伤较TUI大,其临床安全性及远期效果有待确定,不推荐应用。
共识7 TUI术以控制感染、解除梗阻为目的,建议TUI主要适用于:①抗生素控制不佳、败血症的发热性UTI等紧急情况;②3~6个月以下存在BOO、HUN加重/上肾功能下降、CAP治疗仍有反复UTI者;③有手术指征的原位型输尿管膨出患儿[49]。原位型输尿管膨出行TUI效果明显好于异位输尿管膨出,部分可达治愈。TUI术后新发VUR可能需行输尿管膨出切除甚至下尿路重建术处理,手术复杂且可能导致膀胱功能障碍,所以TUI临床应用仍需谨慎,不建议常规作为一线治疗手段。
此手术包括上肾及输尿管膨出切除、下肾输尿管抗反流再植、膀胱颈/膀胱三角区重建手术等,既切除无功能上肾,又解决输尿管反流,也可防止远期膀胱功能障碍和尿失禁,适用于上肾无功能、下肾高度VUR、有巨大异位输尿管膨出并可耐受此手术的年长儿童。
共识8 完全重建手术虽然安全有效,但创伤大,多数可以通过简单的分次手术解决,所以上下尿路完全重建手术的必要性仍存在争议[46],不常规推荐。
输尿管异位开口手术方式选择取决于重复肾上肾功能,如果上肾无功能,建议首选UHN。上肾有功能需保留,取决于下肾输尿管是否存在VUR:下肾输尿管没有VUR,则行UU术[50];如果存在VUR则进行上、下输尿管共鞘再植或UU后再行下肾输尿管膀胱再植术。如果肾功能不明确,可暂行姑息性输尿管末端造口术进行减压后再评估肾功能,尤其是输尿管严重扩张或脓毒症的病例。
上肾血管、输尿管结扎[51]及选择性上肾血管栓塞术[52,53]治疗上肾功能差并输尿管异位开口尿失禁者,术后效果良好,但临床报道病例较少,缺乏远期疗效评价,不常规推荐。
共识9 输尿管异位开口的治疗根据上肾功能选择保留或切除肾单位,对于保留上肾者根据下肾输尿管是否有反流选择行UU或输尿管再植手术。
重复肾合并UPJO发病率较低,为2%~7%[54],多发生于不完全重复肾之下肾,上肾UPJO罕见。评估和治疗原则类似于单系统UPJO,手术方案应根据梗阻部位解剖特点、距离输尿管汇合处距离、狭窄段长度、下肾功能等综合决定。若下肾输尿管狭窄段短且距"Y"形输尿管汇合点距离足够长时,可行标准的离断式肾盂输尿管成形术;如果狭窄段较长,可行下肾盂与上输尿管端侧吻合术,或上下肾盂吻合后下肾盂与输尿管再吻合术等[55]。下肾积水重或发育差,肾功能<10%,可选择下肾切除。
肾输尿管切除术后残留的远端输尿管引发的泌尿系感染、下腹部疼痛、血尿等症状被称为输尿管残端综合征(ureteral stump syndrome,USS)。术后USS发病率约为0.8%~1.0%[56],与术前输尿管形态及远端有无梗阻、VUR、UTI等有关。UHN和UU术后均存在发生USS的可能。重复肾输尿管切除手术时对输尿管远端的处理应在避免损伤下肾输尿管的原则下尽可能低位切除。对USS应予积极抗感染治疗,对于难控制感染、反复发作USS者需行输尿管残端切除术。而残端与下输尿管相邻紧密者,可同时行上肾输尿管再植术。对残端存在输尿管膨出并梗阻者也可行TUI[57],若术后仍反复感染再行膨出切除术。
共识10 重复肾合并UPJO评估和治疗原则同于单系统UPJO,手术方案应根据梗阻部位解剖特点选择;输尿管残端综合征多保守治疗,保守无效或反复发作可选择手术治疗。
随访首选超声检查,术后3个月、6个月、1年行泌尿系超声检查,了解肾发育、HUN缓解程度、输尿管膨出等变化以及有无尿性囊肿等。术前存在输尿管末端膨出、VUR、或行下尿路重建手术者术后3~6个月行VCUG检查。术后半年行肾脏核素显像检查了解肾功能的恢复情况。除影像学检查外,还需观察有无USS、排尿功能障碍、尿失禁等临床症状,术后随访存在膀胱功能障碍的患儿除影像学检查外建议行尿流率或尿流动力学评估。因远期有发生结石、肿瘤等可能[58],建议远期每隔1~2年行超声学检查。
目前,重复肾治疗遵循"简单即更好"的总体趋势,其并发畸形病理状态的复杂性决定治疗方案多样性。不可能用一种方案解决所有问题,一种方案也适用于多种病理状态,同一病理状态可有多种治疗方案,同一病理状态的严重程度不同治疗方案也可不同,而且随着一些新的理念和技术的成熟,治疗方案只会越来越多,医生需根据自己经验及技术水平仔细选择权衡,不可盲从,同一方案在不同医生实施后效果可能会有很大不同,尽量以安全、简单、有效的方法达到治疗目的。重复肾治疗方案也需个体化,患儿年龄、临床表现、并发畸形的复杂程度不同,治疗方案也可能有很大的不同,术前需全面系统评估泌尿系形态及功能,结合患儿临床症状、监护人意愿、医生技术水平等综合考虑制订个体化治疗方案。肾输尿管重复畸形是小儿泌尿外科常见疾病中病理改变极为复杂的一种先天畸形,其治疗方案呈多样性,希望通过全国同道们共同努力,建立大样本多中心临床平台,以期能获得更可靠的、有价值的临床研究成果及治疗方案,对此病的诊治有更加深入的认识(图1)。
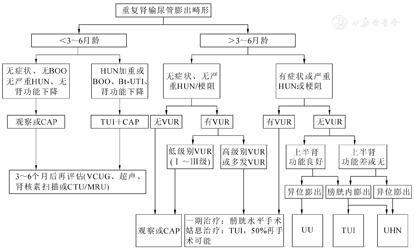

注:BOO,膀胱出口梗阻;HUN,肾输尿管积水;Bt-UTI,突破性尿路感染;CAP,持续口服抗生素预防;TUI,经尿道内切开术;VCUG,排尿性膀胱尿道造影;VUR,膀胱输尿管反流;UU,输尿管-输尿管端侧吻合术;UHN,上肾切除术;MRU,磁共振尿路造影;CTU,CT尿路造影
参与共识制定的专家(按姓氏首字拼音排序):毕允力(复旦大学附属儿科医院);陈方(上海市第六医院);耿红全(上海交通大学附属新华医院);何大维(重庆医科大学附属儿童医院);黄鲁刚(四川大学华西医院);黄轶晨(上海市儿童医院);李守林(深圳市儿童医院);孙宁(首都医科大学附属北京儿童医院);宋宏程(首都医科大学附属北京儿童医院);唐达星(浙江大学医学院附属儿童医院);吴荣德(山东省立医院);文建国(郑州大学第一附属医院);杨屹(中国医科大学附属盛京医院);张潍平(首都医科大学附属北京儿童医院);赵夭望(湖南省儿童医院)
执笔专家:李守林(深圳市儿童医院)、姜俊海(深圳市儿童医院)
所有作者均声明不存在利益冲突


























