
甲状旁腺激素相关蛋白(parathyroid hormone-related protein,PTHrP)、组蛋白去乙酰化酶4(histone deacetylase 4,HDAC4)及印度刺猬蛋白(indian hedgehog,Ihh)对生长板软骨细胞的增殖、分化有重要的调控作用,上述基因的缺失在小鼠模型上均表现为短肢畸形。因此,对PTHrP-HDAC4/Ihh信号通路调控机制的研究可为治疗矮小症、侏儒症等软骨发育相关疾病提供临床新思路和干预新靶点。本综述主要总结近年来以该通路为主的相关因子对生长板发育调控机制的新进展,以期为儿童软骨发育相关疾病病理机制的深入研究提供新视角。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
生长板是重要的软骨结构,主要由细胞外基质和软骨细胞组成。与永久性软骨不同,生长板软骨不断地被骨取代,从而完成肢体的纵向延长及生长。软骨内骨形成初期,间充质细胞凝聚中心分化为软骨细胞,软骨细胞经历增殖、分化、矿化等过程,形成具不同形态的细胞层:静息区、增殖区、前肥大区和肥大区域,最终完成骨的形成。生长板在软骨内骨化和骨形成过程中发挥重要作用,是骨纵向生长的主要分化区域。软骨细胞的异常调控影响生长板发育进程,导致生长板结构和骨骼发育的异常,最终可引起多种软骨相关疾病如矮小症、侏儒症。生长板发育调控涉及细胞内多条信号通路和转录因子,甲状旁腺激素相关蛋白(parathyroid hormone-related protein, PTHrP)与印度刺猬蛋白(indian hedgehog, Ihh)组成的负反馈环路对软骨细胞的增殖及分化有重要的调控作用。此外,作为经典的IIa型HDACs的成员——组蛋白去乙酰化酶4(Histone deacetylase 4, HDAC4)通过促进染色质凝聚和转录抑制参与多种组织发育中的相关信号网络。生长板发育期间,HDAC4参与PTHrP-Ihh信号通路并在其中发挥重要作用(图1),本研究主要对PTHrP-HDAC4/Ihh信号通路为主的生长板发育的调控机制进行综述,以期为儿童软骨发育相关疾病病理机制的深入研究提供新视角。
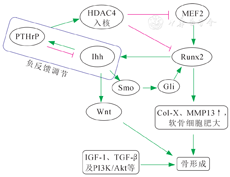

注:PTHrP,甲状旁腺激素相关蛋白;HDAC4,组蛋白去乙酰化酶4;Ihh,印度刺猬蛋白;MEF2,肌细胞增强因子;Runx2,runt相关转录因子2;MMP13,基质金属蛋白酶13;Col-X,X型胶厚;IGF-1,胰岛素样生长因子1;TGF-β,转录生长因子β;PI3K/Akt,磷脂酰肌醇三激酶/丝氨酸/苏氨酸激酶
甲状旁腺素(parathyroid hormone,PTH)是由甲状旁腺分泌,含84个氨基酸的多肽类物质,PTH及其相关分子PTHrP拥有共同受体PTHR,生物学功能相似。目前认为,PTH调节出生后生物体内的钙磷平衡,而PTHrP通过调控软骨细胞的增殖和分化指导生长板的发育[1]。HDAC4是PTHrP调控软骨细胞分化所必需的,PTHrP对其核质定位的调节最终影响HDAC4下游靶向基因的表达,调节软骨细胞生长分化。PTHrP信号可借助蛋白磷酸酶2A(protein phosphatase 2A, PP2A)作用使HDAC4去磷酸化,诱导HDAC4入核,阻断肌细胞增强因子2(muscle enhance factor 2, MEF2)/Runt相关转录因子2(runt-related transcription factor 2, Runx2)信号级联反应,从而抑制软骨细胞肥大以及骨形成过程[2];体内实验也证实了该信号通路在软骨细胞肥大中的重要作用,且PTHrP基因敲除鼠软骨细胞异常肥大和矿化,PTHR基因鼠表型与此相似[3]。另外,PTHrP/cAMP/PKA信号途径通过抑制Sik3激酶活性,使HDAC4从14-3-3结合位点释放并入核影响软骨细胞肥大;Sik3或HDAC4活性低时,Sik1/2和HDAC5可分别介导此过程[4]。
组蛋白去乙酰化酶(histone deacetylases,HDACs)是一类蛋白酶,能够通过改变染色体结构、抑制特定转录因子活性、影响基因表达修饰等方式对细胞的生长和分化过程进行调控。HDAC4属于经典的IIa型HDACs家族成员,是生长板软骨发育中重要的调控因子,具有核质穿梭的特殊能力,通过在磷酸化与去磷酸化状态之间的转换,控制自身的核质定位,从而激活或抑制靶向基因表达。生长板增殖区中,HDAC4定位于核内,软骨细胞具有较强的增殖能力;肥大区中HDAC4定位于胞质,软骨细胞呈肥大化状态且增殖能力弱,表明HDAC4核内外分布与生长板软骨细胞的增殖及肥大化调节密切相关[5]。软骨发育期间,HDAC4作为重要的调控因子参与软骨细胞生长、分化及矿化的整个生物学过程。HDAC4基因敲除鼠表现为软骨细胞异常肥大,软骨过早骨化,并在围产期死亡;增殖软骨细胞中HDAC4过表达抑制软骨细胞的肥大和分化[6],HDAC4基因的敲除或过表达最终都可通过生长板软骨细胞增殖分化状态的改变表现出来。HDAC4作为一个负调控因子,参与调控生长板软骨发育,在软骨发育相关疾病中具有重要作用。因此,对生长板发育中HDAC4作用的清楚认识也能为相关疾病的临床治疗提供新的思路。
HDAC4基因全敲除鼠体型矮小且在1周左右死亡[7],表明HDAC4基因与小鼠生长发育存在密切关系。目前对在不同发育阶段和不同部位敲除HDAC4基因的研究发现,软骨细胞中特异性敲除HDAC4的基因鼠表现为矮小且生长缓慢的特征,同时生长板缩短、二次骨化中心增大[8]。Nishimori等[3]报道软骨细胞内HDAC4条件性敲除鼠在14 d左右死亡,而在肥大软骨细胞、软骨膜及成骨细胞中具有特异性敲除HDAC4的基因小鼠表型正常且能存活到成年,表明HDAC4对生长板软骨细胞增殖分化的调控主要体现在早期阶段。同时,Nakatani等[9]构建了HDAC4的成骨细胞特异性敲除鼠,发现HDAC4能够影响骨发育过程中的合成代谢和分解代谢。因此,HDAC4对软骨和成骨生长发育都有影响,但其机制可能不同。HDAC4与其他IIa型HDACs(HDAC5、HDAC7和HDAC9)相似,受到PTHrP-Ihh等多种信号转导途径的紧密调控,从而将基因表达与环境变化联系起来。
Ihh是Hh家族成员之一,主要在前肥大软骨细胞中表达分泌,有抑制软骨细胞由前肥大状态向肥大状态转化的作用。作为Hh信号主要的直接下游靶向分子,在肥大软骨细胞和软骨-骨结节处检测到Ptc和Gli基因的表达。Hh配体的存在能够解除Ptc对七次跨膜蛋白Smo胞内信号活性的抑制,随后释放的Smo诱导Gli以活化形式入核激活Ihh下游靶向基因转录[10]。体内实验已经表明Ihh参与调控软骨细胞的增殖和分化;同时敲除Ihh基因的软骨细胞其细胞生长被显著抑制而凋亡水平增强[11],软骨细胞内Ihh基因的下调能够维持细胞表型,从而延缓人软骨终板细胞的退变[12],这一结果或许能为临床上预防和治疗骨关节炎提供新的策略。
Onodera等[13]通过分析两种与Hh信号相关的疾病,发现Hh信号活性与成骨细胞生成和矿化有关。利用Runx2和Ihh基因敲除鼠相互印证发现,Runx2与Ihh信号分子可共同介导成骨细胞的分化过程[14]。生物体内Ihh主要通过Runx2诱导成骨细胞分化,但不能排除存在其他细胞因子参与Ihh介导的成骨细胞生长进程。例如,Maeda等[15]利用转基因小鼠说明出生后软骨细胞来源的Ihh能够通过Wnt信号的激活参与成骨细胞的分化过程,具体机制还需更多的实验进行验证。
Ihh能够直接作用于关节周围软骨细胞,刺激其向柱状增殖软骨细胞的转变,从而以不依赖PTHrP的方式调节胎儿晚期生长板的长度[16]。PTHrP与Ihh主要还是通过互作的方式参与生长板软骨生长发育过程。Ihh刺激关节周围软骨细胞和软骨膜细胞中PTHrP的表达,防止软骨细胞过早肥大分化,同时也抑制Ihh本身的表达,PTHrP-Ihh反馈通路与软骨细胞的增殖分化共同维持生长板结构的正常发育。PTHrP与Ihh在反馈通路中发挥作用,一个信号分子的减少会诱导另一信号分子的补偿性增加,直至生长板软骨细胞增殖分化处于稳定状态。PTHrP和Ihh及其相关蛋白在胫骨生长板中表达部位的验证,也进一步强调PTHrP-Ihh信号通路在胫骨生长板纵向生长中的重要作用[17]。
研究表明,外源性PTHrP会刺激生长板软骨细胞增殖、抑制肥大分化,而Ihh信号刺激使软骨细胞肥大化[18]。他汀类药物(氟伐他汀)作用引起Ihh表达水平升高,促进软骨细胞增殖同时诱导PTHrP生成,进一步改变Ihh的分泌最终控制软骨内骨化的发生[19]。胞内胶原蛋白[20]的缺乏同样改变了PTHrP与Ihh之间的表达平衡,影响软骨细胞的分化。外源性物质和内源性细胞因子都能够作用于生物体内PTHrP-Ihh信号通路,影响生长板软骨细胞的增殖分化,间接说明该信号通路在生长板发育中的重要作用。然而目前并没有文献明确表示Ihh与HDAC4在介导软骨细胞肥大分化中存在直接的相互作用,但从以上研究中或许可以推测出HDAC4与Ihh能够以某种未知的方式调控生长板生长发育。Ihh与Runx2在成骨细胞分化中具有协调作用,Runx2作为Ihh的互作因子,也同样参与软骨细胞增殖分化。
Runx2作为软骨内骨形成过程中软骨细胞肥大分化所必需的转录因子,在前肥大和肥大软骨细胞中表达,参与软骨细胞成熟以及成骨细胞分化。Runx2可通过直接作用于Ihh参与软骨细胞的增殖活性和肥大,同时也参与PTHrP-Ihh负反馈信号通路[21]。另外,Vega等[6]已经证实HDAC4可直接结合并抑制Runx2的表达,调控软骨细胞肥大化。HDAC4由细胞核到胞质的亚细胞定位的改变可引起Runx2活性增强,并促使软骨细胞从增殖状态向前肥大状态转变[5],说明HDAC4可通过改变Runx2的活性影响软骨细胞的成熟,随后也可能作用于Ihh进而调控软骨细胞的增殖分化。
在成骨细胞中,HDAC4与Runx2形成复合物结合到基质金属蛋白酶13(matrix metalloproteinase, MMP13)启动子的runt域(runt domain,RD)结合位点,抑制MMP13转录;PTH处理能够激活核内PKA,从而使HDAC4磷酸化而与Runx2解离,随后Runx2招募组蛋白乙酰转移酶,MMP13重新起始转录[22]。MMP13参与软骨内骨化和骨重塑,在软骨胞外基质成分的降解中发挥重要作用[7],PTH对HDAC4与Runx2共同参与调控的MMP13表达的影响,体现在软骨胞外基质成分的改变上,使软骨细胞生存微环境发生变化,影响软骨细胞增殖分化等生命活动。另外,Runx家族另一成员Runx1也能够直接与Runx2启动子结合,影响其表达,进而调控软骨细胞和成骨细胞分化及终末成熟[23]。Runx2不仅是软骨细胞成熟和成骨细胞分化过程重要的转录因子,也参与骨代谢、牙齿发育、肿瘤和器官纤维化等疾病的发生发展[24]。MEF2C作为Runx2的上游因子,促进Runx2表达且在软骨细胞肥大过程中发挥重要作用。
MEF2属于转录因子的MADS家族,参与多种人类细胞的早期发育。骨发育期间,HDAC4与MEF2C的相互作用响应多种信号转导途径,并将信号从胞外环境传递到细胞核内。MEF2C能够激活Col10a1启动子,核内HDAC4又通过MEF2C抑制Col10a1的启动子活性,并且MEF2C杂合敲除小鼠出生后胸骨骨化严重缺乏[25],揭示了软骨细胞肥大和软骨内骨化依赖于MEF2C转录激活与HDAC4转录抑制之间的平衡,MEF2C在骨形成中具有重要作用。MEF2C是Runx2基因表达所必需的转录因子,MEF2C与c-FOS的结合能够参与PTH刺激的MMP13基因表达[22];另外,MEF2C诱导c-FOS表达影响破骨细胞形成,在炎症性骨关节炎中MEF2C缺乏可保护小鼠免受病理性骨侵蚀[26],以上实验说明,MEFC2可通过影响不同类型细胞参与骨骼发育。
软骨细胞增殖分化过程受到细胞内信号分子以及软骨细胞自身的复杂调控。胰岛素样生长因子1(insulin-like factor 1, IGF-1)信号正向调控软骨细胞增殖且与PTHrP-Ihh信号通路共同调节生长板发育。生长激素(growth hormone,GH)/IGF-1信号轴通过刺激生长板软骨细胞增殖和分化来介导骨生长,同时伴随着成骨细胞和破骨细胞的变化[27]。IGF-1和其他信号分子以及外部环境,如温度、营养因素等相互作用共同调节生长板发育[28]。作为TGF-β超家族的成员,转化生长因子β(transforming growth factor,TGF-β)在多种生物过程中发挥重要作用,TGF-β信号通过影响软骨细胞增殖、凋亡、胞外基质降解[29]以及肥大分化[30]等过程参与调控软骨细胞的生长和分化。已有文献报道,HDAC4对Runx2转录活性的作用参与TGF-β信号调控的成骨细胞增殖分化过程;而TGF-β也可通过其受体Smad2控制HDAC4蛋白表达或稳定,随后将HDAC4招募到Ihh启动子上的抑制复合物改变Ihh基因表达[31]。Runx2作为成骨细胞分化和骨形成中重要的转录因子,其活性可由ERK/MAPK依赖的磷酸化激活[32];而HDAC4与MEF2D借助SPRY4下调ERK/MAPK信号活性,引起肝细胞癌的耐药性[33];上述涉及转录因子和信号通路或许在软骨细胞增殖分化中也存在潜在联系,影响生长板发育。
软骨细胞分化被多个步骤调控,而其中涉及的一些信号通路也参与成骨细胞的分化。例如经典Wnt/β-catenin信号参与生长板软骨祖细胞调控[34],而Hh信号诱导Wnt配体表达驱动成骨细胞分化。HDAC4抑制IL-1β诱导软骨细胞胞外基质降解的作用,受到Wnt3a/β-catenin通路的部分调控[35],且胶原蛋白具有通过Ihh/PTHrP和Wnt/β-catenin促进小鼠骨折愈合的作用[36]。有趣的是,Sost的表达受SIK/HDAC/MEF2轴的控制,PTH通过SIK靶向PKA抑制骨细胞中Sost的表达,该模式与生长板中PTHrP靶向SIK3去抑制软骨细胞肥大过程相似[4]。此发现解释了骨骼中同一调控机制通过控制两种不同的信号通路来影响两种类型细胞的生长发育即生长板发育和成骨细胞稳态的过程。
生长板生长发育受到多条信号通路和细胞因子的调控,它们能够组成一个复杂的调控网络,共同维持正常的骨骼发育。如图1所示,随着对生长板生长发育相关调控机制研究的深入,PTHrP作为上游,调控HDAC4和Ihh通路在软骨细胞增殖和肥大分化中起重要作用。前肥大软骨细胞分泌的Ihh作用于PTHrP,使其与受体PTHR结合促进软骨细胞增殖,抑制肥大分化;PTHrP又以负反馈方式抑制Ihh表达,抑制增殖促进肥大化。另一方面,PTHrP信号能够促进HDAC4的核转运,增强HDAC4对软骨细胞肥大的抑制作用,但HDAC4与Ihh之间的相互作用仍然未知。HDAC4作为表观遗传调控的重要因子,参与多条信号途径并通过核内外易位发挥重要作用。PTHrP及其受体的基因缺失,在小鼠模型上表现为短肢畸形,而HDAC4和Ihh在肥大分化中的调节作用虽然相反,但HDAC4基因敲除小鼠和Ihh基因敲除小鼠均呈现生长板发育紊乱,亦均呈现短指畸形表现。对生长板调控机制的研究可为临床上治疗矮小症、侏儒症等软骨发育相关疾病提供新思路和干预新靶点。
所有作者均声明不存在利益冲突



























