
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
心脏移植是治疗一些复杂先天性心脏病终末期的有效方法之一。目前,矫正型大动脉转位行全腔静脉肺动脉连接术(TCPC)后再施行心脏移植的病例国内尚未见报道。2017年8月我院为1例矫正型大动脉转位行TCPC术后12年的患者施行原位心脏移植,现报道如下。
患者为男性,15岁,身高152 cm,体重40 kg。2005年患者被诊断为矫正型大动脉转位,室间隔缺损,房间隔缺损,肺动脉狭窄,在外院行TCPC(心房内隧道方法)手术,术后恢复良好。2014年(TCPC术后第9年)起患者出现胸闷、心悸及腹胀、全身浮肿,长期服用利尿及扩肺血管药物,症状仍反复并逐渐加重,内科治疗效果不佳。2017年(TCPC术后第12年)入住我院。查体:重度营养不良,颈静脉怒张,巩膜黄染,双下肺叩诊浊音,肝肋下4指,蛙状腹,移动性浊音阳性,双下肢浮肿。生化显示:总胆红素73.2 mmol/L,结合胆红素36.7 mmol/L,非结合胆红素36.5 mmol/L,丙氨酸转氨酶(ALT)1120 U/L,天冬氨酸转氨酶(AST)981 U/L,白蛋白18 g/L,球蛋白17.1 g/L。超声波心动图提示:心房及内脏正位,心室反位;主动脉从解剖右心室相连,右位主动脉弓;无肺动脉主干;上腔静脉与右肺动脉相连,下腔静脉通过右心内隧道与右肺动脉相连,吻合口通畅,正向血流;室间隔缺损;房间隔缺损;双侧胸腔积液。腹部超声波提示:下腔静脉扩张,肝、脾明显扩大,腹腔积液。心电图示:频发房性早搏,右心室肥大。胸部X线片示:心胸比率0.49。群体反应性抗体(PRA)阴性。诊断为矫正型大动脉转位,室间隔缺损,房间隔缺损,肺动脉狭窄,TCPC术后;房性早搏;蛋白丢失性肠病;胸腔积液,腹腔积液;淤血肝;肝功能不全,心力衰竭(NYHA)分级IV级。伦理委员会讨论认为患者有心脏移植指征。
术前适当利尿,积极补充白蛋白,使白蛋白维持在32 g/L以上。术前2 h采用巴利昔单抗10 mg静脉注射,术中应用甲泼尼龙1 200 mg。供者为脑死亡者(女性,体重50 kg),切取心脏时尽量长的保留上、下腔静脉和肺动脉,灌注冷组氨酸-色氨酸-酮戊=酸盐液(HTK液)1 000 ml,缺血时间180 min。受者沿原正中手术路径入胸,仔细分离粘连,游离出上、下腔静脉,升主动脉及左、右肺动脉。双腔法行原位心脏移植:先完成左心房吻合,再完成下腔静脉吻合;肺动脉横行切开肺动脉至两边上、下肺动脉开口处,牛心包片加宽肺动脉,于心包片上切开足够大开口,取20号Gortex人造血管连接至供者肺动脉;再取人造血管连接供、受者的主动脉;最后连接上腔静脉。
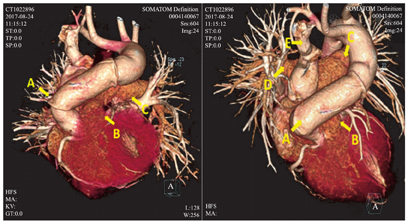
主动脉阻断时间55 min,体外循环总时间260 min。并行循环时供心收缩无力,采用体外膜肺氧合(ECMO)辅助后顺利停体外循环。术后的前24 h内不抗凝,监测D-二聚体及活化部分凝血活酶时间(APTT),无明显胸液后再开始应用小剂量肝素,APTT维持在50~60 s左右;术后第3天后复查心彩超供心收缩功能恢复,撤除ECMO;第4天拔除气管插管,并使用第2剂巴利昔单抗;第7天转出重症监护病房(ICU);第8天开始应用环孢素A、吗替麦考酚酯及泼尼松;第20天恢复良好后出院。出院时查环孢素A浓度谷值130.5 ng/mL,峰浓度1 153.2 ng/mL,肝功能恢复正常;心脏彩色超声波示,心脏收缩及舒张功能正常,新建肺动脉通畅,吻合口无狭窄;心脏CT示肺动脉走行顺畅,吻合口无狭窄(图1)。出院后3个月随访,NYHA分级I级;环孢素A浓度谷值188.4 ng/ml,峰浓度1 022.5 ng/ml;肝功能正常;心脏彩色超声波示,心脏收缩及舒张功能正常,肺动脉通畅,吻合口无狭窄。

TCPC常用于治疗复杂的先天性心脏病患者[1]。但其远期可出现蛋白丢失性肠病、纤维性支气管炎、血栓形成、心律失常及Fontan功能丧失等,严重影响了患者的生活质量和远期生存率[2,3,4]。心脏移植是根治TCPC远期并发症的一个重要治疗方法[2,3,4,5,6,7]。但由于行TCPC的患者常伴有心内结构位置的异常,如右位心、大动脉转位等,大大增加了心脏移植的难度;且需要行心脏移植的TCPC患者常常伴有静脉淤血、肝功能损害、低蛋白血症,营养状况差,术后恢复困难。
通过对这例心脏移植病例的诊治,我们得到以下经验。
患者术前有严重低蛋白、营养不良,予积极补充白蛋白及球蛋白,适当利尿,为手术做好充分准备。
本例受者为未成年儿童,营养不良,心腔较小,且大血管走行异常,因此供心的选择宜小不宜大;同时摘取供心时应尽量保留足够长的腔静脉和大动脉,以备吻合时血管改道的需要。
肺动脉的连接是心脏移植中最重要的步骤。左、右肺动脉必须充分游离以减少吻合口张力;人造血管型号的选择要与肺动脉匹配;用人造血管连接供、受者肺动脉时要非常重视血管的走行,不能扭曲;重建的升主动脉应在肺动脉前方,且要适当留长,避免压迫重建后的肺动脉。
因患者术前淤血肝,术后应用ECMO等侵入性操作,免疫抑制剂不宜太早使用。我们在术后第4天使用第2剂巴利昔单抗后第8天才开始应用免疫抑制剂。同时环孢素A药物浓度不宜太高,并应密切监测血药浓度及肝功能。
有部分心脏移植术后需要ECMO的辅助。肝功能不全的患者由于凝血功能受损,使用ECMO需要更加重视对抗凝的把握。该例患者应用ECMO抗凝时有以下顾虑:(1)患者术前肝功能不全,凝血功能受损;(2)二次手术,创面较大;(3)在凝血功能受抑制时应用人造Gortex管道易出现吻合口渗血。因此,我们在术后早期并不使用肝素抗凝,但严密监测D-二聚体和APTT;当无明显出血时再适量应用肝素,维持适当升高的APTT;心功能恢复后尽早脱离ECMO,避免相关并发症发生。


























