
评估体外膜肺氧合(ECMO)技术对特发性肺纤维化(Idiopathic pulmonary fibrosis,IPF)患者单肺移植术中情况及预后的影响。
回顾性分析IPF单肺移植手术共55例,男性49例,女性6例,年龄18~75岁,美国麻醉医师协会(ASA)为Ⅲ或Ⅳ级。根据是否应用ECMO分成2组,ECMO组41例患者术中应用ECMO,未用ECMO组14例患者术中未用ECMO。记录手术时间及移植肺缺血时间;术中输入晶体、胶体、红细胞、白蛋白量、术中失血量及尿量;ECMO使用时间、术后带气管插管时间、重症监护室(ICU)停留时间、住院时间及患者住院期间预后。
ECMO组术中输入血浆量大于未用ECMO组( P<0.01 ),其他术中及术后2组的指标比较,差异均无统计学意义。ECMO组中,ECMO使用时间与术后带气管插管时间、ICU停留时间、住院期间死亡率呈正相关关系(P<0.01)。
ECMO不影响患者的术中情况和预后,ECMO使用时间对判断患者的预后情况有一定预测价值。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
肺移植是治疗终末期肺疾病的有效方法,随着肺移植手术技术的不断完善及体外膜肺氧合(ECMO)技术的进步,肺移植手术的成功率和生存时间都明显提高[1]。ECMO作为肺移植围手术期呼吸和循环系统的支持手段,能有效改善机体的氧合状态,提高肺移植成功率[2]。也有研究提出,肺移植患者使用ECMO可能导致死亡率升高、术中出血量增加等并发症[1,2,3]。本研究拟通过对ECMO在特发性肺纤维化(Idiopathic pulmonary fibrosis,IPF)单肺移植术中的应用情况及患者预后的进行回顾性分析,为临床的应用提供参考。
本研究获医院伦理委员会批准,患者及家属签署知情同意书(2018-91-K65号)。选择无锡市人民医院2015年4月1日至2016年12月30日期间完成的单肺移植手术,性别不限,年龄18~80岁。受者的原发疾病均为IPF。所有患者分成2组,ECMO组患者术中应用ECMO,另一组患者术中未用ECMO。排除标准:手术前已经应用ECMO等待供者;肺移植术后由于各种原因行二次肺移植手术及术后随访数据采集不完整。
患者入室后常规监测无创血压、心电图、指尖氧饱和度和BIS。行桡动脉穿刺置管,监测有创动脉压力及术中血气。麻醉诱导方法:咪唑安定0.02~0.04 mg/k、舒芬太尼0.4 μg/kg、依托咪酯0.2~0.4 mg/kg。顺苯磺酸阿曲库胺0.2~0.4 mg/kg辅助肌肉松弛行气管插管(所有患者均选用左双腔支气管插管)。插管后连接麻醉机行机械通气。通气方式均采用压力控制,吸气压力为18~35 cmH2O(1 cmH2O=0.098 kPa),呼吸频率为12~20次/分,根据血气分析及生命体征调节通气参数。诱导完成后经颈内静脉置入Swan-Ganz漂浮导管,监测肺动脉压力。麻醉维持以丙泊酚0.03~0.05 mg·kg-1·min-1静脉持续泵注、顺苯磺酸阿曲库胺4~6 μg·kg-1·min-1静脉持续泵注,间断静注舒芬太尼。移植肺开放后,下调机械通气参数:吸气压力为18~25 cmH2O,呼吸频率为8~12次/分,PEEP 6~8 cmH2O,吸入氧浓度降至40%以下,以尽量减少肺实质损伤。
患者完成麻醉后,非术侧予以单肺通气,根据患者氧合情况、肺动脉压力及心功能等情况判断是否需要在ECMO以辅助下完成单侧肺移植。使用ECMO指征[4]:(1)患者给予非术侧肺适宜的通气参数单肺通气15 min后,行血气分析,PaO2<60 mmHg(1 mmHg=0.133 kPa)。(2)患者置入漂浮导管后监测肺动脉压力,肺动脉收缩压>50 mmHg。(3)心功能NYHA分级IV级。满足上述任意一个条件即选择ECMO转流辅助。
如果需要ECMO支持ECMO均采用VA-ECMO,即经右侧股动、静脉切开置动静脉插管,根据股动、静脉粗细,动脉选用15-17F管道,插管置髂总动脉水平;静脉选用19-21F管道,插管至下腔静脉水平。采用Medtronic Inc公司或Maquet公司提供的Bio-Medicus BP-80离心泵和氧合器套包。股动静脉插管均为Medtronic Inc公司提供的肝素涂层动静脉插管。预充液由复方乳酸钠、新鲜血浆或代血浆、5%碳酸氢钠及肝素组成。肝素首量[5]为0.5~1 mg/kg,追加量根据激活凝血时间(ACT)调整。ECMO转流期间维持ACT在160~200 s之间。血流量控制在1.8~2.5 L·m-2·min-1。转流期间维持右侧桡动脉PaO2≥75 mmHg。术中连续监测受者右上肢和下肢的氧饱和度。
手术结束后,将ECMO流量降至1 L·min-1·m-2以下,如果血流动力学平稳,氧合指数>300,即可撤除ECMO。若血流动力学不平稳,氧合指数<300,则维持使用ECMO,带入重症监护室(ICU)。在ICU期间血流动力学稳定、氧合功能良好的情况下降低ECMO流量,当流量降到1 L·min-1·m-2以下时,可撤除ECMO。停止ECMO后,当PEEP<8 cmH2O、气道峰压<25 cmH2O、通气频率12次/分、吸入氧浓度40%、氧合指数>300时,可停止机械通气,拔除气管导管。
记录患者基本数据:性别,年龄,身高,体重。手术和麻醉信息:手术时间及移植肺缺血时间,术中输入晶体、胶体、红细胞、白蛋白量、术中失血量及尿量。ECMO使用时间、术后带气管插管时间、ICU停留时间、住院时间及患者住院期间预后。
统计分析采用SPSS(20版) (IBM, Armonk, NY)进行统计学处理。所有计量资料(如年龄、身体质量(Body Mass Index, BMI)指数、手术时间、术中失血量、术中尿量、术中输血量、术中入液量、ECMO使用时间、术后带气管插管时间、ICU停留时间、住院时间等)采用平均值±标准差表示,计数资料(如性别、死亡率等)采用百分比表示。通过卡方检验、t检验验证ECMO组和未用ECMO组变量是否有统计学差异。通过Pearson相关分析ECMO使用时间与气管插管时间、ICU停留时间、住院时间及住院期间死亡率的相关性。
本研究共纳入55例患者,其中ECMO组有41例患者,未用ECMO组有14例患者。2组患者性别、年龄、BMI及术前肺动脉压力比较,差异无统计学意义(表1)。
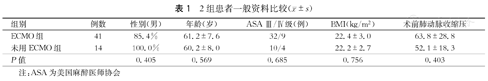
2组患者一般资料比较( ±s)
±s)
2组患者一般资料比较( ±s)
±s)
| 组别 | 例数 | 性别(男) | 年龄(岁) | ASA Ⅲ/Ⅳ级(例) | BMI(kg/m2) | 术前肺动脉收缩压 |
|---|---|---|---|---|---|---|
| ECMO组 | 41 | 85.4% | 61.2±7.6 | 32/9 | 22.4±3.0 | 63.8±28.8 |
| 未用ECMO组 | 14 | 100.0% | 60.2±8.0 | 10/4 | 22.2±2.7 | 52.1±18.3 |
| P值 | 0.405 | 0.569 | 0.685 | 0.756 | 0.403 |
注:ASA为美国麻醉医师协会
手术时间及移植肺缺血时间比较,差异无统计学意义;术中输入的晶体、胶体、红细胞、白蛋白量比较,差异无统计学意义;术中失血量及尿量比较,差异无统计学意义。术后带气管插管时间、ICU停留时间、住院时间及住院期间死亡率比较,差异均无统计学意义。术中输入血浆量ECMO组(9.3±4.5) ml/kg大于未用ECMO组(5.4±4.2) ml/kg (P<0.01,表2)。
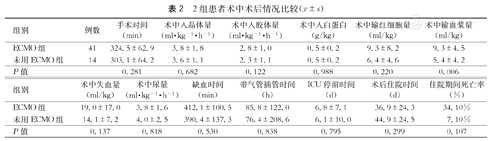
2组患者术中术后情况比较( ±s)
±s)
2组患者术中术后情况比较( ±s)
±s)
| 组别 | 例数 | 手术时间(min) | 术中入晶体量(ml·kg-1·h-1) | 术中入胶体量(ml·kg-1·h-1) | 术中入白蛋白(g/kg) | 术中输红细胞量(ml/kg) | 术中输血浆量(ml/kg) |
|---|---|---|---|---|---|---|---|
| ECMO组 | 41 | 324.5±62.9 | 3.8±1.8 | 2.8±1.0 | 0.5±0.2 | 9.3±8.2 | 9.3±4.5 |
| 未用ECMO组 | 14 | 303.1±64.2 | 3.6±1.1 | 2.3±1.1 | 0.5±0.2 | 6.4±4.6 | 5.4±4.2 |
| P值 | 0.281 | 0.682 | 0.122 | 0.988 | 0.220 | 0.006 |
| 组别 | 术中失血量(ml/kg) | 术中尿量(ml·kg-1·h-1) | 缺血时间(min) | 带气管插管时间(h) | ICU停留时间(d) | 术后住院时间(d) | 住院期间死亡率(%) |
|---|---|---|---|---|---|---|---|
| ECMO组 | 19.0±17.0 | 3.8±1.6 | 412.1±100.5 | 85.8±122.0 | 6.8±7.1 | 36.9±24.3 | 34.10% |
| 未用ECMO组 | 14.1±7.2 | 4.0±2.5 | 390.4±137.3 | 76.4±208.6 | 6.1±10.0 | 44.9±24.5 | 7.10% |
| P值 | 0.137 | 0.818 | 0.530 | 0.838 | 0.795 | 0.299 | 0.107 |
ECMO使用时间与术后带气管插管时间、ICU停留时间、住院期间死亡率呈正相关关系(P<0.01),ECMO使用时间与术后住院时间无相关关系(图1)。
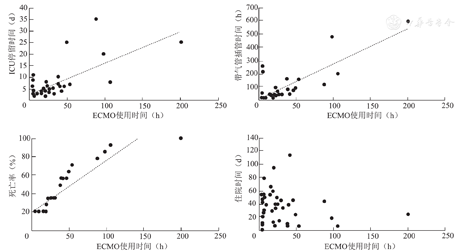

IPF是一种特殊类型的慢性致纤维化间质性肺炎,主要发生于老年,表现为进行性加重的呼吸困难和肺功能恶化。对中国患者的流行病调查提示,约有23.5%的IPF患者合并肺动脉高压,如果患者合并肺动脉高压,则预后较差[6]。目前终末期IPF患者的中位生存时间为38个月。对终末期IPF患者而言,除了常规的内科治疗手段,肺移植是有效的治疗手段[7]。
肺移植术中需要有效的呼吸循环支持,由于患者肺功能多数情况下肺功能较差,需要评估术中患者能否耐受单肺通气。ECMO可以有效改善手术中氧合情况,如果患者无法支持单肺通气,则肺移植术中需要ECMO辅助通气。部分IPF患者同时合并肺动脉高压,手术风险较大,术中应用ECMO可以分流心输出量,降低肺动脉灌注压力,减轻心脏负荷,减少对血管内皮细胞的机械压力和损伤[8,9]。本研究41例ECMO辅助患者均采用静脉—动脉通路(V-A通路)模式,V-A通路除了满足一定程度氧合功能,还可以分流回心血量,显著降低肺动脉压力[5]。术中我们通过调整ECMO转速和流量,保证术中氧合,降低PaCO2、肺动脉压及右心房压力,其对术中受者心功能辅助的效果明显。
肺移植手术本身创面较大,使用ECMO过程中应用肝素抗凝会影响患者的凝血功能,Cottini等研究显示,ECMO会增加出血量[10]。但是本研究提示ECMO并不会增加术中出血量。主要原因可能是单肺手术创伤较小,并且手术中控制肝素用量,保证ACT<200 s。统计分析显示,ECMO组血浆用量明显高于C组(P<0.01)。由于血浆中含有大量凝血因子,可以有效增强凝血功能,这也是ECMO组失血量并无明显增加的原因之一。
ECMO置入操作本身会占用一定时间,但是在实际应用中,ECMO置管多在麻醉诱导插管后,此时正在进行中心静脉穿刺和漂浮导管置入等操作。而本研究中,VA-ECMO均选择股动静脉穿刺,可与中心静脉穿刺同时进行。所以本研究提示,置入ECMO操作并不会增加整体手术时间。
分析显示,ECMO组术后死亡率(34.1%)高于未用ECMO组(7.1%),但差异并无统计学意义,表示使用ECMO并不会增加患者的死亡率。Hayanga等的研究提示,使用ECMO会增加术后短期死亡率[11]。Fabio等的研究提示,虽然使用ECMO患者住院期间并发症的发生率增加,但是死亡率与未使用ECMO患者相同[12]。但是我们发现,随着ECMO使用时间延长,术后带气管插管时间、ICU停留时间延长,住院期间死亡率提高。ECMO使用时间超过48小时的患者有6例,死亡率为100%。而ECMO使用时间在12 h以内的患者有15例,死亡率为20%。说明ECMO使用时间越短,对患者影响越小。所以手术结束后,应尽早撤除ECMO。随着ECMO使用时间的延长,出现并发症的风险也随之增加[13],主要并发症为急性肾损伤(35.5%~74.0%)[14]。其次,由于长期应用肝素及凝血因子逐渐消耗,出血风险随之增大(26.8%~56.1%)[3],以颅内出血最为严重[8]。随着长时间卧床及全身携带的各种管路,严重感染发生率也随之增加(19.5%~44.0%)[15]。如果ECMO使用时间较长,也说明患者本身基本情况较差,无法脱离ECMO满足氧合或循环的要求。本研究ECMO使用时间超过48 h的6例患者中,4例患者是由于心功能较差无法脱机,2例患者由于术后出现原发性移植物失功无法脱机。这些患者的预后都比较差。所以根据ECMO使用时间的长短,可以有助于判断患者预后情况。
本研究中使用ECMO患者平均住院时间(36.9±24.3) d小于未用ECMO组患者(44.9±24.5) d。主要原因是死亡患者平均住院时间(16.0±12.6) d较短。如果排除死亡患者,ECMO组平均住院时间为(47.4±21.8) d,未用ECMO组平均住院时间为(47.6±23.3) d,几乎不存在差异。
综上所述,ECMO作为一种成熟的心肺辅助装置,可以在肺移植围手术期发挥巨大的作用,有效帮助患者手术进行及术后恢复。手术期间使用ECMO并不会影响患者术中情况及预后,ECMO使用时间对判断患者的预后情况有一定预测价值。



























