
研究器官捐献肾移植中,单克隆和多克隆抗体免疫诱导方案的效果及安全性。
回顾性分析解放军总医院第三医学中心2016年1月至12月31日的104例肾移植受者资料,比较以巴利昔单克隆抗体和抗胸腺细胞免疫球蛋白多克隆抗体(thymoglobulin,ATG)诱导的两组供、受者基本资料、术后肌酐、主要并发症、移植物及受者存活率。
44例受者采用巴利昔单抗诱导,60例受者采用ATG诱导。术前资料对比,两组在供者年龄、原发病、术前肌酐,及受者年龄、原发病比例等方面差异均无统计学意义,而ATG组男性比例(87%)和体重(70±13)kg较巴利昔组的比例(55%)和体重(64±12)kg高。手术后的存活率及并发症对比,巴利昔组急性排斥反应发生率为9%,术后1、3、6个月平均肌酐分别为112.4、127.0、107.8 μmol/L,总的感染发生率16%,移植物及受者6个月存活率为95%(42/44)和98%(43/44)。ATG组急性排斥反应发生率为3%,术后1、3、6个月平均肌酐分别为135.6、119.0、118.0 μmol/L,总的感染发生率22%,移植物和受者6个月存活率均为100%(60/60)。
以单克隆抗体和多克隆抗体为主的诱导方案,在肾移植术后早期均能良好地预防急性排斥反应,在感染、移植物功能以及移植物和受者早期存活率等方面未能证明两组差异有统计学意义,术后近期预后均良好。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
免疫诱导是预防肾移植术后排斥反应的重要方法,目前最常用的免疫诱导药物有单克隆抗体巴利昔单抗和多克隆抗体抗胸腺免疫球蛋白(thymoglobulin,ATG)两类,两者各有优势和适用范围。国内外有很多相关研究,但仍缺乏两者间的大样本、长期随访的随机对照试验。目前,在我国器官捐献肾移植数量迅速增长的新形势下,肾移植排斥、感染等风险因素均发生变化,以往关于免疫诱导研究的结果未必适用于新的供肾来源。本文总结了一组在器官捐献肾移植受者中,使用巴利昔单抗和抗胸腺细胞免疫球蛋白多克隆抗体(ATG)用于免疫诱导的相关经验。
在2016年1月1日至2016年12月30日我院同一治疗组完成的肾移植受者中,对比研究使用巴利昔单抗与ATG进行免疫诱导后,观察受者和移植物的预后、并发症情况。
入选标准:(1)选取一个自然年中,连续完成的全部器官捐献肾移植受者;(2)接受巴利昔或ATG诱导治疗;(3)年龄>6周岁。排除标准:同时或先后接受肝脏、胰腺等其他器官的联合器官移植。
急性排斥反应诊断标准:(1)移植肾脏穿刺活检证实的急性细胞性、体液性排斥反应IA级及以上;(2)或者临床出现肌酐明显升高>基础值30%以上,排除钙调磷酸酶抑制剂(CNI)药物浓度过高、移植肾血流异常、病毒感染、容量不足等其他因素,并经激素或抗体冲激治疗后明显好转,临床诊断明确。
(1)巴利昔单抗诱导方案:巴利昔单抗术中、术后第4天各20 mg。甲泼尼龙术中1 000 mg,术后第1~3天每天500 mg,术后第4、5天每天250 mg。(2)ATG诱导方案:ATG术中及术后每天50~75 mg,至总量4 mg/kg。甲泼尼龙术中500 mg,术后在ATG使用期间每天40~120 mg。(3)维持免疫抑制方案:他克莫司+霉酚酸酯+口服激素三联方案。对于他克莫司使用后糖尿病血糖不易控制、不能耐受或者浓度不理想的,改为环孢素A治疗。泼尼松片在静脉甲泼尼龙使用结束后第2天开始,每天30 mg口服,每5~7d减量5 mg,至10 mg/d口服长期维持。霉酚酸(酯)类药物,常规术后为吗替麦考酚酯每天1 500 mg,或麦考酚钠肠溶片每天1 080 mg。
预防感染采用三代头孢类抗生素+(缬)更昔洛韦+磺胺+棘白菌素类抗真菌联合方案。术后常规使用头孢曲松钠2 g/d、更昔洛韦0.25 g静脉滴注2次/d、米卡芬净100 mg 1次/d或卡泊芬净50 mg 1次/d静脉滴注预防感染1~2周,序贯以更昔洛韦0.5g 3次/d或缬更昔洛韦450 mg或900 mg 1次/d、复方磺胺甲恶唑0.48 g 1次/d口服预防感染。
采用SAS 9.3统计学软件,对计数资料进行卡方检验或Fisher检验,对计量资料进行t检验或秩和检验;采用混合线性模型(mixed),对他克莫司浓度、肌酐数据进行重复测量的方差分析,并进行同一药物组的多个时间点间的两两比较,以及同一时间点间的两个药物组间的比较。P<0.05为差异有统计学意义。
统计分析两个治疗组的性别、年龄、体重、原发病、透析情况(表1)。结果表明,巴利昔组受者男性比例55%,小于ATG组的87%。相应的,巴利昔组体重64 kg,小于ATG组的70 kg。其余构成比例差异无统计学意义。
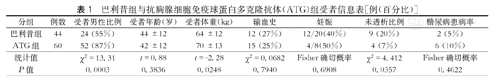
巴利昔组与抗胸腺细胞免疫球蛋白多克隆抗体(ATG)组受者信息表[例(百分比)]
巴利昔组与抗胸腺细胞免疫球蛋白多克隆抗体(ATG)组受者信息表[例(百分比)]
| 分组 | 例数 | 受者男性比例 | 受者年龄(岁) | 受者体重(kg) | 输血史 | 妊娠 | 未透析比例 | 糖尿病患病率 |
|---|---|---|---|---|---|---|---|---|
| 巴利昔组 | 44 | 24 (55%) | 44 ±12 | 64 ±12 | 12 (27%) | 12/20(40%) | 9 (20%) | 2 (5%) |
| ATG组 | 60 | 52 (87%) | 42 ±12 | 70 ±13 | 15 (25%) | 4/8(50%) | 4 (7%) | 6 (10%) |
| 统计值 | χ2=13.31 | t=0.88 | t=-2.28 | χ2=0.0682 | Fisher确切概率 | χ2=4.412 | Fisher确切概率 | |
| P值 | 0.0003 | 0.3836 | 0.0248 | 0.7940 | 0.6908 | 0.0357 | 0.4622 |
巴利昔组和ATG组的供者年龄分别(44±14)岁和(44 ±12)岁,差异无统计学意义(t=-0.21,P=0.8344)。两组的末次肌酐的中位数(四分位数)值分别为76(51)μmol/L和67(50)μmol/L,差异均无统计学意义(Wilcoxon秩和检验Z=1.0910,P=0.2753)。供者的原发病差异无统计学意义(Fisher确切概率,P=0.4720,表2)。两组分别有1例术前PRA阳性受者,但PRA均未超过20%。
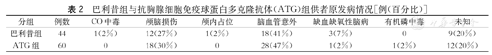
巴利昔组与抗胸腺细胞免疫球蛋白多克隆抗体(ATG)组供者原发病情况[例(百分比)]
巴利昔组与抗胸腺细胞免疫球蛋白多克隆抗体(ATG)组供者原发病情况[例(百分比)]
| 分组 | 例数 | CO中毒 | 颅脑损伤 | 颅内占位 | 脑血管意外 | 缺血缺氧性脑病 | 有机磷中毒 | 未知 |
|---|---|---|---|---|---|---|---|---|
| 巴利昔组 | 44 | 1(2%) | 12(27%) | 1(2%) | 18(41%) | 3(7%) | 0 | 9(20%) |
| ATG组 | 60 | 0 | 18(30%) | 0 | 28(47%) | 1(2%) | 1(2%) | 12(20%) |
两组受者在使用巴利昔单抗与ATG诱导的方案中,使用不同剂量的甲泼尼龙作为辅助诱导治疗。静脉滴注甲泼尼龙实际使用量巴利昔组为(2.96±0.36)g,ATG组为(1.40±0.37)g。两组的长期口服激素维持剂量均为10 mg/d。
在维持阶段,采用以他克莫司为主的三联免疫方案。在术后不同时间点(1~4周,2个月,3个月及6个月时)他克莫司谷浓度的变化情况见表3。
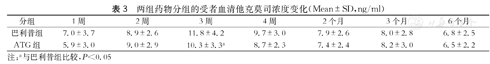
两组药物分组的受者血清他克莫司浓度变化(Mean±SD,ng/ml)
两组药物分组的受者血清他克莫司浓度变化(Mean±SD,ng/ml)
| 分组 | 1周 | 2周 | 3周 | 4周 | 2个月 | 3个月 | 6个月 |
|---|---|---|---|---|---|---|---|
| 巴利昔组 | 7.0±3.7 | 8.9±2.6 | 11.8±4.2 | 9.7±3.0 | 7.9±2.6 | 8.0±2.8 | 6.8±2.5 |
| ATG组 | 5.9±3.0 | 9.0±2.9 | 10.3±3.3a | 8.7±2.3 | 7.4±2.4 | 8.2±3.0 | 6.5±2.2 |
注:a与巴利昔组比较,P<0.05
6个月移植物生存率巴利昔组为95%(42/44),ATG组为100%(60/60),差异无统计学意义(P=0.18)。6个月受者存活率巴利昔组为98%(43/44),ATG组为100%(60/60),差异无统计学意义(P=0.42)。
巴利昔组和ATG组术后1个月肌酐分别为(112±66)μmol/L和(136±58)μmol/L,差异有统计学意义,但在术后3个月、6个月分别为(127±63)μmol/L、(108±50)μmol/L和(119±41)μmol/L、(118±56)μmol/L,差异无统计学意义。
两组术后6个月内活检证实的急性排斥反应发生率在巴利昔组为9%(4/44),ATG组为3%(2/60),差异无统计学意义(Fisher确切概率,P=0.2389)。巴利昔组与ATG组的术后肾功能恢复延迟(DGF)发生率分别为2%(1/44)与5%(3/60),差异无统计学意义(Fisher确切概率,P=0.6358)。两组术后总感染及重症感染发生率差异均无统计学意义(表4)。
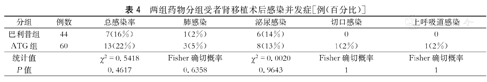
两组药物分组受者肾移植术后感染并发症[例(百分比)]
两组药物分组受者肾移植术后感染并发症[例(百分比)]
| 分组 | 例数 | 总感染率 | 肺感染 | 泌尿感染 | 切口感染 | 上呼吸道感染 |
|---|---|---|---|---|---|---|
| 巴利昔组 | 44 | 7(16%) | 1(2%) | 6(14%) | 0 | 0 |
| ATG组 | 60 | 13(22%) | 3(5%) | 8(13%) | 1(2%) | 1(2%) |
| 统计值 | χ2=0.5418 | Fisher确切概率 | χ2=0.0020 | Fisher确切概率 | Fisher确切概率 | |
| P值 | 0.4617 | 0.6358 | 0.9643 | 1 | 1 |
本研究结果表明,在当前国内新的器官捐献肾移植条件下,巴利昔单抗与ATG诱导预防肾移植术后急性排斥反应发生率为9%和3%,感染发生率分别为16%和22%,巴利昔组的排斥反应发生率较高,感染发生率较低,趋势与以往研究相符,但差异均无统计学意义。本组病例急性排斥反应发生率较多数中心略偏低,原因可能为:(1)诱导治疗用量较大。本研究巴利昔方案中,单抗2次共40 mg,配合甲泼尼龙3g,ATG方案中,ATG 4 mg/kg,并且配合甲泼尼龙1.4g,经过交流及阅读文献,较国内多数中心剂量更大。(2)统计时间较短,本研究随访时间为6个月,因此应较一般的1年急性排斥反应发生率更低。(3)本组病例很少有群体反应性抗HLA-IgG抗体(PRA)阳性患者,排斥反应高危的受者很少。以上这些原因都可能使急性排斥反应发生率偏低。
自巴利昔单抗与ATG诱导问世以来,两者在降低早期急性排斥反应方面均获得肯定的效果。而关于两者疗效和安全性的比较性研究也层出不穷。(1)对移植物和受者存活率的影响。一项针对以往文献的研究,对截至2014年11月18日的PubMed、EMbase、Cochrane数据库和Web of Science数据库等多个大型数据库中的89个随机对照临床试验进行分析,关于诱导治疗,巴利昔单抗与ATG没有显示出其中一种方法较另一种在降低移植物丢失率或受者死亡率方面更有效[1]。另一项利用大型移植登记数据库分析,将OPTN数据与Medicare数据库连接,1:1配对比较9 378对受者,分别用巴利昔单抗与ATG肾移植诱导,与ATG受者相比,巴利昔受者死亡率更高(风险比HR=1.08,95% CI为1.01~1.16,P=0.03),淋巴瘤风险更高(风险比HR=1.12,95% CI为1.01~1.23,P=0.03),但在亚组分析中这些区别均未经证实[2]。本研究中,也未能观察到两种诱导方法在术后早期移植物和受者存活率方面的差别。(2)对于排斥反应的预防效果,总体而言,ATG显示出一定的优势。研究显示,ATG较巴利昔单抗在黑人肾移植受者中早期急性排斥反应的发生率降低。对于抗体介导的排斥反应[3]。Brokhof等[4]的回顾性研究表明,在术前供体特异性抗体(DSA)阳性而淋巴试验毒阴性的轻度致敏患者中,ATG术后新生DSA和慢性排斥反应发生率均较巴利昔组低。但在另一项前瞻性随机对照研究中,未能证实致敏受者中ATG的优势[3]。(3)对于DGF的影响。国内林凯临等[5]发现,采用ATG诱导病例术后的DGF发生率较低。这一结果也与国外研究吻合。但在本研究中,未能观察到两者DGF发生率的差异有统计学意义。(4)对术后感染的影响。尽管ATG作为淋巴细胞清除性抗体,理论上免疫抑制强度高于单克隆抗体,但这种作用和剂量是明显相关的。国外研究表明,较低剂量的ATG(总量<7.5 mg/kg),术后感染发生率并不升高[6]。由于人种差异,在国内一般认为,这一"安全"剂量低于国外。本研究中采用4 mg/kg,感染总发生率略高于巴利昔单抗组,但差异无统计学意义,这一结论也与林凯临等[5]的研究吻合。
根据以往研究结果,改善全球肾脏病预后组织(KDIGO)指南当中总结了两种诱导药物的用法[7],但这些研究也有局限性,因为包含很多早期数据,而这些研究很多伴随药物都是基于环孢素A和硫唑嘌呤为主,与现今的临床实践并不相同。迄今两者的疗效优劣仍未能达成统一结论,甚至引起了颇为激烈的讨论[8,9]。而由于肾移植供、受者的人种等诸多差异,国外的药物治疗经验未必能够完全适用于中国。以往国内曾有相关研究报道[5],但仍缺乏在器官捐献时代的随机对照的前瞻性临床试验数据。
本研究两组病例在性别、体重方面存在差别,其中体重差别可能与性别比例不均衡有关,两组诱导治疗的受者之间可能存在一定的选择偏倚的风险。但以往研究未能证实受者性别、体重对排斥反应、感染的发生率有显著影响[10]。仅有部分研究认为,供、受者年龄及体重之间如果差别很大,可能影响预后[11,12]。本研究两组病例中,没有HLA抗体特异性(PRA)>30%的高致敏受者,这使得结论的推广方面受到一定限制。由于开展器官捐献肾移植初期,部分外院分配供者资料不全,针对冷缺血时间及HLA错配等因素的统计分析所需部分病例数据不足,限制了本研究的分析因素选择。此外,由于我国开展器官捐献肾移植时间尚短,病例积累及随访时间不足,尚缺乏大规模长期随访的病例积累,仅能反映术后早期变化。
本研究回顾性分析了在器官捐献肾移植受者中,巴利昔单抗与ATG诱导治疗术后受者和移植物近期预后良好,感染及DGF发生率差异无统计学意义,两种免疫诱导药物在器官捐献时代免疫低危的受者中均能取得同样的良好疗效。
所有作者均声明不存在利益冲突



























