
回顾性分析肾移植术后稳定期受者他克莫司普通剂型转换为缓释剂型的不同转换方案的疗效和安全性,为肾移植受者他克莫司转换策略提供参考。
收集2020年1月至2020年6月中山大学附属第一医院术后稳定期他克莫司普通剂型转换为他克莫司缓释剂型的101例肾移植受者资料,男性62例,女性49例,年龄19~69岁,转换时按照等剂量转换和增加剂量转换两种方案进行分组,先对比他克莫司普通剂型转换为缓释剂型后的变化,再根据他克莫司普通剂型转换为缓释剂型不同转换剂量,将受者分为两组:按照1∶1转换组受者55例;按照>1∶1(1∶1.2~1∶1.4)转换组受者46例。比较两组间转换后各项临床指标,如血清肌酐(serum creatinine,Scr)、血尿素氮(blood urea nitrogen,BUN)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、碱性磷酸酶(alkaline phosphatase,ALP)、血清白蛋白(albumin,ALB)、白细胞计数(white blood cell,WBC)、尿白细胞、血红蛋白(hemoglobin,Hb)及空腹血糖(glucose,Glu)等。
从数值变化趋势来看,转换为他克莫司缓释剂型后药物剂量/变异趋势更小,血药浓度更平稳。在按1∶1和1>1初始剂量进行转换的两个亚组中,1∶1转换组剂量/血药浓度变化趋势上显得更平稳一些,但长期观察两组无区别。转换为缓释剂型后1周、3个月时Scr更低(P<0.05),并且2周时BUN更低(P<0.05)。此外,转换后5个月时,ALT及AST均较普通剂型明显改善(P<0.05)。在2周、3周时UWBC差异有统计学意义(P<0.05)。转换2周时,Hb较普通剂型明显改善(P<0.05)。ALP、ALB、Glu等各个时间点和转换前差异无统计学意义(P>0.05)。在按照1∶1转换组中,肾功能有改善趋势。2周时,BUN较转换前降低;1周和3周时,Scr较转换前降低(P<0.05)。此外,按照1∶1转换组在肝功能方面也有改善趋势。1周和5个月时,ALT较转换前降低(P<0.05)。然而,两不同剂量转换组各个时间点的AST、ALB、ALP、Glu、尿白细胞及血清WBC差异均无统计学意义(P>0.05)。转换后较转换前他克莫司谷浓度个体内变异度明显改善(P<0.05)。
他克莫司缓释剂型具有与普通剂型相同的安全性及疗效,并可改善个体内药物变异度。将普通剂型转换至缓释剂型时应考虑个体化差异,合理监测谷浓度并结合临床各项指标调整剂量。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
他克莫司联合霉酚酸(MPA)和糖皮质激素三联方案是肾移植术后标准免疫抑制方案[1]。既往他克莫司普通剂型均为2次/d服用,近年来他克莫司缓释剂型(1次/d)在国外临床已广泛应用。国外的临床数据表明,与他克莫司普通剂型(2次/d)相比,他克莫司缓释剂型不仅提高了受者的依从性及耐受性[2],其安全性及疗效也得到证实[3]。但在国内,有关肾移植受者从他克莫司普通剂型转换为缓释剂型的研究资料仍然有限。本研究旨在回顾性分析2020年1月至2020年6月中山大学附属第一医院他克莫司普通剂型按不同转换剂量转换为缓释剂型的肾移植术后肾功能稳定的101例受者的临床特点,为肾移植术后调整更优化的免疫抑制方案提供一定的借鉴经验。
回顾性分析中山大学附属第一医院2020年1月至2020年6月他克莫司普通剂型按不同剂量转换为缓释剂型的肾移植术后肾功能稳定的101例受者的临床资料。收集纳入受者基本信息及转换组前后给药剂量、血药浓度和各临床指标。其中,42例受者检测代谢类型,快、慢代谢型分别为22例、20例。所有受者免疫抑制方案为:他克莫司+MPA+糖皮质激素。
101例肾移植功能稳定的受者中,男性62例,女性49例,年龄19~69岁,转换前他克莫司给药剂量及药物浓度。此外包括临床各项临床生理指标,如血清肌酐(serum creatinine,Scr)、血尿素氮(blood urea nitrogen,BUN)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、尿白细胞(urinary white blood cells,UWBC)、血清白蛋白(albumin,ALB)、碱性磷酸酶(alkaline phosphatase,ALP)、白细胞计数(white blood cell,WBC)、血红蛋白(hemoglobin,Hb)及空腹血糖(glucose,Glu)。除了他克莫司给药剂量差异有统计学意义外(P<0.05),其他各项数据差异均无统计学意义(P>0.05,表1)。
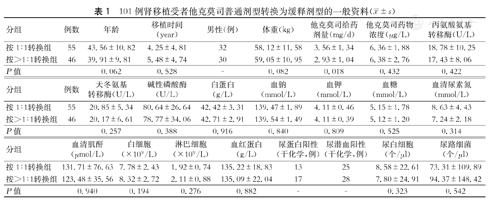
101例肾移植受者他克莫司普通剂型转换为缓释剂型的一般资料( ±s)
±s)
101例肾移植受者他克莫司普通剂型转换为缓释剂型的一般资料( ±s)
±s)
| 分组 | 例数 | 年龄 | 移植时间(year) | 男性(例) | 体重(kg) | 他克莫司给药剂量(mg/d) | 他克莫司药物浓度(μg/L) | 丙氨酸氨基转移酶(U/L) |
|---|---|---|---|---|---|---|---|---|
| 按1∶1转换组 | 55 | 43.56±10.82 | 4.25±4.81 | 32 | 58.12±11.58 | 3.56±1.34 | 6.36±1.88 | 18.78±10.25 |
| 按>1∶1转换组 | 46 | 39.91±9.81 | 5.48±4.74 | 30 | 59.05±10.95 | 2.93±1.04 | 6.38±2.76 | 17.43±8.06 |
| P值 | 0.062 | 0.528 | - | 0.082 | 0.018 | 0.432 | 0.422 |
| 分组 | 例数 | 天冬氨基转移酶(U/L) | 碱性磷酸酶(U/L) | 白蛋白(g/L) | 血钠(mmol/L) | 血钾(mmol/L) | 血糖(mmol/L) | 血清尿素氮(mmol/L) |
|---|---|---|---|---|---|---|---|---|
| 按1∶1转换组 | 55 | 20.85±5.34 | 80.64±26.64 | 42.42±3.31 | 139.47±1.89 | 4.11±0.46 | 5.15±1.78 | 8.63±4.43 |
| 按>1∶1转换组 | 46 | 20.17±6.61 | 78.77±34.06 | 42.71±2.91 | 139.54±1.49 | 4.11±0.39 | 5.12±1.20 | 7.24±2.18 |
| P值 | 0.257 | 0.388 | 0.916 | 0.840 | 0.809 | 0.525 | 0.314 |
| 分组 | 血清肌酐(μmol/L) | 白细胞(×109/L) | 淋巴细胞(×109/L) | 血红蛋白(g/L) | 尿蛋白阳性(干化学,例) | 尿潜血阳性(干化学,例) | 尿白细胞(个/μl) | 尿路细菌(个/μl) |
|---|---|---|---|---|---|---|---|---|
| 按1∶1转换组 | 131.71±76.63 | 7.78±2.43 | 1.92±0.74 | 135.22±18.83 | 13 | 25 | 8.58±22.61 | 73.31±109.89 |
| 按>1∶1转换组 | 123.48±35.56 | 8.32±2.72 | 2.11±0.88 | 135.09±22.04 | 17 | 28 | 7.80±24.91 | 94.37±148.42 |
| P值 | 0.940 | 0.194 | 0.276 | 0.882 | - | - | 0.323 | 0.542 |
以肾移植术后肾功能稳定的101例受者为研究对象。先对比他克莫司普通剂型转换为缓释剂型后的变化,再根据他克莫司普通剂型转换为缓释剂型不同转换剂量,将受者分为两组:按照1∶1转换组受者55例;按照>1∶1(1∶1.2~1∶1.4)转换组受者46例。分组后抽取受者的静脉血,检测转换前后不同时间点各项临床指标,如肾功能、肝功能、血药浓度、血常规、血生化及尿常规等。
为了探索转换为缓释剂型后能否改善个体内变异度(intrapatient variability,IPV),我们选取同时满足以下两个标准:(1)转换前有10次血药浓度记录,选取前6次;(2)转换后有至少6次血药浓度记录,选取最近6次,选取同时符合以上标准的受者共29例,进行变异度计算,计算公式:IPV=标准差/平均数(一般取6次数值)。
使用非参检验方法Mann-Whitney U test(paired,two-sided)来检验两组受者转换药物前后不同时间点各项生理指标。同时使用Mann-Whitney U test(unpaired,two-sided)来检验两组受者转换药物后不同时间点各项生理指标。P<0.05为差异具有统计学意义。
通过观察在不同时间点他克莫司普通剂型转换为缓释剂型、不同代谢基因型及不同转换组的剂量和浓度的值变化可知,由他克莫司普通剂型转换为他克莫司缓释剂型后的1周、2周、4周、2个月及5个月的药物浓度分别为(5.06±1.36)μg/L、(5.71±1.77)μg/L、(5.28±1.58)μg/L、(5.69±1.63)μg/L及(6.83±1.71)μg/L。转换后快代谢型组1周、2周、4周、2个月及5个月的他克莫司药物浓度分别为(5.98±1.49)μg/L、(7.20±3.91)μg/L、(6.17±1.6)μg/L、(6.36±1.39)μg/L及(6.83±1.71)μg/L;转换后慢代谢型组1周、2周、4周、2个月及5个月的他克莫司药物浓度分别为(6.00±0.84)μg/L、(3.98±2.23)μg/L、(5.39±1.85)μg/L、(5.85±1.26)μg/L及(6.80±1.16)μg/L。(表2)
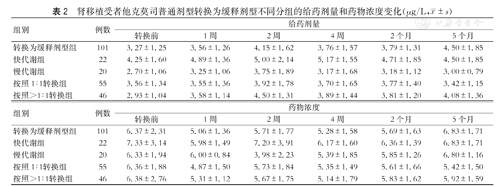
肾移植受者他克莫司普通剂型转换为缓释剂型不同分组的给药剂量和药物浓度变化(μg/L, ±s)
±s)
肾移植受者他克莫司普通剂型转换为缓释剂型不同分组的给药剂量和药物浓度变化(μg/L, ±s)
±s)
| 组别 | 例数 | 给药剂量 | |||||
|---|---|---|---|---|---|---|---|
| 转换前 | 1周 | 2周 | 4周 | 2个月 | 5个月 | ||
| 转换为缓释剂型组 | 101 | 3.27±1.25 | 3.56±1.26 | 4.15±1.62 | 3.76±1.57 | 3.79±1.31 | 4.50±1.85 |
| 快代谢组 | 22 | 4.25±1.60 | 4.89±1.36 | 5.00±2.14 | 5.17±1.55 | 4.71±1.85 | 4.50±1.85 |
| 慢代谢组 | 20 | 2.70±1.06 | 3.25±1.06 | 3.75±1.89 | 3.17±1.68 | 3.18±1.12 | 3.00±0.79 |
| 按照1∶1转换组 | 55 | 3.56±1.34 | 3.55±1.36 | 3.92±1.78 | 3.70±1.65 | 3.77±1.40 | 3.42±1.15 |
| 按照>1∶1转换组 | 46 | 2.93±1.04 | 3.58±1.14 | 4.50±1.31 | 3.89±1.44 | 3.81±1.20 | 4.08±1.36 |
| 组别 | 例数 | 药物浓度 | |||||
|---|---|---|---|---|---|---|---|
| 转换前 | 1周 | 2周 | 4周 | 2个月 | 5个月 | ||
| 转换为缓释剂型组 | 101 | 6.37±2.31 | 5.06±1.36 | 5.71±1.77 | 5.28±1.58 | 5.69±1.63 | 6.83±1.71 |
| 快代谢组 | 22 | 7.33±3.14 | 5.98±1.49 | 7.20±3.91 | 6.17±1.60 | 6.36±1.39 | 6.83±1.71 |
| 慢代谢组 | 20 | 6.33±1.94 | 6.00±0.84 | 3.98±2.23 | 5.39±1.85 | 5.85±1.26 | 6.80±1.16 |
| 按照1∶1转换组 | 55 | 6.36±1.88 | 4.87±1.50 | 5.73±1.84 | 5.35±1.49 | 5.61±1.66 | 5.42±1.50 |
| 按照>1∶1转换组 | 46 | 6.38±2.76 | 5.31±1.12 | 5.67±1.75 | 5.14±1.79 | 5.83±1.62 | 5.92±1.59 |
此外,通过观察在不同剂量转换的剂量和浓度变化可知,按照1∶1转换组的1周、2周、4周、2个月及5个月的药物浓度分别为(4.87±1.5)μg/L、(5.73±1.84)μg/L、(5.35±1.49)μg/L、(5.61±1.66)μg/L及(5.42±1.50)μg/L,而按照>1∶1转换组的1周、2周、4周、2个月及5个月的药物浓度分别为(5.31±1.12)μg/L、(5.67±1.75)μg/L、(5.14±1.79)μg/L、(5.83±1.62)μg/L及(5.92±1.59)μg/L。
通过不同治疗时间点观察他克莫司普通剂型转换为缓释剂型后各临床指标的变化情况(表3)。与他克莫司普通剂型相比:转换为缓释剂型后1周、3个月时SCr更低(P<0.05),并且2周时BUN更低(P<0.05)。此外,转换后5个月时,ALT及AST均较普通剂型明显改善(P<0.05)。在2周、3周时UWBC差异有统计学意义(P<0.05)。转换2周时,Hb较普通剂型明显改善(P<0.05)。ALP、ALB、Glu等各个时间点和转换前差异无统计学意义(P>0.05)。
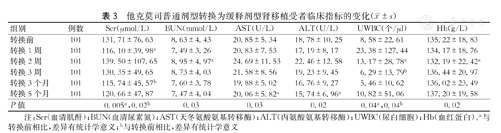
他克莫司普通剂型转换为缓释剂型肾移植受者临床指标的变化( ±s)
±s)
他克莫司普通剂型转换为缓释剂型肾移植受者临床指标的变化( ±s)
±s)
| 组别 | 例数 | Scr(μmol/L) | BUN(mmol/L) | AST(U/L) | ALT(U/L) | UWBC(个/μl) | Hb(g/L) | |
|---|---|---|---|---|---|---|---|---|
| 转换前 | 101 | 131.71±76.63 | 8.63±4.43 | 20.85±5.34 | 18.78±10.25 | 8.58±22.61 | 135.22±18.83 | |
| 转换1周 | 101 | 116.10±39.98a | 7.49±3.26 | 20.83±7.53 | 17.19±8.17 | 23.38±127.44 | 134.17±18.76 | |
| 转换2周 | 101 | 139.50±107.65 | 8.95±4.97a | 24.69±11.53 | 22.46±12.58 | 13.17±28.78a | 132.19±22.42a | |
| 转换3周 | 101 | 130.35±49.65 | 8.73±4.03 | 21.58±8.56 | 19.23±9.45 | 6.29±13.79b | 136.44±20.97 | |
| 转换3个月 | 101 | 115.74±45.57b | 7.60±3.78 | 19.88±5.02 | 16.76±9.27 | 5.46±10.62 | 136.02±23.49 | |
| 转换5个月 | 101 | 120.66±47.87 | 7.47±4.04 | 20.06±5.82a | 15.74±6.96a | 10.82±51.06 | 137.20±19.58 | |
| P值 | 0.005a,0.02b | 0.03 | 0.03 | 0.02 | 0.04 a,0.04 b | 0.02 |
注:Scr(血清肌酐);BUN(血清尿素氮);AST(天冬氨酸氨基转移酶);ALT(丙氨酸氨基转移酶);UWBC(尿白细胞);Hb(血红蛋白)。a与转换前相比,差异有统计学意义;b与转换前相比,差异有统计学意义
通过观察不同剂量转换组间各项指标评估两者之间的疗效及安全性。在按照1∶1转换组中,肾功能有改善趋势。2周时,BUN较转换前降低;1周和3周时,Scr较转换前降低(P<0.05)。此外,按照1∶1转换组在肝功能方面也有改善趋势。1周和5个月时,ALT较转换前降低(P<0.05)。然而,两不同剂量转换组各个时间点的AST、ALB、ALP、Glu、UWBC及WBC差异均无统计学意义(P>0.05,表4)。
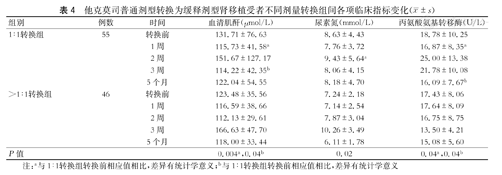
他克莫司普通剂型转换为缓释剂型肾移植受者不同剂量转换组间各项临床指标变化( ±s)
±s)
他克莫司普通剂型转换为缓释剂型肾移植受者不同剂量转换组间各项临床指标变化( ±s)
±s)
| 组别 | 例数 | 时间 | 血清肌酐(μmol/L) | 尿素氮(mmol/L) | 丙氨酸氨基转移酶(U/L) |
|---|---|---|---|---|---|
| 1∶1转换组 | 55 | 转换前 | 131.71±76.63 | 8.63±4.43 | 18.78±10.25 |
| 1周 | 115.73±41.58a | 7.76±3.72 | 16.87±8.35a | ||
| 2周 | 151.67±127.17 | 9.43±5.64a | 25.00±13.38 | ||
| 3周 | 114.22±42.35b | 8.06±4.15 | 21.78±10.08 | ||
| 5个月 | 122.04±54.55 | 8.18±4.70 | 16.09±7.67b | ||
| >1∶1转换组 | 46 | 转换前 | 123.48±35.56 | 7.24±2.18 | 17.43±8.06 |
| 1周 | 116.59±38.66 | 7.14±2.54 | 17.64±8.09 | ||
| 2周 | 112.13±29.61 | 7.87±3.04 | 16.75±8.75 | ||
| 3周 | 166.63±47.70 | 10.26±3.49 | 13.50±4.21 | ||
| 5个月 | 118.00±33.44 | 6.11±1.78 | 15.08±5.60 | ||
| P值 | 0.004a,0.04b | 0.02 | 0.04a,0.04b |
注:a与1∶1转换组转换前相应值相比,差异有统计学意义;b与1∶1转换组转换前相应值相比,差异有统计学意义
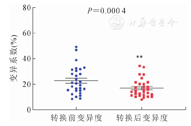
此外,为了探索他克莫司普通剂型转换为缓释剂型后能否改善个体内药物变异度,对符合标准的29例进行变异度计算。结果显示,转换后较转换前谷浓度个体内变异度明显改善(P<0.05,图1)。

美国食品药品监督管理局(FDA)及改善全球肾脏病预后组织(KDIGO)指南均建议他克莫司联合霉酚酸及糖皮质激素作为肾移植术后标准免疫抑制方案[1]。他克莫司普通剂型因服药次数多易造成受者漏服或者不按时服用,是移植术后移植物丧失功能的主要原因之一[4]。肾移植术后稳定期他克莫司普通剂型转换为他克莫司缓释剂型后能够在整个胃肠道吸收及代谢,影响他克莫司代谢的CYP3A4和CYP3A5主要分布在近端小肠,对他克莫司缓释剂型的影响更小[5]。因此,每天服药一次,提高受者的依从性及耐受性,降低少服、漏服现象,并在一定程度上减少了移植物丢失的发生率。这一现象可能跟他克莫司缓释剂型的药代动力学特点有关。
目前国内已有中心研究表明肾移植不同时期他克莫司缓释剂型具有与普通剂型具有相同的安全性及有效性,转换后降低了佐剂的用量,血药浓度及血清肌酐更为稳定[6]。同样地,国外相关研究已证实他克莫司缓释剂型在肾移植术后受者的长期疗效。一项亚洲国家开展的多中心、非干预性研究结果表明,肾移植术后由他克莫司普通剂型转换为他克莫司缓释剂型后,活检证实的急性排斥反应发生率低、移植肾和受者存活率高,安全性好[7]。Tinti等[8]开展的一项研究表明他克莫司缓释胶囊使肾移植术后受者维持有效的免疫抑制状态,肾功能长期保持稳定,部分受者肾功能改善。本中心101例肾移植受者他克莫司转换剂型的回顾性观察研究,表明转换为缓释剂型较普通剂型肝肾功能明显改善,进一步证实了他克莫司普通剂型转换为缓释剂型后的疗效及安全性。同时,本次转换受者在随访期中未发现需住院治疗的感染及急性排斥反应严重并发症,蛋白尿程度较转换前未加重,表明肾移植术后稳定期转换他克莫司缓释剂型具有一定的疗效。Turunc等[9]开展的一项单中心、回顾性研究证实对于糖尿病肾移植受者,以他克莫司缓释胶囊为基础的免疫抑制方案均可改善糖代谢。然而,本中心的回顾性研究结果显示他克莫司普通剂型转换为缓释剂型后空腹血糖趋于平稳,并维持在正常范围内。
他克莫司是一种狭窄治疗指数药物,血药浓度低于目标范围,将会增加排斥反应发生风险,若血药浓度过高,则将会增加毒性反应,IPV高可增加移植肾丢失风险,因此,应重视他克莫司谷浓度IPV[10]。他克莫司普通剂型谷浓度IPV高可显著增加急性排斥反应发生风险、降低移植肾长期存活率以及显著加重移植肾间质纤维化和肾小管萎缩[11]。此外,Süsal和Döhler[12]一项回顾性分析也证实他克莫司谷浓度个体内变异度过高使肾移植受者长期存活率降低。本中心通过计算29例受者转换前后6次个体内血药浓度的波动幅度,结果显示转换后的变异度较转换前明显降低,表明转换为他克莫司缓释剂型后可降低他克莫司谷浓度个体内变异度。因此,转换为他克莫司缓释剂型可能降低移植肾急性排斥反应发生风险及提高移植肾长期存活率。此外,Rummo等[13]开展一项5年的非干预、前瞻性的研究也证实以他克莫司缓释剂型为基础的免疫抑制方案在肾移植临床实践中的长期疗效。
他克莫司普通剂型转换为缓释剂型后各项临床指标波动较小且维持在相对值正常范围内,证实了他克莫司缓释剂型具有与普通剂型相同的安全性及疗效。Kamińska等[14]一项回顾性研究结果表明,肾移植受者术后稳定期转换为他克莫司缓释剂型后,谷浓度水平可长期保持稳定。本中心通过对比两个不同剂量转换组的结果显示在剂量/血药浓度变化趋势发现,按1∶1转换组更平稳,长期观察两组无区别。此外,稳定期按1∶1转换组在肝功能、肾功能等指标上表现一定改善趋势。因此,在他克莫司普通剂型转换成他克莫司缓释剂型后,对于转换早期而言,按1∶1初始剂量服用似乎更加获益,而从长期效果来看,两者具有同等的疗效及安全性。Sukkha等[15]一项开放性、前瞻性研究结果表明肾移植术后受者早期按1∶1转换为他克莫司缓释剂型,他克莫司AUC保持稳定,无须调整剂量,仅在谷浓度降低大于30%时需进行额外的剂量调整。然而个体差异较大,如转换前谷浓度水平、基因型、移植时间等不同,根据受者转换前的这些因素,需个性化地推荐转换剂量。对于目标谷浓度中上水平的可考虑推荐1∶1,中下游或者快代谢型的建议按大于1∶1转换。同时,基于他克莫司缓释剂型需5~7 d达稳态血药浓度,建议转换后1周监测首次谷浓度,不宜过早或者过晚。
综上所述,本中心研究表明他克莫司缓释剂型具有与普通剂型相同的安全性及疗效,并可改善个体内药物变异度。将普通剂型转换至缓释剂型时应考虑个体化差异,合理监测谷浓度并结合临床各项指标调整剂量。
所有作者声明无利益冲突



























