
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
吞咽障碍是指由于下颌、唇、舌、软腭、咽喉、食管等器官结构和(或)功能受损,不能安全有效地把食物输送到胃内的过程[1]。脑卒中后吞咽障碍引起的误吸使患者死亡风险增加3倍,其中需要肠内营养支持的患者30 d内死亡率高达28%[2]。目前,对于经积极吞咽康复治疗6个月以上仍不能经口进食的慢性重度神经源性吞咽困难(severe chronic neurogenic dysphagia,SCND)患者,仍缺乏有效的治疗方法[3]。有研究报道,咽腔电刺激(pharyngeal electrical stimulation,PES)可改善急性和恢复期幕上卒中患者的吞咽功能,降低渗漏误吸评分[4,5,6],在重度吞咽障碍中具有潜在疗效[7,8]。
目前,临床上PES治疗参数为:方波,脉宽1 ms,频率5 Hz,每日10 min[5]。该参数下,PES的电刺激强度大于20 mA,并存在可能与刺激强度相关的不良反应,如恶心等[9]。既往PES研究对象基本均为大脑半球或幕上病变,仅有部分研究涉及了幕下病变[7,8,10],尚缺乏PES对SCND长期作用的相关研究。并且PES操作过程中存在定位困难的问题[9,11,12]。因此,本研究在原有基础上对PES进行了改良,称之为咽腔感觉电刺激(pharyngeal sensory electrical stimulation, PSES),其参数为方波和三角波的组合波,脉宽10 ms,频率5 Hz,每日10 min。本研究采用PSES治疗1例SCND患者,报道如下。
现病史:患者,男性,33岁,未婚,汉族,2021年5月9日因"吞咽困难7月余"入院。患者7月前因蛛网膜下腔出血(图1A)行左侧椎动脉瘤栓塞术,术后复查颅脑CT未见新发出血(图1B)。后因呼吸衰竭行气管切开术,经抗感染、呼吸机辅助呼吸、床边康复等治疗2个月后,拔除气切套管。后经系统康复治疗5个月仍不能经口进食,伴言语欠清、四肢活动欠灵活。
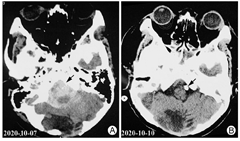

注:图1A,颅脑CT结果示蛛网膜下腔出血(箭头所示),枕骨骨质缺损。图1B,颅脑CT结果示右小脑术后改变,右枕部硬膜下积液,颅内动脉瘤栓塞术后改变(箭头所示),蛛网膜下腔出血
既往史:患者1岁时因右侧小脑半球星形细胞瘤行手术治疗,术后饮食及日常活动正常。1年前测血压高未予诊治。
查体:神清,一般状况可,声音嘶哑,伸舌右偏,软腭抬升差,悬雍垂偏左,咽反射消失,喉上抬不充分。四肢肌力5-级。双侧指鼻、轮替、跟膝胫试验阳性。搀扶下可步行。
入院诊断:①左侧椎动脉瘤破裂伴蛛网膜下腔出血,吞咽困难、构音障碍、共济失调;②高血压病3级、极高危组。
患者入院后采用功能性经口摄食量表(functional oral intake scale, FOIS)评估,结果为1分(完全不能经口进食),给予间歇胃管注食(每日6餐)。
视频透视吞咽检查(videofluoroscopic swallowing study,VFSS):患者在自然坐位下吞咽2号食物(100 ml 60%硫酸钡混悬液与2 g增稠剂混合)3 ml,造影显示口腔控制正常,运送正常,吞咽启动明显延迟,渗漏-误吸量表(penetration and aspiration scale, PAS)8分(隐性误吸),咳嗽力量弱,不能有效清除。改良钡剂吞咽障碍评估(modified barium swallowing study measurement tool for swallowing impairment, MBSImp)[13](图2A)。
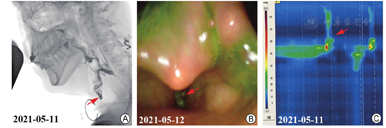

注:图2A,VFSS示患者进食2号食物3 ml出现隐性误吸(PAS 8级)(红色箭头),不能有效清除;UES未开放。图2B,FEES示患者进食2号食物3 ml时,会厌谷及双侧梨状窦中重度残留;存在隐性误吸;咳嗽力量弱,不能有效清除(红色箭头)。图2C,治疗前HRM示患者下咽收缩压28.4 mmHg (正常值范围110~200 mmHg,红色箭头)
软管喉内窥镜吞咽功能检查(flexible endoscopic evaluation of swallowing, FEES)[14]结果显示,喉前庭分泌物持续存在(提示Murray分级[15]3分);左侧声带内收外展减弱,右侧声带固定,舌根后缩减弱,无自主吞咽;会厌谷中度残留(Yale分级[16]4分,会厌韧带不可见)、双侧梨状窦重度残留(Yale分级5分,绿染食物溢到杓状会厌襞);存在隐性误吸(PAS 8分);咳嗽力量弱,不能有效清除,需吸痰(图2B)。
高分辨率测压(high-resolution manometry, HRM)结果显示,患者吞咽2号食物3 ml时,下咽峰值压力为28.4 mmHg,腭咽峰值压力为32.4 mmHg,食管上括约肌(upper esophageal sphincter, UES)平均静息压为36.3 mmHg,平均残余压为3.4 mmHg,松弛持续时间640 ms(图2C)。患者主动咳嗽分级[17]为2分(咳嗽声音微弱)。
入院后评估提示患者吞咽启动延迟,气道保护功能弱,咽缩肌无力,环咽肌开放不完全。患者入院后行常规吞咽障碍康复治疗[1]15 d仍无好转,考虑加用PSES治疗。患者及家属签署知情同意书后,开始行喉镜和肌电定位下PSES治疗(图3A)。采用德国Zimmer公司产PSES仪对患者进行治疗,参数为方波和三角波的组合波,脉宽10 ms,频率5 Hz,每日10 min,刺激强度按每次0.5 mA的幅度增加,患者开始感受到刺激时为感受阈,感到疼痛不适、不想再增加刺激强度时为耐受阈,最终刺激值=感受阈+75%(耐受阈-感受阈)(图3B)。
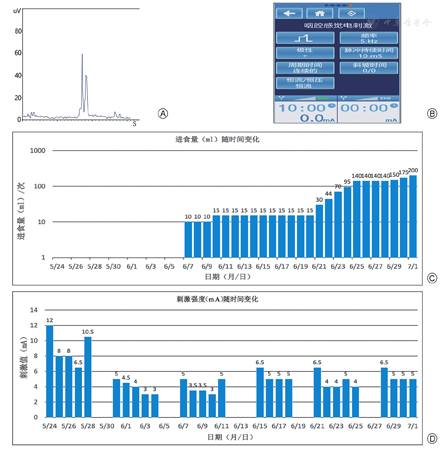

注:图3A,PSES首次喉镜下定位可见导管刺激电极与咽缩肌接触良好时,咽部肌电信号稳定在20 μV以下,当患者吞咽时肌电信号明显升高。图3B,PSES治疗参数;图3C,随时间变化,患者每次进食量情况。图3D,PSES强度随刺激次数增加而减小,并稳定在8 mA以下
经28次PSES治疗后(总周期39 d),患者可右转头进食高稠食物,每次约200 ml(FOIS 3分)(图3C)。PSES强度随刺激次数增加而减小,并稳定在8 mA以下(图3D)。治疗28次后复查:①VFSS示患者自然坐位进食2号食物3 ml时,口腔控制正常,运送正常,吞咽启动延迟,可有效清除(PAS 3分);UES开放情况好转(MBSImp评分1分)(图4A);②FEES示患者右转头进食2号食物3 ml时,喉前庭分泌物持续存在(Murray分级3分);左侧声带内收外展正常,右侧声带活动减弱,舌根后缩减弱,吞咽频率为每分钟3次;会厌谷及双侧梨状窦微量残留(Yale分级2分,可见微量绿染食物痕迹);偶有渗漏可自主清除(PAS 3分);咳嗽力量好转,可有效清除(图4B);③HRM示患者右转头吞咽2号食物3 ml时,下咽峰值压力为97.7 mmHg,腭咽峰值压力为120.1 mmHg,UES平均静息压为53.3 mmHg,平均残余压为3.3 mmHg,松弛持续时间为690 ms(图4C)。患者吞咽启动、协调性、咽缩肌收缩、气道保护、环咽肌开放均较前改善。主动咳嗽分级[17]5分(可连续较大力量咳嗽)。相关功能评估结果见表1、表2。

治疗前、后患者的吞咽评估结果
治疗前、后患者的吞咽评估结果
| FOIS(分) | PAS(分) | MBSImp(分) | Murray分级(分) | Yale分级(分) | 主动咳嗽分级(分) | ||
|---|---|---|---|---|---|---|---|
| 会厌谷 | 梨状窦(左/右) | ||||||
| 治疗前 | 1 | 8 | 3 | 3 | 4 | 5/5 | 2 |
| 治疗后 | 3 | 3 | 1 | 3 | 2 | 2/2 | 5 |

治疗前、后患者的咽腔测压结果
治疗前、后患者的咽腔测压结果
| 腭咽峰值压力(mmHg) | 下咽峰值压力(mmHg) | UES平均静息压(mmHg) | UES平均残余压(mmHg) | 松弛持续时间(ms) | |
|---|---|---|---|---|---|
| 治疗前 | 32.4 | 28.4 | 36.3 | 3.4 | 640 |
| 治疗后 | 120.1 | 97.7 | 53.3 | 3.3 | 690 |
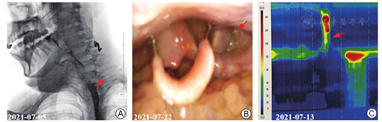

注:图4A,VFSS示患者进食2号食物3 ml无误吸(PAS 3级);可有效清除;UES开放好转(红色箭头)。图4B,FEES示患者进食2号食物3 ml时,会厌谷和双侧梨状窦微量残留(红色箭头),偶有渗漏可自主清除(PAS 3级)。图4C,HRM示患者下咽收缩压97.7 mmHg(红色箭头)
随访90 d,患者可右转头进食饺子、香蕉、粥,每次300~400 ml,每日2~3次(FOIS 6分)。无发热、咳痰等感染症状。
本研究采用PSES治疗慢性重度幕下出血后吞咽障碍,取得了良好的治疗效果。患者经常规吞咽治疗7月余无好转(FOIS 1分),经28次PSES治疗后,其下咽收缩压力、残留、渗漏、误吸、咳嗽能力均得到明显改善,可经口进食中稠食物(FOIS 3分),后停用PSES,仅进行常规的吞咽康复训练,90 d后随访时,患者可进食多种性状食物(FOIS 6分)。因前7个月的常规治疗未见明显疗效,故该例SCND患者吞咽功能明显好转的原因可能与PSES有关。虽有好转,但患者后续吞咽功能的整体协调还需配合常规吞咽治疗。表明延长治疗周期的PSES对幕下病变引起的SCND可能具有积极疗效。PSES结合喉镜及肌电采集设备可快速准确定位,操作者经培训后,可在20 min内完成操作,且PSES治疗强度多小于10 mA(咽部感觉神经可能对PSES具有更高的敏感性),副作用小。PSES在SCND中的有效性和安全性,尚需大规模多中心临床实验进一步验证。
目前,PSES的作用机制尚未阐明,可能与PES的作用机制相似,如通过增加吞咽皮质的兴奋性及兴奋范围,增强咽部的感觉输入,进而提高脑损伤后的神经可塑性、促进功能恢复[18];或通过提高唾液中促进吞咽反射的神经肽—P物质[19]水平,"正反馈"促进吞咽反射等。上述机制是否与PSES有所关联,尚需进一步研究。


























