
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者,男,59岁,因体检B超发现脾脏占位于2017年7月23日入本院肝胆外科。患者无自觉不适症状,既往有糖尿病病史,曾因腹股沟疝和消化道溃疡穿孔行手术治疗。查体未发现阳性体征。检验血常规:白细胞3.39×109/L,血小板75×109/L,淋巴细胞0.85×109/L,均稍低于正常下限,血清肿瘤标记物正常。肿物在B超描述:稍增强回声,内见点条状血流信号。CT检测:平扫稍低密度类圆形肿块,边界不清,增强扫描动脉期不均匀强化,强化程度低于脾脏,7.5 cm×5.7 cm×5.5 cm(图1)。CT诊断意见:淋巴瘤、不典型血管瘤或血管淋巴瘤。PET-CT:氟脱氧葡萄糖(FDG)代谢稍高,最大标准摄取值(SUXmax)2.99,倾向良性肿瘤。
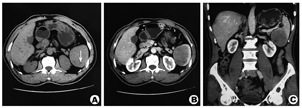

基于上述结果,术前诊断为脾脏良性肿瘤,随后进行了脾脏切除手术,术后病理检查,大体:脾脏切开见6 cm×5 cm×4 cm肿物,切面呈暗褐色,与脾组织分界不清。镜下:见大量异型内皮细胞构成不规则血管组分(图2)。免疫组化显示血管内皮细胞标记CD31、CD34、FLI-1、FVIII阳性,角蛋白系列、粒细胞和单核细胞标记CD15、S-100、淋巴细胞标记CD30阴性,Ki-67 20%。最终病理诊断为脾血管肉瘤(primary splenic angiosarcoma,PSA)。借鉴其他PSA早期肿瘤治疗经验,患者术后未进行辅助治疗。术后常规随访,最近随访是在术后1年,无复发征象,未出现手术相关近期或远期并发症,生活质量同术前无明显改变。
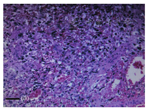

PSA起源于脾血窦内皮细胞,是一种极其罕见的恶性间叶肿瘤,发病率在(0.14~0.25)/100万[1],恶性程度极高,早期容易发生转移,多数患者在诊断后1年内死亡[2]。病因不明,研究报道,PSA可并发于脾良性肿瘤、其他肿瘤放化疗、其他部位血管瘤之后,但具体的相关性尚待证实[3]。
PSA缺乏特异临床表现,多数患者可出现腹部不适等一些非特异性表现。约10%表现出恶性肿瘤警示征:不明原因发热、乏力、体重减轻等,约30%因脾自发破裂就诊。实验室检查同样缺乏特异性,常有贫血、血小板减少,也可能观察到血小板增多、白细胞增多,血沉加快等。超声、CT、MRI等检查都可能发现脾脏的异常,但很难同脾脏的其他良性或恶性肿瘤鉴别。CT具有相对较高的诊断效能,在平扫时可以发现增大的脾脏,内有高密度或低密度结节,增强时结节不均匀强化,有时可以发现大量钙化点[4]。PET-CT在鉴别良恶性上有一定帮助,SUXmax>6需高度怀疑恶性肿瘤。此患者在术前未准确诊断,这也说明影像学在诊断PSA上存在较大局限性。此外,回顾患者入院前1年体检时的CT平扫,在脾脏下极已经能够发现可疑病灶(图3),但被CT诊断所忽视。所幸疾病未发生质变,这说明影像医生对于脾脏肿瘤的认识和重视还需提升。其最终的诊断需依赖病理学检查,但不推荐活检,因为存在出血及肿瘤破裂播散的风险。
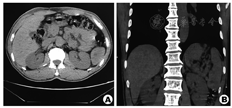

脾脏切除是首选治疗手段,在脾破裂之前进行手术的预后优于破裂之后。如不能手术,可采用化疗及放疗。目前推荐阿霉素联合抗血小板源性生长因子受体α靶向药物Olaratumab[5],肿瘤高表达TEF3提示对紫杉醇反应性良好[6]。放疗常作为辅助手段,Bilski等[7]报道了一例PSA脾破裂后,联合手术、放疗和化疗,患者的生存时间达到23个月,远超平均水平(6个月)。其他一些探索性的治疗包括外周血干细胞移植、抗血管生成靶向治疗尚处于研究阶段。
PSA预后较差,Neuhauser等[8]报道了28例经手术治疗的PSA患者的临床结局:25例患者在29月内死亡(中位生存期5个月),1例失访,2例存活,生存时间分别为8年和10年。在其他研究中报道的总体生存时间为4~14个月,脾破裂后80%的患者生存期<6个月[9],在脾破裂前进行手术,中位生存期能够达到11个月[10]。
综上所述,PSA是一种罕见的高侵袭性恶性肿瘤,因为缺乏特异症状、体征和肿瘤标记物,诊断较为困难。早期诊断只能依靠影像检查,尽早行脾切除术,是改善预后的关键。
所有作者均声明不存在利益冲突


























