
探讨胃癌根治术后患者在加速康复外科(ERAS)策略执行中的体验以及影响治疗体验的因素。
本研究采用前瞻性队列研究的方法,连续纳入2019年12月至2020年12月期间在空军军医大学第一附属医院(西京消化病医院)收治的经病理确诊为胃癌并接受胃癌根治术的患者;排除急诊手术、残胃癌、术前接受新辅助化疗和术中肿瘤不可根治切除或发现腹腔转移以及合并其他恶性肿瘤者。通过发放问卷的方式,调查患者对ERAS策略的期待和治疗期间的体验。患者对期待和体验方面的调查问题进行评分,0分表示完全不期待或不满意,10分表示很期待或十分满意。根据患者对于ERAS的不同体验,将患者根据出院时填写问卷中的“是否认可ERAS策略”项目分为ERAS认可组和抵触组。观察指标:(1)入组患者情况;(2)了解全组并比较两组患者对于ERAS的期望、偏好和住院体验;(3)两组促进和阻碍ERAS认可因素的比较;(4)了解全组并比较两组患者出院后的转归,采用电话方式进行随访,随访内容为术后30 d内并发症和身体是否不适,并发症按照Clavien-Dindo分类标准进行程度分级。正态分布的计量资料组间比较采用Student t检验。偏态分布的计量资料使用M(Q1,Q3)表示,组间比较采用独立样本的Mann-Whitney U检验。自身前后对照的正态分布与偏态分布资料分别采用配对Student t检验或Wilcoxon配对秩和检验。计数资料组间比较使用χ2检验。
纳入符合条件的患者112例,男88例,女24例;年龄(57.8±10.0)岁;其中ERAS认可组77例、抵触组35例。住院时,胃癌根治术患者普遍存在焦虑情绪,56.2%(63/112)患者的住院焦虑评分超过了8分。住院时患者对ERAS策略的了解程度不高[2(0,5)分],通过住院宣教,这一状况较前明显改善[8(4,10)分],差异有统计学意义(Z=-7.130,P<0.001)。患者预期的术后住院时间要长于实际住院时间[7(7,10)d比6(6,7)d],差异有统计学意义(Z=-4.800,P<0.001)。51.8%(58/112)的患者希望能够出院后直接返回家中继续康复,但32.1%(36/112)的患者更希望能够在医院继续治疗直到自己感觉身体完全康复。与ERAS抵触组相比,认可组患者的预期住院时间更短[7(6,10)d比10(7,15)d,Z=-2.607,P=0.009],康复效率提高评分更高[9(8,10)分比7(5,9)分,Z=-3.078,P=0.002],期望缓解疼痛[8(6,10)分比6(5,9)分,Z=-1.996,P=0.046]、体力恢复加速[8(6,10)分比6(4,9)分,Z=-2.200,P=0.028]、期待减少引流管[8(8,10)分比8(5,10)分,Z=-2.075,P=0.038]的评分均更高,差异均有统计学意义(均P<0.05)。在随访过程中,有105例患者接听了随访电话。57.1%(60/105)的患者在出院后经历了各种不适,其中包括疼痛(28.6%)、腹胀(20.0%)、恶心(12.4%)、疲乏(7.6%)和发热(2.9%)。出院30 d内,6.7%(7/105)的患者发生了Clavien-DindoⅠ、Ⅱ级手术相关并发症,包括伤口愈合不良、肠梗阻、腹腔出血、伤口感染,均经保守治疗治愈;全组术后未发生Ⅲ级以上并发症。与认可组相比,抵触组中更多的患者在出院时认为自己尚未达到自我预期的康复[22.9%(8/35)比57.1%(44/77),χ2=11.372,P<0.001],且并不急于回归日常生活[8.6%(3/35)比39.0%(30/77),χ2=10.693,P<0.001],差异均有统计学意义(均P<0.05)。仅52.4%(55/105)的患者返回家中进行后续康复,其余患者在出院后选择前往其他医院继续住院,再次住院时间的中位数为7(7,9)d。与ERAS抵触组比较,ERAS认可组居家康复比例更高[59.7%(12/33)比36.4%(43/72),χ2=4.950,P=0.026]、自我认为术后完全康复时间更短[14(10,20)d比15(14,20)d,Z=2.100,P=0.036],差异均有统计学意义(均P<0.05)。
尽管ERAS在保证手术安全的前提下促进了术后的康复,但尚未得到患者的一致认可。充分的康复宣教、良好的镇痛、较好的体力恢复以及引流管的早期去除,可能改善患者对于ERAS的体验。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
加速康复外科(enhanced recovery after surgery,ERAS)策略在患者的术后康复中已经被广泛采纳,其主要目的是让患者在术后尽快实现身体生理功能的康复。在ERAS策略推进的过程中,胃癌患者术后的住院天数逐渐由最初的7~9 d缩短至5 d[1, 2, 3, 4]。在不增加再入院率的前提下,一些医疗机构也在尝试能否实现术后住院时间的进一步缩短[4, 5, 6]。
然而,对于患者而言,不断削减的住院时间完全颠覆了他们对于术后康复的固有认知。早期出院将术后康复的压力转移给了患者。ERAS策略中出院标准的制订依据于一些从机体功能康复出发的生理学指标,而患者对于ERAS的体验并未被考虑在内[2,7, 8]。从ERAS制订的本意来看,患者应处于ERAS策略推进的中心地位,更好地理解患者对于术后康复的期待和患者在治疗期间的体验,可能有助于提高ERAS的依从性,缓解患者出院后的焦虑[9]。但是,目前较少有研究关注患者在ERAS策略推进过程中的处境[10, 11, 12]。患者在执行ERAS策略过程中的体验如何,对于ERAS策略的接受程度如何,对于ERAS的认可程度是否影响出院后的转归,目前均尚不明确。即使在胃手术的ERAS指南中,是否有必要将患者的体验作为ERAS策略的出院标准,也没有明确说明[13]。
故本研究探讨胃癌根治术后患者在ERAS策略执行过程中的主观体验,分析患者对于ERAS的理解程度、对于ERAS策略的期望、对于ERAS各项措施的认可程度,并比较对ERAS策略持不同态度患者出院后30 d内的临床结局,以期为临床提供参考。
本研究采用前瞻性队列研究的方法,连续纳入2019年12月至2020年12月拟在空军军医大学第一附属医院(西京消化病医院)消化外科接受胃癌根治术的患者。根据患者出院时填写调查问卷中的“是否认可ERAS策略”项目,将患者分为ERAS认可组和抵触组。
本研究通过空军军医大学第一附属医院(西京消化病医院)伦理委员会审批(审批号:KY20192086-F-1号)。患者及家属均签署知情同意书。研究项目在中国临床试验网进行了注册(注册编号为ChiCTR1900026354),本研究的报告格式遵循STROBE(Strengthening the Reporting of Observational Studies in Epidemiology)规范[14]。
纳入标准:(1)病理确诊为胃癌;(2)拟行胃癌根治术。
排除标准:(1)急诊手术;(2)残胃癌;(3)术前接受新辅助化疗;(4)术中发现肿瘤不可切除或腹腔转移;(5)合并其他恶性肿瘤。
使用本研究专用的调查问卷采集患者资料,本文使用的问卷请通过扫描本文首页的二维码获取。调查问卷分为3个部分:(1)患者对于ERAS的认识和期待;(2)治疗期间患者对于ERAS策略的体验;(3)患者出院30 d内的临床转归。
患者对期待和体验方面的调查问题进行评分,0分表示完全不期待或不满意,10分表示很期待或十分满意。入院和出院当日,患者分别将调查问卷的第1和第2部分交给研究者。出院后第30天,研究者通过电话方式联系患者,询问患者出院后的康复情况并完成问卷的第3部分。
本研究中的ERAS策略按照指南规范的原则执行[13]。出院标准参照既往研究的标准制定[6,15]:视觉疼痛模拟评分<4分,体温、白细胞计数正常,每日自主活动6 h以上,经口饮食能够满足日常能量和液体需要,无恶心、呕吐、腹胀等消化道症状,正常排气、排粪,患者及家属同意出院。
观察指标:(1)入组患者情况:性别、年龄、体质指数、美国东部肿瘤协作组体力状况评分、术前合并症(高血压、糖尿病、冠心病)、营养风险评分2002、血清总蛋白、血清白蛋白、血清总淋巴计数、血红蛋白、腹腔镜手术比例、全胃切除比例、术后并发症、术中出血量、手术时间、肿瘤分期、总住院天数和术后住院时间。(2)了解全组并比较ERAS抵触组和认可组患者的期望、偏好和住院体验。(3)分析促进和阻碍ERAS认可的因素:比较ERAS抵触组和认可组对ERAS认可差异的因素。(4)了解全组并比较两组患者出院后的转归。并发症按照Clavien-Dindo分类标准进行程度分级,其中Ⅲa级以上需要手术干预[16]。
患者出院后第30天,通过电话对患者进行康复状况的随访。随访内容包括出院后的康复地点、身体任何不适、手术相关并发症、自认为达到康复所需的时间。随访时间截至2021年2月。
使用SPSS 17.0进行统计分析。正态分布的计量资料使用x±s表示,组间比较采用Student t检验。偏态分布的计量资料使用M(Q1,Q3)表示,组间比较采用独立样本的Mann-Whitney U秩合检验。自身前后对照的正态分布与偏态分布资料分别采用配对Student t检验、Wilcoxon配对秩和检验。计数资料采用例(%)表示,组间比较使用χ2检验。在任何统计阶段均采用概率P值进行统计推断,统计学显著性差异界值用0.05 表示。由于本研究的探索性质,故没有进行样本量的计算。
纳入符合条件的患者112例,男88例,女24例;年龄(57.9±8.9)岁。其中ERAS认可组35例、抵触组77例,两组患者的一般临床资料的比较,差异均无统计学意义(均P>0.05)。见表1。
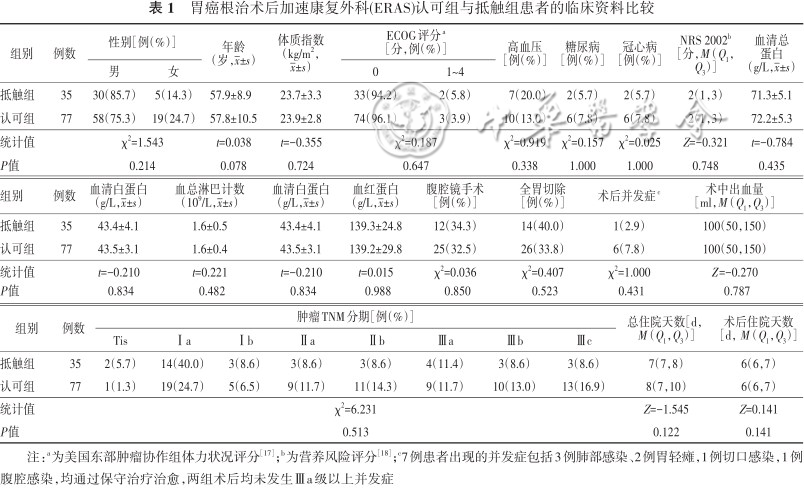
胃癌根治术后加速康复外科(ERAS)认可组与抵触组患者的临床资料比较
胃癌根治术后加速康复外科(ERAS)认可组与抵触组患者的临床资料比较
| 组别 | 例数 | 性别[例(%)] | 年龄 (岁,x±s) | 体质指数 (kg/m2, x±s) | ECOG评分a [分,例(%)] | 高血压 [例(%)] | 糖尿病 [例(%)] | 冠心病 [例(%)] | NRS 2002b[分,M(Q1,Q3)] | 血清总 蛋白 (g/L,x±s) | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 男 | 女 | 0 | 1~4 | |||||||||||
| 抵触组 | 35 | 30(85.7) | 5(14.3) | 57.9±8.9 | 23.7±3.3 | 33(94.2) | 2(5.8) | 7(20.0) | 2(5.7) | 2(5.7) | 2(1,3) | 71.3±5.1 | ||
| 认可组 | 77 | 58(75.3) | 19(24.7) | 57.8±10.5 | 23.9±2.8 | 74(96.1) | 3(3.9) | 10(13.0) | 6(7.8) | 6(7.8) | 2(1,3) | 72.2±5.3 | ||
| 统计值 | χ2=1.543 | t=0.038 | t=-0.355 | χ2=0.187 | χ2=0.919 | χ2=0.157 | χ2=0.025 | Z=-0.321 | t=-0.784 | |||||
| P值 | 0.214 | 0.078 | 0.724 | 0.647 | 0.338 | 1.000 | 1.000 | 0.748 | 0.435 | |||||
| 组别 | 例数 | 血清白蛋白 (g/L,x±s) | 血总淋巴计数 (109/L,x±s) | 血清白蛋白 (g/L,x±s) | 血红蛋白 (g/L,x±s) | 腹腔镜手术 [例(%)] | 全胃切除 [例(%)] | 术后并发症c | 术中出血量 [ml,M(Q1,Q3)] | |||||
| 抵触组 | 35 | 43.4±4.1 | 1.6±0.5 | 43.4±4.1 | 139.3±24.8 | 12(34.3) | 14(40.0) | 1(2.9) | 100(50,150) | |||||
| 认可组 | 77 | 43.5±3.1 | 1.6±0.4 | 43.5±3.1 | 139.2±29.8 | 25(32.5) | 26(33.8) | 6(7.8) | 100(50,150) | |||||
| 统计值 | t=-0.210 | t=0.221 | t=-0.210 | t=0.015 | χ2=0.036 | χ2=0.407 | χ2=1.000 | Z=-0.270 | ||||||
| P值 | 0.834 | 0.482 | 0.834 | 0.988 | 0.850 | 0.523 | 0.431 | 0.787 | ||||||
| 组别 | 例数 | 肿瘤TNM分期[例(%)] | 总住院天数[d,M(Q1,Q3)] | 术后住院天数 [d,M(Q1,Q3)] | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Tis | Ⅰa | Ⅰb | Ⅱa | Ⅱb | Ⅲa | Ⅲb | Ⅲc | ||||
| 抵触组 | 35 | 2(5.7) | 14(40.0) | 3(8.6) | 3(8.6) | 3(8.6) | 4(11.4) | 3(8.6) | 3(8.6) | 7(7,8) | 6(6,7) |
| 认可组 | 77 | 1(1.3) | 19(24.7) | 5(6.5) | 9(11.7) | 11(14.3) | 9(11.7) | 10(13.0) | 13(16.9) | 8(7,10) | 6(6,7) |
| 统计值 | χ2=6.231 | Z=-1.545 | Z=0.141 | ||||||||
| P值 | 0.513 | 0.122 | 0.141 | ||||||||
1.总体情况:本组患者住院时,普遍存在焦虑情绪,56.2%(63/112)住院焦虑评分超过了8分。初住院时,患者对ERAS策略的了解程度为2(0,5)分,通过住院宣教,较前提高到8(4,10)分,前后比较,差异有统计学意义(Z=-7.130,P<0.001)。在了解ERAS策略之后,患者对于更多的康复期望值和更舒适的治疗体验有了期待。具体见表2。
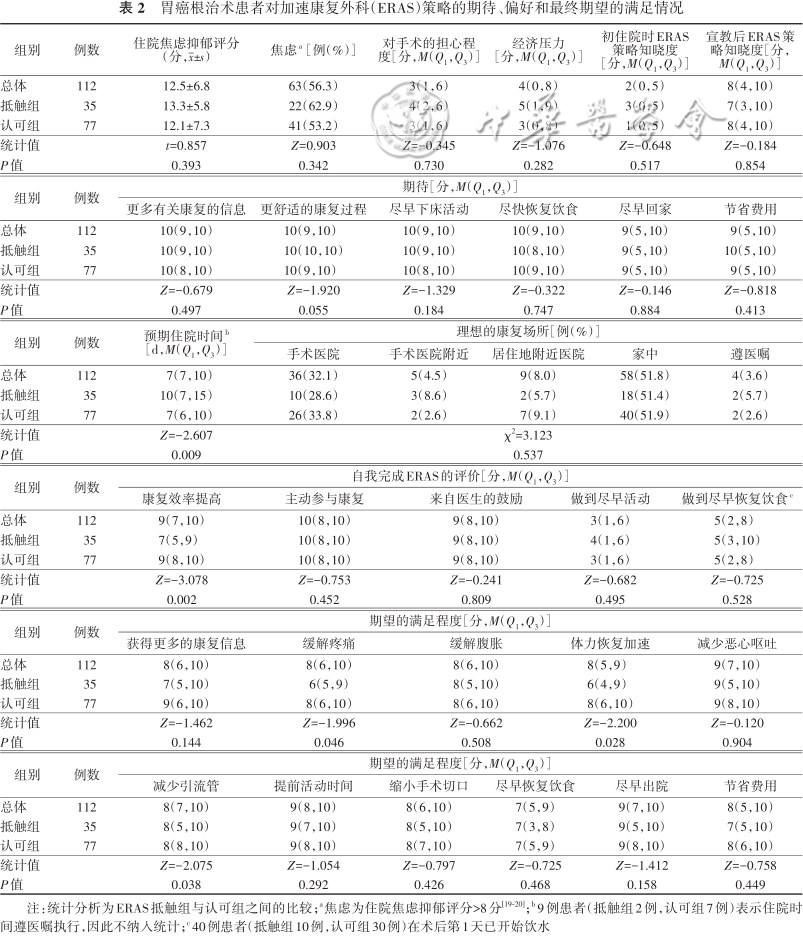
胃癌根治术患者对加速康复外科(ERAS)策略的期待、偏好和最终期望的满足情况
胃癌根治术患者对加速康复外科(ERAS)策略的期待、偏好和最终期望的满足情况
| 组别 | 例数 | 住院焦虑抑郁评分 (分,x±s) | 焦虑a[例(%)] | 对手术的担心程度[分,M(Q1,Q3)] | 经济压力 [分,M(Q1,Q3)] | 初住院时ERAS策略知晓度 [分,M(Q1,Q3)] | 宣教后ERAS策略知晓度[分, M(Q1,Q3)] | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 总体 | 112 | 12.5±6.8 | 63(56.3) | 3(1,6) | 4(0,8) | 2(0,5) | 8(4,10) | |||||
| 抵触组 | 35 | 13.3±5.8 | 22(62.9) | 4(2,6) | 5(1,9) | 3(0,5) | 7(3,10) | |||||
| 认可组 | 77 | 12.1±7.3 | 41(53.2) | 3(1,6) | 3(0,8) | 1(0,5) | 8(4,10) | |||||
| 统计值 | t=0.857 | Z=0.903 | Z=-0.345 | Z=-1.076 | Z=-0.648 | Z=-0.184 | ||||||
| P值 | 0.393 | 0.342 | 0.730 | 0.282 | 0.517 | 0.854 | ||||||
| 组别 | 例数 | 期待[分,M(Q1,Q3)] | ||||||||||
| 更多有关康复的信息 | 更舒适的康复过程 | 尽早下床活动 | 尽快恢复饮食 | 尽早回家 | 节省费用 | |||||||
| 总体 | 112 | 10(9,10) | 10(9,10) | 10(9,10) | 10(9,10) | 9(5,10) | 9(5,10) | |||||
| 抵触组 | 35 | 10(9,10) | 10(10,10) | 10(9,10) | 10(8,10) | 9(5,10) | 10(5,10) | |||||
| 认可组 | 77 | 10(8,10) | 10(9,10) | 10(8,10) | 10(9,10) | 9(5,10) | 9(5,10) | |||||
| 统计值 | Z=-0.679 | Z=-1.920 | Z=-1.329 | Z=-0.322 | Z=-0.146 | Z=-0.818 | ||||||
| P值 | 0.497 | 0.055 | 0.184 | 0.747 | 0.884 | 0.413 | ||||||
| 组别 | 例数 | 预期住院时间b [d,M(Q1,Q3)] | 理想的康复场所[例(%)] | |||||||||
| 手术医院 | 手术医院附近 | 居住地附近医院 | 家中 | 遵医嘱 | ||||||||
| 总体 | 112 | 7(7,10) | 36(32.1) | 5(4.5) | 9(8.0) | 58(51.8) | 4(3.6) | |||||
| 抵触组 | 35 | 10(7,15) | 10(28.6) | 3(8.6) | 2(5.7) | 18(51.4) | 2(5.7) | |||||
| 认可组 | 77 | 7(6,10) | 26(33.8) | 2(2.6) | 7(9.1) | 40(51.9) | 2(2.6) | |||||
| 统计值 | Z=-2.607 | χ2=3.123 | ||||||||||
| P值 | 0.009 | 0.537 | ||||||||||
| 组别 | 例数 | 自我完成ERAS的评价[分,M(Q1,Q3)] | ||||||||||
| 康复效率提高 | 主动参与康复 | 来自医生的鼓励 | 做到尽早活动 | 做到尽早恢复饮食c | ||||||||
| 总体 | 112 | 9(7,10) | 10(8,10) | 9(8,10) | 3(1,6) | 5(2,8) | ||||||
| 抵触组 | 35 | 7(5,9) | 10(8,10) | 9(8,10) | 4(1,6) | 5(3,10) | ||||||
| 认可组 | 77 | 9(8,10) | 10(8,10) | 9(8,10) | 3(1,6) | 5(2,8) | ||||||
| 统计值 | Z=-3.078 | Z=-0.753 | Z=-0.241 | Z=-0.682 | Z=-0.725 | |||||||
| P值 | 0.002 | 0.452 | 0.809 | 0.495 | 0.528 | |||||||
| 组别 | 例数 | 期望的满足程度[分,M(Q1,Q3)] | ||||||||||
| 获得更多的康复信息 | 缓解疼痛 | 缓解腹胀 | 体力恢复加速 | 减少恶心呕吐 | ||||||||
| 总体 | 112 | 8(6,10) | 8(6,10) | 8(6,10) | 8(5,9) | 9(7,10) | ||||||
| 抵触组 | 35 | 7(5,10) | 6(5,9) | 8(5,10) | 6(4,9) | 9(5,10) | ||||||
| 认可组 | 77 | 9(6,10) | 8(6,10) | 8(6,10) | 8(6,10) | 9(8,10) | ||||||
| 统计值 | Z=-1.462 | Z=-1.996 | Z=-0.662 | Z=-2.200 | Z=-0.120 | |||||||
| P值 | 0.144 | 0.046 | 0.508 | 0.028 | 0.904 | |||||||
| 组别 | 例数 | 期望的满足程度[分,M(Q1,Q3)] | ||||||||||
| 减少引流管 | 提前活动时间 | 缩小手术切口 | 尽早恢复饮食 | 尽早出院 | 节省费用 | |||||||
| 总体 | 112 | 8(7,10) | 9(8,10) | 8(6,10) | 7(5,9) | 9(7,10) | 8(5,10) | |||||
| 抵触组 | 35 | 8(5,10) | 9(7,10) | 8(5,10) | 7(3,8) | 9(5,10) | 7(5,10) | |||||
| 认可组 | 77 | 8(8,10) | 9(8,10) | 8(7,10) | 7(5,9) | 9(8,10) | 8(6,10) | |||||
| 统计值 | Z=-2.075 | Z=-1.054 | Z=-0.797 | Z=-0.725 | Z=-1.412 | Z=-0.758 | ||||||
| P值 | 0.038 | 0.292 | 0.426 | 0.468 | 0.158 | 0.449 | ||||||
2.两组比较:与ERAS抵触组相比,认可组患者的预期住院时间更短,康复效率提高评分更高,期望缓解疼痛、体力恢复加速以及减少引流管的评分更高,且差异均有统计学意义(均P<0.05)。见表2。
1.总体情况:在促进ERAS认可程度的因素中,自认为已经康复是对于ERAS策略认可的主要因素(46.4%),而是否能够节省费用并非患者优先考虑的问题(8.9%);在阻碍ERAS认可程度的诸多因素中,出院后并发症风险的担忧位居首位(49.1%)。见表3。
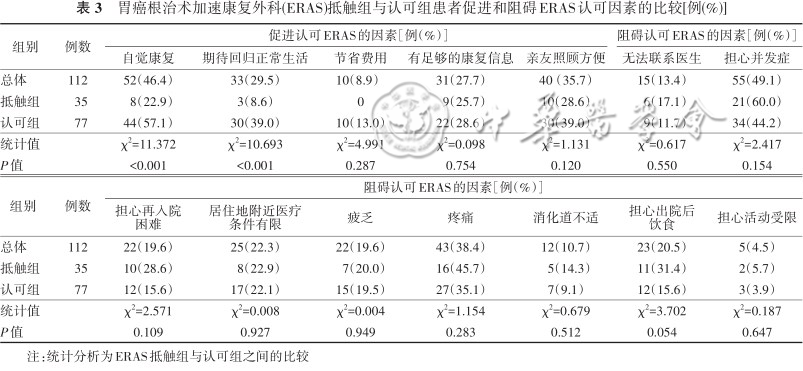
胃癌根治术加速康复外科(ERAS)抵触组与认可组患者促进和阻碍ERAS认可因素的比较[例(%)]
胃癌根治术加速康复外科(ERAS)抵触组与认可组患者促进和阻碍ERAS认可因素的比较[例(%)]
| 组别 | 例数 | 促进认可ERAS的因素[例(%)] | 阻碍认可ERAS的因素[例(%)] | |||||
|---|---|---|---|---|---|---|---|---|
| 自觉康复 | 期待回归正常生活 | 节省费用 | 有足够的康复信息 | 亲友照顾方便 | 无法联系医生 | 担心并发症 | ||
| 总体 | 112 | 52(46.4) | 33(29.5) | 10(8.9) | 31(27.7) | 40(35.7) | 15(13.4) | 55(49.1) |
| 抵触组 | 35 | 8(22.9) | 3(8.6) | 0 | 9(25.7) | 10(28.6) | 6(17.1) | 21(60.0) |
| 认可组 | 77 | 44(57.1) | 30(39.0) | 10(13.0) | 22(28.6) | 30(39.0) | 9(11.7) | 34(44.2) |
| 统计值 | χ2=11.372 | χ2=10.693 | χ2=4.991 | χ2=0.098 | χ2=1.131 | χ2=0.617 | χ2=2.417 | |
| P值 | <0.001 | <0.001 | 0.287 | 0.754 | 0.120 | 0.550 | 0.154 | |
| 组别 | 例数 | 阻碍认可ERAS的因素[例(%)] | ||||||
担心再入院 困难 | 居住地附近医疗 条件有限 | 疲乏 | 疼痛 | 消化道不适 | 担心出院后 饮食 | 担心活动受限 | ||
| 总体 | 112 | 22(19.6) | 25(22.3) | 22(19.6) | 43(38.4) | 12(10.7) | 23(20.5) | 5(4.5) |
| 抵触组 | 35 | 10(28.6) | 8(22.9) | 7(20.0) | 16(45.7) | 5(14.3) | 11(31.4) | 2(5.7) |
| 认可组 | 77 | 12(15.6) | 17(22.1) | 15(19.5) | 27(35.1) | 7(9.1) | 12(15.6) | 3(3.9) |
| 统计值 | χ2=2.571 | χ2=0.008 | χ2=0.004 | χ2=1.154 | χ2=0.679 | χ2=3.702 | χ2=0.187 | |
| P值 | 0.109 | 0.927 | 0.949 | 0.283 | 0.512 | 0.054 | 0.647 | |
注:统计分析为ERAS抵触组与认可组之间的比较
2.两组比较:与认可组相比,抵触组中更多的患者在出院时认为自己尚未达到自我预期的康复(22.9%比57.1%),且并不急于回归日常生活(8.6%比39.0%),差异均有统计学意义(均P<0.001);两组患者其余各项促进或阻碍ERAS认可因素比较,差异均无统计学意义(均P>0.05)。见表3。
1.总体情况:共105例(93.8%)患者接受随访。57.1%的患者在出院后经历了各种不适,其中包括疼痛、腹胀、恶心、疲乏和发热。出院30 d内,6.7%的患者发生了Ⅰ~Ⅱ级手术相关并发症,包括伤口愈合不良、肠梗阻、腹腔出血、伤口感染,均经保守治疗治愈;全组术后均未发生Ⅲ级以上并发症。出院后有52.4%的患者返回家中进行后续康复,其余患者在出院后选择前往其他医院继续住院恢复。见表4。
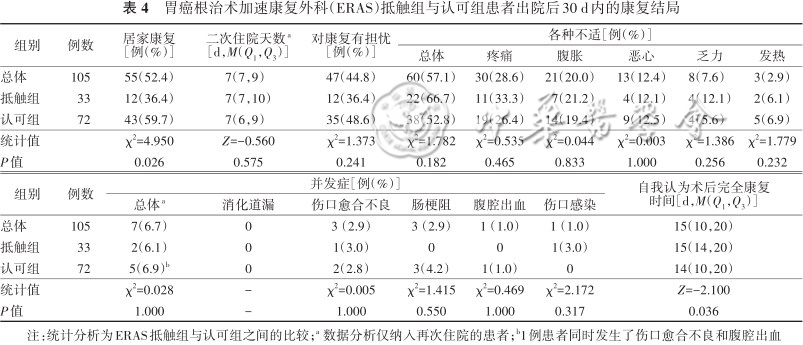
胃癌根治术加速康复外科(ERAS)抵触组与认可组患者出院后30 d内的康复结局
胃癌根治术加速康复外科(ERAS)抵触组与认可组患者出院后30 d内的康复结局
| 组别 | 例数 | 居家康复 [例(%)] | 二次住院天数a [d,M(Q1,Q3)] | 对康复有担忧[例(%)] | 各种不适[例(%)] | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| 总体 | 疼痛 | 腹胀 | 恶心 | 乏力 | 发热 | |||||
| 总体 | 105 | 55(52.4) | 7(7,9) | 47(44.8) | 60(57.1) | 30(28.6) | 21(20.0) | 13(12.4) | 8(7.6) | 3(2.9) |
| 抵触组 | 33 | 12(36.4) | 7(7,10) | 12(36.4) | 22(66.7) | 11(33.3) | 7(21.2) | 4(12.1) | 4(12.1) | 2(6.1) |
| 认可组 | 72 | 43(59.7) | 7(6,9) | 35(48.6) | 38(52.8) | 19(26.4) | 14(19.4) | 9(12.5) | 4(5.6) | 5(6.9) |
| 统计值 | χ2=4.950 | Z=-0.560 | χ2=1.373 | χ2=1.782 | χ2=0.535 | χ2=0.044 | χ2=0.003 | χ2=1.386 | χ2=1.779 | |
| P值 | 0.026 | 0.575 | 0.241 | 0.182 | 0.465 | 0.833 | 1.000 | 0.256 | 0.232 | |
| 组别 | 例数 | 并发症[例(%)] | 自我认为术后完全康复 时间[d,M(Q1,Q3)] | |||||||
| 总体a | 消化道漏 | 伤口愈合不良 | 肠梗阻 | 腹腔出血 | 伤口感染 | |||||
| 总体 | 105 | 7(6.7) | 0 | 3(2.9) | 3(2.9) | 1(1.0) | 1(1.0) | 15(10,20) | ||
| 抵触组 | 33 | 2(6.1) | 0 | 1(3.0) | 0 | 0 | 1(3.0) | 15(14,20) | ||
| 认可组 | 72 | 5(6.9)b | 0 | 2(2.8) | 3(4.2) | 1(1.0) | 0 | 14(10,20) | ||
| 统计值 | χ2=0.028 | - | χ2=0.005 | χ2=1.415 | χ2=0.469 | χ2=2.172 | Z=-2.100 | |||
| P值 | 1.000 | - | 1.000 | 0.550 | 1.000 | 0.317 | 0.036 | |||
注:统计分析为ERAS抵触组与认可组之间的比较;a 数据分析仅纳入再次住院的患者;b1例患者同时发生了伤口愈合不良和腹腔出血
2.两组比较:与ERAS抵触组比较,认可组居家康复比例更高、自我认为术后完全康复时间更短,差异均有统计学意义(均P<0.05),见表4。在随访时,有17例(16.2%)表示他们没有达到完全康复。
本研究从胃癌患者的角度,调查了ERAS执行过程中的主观体验。结果显示,31.2%(35/112)的患者并不认可ERAS策略,其中主要问题集中在对出院后康复的各种主观担忧。尽管患者在出院时达到了生理的出院标准,术后并发症发生率仅为6.7%,而且没有发生Ⅲ级以上严重并发症,但是近半数的患者仍然选择出院后前往其他医疗机构继续进行中位数为7 d的康复治疗。而这种现象在不认可ERAS策略的患者中表现尤为明显。为减少出院后不必要的再入院,我们在ERAS的执行过程中,需要考虑到患者的主观体验,通过加强宣教和增强出院指导的方式,增强患者的康复信心,改善患者的治疗体验。
患者对于术后康复的认知可能是他们对ERAS持消极态度的主要原因。首先,ERAS达到了术后短期内生理功能恢复的目的,但从本研究的诸多期待因素中可以看出,尽早出院和通过缩短住院时间节省医疗费用这两大问题是患者较少关注的事情。其次,在患者固有的观念里,认为术后可能需要较长的恢复时间。从表1所示的术后住院天数与表2所示的患者预期住院天数的比较来看,患者对于住院时间的期待超过了患者实际达到ERAS出院标准的天数;而抵触组的患者入院时自我预期的术后住院时间更长。最后,无法达成预期的康复目标可能降低了患者对自身康复的认可程度。一些ERAS的具体项目对术后患者而言,显得较为难以接受,比如患者普遍对术后尽早活动以及尽早恢复饮食的自我评分不高,其分值的中位数仅为3分和5分。
尽管患者出院时在客观的生理康复方面已经达标,但是从主观的心理上未必做好出院的准备。首先,通过ERAS策略的实施,虽然患者在短期内已达到了出院标准,但明显早于患者的预期。既往研究显示,患者接受腹腔镜根治性远端胃切除后,在(111.6±34.3)h即可达到出院标准[6]。在本研究中,患者达到出院标准的中位时间是6 d,而在随后的随访过程中,患者表示他们达到自我感觉基本康复的中位时间是15 d。其次,本研究患者出院后并发症率为6.7%,但57.1%的患者在出院后经历了各种不适,其中包括疼痛、恶心、腹胀、乏力,甚至发热,然而,这些不适症状并未对患者造成实质性的危害。既往一项包含了1 442例患者的大样本研究也表明,遵循ERAS策略康复的胃癌术后患者并发症发生率不高,在出院后的180 d内仅为3.8%,且几乎没有严重并发症[3]。但是,这些不适感可能引发患者的焦虑和担忧,直接导致患者前往居住地附近医院继续住院治疗。另外,患者对于ERAS出院标准的体验因人而异。既往一项针对结肠术后ERAS策略执行的研究显示,一些患者虽然认为出院比较仓促,但这并不意味着他们希望继续住院[21]。一些患者希望尽快出院回到熟悉的环境,而另一些患者则认为出院后难以进行康复,继续住院才能够获得足够的治疗和康复信息,直至他们自己感觉到完全康复后才会考虑出院[22]。尽管如此,这些对于ERAS策略的消极看法不能完全归咎于现有的出院标准。与其让患者延长非必要的住院时间,不如在ERAS的执行过程中增强患者的体验,通过加强康复宣教的方式,缓解患者出院后的焦虑情绪,比如入院时告知患者预期的住院时间可能就是一种比较合理的举措[9]。
本研究存在以下几个缺陷。(1)这是一项单中心的研究,考虑到各地医疗政策的差异,本研究的结果可能并不完全适用于所有的医疗单位。(2)本研究并未调查患者对于各项ERAS策略的执行情况,因此,我们无法知晓那些不认同ERAS策略的患者的消极态度是否由ERAS措施的执行不到位所致。(3)由于先前较少有研究从患者的角度看待ERAS的体验,本研究性质应归为探索性研究,因此并未对样本量进行计算。
总之,在目前ERAS策略的实施过程中,有相当一部分患者并不认可ERAS 策略。这些对ERAS策略持抵触情绪的患者更有可能在出院后前往其他医院继续治疗,这一结局违背了ERAS策略执行的初衷。因此,在ERAS的执行过程中,我们需要关注患者的体验,通过提前告知预期住院时间、加强早期离床活动宣教、初期饮食恢复指导,并提供充足的术后康复指导信息等措施增强患者对ERAS措施的认可、接纳程度。
西京消化病医院消化三科护理团队的大力协助
所有作者均声明不存在利益冲突



























