
总结扩张的胸廓内动脉穿支(IMAP)皮瓣联合血管增压在面颈部瘢痕整复中的临床应用经验。
采用回顾性观察性研究方法。2012年9月—2021年5月,上海交通大学医学院附属第九人民医院收治23例符合入选标准的烧创伤后面颈部瘢痕患者,其中男18例、女5例,年龄11~58岁,均采用扩张的IMAP皮瓣整复。Ⅰ期根据瘢痕部位和范围在前胸置入1个或2个合适额定容量的皮肤软组织扩张器,术中注意保护IMAP、锁骨上动脉胸支和胸外侧动脉,术后注入生理盐水进行扩张。Ⅱ期行皮瓣转移术,术前使用彩色多普勒超声血流探测仪明确优势IMAP。切除面颈部瘢痕,形成面积为9 cm×7 cm~28 cm×12 cm的创面,术中注意保留颞浅动静脉或面动静脉穿支。以优势IMAP为蒂,根据瘢痕切除后创面面积和位置设计皮瓣:对于中小面积的创面,采用IMAP单蒂皮瓣转移修复;对于缺损面积较大者,利用吲哚菁绿血管造影(ICGA)评价前胸各血管的供血范围,当IMAP不足以供养整块皮瓣时,利用锁骨上动脉胸支或胸外侧动脉进行血管增压,设计双蒂皮瓣。根据供受区间的距离,选择带蒂或游离转移皮瓣。转移皮瓣后再次行ICGA判断皮瓣血供。将供瓣区直接拉拢缝合。统计皮肤软组织扩张器置入个数、额定容量、注射生理盐水量和扩张周期,优势IMAP位置,采用皮瓣总个数和不同血管蒂类型皮瓣个数、皮瓣面积,Ⅱ期术后皮瓣存活情况、供受区常见并发症发生情况和随访情况。
共置入25个皮肤软组织扩张器,皮肤软组织扩张器额定容量为200~500 mL,注射生理盐水量855~2 055 mL,扩张周期4~16个月。术前在第2肋间(20侧)或第3肋间(5侧)探及优势IMAP。共切取25个扩张皮瓣,其中2个IMAP带蒂皮瓣、11个IMAP游离皮瓣、4个锁骨上动脉胸支带蒂+IMAP游离皮瓣、8个IMAP+胸外侧动脉游离皮瓣,皮瓣面积10 cm×8 cm~30 cm×14 cm。Ⅱ期术后3例患者出现皮瓣尖端坏死,经常规换药后愈合;1例患者IMAP和面动脉吻合处出现血管蒂局部扭转、血栓栓塞,手术探查取出血栓、重新吻合血管后,血供恢复正常。14例患者在Ⅱ期术后1~6个月进行了皮瓣修薄手术。随访4个月~9年,所有患者皮瓣外观良好,面颈部功能改善,供区可见线性瘢痕形成;1例女性患者出现明显乳头移位,双侧乳房不对称。
扩张IMAP皮瓣颜色、质地与面颈部皮肤组织匹配,且切取后对胸部供区的损伤小,联合血管增压可灵活设计双蒂皮瓣,进一步改善血供,扩大皮瓣切取面积,是大面积面颈部瘢痕整复的良好选择。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
面颈部是人体重要的功能和美学单位,严重的烧创伤会使头颈部运动受限,面部五官牵拉变形,影响患者的视物、呼吸、进食等功能[1, 2]。同时,畸形的外观给患者带来极大社交障碍和心理负担[3]。面颈部修复重建要求高,供区选择应遵循“MLT”原则,即选择颜色质地匹配(match)、面积足够大(large)、厚度足够薄(thin)的组织进行修复[4]。前胸位置毗邻面颈部,面积大,有胸廓内动脉穿支(internal mammary artery perforator,IMAP)、锁骨上动脉胸支、胸外侧动脉和胸尖峰动脉等多重血供,是面颈部大面积缺损修复的良好供区。自1965年Bakamjian[5]初次报道以胸廓内动脉多穿支为蒂的胸三角皮瓣以来,国内外学者对IMAP进行了深入的解剖学研究[6, 7, 8],并将胸三角皮瓣及其改良后单穿支供血的IMAP皮瓣广泛应用于面颈部重建[9]。本研究团队结合皮肤软组织扩张技术和吲哚菁绿血管造影(indocyanine green angiography,ICGA)技术,联合血管增压设计扩张单蒂、双蒂IMAP皮瓣,成功修复23例患者面颈部大面积缺损,取得良好效果。
本回顾性观察性研究符合《赫尔辛基宣言》的基本原则,患者及其家属签署知情同意书,同意将相关临床资料用于临床、教学研究。
纳入标准:因多种原因导致面颈部瘢痕形成,采用扩张的IMAP皮瓣移植整复,术后随访3个月以上。排除标准:临床资料不完整者。
2012年9月—2021年5月,上海交通大学医学院附属第九人民医院收治23例符合入选标准的面颈部瘢痕患者,其中男18例、女5例;年龄11~58岁,平均年龄29.35岁。患者均因烧创伤导致面颈部瘢痕增生或挛缩,烧创伤后至瘢痕整复手术时间为2~35年。根据马显杰团队结合Zan等[10]报道的面部软组织畸形分类标准提出的面颈部病损类型分类[11],将本组患者面颈部畸形分为Ⅱ型4例(17.4%)、Ⅲ型8例(34.8%)、Ⅳ型1例(4.3%)、Ⅴ型10例(43.5%)。
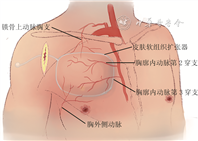
前胸供瓣区内侧以胸骨旁1~2 cm为界,外侧可达三角肌区,上界为锁骨下,下界至第5肋间[12]。术前根据瘢痕大小、位置,选择放置皮肤软组织扩张器的数量和额定容量。当预计单侧皮瓣不能修复全部病损时,可双侧置入皮肤软组织扩张器,采用双侧皮瓣进行修复。选择胸大肌外侧肩部纵向切口,剥离胸大肌和皮下深筋膜之间的腔隙,置入皮肤软组织扩张器,术中注意保护IMAP、锁骨上动脉胸支和胸外侧动脉,见图1。术后10~14 d拆线,注射生理盐水进行扩张,每次注水量为皮肤软组织扩张器额定容量的10%~15%[13],总注水量达到额定容量后逐渐减量,并根据皮肤张力和毛细血管反应进行调节,每周注射1次或2次,直至预计扩张皮瓣面积达到预估的创面面积的120%时停止注水。

术前使用彩色多普勒超声(CDU)血流探测仪探查IMAP,评估穿支口径、血流方向和速度等血流动力学指标,标记优势穿支的起点和走行[14]。患者全身麻醉后,用亚甲蓝标记需切除的瘢痕范围,沿标记线切除面颈部瘢痕,形成面积为9 cm×7 cm~28 cm×12 cm的创面,术中注意保留颞浅动静脉或面动静脉穿支。在扩张皮肤上按创面面积扩大20%设计皮瓣,逐层分离皮肤、皮下组织和肌肉,显露优势穿支至胸廓内动脉主干水平,并于胸大肌和肋间内肌中剥离IMAP,在胸大肌肌膜浅面完整游离皮瓣。
皮瓣设计原则:根据创面缺损面积,设计IMAP单蒂或双蒂皮瓣;根据供受区位置,选择带蒂或游离转移皮瓣。对于本组中5个中小面积的创面,采用IMAP单蒂皮瓣修复,优先带蒂转移;供受区距离较远时进行游离转移,选择将口径、位置与IMAP匹配的颞浅动静脉或面动静脉作为受区血管与IMAP吻合。其余面积较大的创面,所需皮瓣超过单一IMAP供血范围,切取皮瓣时保留并分离锁骨上动脉胸支或胸外侧动脉。各血管分离完成后,依次夹闭,利用ICGA评估各血管的灌注范围。ICGA操作如下:将25 mg吲哚菁绿溶解于10 mL灭菌注射用水中配制成2.5 mg/mL溶液。从外周静脉注射3 mL该溶液,即刻关闭环境光源并使用SPY成像系统(加拿大Novadaq 科技公司)收集皮瓣荧光信号。最大灌注期造影剂可以完全灌注皮瓣,则提示皮瓣动脉灌注良好;若静脉相末期皮瓣与周围组织中造影剂同时完全回流,则提示皮瓣静脉回流良好。当皮瓣动脉灌注和静脉回流均良好时进行单蒂皮瓣转移。夹闭锁骨上动脉胸支或胸外侧动脉后,行ICGA提示8个IMAP皮瓣血运良好,直接采用IMAP单蒂皮瓣带蒂或游离移植;12个IMAP单蒂皮瓣血运不佳,开放锁骨上动脉胸支或胸外侧动脉进行增压,再次利用ICGA检查皮瓣血流灌注,设计双蒂皮瓣。颈部和下面部的创面可利用锁骨上动脉胸支带蒂+IMAP游离皮瓣转移修复,将IMAP与面动静脉吻合;中上面部创面则采用IMAP+胸外侧动脉游离皮瓣修复,将IMAP和胸外侧动静脉分别与颞浅动静脉和面动静脉进行吻合。吻合血管后,松开血管夹观察血运,再次进行ICGA评估,若ICGA提示皮瓣灌注不足或回流不佳,积极寻找原因并进行相应处理。将供瓣区直接拉拢缝合,留置引流管。常规于术后1~2周拆线,皮瓣臃肿者术后择期行皮瓣修整术。
记录置入皮肤软组织扩张器个数、额定容量、注射生理盐水量和扩张周期,优势IMAP位置,采用皮瓣总个数和不同血管蒂类型皮瓣个数、皮瓣面积,Ⅱ期术后皮瓣存活情况、供受区常见并发症发生情况和随访情况。
本组23例患者共使用25个皮肤软组织扩张器,其中21例患者单侧置入1个,2例患者双侧分别置入1个。皮肤软组织扩张器额定容量为200 mL者5个、300 mL者5个、400 mL者7个、500 mL者8个;注射生理盐水量855~2 055 mL,为皮肤软组织扩张器额定容量的3.4~5.0倍,扩张周期4~16个月。术前在第2肋间(20侧)或第3肋间(5侧)稳定探及优势IMAP。共切取25个扩张皮瓣进行创面修复,其中2个IMAP带蒂皮瓣,面积12 cm×8 cm~24 cm×13 cm,修复2例患者Ⅴ型畸形部位瘢痕切除后创面;11个IMAP游离皮瓣,面积10 cm×8 cm~24 cm×15 cm,修复4例患者Ⅱ型畸形、2例患者Ⅲ型畸形、1例患者Ⅳ型畸形和4例患者Ⅴ型畸形部位瘢痕切除后创面;4个锁骨上动脉胸支带蒂+IMAP游离皮瓣,面积22 cm×12 cm~25 cm×15 cm,修复1例患者Ⅲ型畸形、3例患者Ⅴ型畸形部位瘢痕切除后创面;8个IMAP+胸外侧动脉游离皮瓣,面积20 cm×14 cm~30 cm×14 cm,修复5例患者Ⅲ型畸形、1例患者Ⅳ型畸形和2例患者Ⅴ型畸形部位瘢痕切除后创面。23个创面中1个Ⅳ型畸形和1个Ⅴ型畸形部位瘢痕切除后创面由一侧IMAP带蒂皮瓣和另一侧IMAP+胸外侧动脉游离皮瓣共同修复。Ⅱ期术后1例患者IMAP和面动脉吻合处出现血管蒂局部扭转、血栓栓塞,手术探查取出血栓、重新吻合血管后,血供恢复正常;3例患者出现皮瓣尖端坏死,坏死面积4.0 cm×1.5 cm~5.0 cm×2.5 cm,经常规换药后愈合;其余患者皮瓣存活良好。14例患者在Ⅱ期术后1~6个月进行了皮瓣修薄手术。随访4个月~9年,所有患者皮瓣外观良好,颜色、质地与周围皮肤相近,面颈部功能改善,供区可见线性瘢痕形成;1例女性患者出现明显乳头移位,双侧乳房不对称。
例1
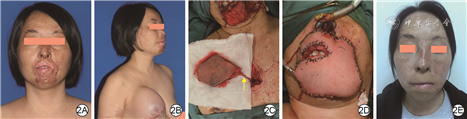
女,39岁,烧伤后面部及四肢增生性瘢痕形成2年入院。入院时可见口周片状瘢痕,质硬、高出皮肤,张口2指,畸形类型为Ⅱ型。Ⅰ期在右侧前胸置入1个额定容量200 mL的皮肤软组织扩张器,扩张周期为5个月,注水量达855 mL。Ⅱ期CDU血流探测仪检查提示右侧胸廓内动脉第2穿支为优势穿支。于全身麻醉下行口周瘢痕切除术,瘢痕切除后创面面积为9 cm×7 cm,切取面积为10 cm×8 cm的IMAP皮瓣进行游离移植,将胸廓内动脉第2穿支与面动静脉于下颌缘水平端端吻合。将供区直接拉拢缝合。术后皮瓣血运佳,7 d后拆线,3个月后行皮瓣修薄手术。随访3年,患者皮瓣颜色、质地与周围皮肤相近,张口达3指。见图2。

例2
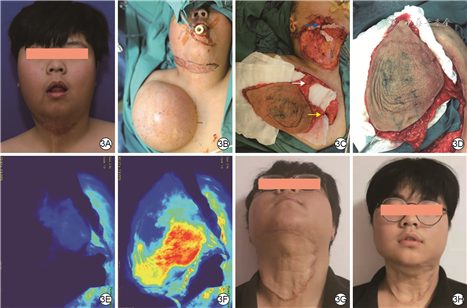
男,13岁,因交通事故伤致颈部增生性瘢痕挛缩畸形形成10年入院。入院时可见颏颈部片状瘢痕、瘢痕挛缩、颏颈粘连,颈部后仰受限,畸形类型为Ⅴ型,前胸皮肤完好。Ⅰ期于右侧前胸置入1个额定容量400 mL的皮肤软组织扩张器,扩张周期为7个月,注水量达1 880 mL。Ⅱ期于全身麻醉下行颈颏部瘢痕切除、松解+颈部轮廓成形术。CDU血流探测仪探测提示右侧胸廓内动脉第3穿支为优势穿支,瘢痕切除后创面面积为23 cm×13 cm,设计面积为25 cm×15 cm的皮瓣。因皮瓣面积较大,切取皮瓣时保留锁骨上动脉胸支和胸廓内动脉第3穿支,首先夹闭IMAP,对锁骨上动脉胸支进行ICGA,提示皮瓣远端靠近IMAP区域供血较差。遂同时开放IMAP和锁骨上动脉胸支,再次行ICGA,提示皮瓣血运良好,于是设计锁骨上动脉胸支带蒂+IMAP游离皮瓣。将锁骨上动脉胸支通过皮下隧道带蒂转移,将IMAP与右侧面动静脉于下颌缘水平端端吻合。将供区直接拉拢缝合。术后皮瓣血运良好,无并发症发生,10 d后拆线,6个月后行皮瓣修整。术后9个月,患者颈部活动功能较前明显改善,皮瓣颜色、质地与周围皮肤相近。见图3。

例3
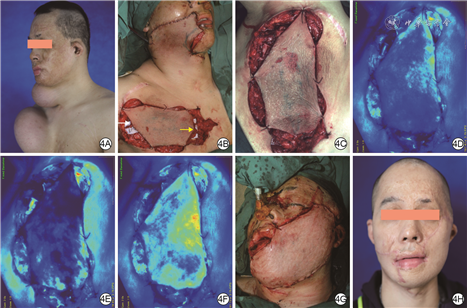
男,24岁,烧伤致面颈部瘢痕形成18年入院。入院时可见面颈部片状瘢痕,颏部瘢痕挛缩,颈部后仰受限,畸形类型为Ⅴ型,前胸皮肤完好。Ⅰ期于右侧颈部和前胸分别置入1个额定容量100、300 mL的皮肤软组织扩张器,扩张6个月,注水总量分别为400、1 350 mL。Ⅱ期于全身麻醉下行面颈部瘢痕切除、松解术,Ⅱ期术前CDU血流探测仪探查提示右侧胸廓内动脉第2穿支为优势穿支。将右颈部扩张皮瓣推进覆盖右侧面部缺损,剩余左侧创面面积约23 cm×11 cm,设计面积为25 cm×13 cm的游离皮瓣。于供区分离胸廓内动脉第2穿支和胸外侧动脉后,分别夹闭胸外侧动脉和IMAP进行ICGA,结果提示IMAP和胸外侧动脉单独供血时皮瓣远端灌注不足。遂同时开放IMAP和胸外侧动脉,再次行ICGA显示皮瓣血运良好,于是采用IMAP+胸外侧动脉游离皮瓣修复创面。分离左侧颞浅动静脉和右侧面动静脉并将其分别与IMAP和胸外侧动静脉进行端端吻合,将前胸供区直接拉拢缝合。术后皮瓣血运良好,6个月后行皮瓣修薄术。随访3年,患者中下面部皮瓣颜色、质地与周围正常皮肤相近,恢复了正常的下颌轮廓。见图4。

胸三角皮瓣被广泛应用于各类头、颈、胸部缺损的整复[15],国内马显杰团队长期致力于胸三角皮瓣的临床应用和技术改进,结合皮肤扩张、手术延迟等技术总结出规范化的分期手术方案,改善了皮瓣血供,减少了皮瓣坏死等并发症,解决了供区无法直接关闭、常需植皮等问题[16, 17, 18]。但胸三角皮瓣依然存在一定局限,如保留多穿支供血增加了皮瓣蒂部宽度,缩小了可旋转弧度,导致皮瓣可利用率降低;同时,将该皮瓣带蒂转移修复面部缺损时,断蒂前患者需长期保持头颈屈曲强迫体位。
随着人们对前胸血管解剖认识的深入,以及穿支皮瓣概念[19]的提出,2006年Yu等[20]对传统胸三角皮瓣进行改进,并首次报道采用单穿支的IMAP皮瓣进行气管造口重建。术中为了获得足够长的血管蒂,一般需要切除肋软骨,但这样易导致气胸、胸廓畸形和肋间神经痛等一系列并发症[21]。同时,也有学者通过解剖并携带部分胸廓内动脉主干血管以增加血管蒂长度[22],这种皮瓣从严格意义上来讲,不属于穿支皮瓣范畴。2013年,宋保强团队设计以胸廓内动脉第2或第3 穿支为血管蒂的皮瓣,断蒂后游离移植整复大面积面部瘢痕,并将IMAP与颞浅动静脉或面动静脉吻合[23],弥补了带蒂胸三角皮瓣旋转度小等不足,可修复更大面积的缺损。然而,由于分离的IMAP管径常小于受区血管,有时需要取额外的血管进行桥接,手术难度较大。
针对传统胸三角皮瓣和IMAP皮瓣的限制,本研究团队提出扩张的IMAP皮瓣联合血管增压进行面颈部瘢痕整复,主要包括以下几项技术要点。
结合皮肤软组织扩张技术,超量扩张获得大面积皮瓣。Saint-Cyr 等[24]于2009年首次报道使用左前胸扩张后12 cm×8 cm的IMAP带蒂皮瓣整复颈前瘢痕。本研究团队从2008年[25]开始尝试使用扩张的IMAP皮瓣带蒂或游离移植修复面颈部缺损,由于收治的部分患者病损面积较大,常需要进行超量扩张,注水量为皮肤软组织扩张器额定容量的3~5倍,联合使用血管增压——对皮瓣远端血管进行额外吻合,可获得血供可靠的大面积皮瓣。本组患者中双蒂皮瓣面积达30 cm×14 cm,远超IMAP单蒂皮瓣面积。在需要修复的皮肤软组织缺损范围更广泛时,比如全面部缺损、全面颈部缺损,本研究团队通常进一步结合皮瓣预构技术,Ⅰ期置入皮肤软组织扩张器的同时获取旋股外侧血管降支联合肌间隔筋膜瓣或其他血管载体,并将其置入颈胸部皮下,与面动静脉或甲状腺上动静脉吻合,构建前胸区预构皮瓣。Ⅱ期时以预构血管为蒂,联合IMAP和胸外侧动脉进行血管增压设计三蒂皮瓣[26, 27]。
术前采用CDU血流探测仪评估胸廓内动脉优势穿支,遵循优势血管原则设计皮瓣。胸廓内动脉沿胸骨两侧紧贴胸前壁第1~6肋骨后方垂直下行,绕每一肋骨向前于胸骨中线旁1~2 cm发出穿支血管穿过肋间肌和胸大肌营养皮肤[6]。1986年,Palmer和Taylor[28]首次描述了胸廓内动脉优势穿支的概念,国内外众多解剖学研究表明,第1~4肋间隙内恒定出现穿支,其中血管管径通常以第2穿支最大,第3穿支次之[29, 30],这与本研究团队采用术前CDU血流探测仪评估观察到本组患者的优势IMAP通常为第2(80%)或第3(20%)穿支相一致。相较于前胸皮肤其他供血血管而言,IMAP位置固定,以胸廓内动脉优势穿支为蒂设计皮瓣,灌注范围大且便于解剖。
利用IMAP解剖技巧,避免部分供区并发症。本研究团队在解剖IMAP时,根据术前CDU血流探测仪探测情况逐层分离显露优势穿支至胸廓内动脉主干水平,在胸大肌和肋间内肌中剥离出穿支,避免了切除肋软骨引起的供区并发症。本组患者均未出现气胸、胸廓畸形和肋间神经痛等情况,且获得的血管蒂与颞浅动脉、面动脉(下颌缘水平处)管径相近,利于血管吻合,无须额外进行血管桥接,缩短了手术时间。
采用ICGA技术,结合不同穿支灵活设计多蒂皮瓣。ICGA是以吲哚菁绿为造影剂,通过实时荧光采集,记录血流情况的一种显影技术,近10年来被广泛应用于皮瓣血流监测[31],具有无辐射、精度高等特点,可用于术中实时监测各血管的血流灌注情况并辅助进行血管增压决策。根据穿支体区理论,血管单个穿支体区范围较小,跨区切取皮瓣时易出现远端坏死。为满足大面积缺损修复要求,时常需要进行血管增压[32],以增强皮瓣远端血流供应。本研究团队前期的临床研究[33]和基础研究[34]均证明血管增压可促进穿支皮瓣存活。前胸皮肤具有多源血供,为灵活设计多蒂皮瓣提供了条件。对于累及多个面颈部单位的大面积缺损,可利用ICGA评估各穿支的灌注范围,设计多蒂皮瓣,提高皮瓣存活率,增加IMAP皮瓣可利用的面积。本组患者采用了12个双蒂皮瓣,成功整复较大面积瘢痕畸形。
采用扩张的IMAP皮瓣联合血管增压进行面颈部瘢痕整复的方法也存在一定局限:(1)前胸供区术后瘢痕形成,影响美观,且易造成女性乳房形态及乳头位置发生改变。(2)血管蒂较短,常需要通过显微外科技术进行游离移植,且穿支管径较小,对医师的技术要求高。(3)超量扩张及分期手术的治疗策略导致治疗周期长、治疗费用较高。临床实际应用中要严格把握适应证,对于女性以及有其他邻近带蒂皮瓣可选择的患者,优先考虑IMAP皮瓣之外的皮瓣,从而使患者最大限度获益。
综上所述,将IMAP皮瓣与皮肤软组织扩张和血管增压技术相结合,根据不同患者情况,灵活地选择IMAP单蒂皮瓣或联合胸外侧动脉或锁骨上动脉胸支设计双蒂皮瓣,可以有效地修复面颈部病损。该术式术后皮瓣颜色、质地与周围皮肤组织匹配,胸部供区损伤小,是大面积面颈部瘢痕整复的良好选择。
所有作者均声明不存在利益冲突



























